Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (7): 1071-1079.doi: 10.12307/2022.853
Previous Articles Next Articles
Application of the interaction between biological scaffolds and macrophages in bone regeneration
Yang Yitian1, 2, Wang Lu1, 2, Yao Wei1, 2, Zhao Bin1, 2
- 1Department of Prosthodontics, Hospital of Stomatology, Shanxi Medical University, Taiyuan 030000, Shanxi Province, China; 2Key Laboratory of Oral Diseases Prevention and New Materials, Taiyuan 030000, Shanxi Province, China
-
Received:2021-11-15Accepted:2021-12-13Online:2023-03-08Published:2022-07-19 -
Contact:Zhao Bin, Chief physician, Doctoral supervisor, Department of Prosthodontics, Hospital of Stomatology, Shanxi Medical University, Taiyuan 030000, Shanxi Province, China; Key Laboratory of Oral Diseases Prevention and New Materials, Taiyuan 030000, Shanxi Province, China -
About author:Yang Yitian, Master candidate, Department of Prosthodontics, Hospital of Stomatology, Shanxi Medical University, Taiyuan 030000, Shanxi Province, China; Key Laboratory of Oral Diseases Prevention and New Materials, Taiyuan 030000, Shanxi Province, China -
Supported by:Scientific and Technological Innovation Programs of Higher Education Institutions in Shanxi Province, No. 2019L0443 (to YW)
CLC Number:
Cite this article
Yang Yitian, Wang Lu, Yao Wei, Zhao Bin. Application of the interaction between biological scaffolds and macrophages in bone regeneration[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1071-1079.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
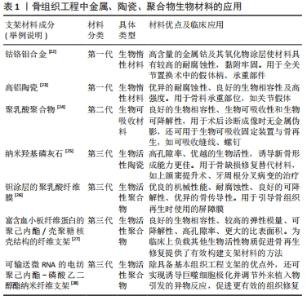
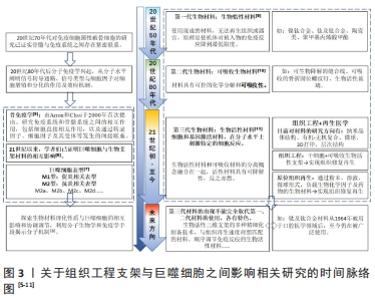
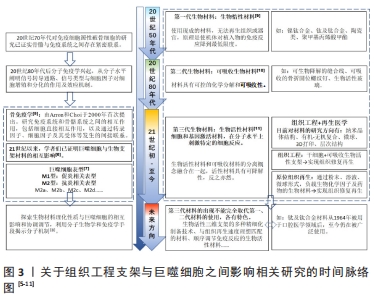
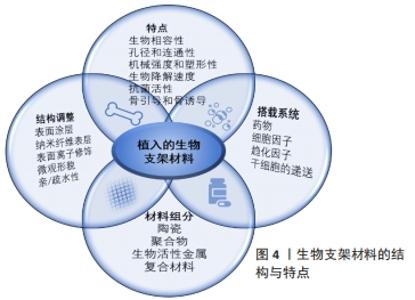
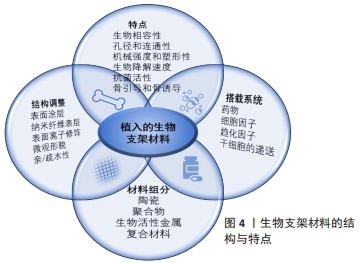
组织工程支架作为一类生物材料,必须具有与周围组织相适应的物理、化学和生物特性,以便在不造成组织损伤的情况下在人体内可靠和安全地发挥功效。考虑到生物材料与周围组织之间的相互作用,可将其分为3类[13]:生物惰性材料、生物可吸收材料和生物活性材料。生物惰性材料是指植入后在体内稳定,被纤维组织包裹和隔离,与相邻组织没有生物相互作用。生物可吸收材料是指植入后降解为无毒产品并最终被新形成的组织替代的材料。生物活性材料是指能够诱导和引导材料与周围组织发生生物反应的材料。以往的观点认为应尽可能避免由于材料本身原因导致机体出现的严重排异等反应,生物惰性材料的运用被视为是金标准[14]。随着细胞生物学与材料学等的逐步发展,生物活性材料应运而生,目标是利用材料的生物活性与机体发生相互作用。从第一代生物惰性材料发展到第二代生物可吸收材料,再到第三代的生物活性材料,不应被简单地按照时间发展顺序单一化的理解,3个分类是概念性的,每一代都涉及到材料的要求和性能的发展,各有所长,现如今第一、二代材料仍在临床上拥有一席之地,今后亦是如此,比如钴铬合金、钛及钛合金。根据材料本身性质,这些材料仍可被视为第一、二代。对于上述生物材料的清晰认识将更有助于在今后研究和开发更符合实际需求的生物材料。目前学者们认为应联合使用多种类型的生物材料,并利用材料对免疫细胞行为进行调控,有效利用材料与组织间的这种相互作用以增强植入物与现有组织之间的整合。 2.2.2 生物活性支架的分类与应用 植入制备组织工程支架的生物活性材料可分为4大类[15]:陶瓷、聚合物、金属和复合材料。陶瓷类生物活性材料主要包括生物活性玻璃、磷酸三钙、羟基磷灰石;羟基磷灰石的合成方法会影响羟基磷灰石颗粒的形态和大小,这两者都会影响这种材料在体内的生物功能性[16];纳米羟基磷灰石显示出比微米羟基磷灰石更高水平的孔隙率、更高的生物活性,含羟基磷灰石/β-磷酸三钙的复合材料诱导新骨形成的能力更佳[17],可考虑用于引导性骨再生术中促进新骨形成,如用于上颌窦提升、牙周根分叉病变的治疗。 生物活性聚合物有甲壳素/壳聚糖、蚕丝、丝胶、胶原蛋白、透明质酸、生物活性金属。不锈钢、钛及其合金、镁和钽等金属通过表面修饰(如碱热处理、过氧化氢处理和直接氧化)或使用其他生物活性材料进行表面涂层后均可得到生物活性金属。如聚多巴胺涂层可通过黏着斑激酶和p38信号通路改善支架的骨整合[18],利用聚多巴胺将镁修饰于多孔钽支架上构成钽-聚多巴胺-镁复合支架,改善了多孔钽支架的表面活性,使支架具有更好的耐腐蚀性、与组织更匹配的弹性模量以及更好的成骨和血管生成能力。 生物活性金属具有应力屏蔽和致敏性,蛋白质和多糖类材料具有免疫原性,为了有效避免不同材料的缺陷,复合材料随之出现,并通过组分设计和物理化学性质调节实现了组织工程生物支架的不断优化。目前发现改变复合支架的制备方式、组成成分、微观形貌、表面结构等会影响支架的性能,有学者采用静电纺丝技术制备了透明质酸/聚己内酯/明胶定向纳米纤维膜,这种定向纤维膜具有更高的亲水性[19]。通过在聚合物基质中添加一些纳米级生物活性剂,可以提高聚合物的生物活性。以锶离子为生物活性因子联合静电纺丝技术制备了无细胞的三维电纺聚己内酯/丝素蛋白/锶支架[20],通过改变制备方法、添加活性因子及调整材料组分比例等调控了支架的生物降解性和机械强度,并且锶的添加有效刺激了血管生长因子(如碱性成纤维细胞生长因子)的表达,有效达到了保护软骨、延缓骨关节炎发展的作用。此外,酰胺、酯类和酸酐属于易受水解侵蚀的常见官能团[21],可通过这些官能团来设计可水解降解的复合支架,优化降解动力学。但值得注意的是,由于复合材料组分及性能的复杂性,其制造方法上受到一定限制。现将骨组织工程中不同种类的生物材料的应用作一归纳[22-28],见表1。 "
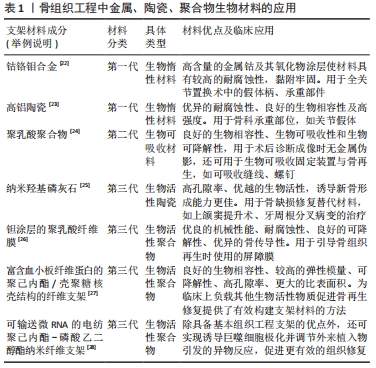
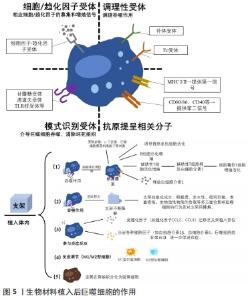
2.3.1 生物支架植入后的巨噬细胞活化 植入物植入体内后,机体免疫系统发挥效能维持机体内环境稳态。免疫反应通常分为2大类:先天免疫和适应性免疫。先天免疫也称非特异性免疫,有物理(如皮肤)和化学屏障(如唾液中的溶酶体和胃酸),以及各类细胞(巨噬细胞、中性粒细胞和树突状细胞)[33]。在非特异性免疫阶段,巨噬细胞可通过Toll样受体识别,激活核因子激活的B细胞的κ-轻链增强或γ-干扰素等启动炎症过程,激活单核/巨噬细胞并招募更多的中性粒细胞和巨噬细胞[34]。随着时间的推移,机体根据外来物(通常称为抗原)被识别的类型不同而发挥特异性免疫,包括体液免疫和细胞免疫。参与特异性免疫反应的主要细胞有B细胞、T细胞、自然杀伤细胞、单核细胞、巨噬细胞、粒细胞(嗜碱性粒细胞、中性粒细胞和嗜酸性粒细胞)、肥大细胞和树突状细胞。抗原进入人体后,首先与巨噬细胞或B细胞接触。巨噬细胞立即包围进入的抗原,将其导入抗原呈递细胞,特别是树突状细胞。随后,辅助性T细胞被这些抗原呈递细胞激活,刺激B细胞和T细胞进行记忆和效应反应[35]。抗原呈递细胞还调节T细胞反应的命运。免疫系统通过细胞间的直接接触和各种细胞因子(如转化生长因子)的分泌调节非自体植入物的炎症反应。其中,巨噬细胞通过分泌细胞因子、趋化因子和生长因子来调节宿主反应,巨噬细胞极化还可以介导下游适应性免疫反应,对组织与外来植入物的整合过程至关重要,具体见图5。"
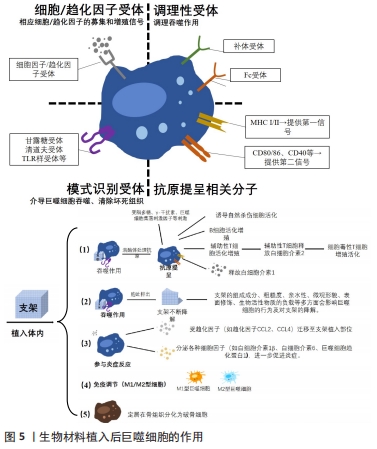
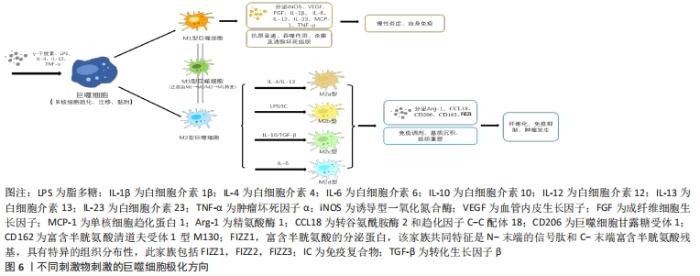
在炎症反应发生的整个周期,巨噬细胞具有高度可塑性[36],可被各种微环境信号激活为不同功能的表型,还可能发生不同表型之间的互相转化。未活化巨噬细胞亚型被视为M0型,有研究表明可能还存在 M3 型巨噬细胞[37],指正处于M1型向M2型或M2型向M1型转化状态的巨噬细胞。目前通常将活化的巨噬细胞分为经典活化M1型巨噬细胞和交替活化M2型巨噬细胞。M2型巨噬细胞又细分为4种亚型[38-39]:M2a ( 由白细胞介素4及白细胞介素13诱导) 、M2b(由脂多糖和免疫复合物共同诱导)、M2c(由白细胞介素10、转化生长因子β或糖皮质激素诱导) 、M2d(由白细胞介素6诱导,与肿瘤相关)。在生物支架植入体内后的炎症早期,M1型巨噬细胞激活后表达高水平的促炎细胞因子[40],如诱导型一氧化氮合酶、血管内皮生长因子、成纤维细胞生长因子、白细胞介素1β、白细胞介素6、白细胞介素12、白细胞介素23、单核细胞趋化蛋白1及肿瘤坏死因子α,负责血管生成和坏死组织的清除。在炎症晚期,M2巨噬细胞激活后表达高水平的精氨酸酶1和抗炎分子,如甘露糖受体、富含半胱氨酸清道夫受体1型M130、Fizz1、转谷氨酰胺酶2和趋化因子C-C配体-18,负责免疫调节、基质沉积和组织重塑[41]。 2.3.2 巨噬细胞对生物支架整合过程的影响 炎症早期会激活M1型巨噬细胞发挥促炎症反应,积极发挥作用抵御外界刺激,然而M1型巨噬细胞的持续表达会导致严重的异物反应以及肉芽肿和纤维包囊的形成,最终导致生物材料整合失败。在炎症后期逐步激活的M2型巨噬细胞所发挥的组织重塑反应十分重要,有助于生物材料的血管化并抑制纤维组织的形成,促进生物材料的整合和性能的稳定发挥,见图6。 "
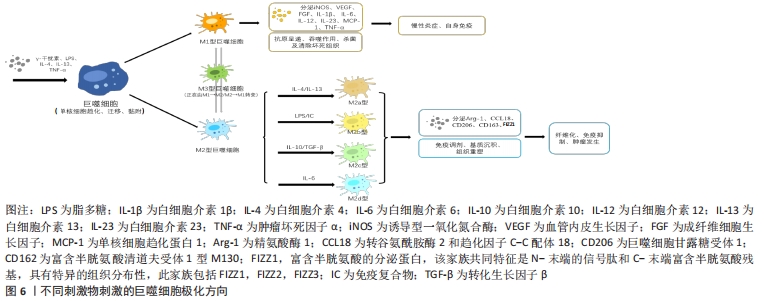

值得注意的是,虽然M1型巨噬细胞过表达在一定程度上影响了支架材料与组织的整合,但它与组织再生相辅相成,发挥着必不可少的作用。单宇华等[42]用3D打印技术制备了β-磷酸三钙支架,使用氯磷酸脂质体去除大鼠牙槽突裂区域的巨噬细胞,结果表明去除巨噬细胞阻碍了新骨的形成,这提示巨噬细胞在骨改建中扮演着重要角色。 此外还需要注意的一点是,运用于骨组织工程的生物支架植入后激发机体的免疫反应,使支架可以与组织成功整合,随后发挥支架的功能性,在这个过程中支架会在体内不断降解直至最终消失,最终新骨完全形成。在支架一边发挥功能性作用,一边降解的过程中,巨噬细胞继续发挥着重要作用。前文提到的多种生物活性材料的降解都与巨噬细胞息息相关,且生物材料的组成成分[43]、微观结构、表面修饰、降解产物等均会影响巨噬细胞对支架的降解作用,并且支架降解时产生的降解产物也会影响巨噬细胞的行为与功能。生物支架在体内降解主要考虑受体内溶解及细胞降解两方面控制[44]。生物陶瓷支架的降解是由细胞介导的主动过程,且材料中钙磷比例、孔隙形状和大小等都会影响破骨细胞样细胞的活性及材料的降解,如碳酸钙/羟基磷灰石/藻酸钠复合材料的凹形孔隙为巨噬细胞源性破骨细胞提供了充足的生长空间,同时支架降解时释放的钙离子及磷酸根离子会被巨噬细胞源性破骨细胞吸收并促进骨髓间充质干细胞分化为成骨细胞,最终导致新骨形成。 天然高分子材料的分子结构多为链状,降解由多种酶的参与发生随机断链和链端切断。如丝素蛋白在体内或体外可通过响应多种蛋白水解酶(例如蛋白酶XIV、α-糜蛋白酶、蛋白酶K、木瓜蛋白酶及胶原酶等)被水解为较小的多肽或形成氨基酸后在体内吸收或代谢,同时植入体内的含丝素蛋白支架的降解还有巨噬细胞及异物巨细胞的吞噬作用及细胞因子的参与,其中丝素蛋白的 β-折叠结构可以增加丝素蛋白对酶的抵抗从而降低降解速率,而具有更高孔隙率的材料有利于细胞渗透和酶的扩散,则加速支架降解速率[45-46]。对于复合支架材料而言,巨噬细胞对支架的降解可概括为两个方面:一方面细胞直接接触材料后吞噬分解支架材料,在细胞的溶酶体内降解;另一方面细胞可分泌多种生物活性分子如生物活性氧、降解酶、细胞因子等),直接与生物材料进行反应达到降解目的。 因此,骨组织工程中的生物支架不仅需要良好的理化性质、机械性能,还希望达到新骨形成与支架降解的平衡,了解支架植入体内后、降解过程中的巨噬细胞的作用是目前学者们关注的热点之一,如何调节巨噬细胞的行为及支架的性能,达到具有良好生物相容性、与新骨形成平衡的可控降解速率的支架是今后需要不断探索的方向。 2.3.3 生物支架对巨噬细胞的影响 骨组织再生依赖于免疫环境稳定有效的发挥作用,二者均受多种信号通路的调节。巨噬细胞的极化受到多种分子及信号通路的调控,包括干扰素调节因子、过氧化物酶体增殖物激活受体γ、非受体型酪氨酸蛋白激酶/信号转导与转录激活因子信号通路、核因子激活的B细胞的κ-轻链增强信号通路、磷脂酰肌醇-3-激酶/蛋白激酶B信号通路、Notch信号通路等。非受体型酪氨酸蛋白激酶/信号转导与转录激活因子信号通路中,信号转导和转录激活因子家族调节着巨噬细胞极化和活性,Toll样受体4激活该通路是巨噬细胞向M1型极化的重要途径。而磷脂酰肌醇-3-激酶/蛋白激酶B信号通路的激活是巨噬细胞中Toll样受体和核因子激活的B细胞的κ-轻链增强信号的负调节因子,该通路的激活有利于激活白细胞介素4诱导的M2型巨噬细胞的激活。 值得注意的是,破骨细胞是骨髓中的髓系祖细胞分化而成的单核巨噬细胞相互融合,所形成的多核巨细胞。所以,支架植入后、降解过程中及发挥功能时对巨噬细胞的刺激都会影响新骨的形成。有研究已证实核因子激活的B细胞的κ-轻链增强受体活化因子配体/核因子激活的B细胞的κ-轻链增强受体活化因子/骨保护素信号轴是免疫系统和骨骼系统共享的信号轴[47],同时影响免疫反应和新骨形成。破骨细胞的形成和功能受到巨噬细胞集落刺激因子和核因子激活的B细胞的κ-轻链增强受体活化因子配体的严格调控。巨噬细胞集落刺激因子通过刺激破骨细胞前体核因子激活的B细胞的κ-轻链增强受体活化因子的表达,促进破骨细胞分化。核转录因子κB受体活化因子配体结合破骨细胞前体和成熟成骨细胞上的核因子ΚB受体活化因子,导致包括肿瘤坏死因子受体相关因子6在内的转接/衔接分子的募集。肿瘤坏死因子受体相关因子6可以激活多种下游信号通路,如核因子激活的B细胞的κ-轻链增强、应激活化蛋白激酶、细胞外信号调节激酶、p38、活化蛋白1转录因子家族、非受体型酪氨酸蛋白激酶/信号转导与转录激活因子、活化T细胞核因子c1,启动破骨细胞的形成和活化[48]。FoxO转录因子家族是非受体型酪氨酸蛋白激酶/信号转导与转录激活因子通路的下游信号分子,FoxO1是氧化还原平衡的主要调节因子,可刺激成骨细胞的增殖和分化,抑制成骨细胞的凋亡。 此外,存在于人体内的miRNA是一类非蛋白质编码小分子单链RNA,在转录及转录后水平发挥调控基因表达的功能,miRNAs与巨噬细胞极化、吞噬活性、肿瘤增殖、炎症激活和代谢稳态等相关。有研究证明miR-142-5p通过磷脂酶和张力蛋白同源物/磷脂酰肌醇激酶/蛋白激酶B/FoxO1信号通路参与骨髓源性巨噬细胞破骨细胞分化的过程[49]。miR-7基因敲减后[50],通过核因子激活的B细胞的κ-轻链增强等信号途径调控,炎性因子白细胞介素1β、白细胞介素6和肿瘤坏死因子ɑ的表达显著升高,巨噬细胞的炎症反应显著增强。 生物材料作为异物植入体内引发机体的炎症反应可分为急性期和慢性期。早期急性炎症会募集嗜中性粒细胞从血流中至损伤部位,血液中的非特异性蛋白质自发黏附于植入物表面,通过细胞表面受体介导细胞相互作用和黏附,这是细胞迁移、炎症和免疫应答的起点。围绕植入物周围形成临时基质,基质中的溶栓剂和血小板释放血小板衍生生长因子、转化生长因子β、白细胞介素和趋化因子,其中趋化因子(如趋化因子配体2)会刺激材料植入部位的巨噬细胞募集和激活。活化的巨噬细胞分泌额外的趋化因子,炎症信号通路会被激活。在这一过程中,蛋白质吸附影响着植入物与组织的相互作用,所以生物植入材料的亲疏水性、表面结构、对蛋白质吸附能力等都是需要考虑的因素。 组织受损部位的巨噬细胞被激活后,持续的急性炎症将导致巨噬细胞融合形成异物巨细胞,以单核-巨噬细胞及淋巴细胞的存在为特征,血管开始增生、结缔组织逐渐形成,在材料植入部位逐步转变为慢性炎性反应, 这一过程可以在植入物的整个生物周期内持续存在。在上述过程中,各种免疫细胞(如巨噬细胞、中性粒细胞及淋巴细胞)处于活跃状态,通过吞噬作用清除体内异物,而无法被细胞吞噬的较大异物会激活“吞噬受阻”,刺激免疫细胞释放化学物质(如炎性因子)并黏附于植入物上,通过这些炎性因子分解较大的异物,达到组织修复的目的。同时,机体又会调节免疫细胞的分泌活动使其在发挥炎症反应的同时不影响组织修复与再生[51]。上述由于外来植入物引发的宿主炎症反应对组织愈合、再生、材料整合等至关重要,这种炎性反应的严重程度及炎症进展受植入物的性质影响,目前研究发现生物材料的化学及物理性能会影响巨噬细胞极化方向。 影响免疫反应的一种策略是支架材料的物理性能,例如材料的硬度,表面几何形状及微观结构等。研究表明,植入物表面的蛋白质吸附和细胞黏附受三维表面形貌的影响,相比平面型支架表面而言,具有纳米纤维结构的、模拟天然细胞外基质结构的电纺支架表面可有效减少巨噬细胞的激活和异物巨细胞的形成[52]。ZHENG等[54]通过调节支架表面形貌实现了巨噬细胞表型的顺序调节,近红外辐射后支架表面形貌从平坦变为微沟槽的转变有效诱导了巨噬细胞从圆形转变为细长,从而导致表型从诱导型一氧化氮合酶阳性及白细胞介素10低表达的巨噬细胞转变为精氨酸酶1阳性及白细胞介素10高表达的巨噬细胞,实现了大量炎性细胞的早期浸润以及在适当的时间点从促炎表型向抗炎表型的转变。通过材料形貌改变对巨噬细胞表型进行调控的过程考虑是通过激活Rho激酶2和Rac相关的C3肉毒素底物1,Rho激酶2调节细胞黏附,Rac相关的C3肉毒素底物 1参与细胞迁移和细胞骨架的构建。通过改变纳米生物材料的表面粗糙度也可以调节局部骨免疫反应,光滑的矿化胶原表面促进了巨噬细胞向M2型极化[55]。张吉昊等[56]利用静电纺丝技术制备了具有电活性的聚偏氟乙烯-三氟乙烯共聚物取向纳米纤维膜,通过电晕极化仪极化,相比未极化无方向的电纺膜对照组,取向极化组和取向未极化组的结果显示出更好的软组织愈合,取向极化组在炎性反应晚期巨噬细胞M1型标志基因CCR7表达显著被抑制,M2型标志基因CD206表达显著高于对照组。 此外,TYLEK等[57]制造了不同几何形状(三角形、盒形、圆形及无序层)的3D多孔聚己内酯纤维支架,结果显示,盒形支架组中巨噬细胞M2型特异性表面标记物CD163上调至所有支架组中的最高水平,M1型标记物(白细胞介素1β及白细胞介素8)被下调至所有支架组中的最低水平,证实支架的几何结构会影响巨噬细胞向M2型极化。随后,该研究者重点研究了在盒形支架组中支架孔径变化对巨噬细胞极化的影响,结果显示40 μm孔径的盒形3D支架上白细胞介素10等抗炎因子释放量最高,炎症初期促炎因子白细胞介素1β、白细胞介素6和白细胞介素8等分泌降低,考虑可能是由于小孔径3D支架有助于细胞在植入物中迁移并形成细长的巨噬细胞,而细胞的这种形态变化增加了巨噬细胞向M2型分化的比例。 影响免疫反应的另一策略是对支架材料进行表面改性,可防止M1型巨噬细胞极化或者促进M2型巨噬细胞极化。生物材料植入的早期会引起局部的蛋白质吸附和临时基质的形成,巨噬细胞与植入物的黏附是由被吸附的细胞外基质蛋白与巨噬细胞上表达的相关细胞表面受体(包括整合素、选择素、多配体蛋白聚糖和CD44)之间的相互作用介导的[58]。 通过调节材料表面亲疏水性,可以防止非特异性蛋白质吸附和不必要的细胞黏附。与疏水性材料表面相比,高亲水性的材料表面可以更好地调节辅助性T细胞和巨噬细胞的募集,促进巨噬细胞向M2型极化并减少白细胞介素类促炎因子的分泌。有学者们通过湿法纺丝将聚乳酸-羟基乙酸共聚物制成宽度可调节的微米级条带状支架[59],并在支架表面涂覆纤维蛋白原,通过模拟体内纤维蛋白原-凝血酶反应的交联机制来启动支架的交联,从而增强了支架的生物相容性、水溶性和可注射性,通过形成的生物相容性表层改善了植入物与宿主的相互作用,从而增强支架的功能性。同时当支架与凝血酶混合时,纤维蛋白原包覆的聚乳酸-羟基乙酸共聚物支架可以被交联成三维结构的支架,并实现了支架可控化的交联性、可注射性、可封装细胞及三维多孔等特性。并且,这种三维多孔支架可以引起巨噬细胞的活化及M1型向M2型的转变达到巨噬细胞数量的动态变化与骨形成及血管化的过程相协调[60]。 此外,将植入材料进行表面处理也可以达到改变材料表面润湿性的目的。如钛表面通过常压等离子体的修饰显著增强了其表面的润湿性[61],同时保持了钛本身的拓扑结构和亲水表面没有改变,常压等离子体修饰的钛与人单核细胞白血病来源的巨噬细胞及人骨髓间充质干细胞共培养,结果显示处理过的钛支架可增加细胞迁移和成骨标志物的基因表达,有效促进了巨噬细胞向M2型极化,在此过程中考虑是纤溶酶原激活物抑制剂1在人骨髓间充质干细胞向成骨细胞分化中起关键作用,重组人黏结蛋白聚糖2调节成骨细胞黏附、肌动蛋白细胞骨架形成及Runx2的表达。支架性能对巨噬细胞极化的影响概括见表2。 "


微粒药物输送系统是一种递送药物、酶、细胞和疫苗等的有效途径之一[67]。研究表明,即使没有药物负载,微球也能刺激天然免疫细胞,激活抗原呈递和触发免疫反应。利用微球对免疫细胞的作用特点,开发一类对巨噬细胞具有靶向性的药物输送系统,实现对炎症反应的调节是学者们研究的方向之一。海藻酸钠中存在Toll样受体2和Toll样受体4的特异性配体,巨噬细胞表面受体如Toll样受体通过识别细菌表面的脂多糖,激活巨噬细胞极化的信号通路,诱导M1型巨噬细胞的表达,在这个过程中利用Toll样受体与Toll样受体配体的结合,实现药物运输系统对巨噬细胞的靶向性递送[68]。ZHANG等[69]通过负载白细胞介素4的水凝胶微球修复大面积颌骨缺损,结果显示白细胞介素4激活的巨噬细胞可高表达精氨酸酶1,提高巨噬细胞增殖能力并抑制其凋亡,促进M2巨噬细胞极化,抑制炎症的发生发展,激活骨髓间充质干细胞中的转化生长因子β1/Smad信号通路,有效促进新骨形成。陈芳浩等[71]在钛种植体表面构建了一种负载了地塞米松的DNA-壳聚糖水凝胶,这种水凝胶能促进巨噬细胞增殖并诱导其M2型极化。 "

| [1] YIN S, ZHANG W, ZHANG Z, et al. Recent advances in scaffold design and material for vascularized tissue-engineered bone regeneration. Adv Healthc Mater. 2019;8(10):e1801433. [2] VILA-PARRONDO C, GARCÍA-ASTRAIN C, LIZ-MARZÁN LM. Colloidal systems toward 3D cell culture scaffolds. Adv Colloid Interface Sci. 2020;283:102237. [3] PIANTANIDA E, ALONCI G, BERTUCCI A, et al. Design of Nanocomposite Injectable Hydrogels for Minimally Invasive Surgery. Acc Chem Res. 2019;52(8):2101-2112. [4] LI J, LI Y, GAO B, et al. Engineering mechanical microenvironment of macrophage and its biomedical applications. Nanomedicine (Lond). 2018;13(5):555-576. [5] ARRON JR, CHOI Y. Bone versus immune system. Nature. 2000;408 (6812):535-536. [6] YU Y, WU RX, YIN Y, et al. Directing immunomodulation using biomaterials for endogenous regeneration. J Mater Chem B. 2016; 4(4):569-584. [7] MILLS CD, KINCAID K, ALT JM, et al. M-1/M-2 macrophages and the Th1/Th2 paradigm. J Immunol. 2000;164(12):6166-6173. [8] SHANLEY LC, MAHON OR, KELLY DJ, et al. Harnessing the innate and adaptive immune system for tissue repair and regeneration:Considering more than macrophages. Acta Biomater. 2021;133:208-221. [9] BRÅNEMARK PI, HANSSON BO, ADELL R, et al. Osseointegrated implants in the treatment of the edentulous jaw. Experience from a 10-year period. Scand J Plast Reconstr Surg Suppl. 1977;16:1-132. [10] HENCH LL, POLAK JM. Third-generation biomedical materials. Science. 2002;295(5557):1014-1017. [11] NAVARRO M, MICHIARDI A, CASTAÑO O, et al. Biomaterials in orthopaedics. J R Soc Interface. 2008;5(27):1137-1158. [12] PENG Z, ZHAO T, ZHOU Y, et al. Bone tissue engineering via carbon-based nanomaterials. Adv Healthc Mater. 2020;9(5):e1901495. [13] WEI F, XIAO Y. Modulation of the Osteoimmune Environment in the Development of Biomaterials for Osteogenesis. Adv Exp Med Biol. 2018;1077:69-86. [14] 魏诗敏,汪媛婧,黄雯,等.异物反应中巨噬细胞调控在骨组织修复中的研究进展[J].口腔疾病防治,2019,27(9):591-597. [15] CHOCHOLATA P, KULDA V, BABUSKA V. Fabrication of scaffolds for bone-tissue regeneration. Materials (Basel). 2019;12(4):568. [16] BARBA A, DIEZ-ESCUDERO A, MAAZOUZ Y, et al. Osteoinduction by foamed and 3D-printed calcium phosphate scaffolds: effect of nanostructure and pore architecture. ACS Appl Mater Interface. 2017; 9(48):41722-41736. [17] DASILVABRUM I, DECARVALHO JJ, DASILVAPIRES JL, et al. Nanosized hydroxyapatite and β-tricalcium phosphate composite: physico-chemical, cytotoxicity, morphological properties and in vivo trial. Sci Rep. 2019;9(18):77-116. [18] MA L, CHENG S, JI X, et al. Immobilizing magnesium ions on 3D printed porous tantalum scaffolds with polydopamine for improved vascularization and osteogenesis. Mater Sci Eng C Mater Biol Appl. 2020;117:111303. [19] UNAL S, ARSLAN S, YILMAZ BK, et al. Polycaprolactone/gelatin/hyaluronic acid electrospun scaffolds to mimic glioblastoma extracellular matrix. Materials (Basel). 2020;13(11):2661. [20] LI Y, CHEN M, ZHOU W, et al. Cell-free 3D wet-electrospun PCL/silk fibroin/Sr2+ scaffold promotes successful total meniscus regeneration in a rabbit model. Acta Biomater. 2020;113(8):196-209. [21] KIROS S, LIN S, XING M, et al. Embryonic mesenchymal multipotent cell differentiation on electrospun biodegradable poly (ester amide) scaffolds for model vascular tissue fabrication. Ann Biomed Eng. 2020; 48(3):980-991. [22] WALKER PS, GOLD BL. The tribology (friction, lubrication and wear) of all-metal artificial hip joints. 1971. Clin Orthop Relat Res. 1996;(329 Suppl):S4-S10. [23] CHRISTEL P, MEUNIER A, DORLOT JM, et al. Biomechanical compatibility and design of ceramic implants for orthopedic surgery. Ann N Y Acad Sci. 1988;523:234-256. [24] MIDDLETON JC, TIPTON AJ. Synthetic biodegradable polymers as orthopedic devices. Biomaterials. 2000;21(23):2335-2346. [25] YANG X, LI Y, HE W, et al. Hydroxyapatite/collagen coating on PLGA electrospun fibers for osteogenic differentiation of bone marrow mesenchymal stem cells. J Biomed Mater Res A. 2018;106(11):2863-2870. [26] HWANG C, PARK S, KANG IG, et al. Tantalum-coated polylactic acid fibrous membranes for guided bone regeneration. Mater Sci Eng C Mater Biol Appl. 2020;115:111112. [27] RASTEGAR A, MAHMOODI M, MIRJALILI M, et al. Platelet-rich fibrin-loaded PCL/chitosan core-shell fibers scaffold for enhanced osteogenic differentiation of mesenchymal stem cells. Carbohydr Polym. 2021;269: 118351. [28] LIN J, MOHAMED I, LIN PH, et al. Modulating Macrophage Phenotype by Sustained MicroRNA Delivery Improves Host-Implant Integration. Adv Healthc Mater. 2020;9(3):e1901257. [29] DING T, KANG W, LI J, et al. An in situ tissue engineering scaffold with growth factors combining angiogenesis and osteo immunomodulatory functions for advanced periodontal bone regeneration. J Nanobiotechnol. 2021;19(1):247. [30] ZHU Z, LIU Y, XUE Y, et al. Tazarotene released from aligned electrospun membrane facilitates cutaneous wound healing by promoting angiogenesis. ACS Appl Mater Interfaces. 2019;11(39):36141-36153. [31] QIAN J, LIN Z, LIU Y, et al. Functionalization strategies of electrospun nanofibrous scaffolds for nerve tissue engineering. Smart Mater Med. 2021;2:260-279. [32] ZHANG Q, BOSCH-RUÉ È, PÉREZ RA, et al. Biofabrication of tissue engineering vascular systems. APL Bioeng. 2021;5(2):021507. [33] NOUR S, BAHEIRAEI N, IMANI R, et al. Bioactive materials: a comprehensive review on interactions with biological microenvironment based on the immune response. J Bionic Eng. 2019;16(4):563-581. [34] CORSI F, CAROTENUTO F, DI NARDO P, et al. Harnessing inorganic nanoparticles to direct macrophage polarization for skeletal muscle regeneration. Nanomaterials (Basel). 2020;10(10):1963. [35] NIU Y, WANG Z, SHI Y, et al. Modulating macrophage activities to promote endogenous bone regeneration: biological mechanisms and engineering approaches. Bioact Mater. 2020;6(1):244-261. [36] GOODMAN SB, PAJARINEN J, YAO Z,et al. Inflammation and bone repair: from particle disease to tissue regeneration. Front Bioeng Biotechnol. 2019;7:230. [37] LAVIN Y, WINTER D, Blecher-Gonen R, et al. Tissue-resident macrophage enhancer landscapes are shaped by the local microenvironment. Cell. 2014;159(6):1312-1326. [38] 张艺,张晓梦,史俊宇,等.巨噬细胞极化在种植体周围组织愈合的作用及研究进展[J].口腔医学,2020,40(7):644-647. [39] 梁蓓蕾,王佐林.巨噬细胞极化与骨组织再生关系的研究进展[J].口腔颌面外科杂志,2020,30(3):187-190. [40] GAO X, WANG YS, LI XQ, et al. Macrophages promote vasculogenesis of retinal neo vascularization in an oxygen-induced retinopathy model in mice. Cell Tissue Res. 2016;364(3):599-610. [41] TANG H, HUSCH JFA, ZHANG Y, et al. Coculture with monocytes/macrophages modulates osteogenic differentiation of adipose‐derived mesenchymal stromal cells on poly (lactic‐co‐glycolic) acid/polycaprolactone scaffolds. J Tissue Eng Regen Med. 2019;13(5):785-798. [42] 单宇华,应惜裕,张晓宇,等.巨噬细胞在β-TCP支架修复牙槽突裂中成骨作用的探讨[J].口腔颌面外科杂志,2021,19(4):315-319. [43] ZHANG YQ, YU W, BA ZY, et al. 3D-printed scaffolds of mesoporous bioglass/gliadin/polycaprolactone ternary composite for enhancement of compressive strength, degradability, cell responses and new bone tissue ingrowth. Int J Nanomed. 2018;13:5433-5447. [44] 焦鑫,王栋梁,干耀恺.骨生物材料通过细胞途径降解的研究进展[J].生物工程学报,2020,36(2):201-209. [45] ZHONG QW, LI WH, SU XP, et al. Degradation pattern of porous CaCO3 and hydroxyapatite microspheres in vitro and in vivo for potential application in bone tissue engineering. Colloids Surf B Biointerfaces. 2016;143:56–63. [46] GUO C, LI C, KAPLAN DL. Enzymatic degradation of bombyx mori silk materials: a review. Biomacromolecules. 2020;21(5):1678-1686. [47] 陈泽涛,林义雄,杨杰婷,等.基于“免疫微环境调控”的屏障膜研发理念[J].口腔疾病防治,2021,29(8):505-514. [48] KO Y, LEE G, KIM B, et al. Modification of the RANKL-RANK-binding site for the immunotherapeutic treatment of osteoporosis. Osteoporos Int. 2020;31(5):983–993. [49] LOU ZK, PENG Z, WANG B. et al. miR-142-5p promotes the osteoclast differentiation of bone marrow-derived macrophages via PTEN/PI3K/AKT/FoxO1 pathway. J Bone Miner Metab. 2019;37(5):815-824. [50] 陈慧子,郭萌萌,赵娟娟,等.miR-7基因敲减对LPS诱导巨噬细胞炎症反应的影响[J].现代免疫学,2019,39(3):195-200, 216. [51] ZHOU P, XIA D, NI Z, et al. Calcium silicate bioactive ceramics induce osteogenesis through oncostatin M. Bioact Mater. 2020;6(3):810-822. [52] LAMICHHANE S, ANDERSON JA, VIERHOUT T, et al. Polytetrafluoroethylene topographies determine the adhesion, activation, and foreign body giant cell formation of macrophages. J Biomed Mater Res A. 2017;105(9):2441-2450. [53] WANG YL, ZHANG YF, SCULEAN AS, et al. Macrophage behavior and interplay with gingival fibroblasts cultured on six commercially available titanium, zirconium, and titanium-zirconium dental implants. Clin Oral Investig. 2019;23(8):3219-3227. [54] ZHENG X, XIN L, LUO Y, et al. Near-infrared-triggered dynamic surface topography for sequential modulation of macrophage phenotypes. ACS Appl Mater Interfaces. 2019;11(46):43689-43697. [55] LI J, ZHANG YJ, LV ZY, et al. The observed difference of macrophage phenotype on different surface roughness of mineralized collagen. Regen Biomater. 2020;7(2):203-211. [56] 张吉昊,白云洋,皇文进.电活性P(VDF-TrFE)取向纳米纤维调控巨噬细胞功能促进软组织愈合[J].临床口腔医学杂志,2021,37(8):451-455. [57] TYLEK T, BLUM C, HRYNEVICH A, et al. Precisely defined fiber scaffolds with 40μm porosity induce elongation driven M2-like polarization of human macrophages. Biofabrication. 2020;12(2):025007. [58] KIM YK, CHEN EY, LIU WF. Biomolecular strategies to modulate the macrophage response to implanted materials. J Mater Chem B. 2016; 4(9):1600-1609. [59] BARATI D, WATKINS K, WANG Z, et al. Injectable and crosslinkable PLGA‐based microribbons as 3D macroporous stem cell niche. Small. 2020;16(22):1905820. [60] TANG Y, TONG X, CONRAD B, et al. Injectable and in situ crosslinkable gelatin microribbon hydrogels for stem cell delivery and bone regenerationin vivo. Theranostics. 2020;10(13):6035-6047. [61] TOYAMA N, TSUCHIYA S, KAMIO H, et al. The effect of macrophages on an atmospheric pressure plasma-treated titanium membrane with bone marrow stem cells in a model of guided bone regeneration. J Mater Sci Mater Med. 2020;31(8):70. [62] PASCUAL-GIL S, ABIZANDA G, IGLESIAS E, et al. NRG1 PLGA MP locally induce macrophage polarisation toward a regenerative phenotype in the heart after acute myocardial infarction. J Drug Target. 2019; 27(5/6):573-581. [63] ALHAMDI JR, PENG T, AL-NAGGAR IM, et al. Controlled M1-to-M2 transition of aged macrophages by calcium phosphate coatings. Biomaterials. 2019;196:90-99. [64] RIBEIRO JS, DAGHRERY A, DUBEY N, et al. Hybrid antimicrobial hydrogel as injectable therapeutics for oral infection ablation. Biomacromolecules. 2020;21(9):3945-3956. [65] INOUE M, MATSUMOTO C, NAKAJIMA K, et al. Alendronate/dexamethasone combination therapy worsens soft and hard tissue wound healing around implants in rat maxillae. Bone. 2021;148:115942. [66] 李莉,卓瑾,郑玲,等.不同诱导极化方式对大鼠骨髓来源巨噬细胞增殖、凋亡及吞噬能力的影响[J].中国组织工程研究,2021, 25(25):4032-4037. [67] VAGHASIYA K, ERAM A, SHARMA A, et al. Alginate microspheres elicit innate M1-inflammatory response in macrophages leading to bacillary killing. AAPS Pharm Sci Tech. 2019;20(6):241. [68] MORAIS AÍS, VIEIRA EG, AFEWERKI S, et al. Fabrication of polymeric microparticles by electrospray: the impact of experimental parameters. J Funct Biomater. 2020;11(1):4. [69] ZHANG J, SHI H, ZHANG N, et al. Interleukin-4-loaded hydrogel scaffold regulates macrophages polarization to promote bone mesenchymal stem cells osteogenic differentiation via TGF-β1/Smad pathway for repair of bone defect. Cell Prolif. 2020;53(10):e12907. [70] SUN X, MA Z, ZHAO X, et al. Three-dimensional bioprinting of multicell-laden scaffolds containing bone morphogenic protein-4 for promoting M2 macrophage polarization and accelerating bone defect repair in diabetes mellitus. Bioact Mater. 2020;6(3):757-769. [71] 陈芳浩,何奕德,李哲,等.钛种植体表面新型DNA水凝胶递送地塞米松诱导巨噬细胞M2极化的研究[J].实用口腔医学杂志,2021, 37(2):192-196. [72] MURRAY PJ. Macrophage polarization. Annu Rev Physiol. 2017;79:541-566. [73] QIU P, LI M, CHEN K, et al. Periosteal matrix-derived hydrogel promotes bone repair through an early immune regulation coupled with enhanced angio- and osteogenesis. Biomaterials. 2020;227:119552. [74] WANG Y, YAO D, LI L, et al. Effect of electrospun silk fibroin–silk sericin films on macrophage polarization and vascularization. ACS Biomater Sci Eng. 2020;6(6):3502-3512. [75] MOORE EM, WEST JL. Harnessing macrophages for vascularization in tissue engineering. Ann Biomed Eng. 2019;47(2):354-365. [76] JULIER Z, PARK AJ, BRIQUEZ PS, et al. Promoting tissue regeneration by modulating the immune system. Acta Biomater. 2017;53:13-28. |
| [1] | Sun Kexin, Zeng Jinshi, Li Jia, Jiang Haiyue, Liu Xia. Mechanical stimulation enhances matrix formation of three-dimensional bioprinted cartilage constructs [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-7. |
| [2] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [3] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [4] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| [5] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [6] | Xu Yan, Li Ping, Lai Chunhua, Zhu Peijun, Yang Shuo, Xu Shulan. Piezoelectric materials for vascularized bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1126-1132. |
| [7] | Li Wenjie, You Aijia, Zhou Junli, Fang Sujuan, Li Chun. Effects of different dressings in the treatment of burn wounds: a network meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1141-1148. |
| [8] | Zong Mingrui, Liu Haiyan, Li Bing, Wu Xiuping. Application of carboxymethyl chitosan in tissue engineering of stomatology [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 447-452. |
| [9] | Zhang Lichen, Chen Liang, Gu Yong. Inorganic ion bionic periosteum regulates immune microenvironment to promote bone repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 346-353. |
| [10] | Dai Xianglin, Zhang Wenfeng, Yao Xijun, Shang Jiaqi, Huang Qiujin, Ren Yifan, Deng Jiupeng. Barium titanate/polylactic acid piezoelectric composite film affects adhesion, proliferation, and osteogenic differentiation of MC3T3-E1 cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 367-373. |
| [11] | Wu Lihao, Shao Anliang, Xu Lin, Ren Kang, Wang Hongjian, Chen Liang, Xu Ling. Evaluation of immunotoxicity of the absorbable macroporous polysaccharides composite hemostatic material [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 329-334. |
| [12] | Ning Ziwen, Wang Xu, Shi Zhengliang, Qin Yihua, Wang Guoliang, Jia Di, Wang Yang, Li Yanlin. Meniscal injury repair methods for non-blood supply area [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 420-426. |
| [13] | Chen Feng, Ren Guowu, Zhang Xiaoyun, Chen Yueping, Shi Rusheng. Receptor activator of nuclear factor-kappa B ligand signal transduction mechanism and osteoclast activation [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(2): 293-299. |
| [14] | Zhang Jie, Tian Ai. Advances in the signaling pathway of M2 macrophages involved in bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(2): 314-321. |
| [15] | Zhang Weiye, Zhan Jiawen, Zhu Liguo, Wang Shangquan, Chen Ming, Wei Xu, Feng Minshan, Yu Jie, Han Tao, Cai Chuhao, Zhou Shuaiqi, Shao Chenchen. Effect of nucleus pulposus cells-derived exosomes under cyclic mechanical tension on endplate chondrocytes [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(2): 223-229. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||