Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (7): 1110-1116.doi: 10.12307/2023.020
Previous Articles Next Articles
Early thrombosis and prevention of small-diameter blood vessel prosthesis
Shi Yehong, Wang Cheng, Chen Shijiu
- The Fifth Affiliated (Zhuhai) Hospital of Zunyi Medical University, Zhuhai 519100, Guangdong Province, China
-
Received:2021-11-18Accepted:2022-01-13Online:2023-03-08Published:2022-07-20 -
Contact:Chen Shijiu, Chief physician, The Fifth Affiliated (Zhuhai) Hospital of Zunyi Medical University, Zhuhai 519100, Guangdong Province, China -
About author:Shi Yehong, Master, The Fifth Affiliated (Zhuhai) Hospital of Zunyi Medical University, Zhuhai 519100, Guangdong Province, China -
Supported by:National Natural Science Foundation of China, No. 81960842 (to WC)
CLC Number:
Cite this article
Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
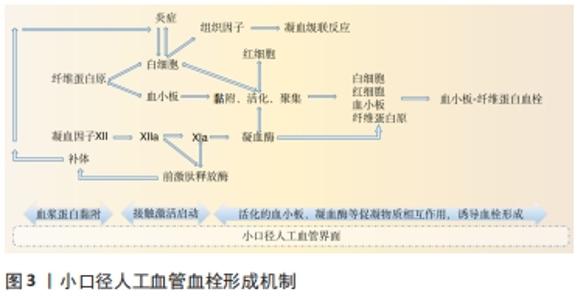
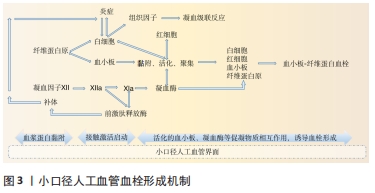
2.1 小口径人工血管血栓形成的机制 血管移植后30 d内通畅率降低通常由急性血栓形成引起,小口径人工血管与自体血管、同种异体血管血栓形成的机制存在共通之处:其一,此类血管灌注压低,血流速度缓慢,血栓形成相关因子的接触时间延长、浓度相对升高,较中、大口径血管更容易形成血栓;其二,当移植血管与重建部位血管的口径、吻合角度及顺应性不匹配时,将造成局部血流速度的空间变化率增大,引发血小板边缘效应,导致该区域血栓形成风险增加[2],小口径人工血较差的顺应性也是术后更容易形成血栓的原因之一;其三,手术医师及患者的主观或客观因素同样可能导致术后早期血栓的形成。首先,血管手术是一个外源性促凝血事件,术者的显微吻合技术、手术时机的判断、移植物的选择均可能使小口径血管移植早期形成血栓;其次,患者自身是否存在导致血液黏稠、血小板聚集程度增高的危险因素,如抽烟、高脂血症、糖尿病、脱水等。此外,当移植血管涉及关节部分时则可能因压迫、扭曲而造成血流速度减慢最终导致血栓形成[3] 区别于自体血管,同种异体血管血栓早期形成的机制主要是机械操作造成内皮损伤和与非自身Ⅰ类和Ⅱ类MHC分子发生的急性免疫排斥反应。小口径人工血管不仅缺乏能够分泌抗血栓因子的内皮细胞作为天然抗凝屏障,而且与血浆蛋白的吸附能力密切相关,见图3。当血液流经时,血浆蛋白质率先吸附至人工血管表面,吸附的纤维蛋白原通过与血小板受体相互作用共同促进二者之间的黏附,同时白细胞通过CD11b/CD18 与纤维蛋白原黏附参与血小板的活化[4]。此外,红细胞被动黏附并释放二磷酸腺苷,激活血小板。激活状态的血小板释放血栓烷A2、二磷酸腺苷和其他激动剂,继续放大血小板的黏附、活化、聚集[5]。吸附的凝血因子Ⅻ自激活为凝血酶活化因子Ⅻa,启动接触激活系统,加速凝血酶的形成[6]。凝血酶与血小板相互刺激的同时,还使可溶性纤维蛋白原变成不可溶的纤维蛋白,形成稳定的血小板-纤维蛋白血栓[7]。接触激活系统中凝血因子Ⅻ与前激肽释放酶形成正反馈,活化的前激肽释放酶将触发补体系统激活,增强对单核细胞和白细胞的吸附,促进组织因子的释放,进一步激活凝血级联反应。 "
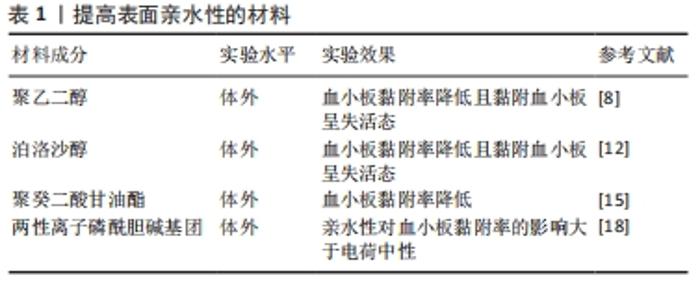
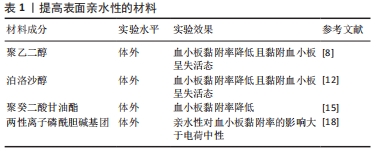
2.2.1 提高小口径人工血管表面亲水性 聚乙二醇:亲水性聚乙二醇作为生物惰性大分子,没有免疫原性,能够紧密结合水分子形成表面水合层,避免蛋白质构象的改变,减少纤维蛋白原等血浆蛋白的吸附,并且可以保持蛋白质的天然特性。由于这些独特的性质,聚乙二醇经常被用来改善生物材料的血液相容性[1]。DIMITRIEVSKA等[8] 用聚乙烯胺作为交联剂将不同浓度聚乙二醇接枝到聚对苯二甲酸乙酯骨架表面进行对照,发现10%聚乙二醇干预组血小板黏附个数为3 900/mm2,是牛胶原涤纶包被组的1/7,黏附的血小板呈圆形或盘状失活态。DAI等[9]在阿加曲班固定的薄膜中加入聚乙二醇发现血小板黏附和激活受到抑制,凝血时间得以延长,凝血酶的产生和补充激活减少。然而,随着聚乙二醇在食品、药品中的应用增多,美国健康献血者的血浆中检测到了高流行率的抗聚乙二醇IgM和IgG抗体,2021年SELLATURAY等[10]报道的5例聚乙二醇过敏患者中1例患者发生严重不良反应导致心脏骤停。因此,含有聚乙二醇成分的人工血管能否安全应用于临床,还需要大量实验来研究证实。 泊洛沙姆(poloxamer):由尾端2个亲水性聚乙二醇单元和1个疏水性聚丙二醇单元组成,呈线性三嵌段结构(PEGx-PPGy-PEGx)。利用聚丙二醇疏水段在骨架上锚定,以达到亲水侧链迁移到表面抑制蛋白质吸附和血小板黏附的目的[11]。LE等[12]将泊洛沙姆共混入聚氨酯/聚己内酯电纺接枝中发现泊洛沙姆浓度每增加1%,血小板黏附率下降10%以上。泊洛沙姆的质量分数大于8%时,超过70%的血小板被排斥出内表面。与此同时,黏附的血小板大多数呈失活状态。据报道,在培养液中使用泊洛沙姆可以提高结肠癌Caco-2细胞的活力和增殖能力[13]。PAZHANIMALA等[14]将泊洛沙姆引入聚己内酯/明胶共混支架中发现随着泊洛沙姆含量的增高,细胞增殖率下降,以80∶10∶10配比的聚己内酯/明胶/泊洛沙姆支架中Caco-2细胞增殖率最高。但目前还没有研究证明泊洛沙姆含量和培养时间对内皮细胞增殖的影响。 聚癸二酸甘油酯:聚癸二酸甘油酯主链上的羟基使其具有良好亲水性。MOTLAGH等[15]报道,聚癸二酸甘油酯上附着的血小板数量大约是聚四氟乙烯上附着血小板数量的1/2,这可能是由于聚癸二酸甘油酯提供的亲水性表面限制了血浆蛋白的吸附。癸二酸及甘油均是体内代谢产物,因而具有较好的生物相容性,但相对较快的降解速度限制了其在组织工程中的应用潜力。ZARGAR KHARAZI等[16]采用静电纺丝技术分别在内层和外层制备了由聚癸二酸甘油酯/聚己内酯纳米纤维和聚己内酯纳米纤维组成的双层管状支架,结果表明聚癸二酸甘油酯/聚己内酯双层纳米纤维支架与聚四氟乙烯抑制血小板黏附的能力无统计学差异,28 d后的质量丢失较单层电纺聚癸二酸甘油酯/聚己内酯下降8%,降解程度得以延缓,聚癸二酸甘油酯与聚己内酯的组合尽管平衡了材料的亲疏水性与降解速率,但仍未达到支架材料12-24个月内降解的合理降解率。 两性聚合物:两性聚合物在同一条链上同时具有阳离子和阴离子基团,而总电荷保持中性,是一种亲水性很强的物质。两性离子甜菜碱通过静电和氢键诱导周围水化与其头部基团形成结构化的水界面,从而减少蛋白质吸附和血小板黏附,有效地控制凝血级联反应[17]。两性离子磷酰胆碱基团通过柔性聚乙二醇链作为间隔物共价连接到聚碳酸酯型聚氨酯表面,组装后的磷酰胆碱基团形成特殊的仿生表面,除了氢键作用外,还能通过结合的水层抵抗生物大分子的非特异性吸附[18]。 小口径人工血管表面亲水性的提高可以改善血液相容性,并从抗非特异性蛋白吸附中获益,见表1。应注意的是,小口径人工血管作为永久性的人体植入物,要求它们在整个使用周期内保持高度的血液相容性,而高亲水性表面也可能会限制内皮细胞的黏附与增殖,这并不利于小口径人工血管的长期使用[19]。此外,表面亲疏性与细菌等微生物附着能力之间的研究相对较少。因此,为了更安全的临床医疗微环境,仍需探索设计既抗凝又抗菌的血管替代材料。 "
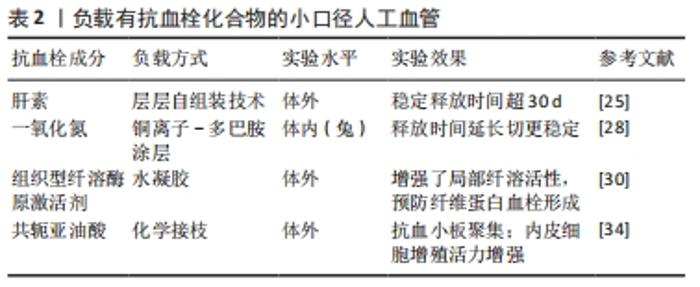
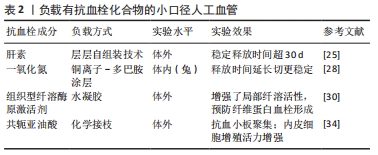
2.2.2 释放抗血栓化合物 肝素:抗凝剂肝素在这个研究领域被深入探索,负电荷的肝素与同样带负电荷的血浆蛋白和血小板相互排斥,减少血浆蛋白的吸附。同时,肝素也是唯一能抑制接触激活的抗凝剂[20]。与利用离子键单独结合肝素在抗凝方面所做的贡献相比,联合其他生物活性物质的共价结合可能会有更好的抗血栓形成效果。WANG等[21]将肝素与胶原结合域的片段连接,促进胶原蛋白选择性与合成材料结合,发挥抗凝作用的同时减少血液与人工表面接触。SMITH等[22]研究证明通过结合血管生长因子可促进肝素化组织工程血管选择性捕获内皮细胞。KONG等[23]交联壳聚糖-肝素后获得的人工血管每周释放的肝素总量为5-15 μg/mL,提高了人工血管的持续抗凝能力。然而,共价键作用使肝素功能团的活性受到影响,新兴的3D打印技术和纳米仿生技术或许是较好的解决办法。ZENG等[24]利用3D打印技术将带负电荷的肝素和带正电荷Tyr-Ile-Gly-Ser-Arg肽(YIGSR)层层组装,由于静电作用,肝素和YIGSR将贯序释放,达到快速抗凝以及通过YIGSR提高内皮细胞的迁移速度和定向迁移行为,快速实现内皮化。中国学者采用逐层自组装技术将明胶、聚赖氨酸和肝素纳米颗粒包裹制成纳米涂层组与单独交联肝素生物活性组进行比较,单独交联肝素生物活性组在第10天的肝素释放量突然释放达75%,纳米涂层组释放则更加平稳,在第1,3,7,21天的释放量分别为16%,24%,41%,56%,释药时间长达35 d。该课题组认为肝素与凝胶中的-OH发生氢键作用,从而显著提高了纳米结构的稳定性[25]。 一氧化氮:内皮细胞产生的一氧化氮是目前已知的一种血小板抑制因子,由于一氧化氮的半衰期非常短,只能扩散100 μm左右,因此一氧化氮必须在疾病部位被动释放或主动产生。有研究通过逐层法制造含有脂质体支架涂层的N-二硝酸盐,以控制一氧化氮的释放,结果显示一氧化氮释放仅持续5 d[26]。为了克服这一缺点,研究学者开发了一氧化氮内源性生成材料,利用硒或铜离子催化剂等物质来刺激一氧化氮生产。香港理工大学学者通过调整硒代胱胺联合多巴胺涂层的摩尔比,控制一氧化氮释放量(0.5-2.2)×10-10 mol/(cm2·min)超过60 d[27]。同年,杨志禄课题组[28]开发了借助多巴胺与铜离子的螯合,利用铜离子催化一氧化氮生成的仿生涂层,该涂层局部生成一氧化氮超过30 d且生成量在(0.5-4.0)× 10-10 mol/(cm2·min)之内。除此之外,基因转染、酶前体化技术、纳米贵金属材料也可发挥催化一氧化氮生成的作用。 组织型纤溶酶原激活剂:组织型纤溶酶原激活剂通过将纤溶酶原转化为纤溶酶,参与溶栓过程。然而,组织型纤溶酶原激活剂在循环中仅留存2-6 min,又常因与合成材料之间共价键结合或静电相互作用而失活。LI等[29]将组织型纤溶酶原激活剂封装在凝血酶可降解的水凝胶外壳中,该涂层在正常等离子体环境中释放少量组织型纤溶酶原激活剂,当凝血酶浓度增加时,水凝胶降解,释放组织型纤溶酶原激活剂,局部纤溶活性增强,将纤维蛋白血栓在形成时溶解。中国学者黄佳磊等[30]通过添加凝血酶可切割的多肽序列(丙烯酸-Gly-dPhe-Pro-Arg-Gly- Phe-Pro-Ala-Gly-Gly-Lys-丙烯酸)确保当且仅当凝血酶存在时组织型纤溶酶原激活剂得以从水凝胶中释放。 共轭亚油酸:共轭亚油酸既是胶原蛋白、二磷酸腺苷、花生四烯酸、凝血酶等诱导血小板聚集因子的抑制剂,还能降低环氧合酶1的活性,阻止血小板聚集[31-32]。MINH等[33]采用工艺相对简单的混合法将共轭亚油酸引入聚己内酯/聚氨酯支架,使用富含血小板的血浆证实了聚己内酯/聚氨酯-共轭亚油酸材料的抗血小板聚集活性,但表现出较差的内皮细胞吸附能力。TRAN等[34]认为共轭亚油酸直接加载到聚合物纤维中阻碍了共轭亚油酸的活动并削弱了聚己内酯/聚氨酯表面的结构完整性和血管支架的力学性能。该课题组使用碳化二亚胺偶联剂酯化共轭亚油酸后,与聚己内酯/聚氨酯表面进行化学接枝,发现随着共轭亚油酸接枝密度的增加,抗血小板黏附及内皮细胞增殖能力不断提高,且不会对表面形态和力学性能造成显著变化,但接枝密度超过(24±2) nmol/cm2时上述积极效果则会减弱。 尽管纳米颗粒技术、水凝胶技术、3D打印技术避免了抗凝分子持续暴露于血液中而导致的活性丧失,在一定程度上提高了此类物质的稳定性,见表2。然而受患者个体间差异的影响,如年龄、种族、内环境、凝血状态等因素可能导致不同的结局。此外,繁琐的工艺将影响人工血管的制作成本,增加患者的经济负担。如何解决患者就医问题的同时减轻经济压力同样值得思考。 "
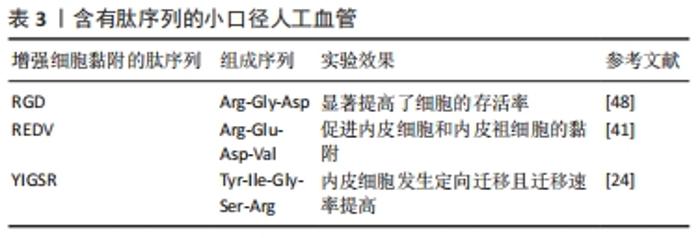
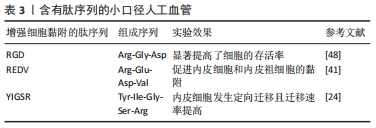
2.2.3 种植种子细胞 脐静脉内皮细胞:脐静脉内皮细胞已经研究了40多年,超过了任何来源的人类内皮细胞。迄今为止,脐静脉内皮细胞仍在该领域占据主导地位[35]。在2013-2018年期间分析的所有研究中,59%的研究将脐静脉内皮细胞作为人类内皮细胞的来源[36]。使用脐静脉内皮细胞的优点是非侵入性获取大量快速生长的内皮细胞,缩短种植时间。然而,随着内皮细胞异质性研究的深入,越来越多的证据表明内皮细胞以特定的组织/器官形式调节再生过程,加之脐静脉内皮细胞的增殖限制,其研究热度可能会逐渐下降。 间充质干细胞:骨髓间充质干细胞和脂肪间充质干细胞均能在特定的条件下诱导分化成血管内皮样细胞[37]。相对于骨髓穿刺获取骨髓间充质干细胞而言,皮下脂肪穿刺活检的创伤更小,获取量更多。FREIMAN等[38]研究发现,人脂肪微血管内皮细胞与脂肪间充质干细胞组合的组织工程血管,其形成和伸长发生在培养后的4 d内,第7天平均长度为150 μm,人脂肪微血管内皮细胞与人包皮成纤维细胞组合接种后前7 d缓慢生长,第14天达到相似长度。通过整合易于采集的人脂肪细胞,包括脂肪间充质干细胞和人脂肪微血管内皮细胞,可以有效地提升生物组织工程的血管化。尽管如此,LIN等[39]研究认为原组织相关的异质性限制了多系分化潜力。是否所有间充质干细胞在体内具有相同的多系潜力仍不清楚,人类各种间充质干细胞来源之间的差异及其对血管的长期影响需进一步研究。 内皮祖细胞:由自体内皮细胞接种的人工血管,移植后通常不会引起宿主的免疫反应,但术前需要考虑患者的年龄及疾病状况等因素,满足条件的患者只有接受活检才能完成获取,给患者带来二次的痛苦。采用无创方式从外周血中获取内皮细胞有着重要的临床应用价值。内皮祖细胞来自骨髓或外周血,可增殖分化成内皮细胞,因此开发特定有效且结构稳定的内皮祖细胞/内皮细胞捕获配体似乎很有必要。先前的一项研究表明,CD133抗体接枝表面获得了71%的内皮祖细胞捕获率[40]。精氨酸-谷氨酸-天冬氨酸-缬氨酸肽链(Arg-Glu-Asp-Val,REDV)和血管内皮生长因子共固定化可以促进内皮祖细胞和内皮细胞的黏附,以避免使用高剂量血管内皮生长因子造成的系统附带损害。DUAN等[41]固定CD133抗体、血管内皮生长因子和REDV到含有亲水性的透明质酸、肝素、多巴胺的聚苯乙烯表面,结果表明,CD133抗体、REDV制备的内皮祖细胞包埋层和血管内皮生长因子共固定表面晚期内皮祖细胞的覆盖面积达92%,远高于仅制备包埋层组(76%)和二者均无组(21%)。二硫化物循环八肽LXW7(cGRGDdvc)是最新发现的内皮祖细胞/内皮细胞捕获配体,它与内皮祖细胞/内皮细胞具有很强的结合亲和力和功能,与血小板的结合较弱。HAO等[42]在大鼠颈动脉旁路模型中植入6周后发现,LXW7修饰的移植物保持了83%的通畅率,而未经处理的移植物的通畅率仅为17%。与脐血含有大量的内皮祖细胞不同,成人外周血内皮祖细胞含量为50-200 L-1[43],受年龄、疾病等因素影响,内皮祖细胞数量可能更低。因此,由成年人内皮祖细胞的低发生率引起的担忧很可能在未来几年内继续存在。 诱导多能干细胞:自从LUO等[44]成功地诱导体细胞产生多能干细胞,诱导多能干细胞已成为研究的焦点,诱导多能干细胞为获得免疫相容的内皮细胞提供了强大的来源。GENERALI等[45]报道了利用诱导多能干细胞分化的平滑肌细胞和内皮细胞接种在可降解聚乙二醇酸-聚4羟丁酸酯(polyglycolic acid- poly-4- hydroxybutyrate,PGA-P4HB)6周后收获包含血管性血友病因子阳性细胞和一个近似于原生血管结构的平滑肌肌动蛋白阳性层。尽管诱导多能干细胞的研究取得了一定的进展,但诱导多能干细胞潜在的致癌性不可忽视,如恶性肿瘤和畸胎瘤[46]。 从目前国内外种子细胞相关研究结果来看,种子细胞种类从异体的脐静脉内皮细胞,到多种自体来源的干细胞,种子细胞来源得到扩充并在体外培养中取得进展,但与原组织相关的细胞异质性、干细胞的获取与安全培养、伦理等问题仍是此类组织工程产品转化为临床实践的挑战。因而,是否存在一种既具有血管再生能力又能避免上述问题的组织工程人工血管。 2.2.4 靶向基因诱导内皮化 肽序列:已有研究证明,肽序列作为配体具有与细胞受体相互识别的能力,在介导细胞迁移和黏附中起关键作用。小口径人工血管通过物理吸附、共价接枝等方法对内皮细胞特异性结合肽序列进行预处理后,内皮细胞的附着与增殖能力显著增强。与蛋白质相比,肽序列结构简单,稳定性高,更利于推广。精氨酸-甘氨酸-天冬氨酸(Arg-Gly-Asp,RGD)肽序列被广泛应用于生物材料的改性以增强细胞黏附。常用于提高表面亲水性的明胶因含有RGD序列而表现出较强的细胞黏附能力。聚己内酯纳米纤维内表面之间的孔隙经明胶修饰后形成仿生的血管基底膜,与单纯使用肝素修饰聚己内酯相比,添加明胶后内膜生长速度增快且长期维持在较高水平[47]。ANTONOVA等[48]用短、长胺链接剂固定不同RGD序列肽修饰的羟基丁酸戊酸共聚酯(polyhydroxybutyrate-co-valerate,PHBV)/聚己内酯聚合物,发现所有经RGD处理的移植物中,存活细胞超过90%,而未经RGD修饰的血管只有约20%的细胞存活,但几乎所有RGD修饰的移植物都引发了较高的血小板聚集并降低了移植物的最终抗拉强度。除此之外,还有前文提到的来源于纤维连接蛋白的REDV、衍生于层粘连蛋白的YIGSR等多肽序列应用于人工血管内皮细胞的特异性黏附识别。当前研究发现,含有肽序列的水凝胶微球可通过注射等非侵入性操作促进组织血管化,小口径人工血管或许可以利用此法改进血液相容性,见表3。 "

基因转染:基因工程通过转染内皮细胞可以在人工血管表面快速生成内皮细胞层,为促进血管内皮化提供了一种有利的选择策略。夏德林课题组[49]将血管内皮生长因子165基因转染的人脐静脉内皮细胞注射至大鼠背部缺血皮瓣后观察血清中血管内皮生长因子表达量,发现第7天血管内皮生长因子表达量最高,是非基因转染组的19.1倍,之后逐渐下降但远高于非基因转染组。由于内皮细胞对外源基因敏感,基因载体缺乏内皮细胞识别,转染效率低。因此,非常有必要开发具有内皮细胞特异性的基因载体。 尽管内皮细胞选择性多肽的表面修饰和靶向基因传递系统在内皮化过程中发挥关键作用,还需要进行更多的基础研究,以了解内皮细胞与材料表面、生长因子以及靶向基因传递系统之间的相互作用机制,达到时间空间上的精确局部控制。 2.3 其他 从医生角度分析,一方面血管移植过程中血供阻断时间与术后并发症的发生密切相关,微小血管吻合器的应用显著缩短了手术时间,减轻了缺血再灌注损伤,避免了因吻合技术问题而造成的血栓形成。但由于人工血管材质偏硬,弹性较差并不适应于此法。吕毅课题组[50]在犬腹主动脉人工血管置换实验中发现,相比于传统手工缝合术后4周发现1/3手术犬发生不同程度的狭窄,磁性吻合环组术后12周均未见血栓形成及血流动力学改变。既往研究认为磁性吻合环模块装置产生局部恒磁场可以促进内皮细胞增殖、降低血液黏度[51-52],但无论是微小血管吻合器还是磁性吻合环模块装置,术后均有异物残留,不适应于动静脉造瘘等浅表部位血管移植,可降解吸收的纳米材料也许是一种可行的替代方法。另一方面,术前通过低分子肝素或前列素E1治疗,维持纤维蛋白原含量;对于动脉硬化严重患者,手术结束前可预防性静推尿激酶;术后低分子肝素联合阿司匹林和华法林连用7 d后停药,继续服用华法林3个月并检测凝血酶原时间[53]。对患者而言,术后应遵嘱服药,定期复查,移植部位涉及关节时注意避免体位压迫。移植部位疼痛肿胀、搏动消失或减弱时应及时就医,避免因血管阻塞而发生严重并发症。 "

| [1] ADIPURNAMA I, YANG MC, CIACH T, et al. Surface modification and endothelialization of polyurethane for vascular tissue engineering applications: a review. Biomater Sci. 2016;5(1):22-37. [2] 施群.移植血管的发展和应用[M].上海:复旦大学出版社,2009. [3] SOUZA DS, DASHWOOD MR, TSUI JC, et al. Improved patency in vein grafts harvested with surrounding tissue: results of a randomized study using three harvesting techniques. Ann Thorac Surg. 2002;73(4):1189-1195. [4] JAFFER IH, FREDENBURGH JC, HIRSH J, et al. Medical device-induced thrombosis: what causes it and how can we prevent it? J Thromb Haemost. 2015;13 Suppl 1:S72-81. [5] LABARRERE CA, DABIRI AE, KASSAB GS. Thrombogenic and Inflammatory Reactions to Biomaterials in Medical Devices. Front Bioeng Biotechnol. 2020;8:123. [6] ASHCRAFT M, DOUGLASS M, CHEN Y, et al. Combination strategies for antithrombotic biomaterials: an emerging trend towards hemocompatibility. Biomater Sci. 2021;9(7):2413-2423. [7] 田小宁,从飞,程一钊,等.血管移植三种术式修复四肢血管损伤的疗效评价[J].中国矫形外科杂志,2017,25(14):1282-1287. [8] DIMITRIEVSKA S, MAIRE M, DIAZ-QUIJADA GA, et al. Low thrombogenicity coating of nonwoven PET fiber structures for vascular grafts. Macromol Biosci. 2011;11(4):493-502. [9] DAI Y, DAI S, XIE X, et al. Immobilizing argatroban and mPEG-NH2 on a polyethersulfone membrane surface to prepare an effective nonthrombogenic biointerface. J Biomater Sci Polym Ed. 2019;30(8): 608-628. [10] SELLATURAY P, NASSER S, EWAN P. Polyethylene Glycol-Induced Systemic Allergic Reactions (Anaphylaxis). J Allergy Clin Immunol Pract. 2021;9(2):670-675. [11] AHMED F, ALEXANDRIDIS P, SHANKARAN H, et al. The ability of poloxamers to inhibit platelet aggregation depends on their physicochemical properties. Thromb Haemost. 2001;86(6):1532-1539. [12] LE AN, TRAN NM, PHAN TB, et al. Poloxamer additive as luminal surface modification to modulate wettability and bioactivities of small-diameter polyurethane/polycaprolactone electrospun hollow tube for vascular prosthesis applications. Materials Today Communications. 2021;26: 101771. [13] KARLETA V, ANDRLIK I, BRAUNMÜLLER S, et al. Poloxamer 188 supplemented culture medium increases the vitality of Caco-2 cells after subcultivation and freeze/thaw cycles. ALTEX. 2010;27(3):191-197. [14] PAZHANIMALA SK, VLLASALIU D, RAIMI-ABRAHAM BT. Engineering Biomimetic Gelatin Based Nanostructures as Synthetic Substrates for Cell Culture. Applied Sciences. 2019;9(8):1583. [15] MOTLAGH D, YANG J, LUI KY, et al. Hemocompatibility evaluation of poly(glycerol-sebacate) in vitro for vascular tissue engineering. Biomaterials. 2006;27(24):4315-4324. [16] ZARGAR KHARAZI A, ATARI M, VATANKHAH E. A nanofibrous bilayered scaffold for tissue engineering of small-diameter blood vessels. Polymers for Advanced Technologies. 2018;29(12):3151-3158. [17] LIU P, CHEN Q, LI L, et al. Anti-biofouling ability and cytocompatibility of the zwitterionic brushes-modified cellulose membrane. J Mater Chem B. 2014;2(41):7222-7231. [18] CHENG CH, CHEN GF, LIN JC. Studies of zwitterionic sulfobetaine functionalized polypropylene surface with or without polyethylene glycol spacer: surface characterization, antibacterial adhesion, and platelet compatibility evaluation. J Biomater Sci Polym Ed. 2020;31(16): 2060-2077. [19] CUI L, YAO Y, YIM EKF. The effects of surface topography modification on hydrogel properties. APL Bioeng. 2021;5(3):031509. [20] SCHMAIER AH. The contact activation and kallikrein/kinin systems: pathophysiologic and physiologic activities. J Thromb Haemost. 2016; 14(1):28-39. [21] WANG M, BAO L, QIU X, et al. Immobilization of heparin on decellularized kidney scaffold to construct microenvironment for antithrombosis and inducing reendothelialization. Sci China Life Sci. 2018;61(10):1168-1177. [22] SMITH RJ JR, YI T, NASIRI B, et al. Implantation of VEGF-functionalized cell-free vascular grafts: regenerative and immunological response. FASEB J. 2019;33(4):5089-5100. [23] KONG X, XU W. Biodegradation and biocompatibility of a degradable chitosan vascular prosthesis. Int J Clin Exp Med. 2015;8(3):3498-3505. [24] ZENG Z, HU C, LIANG Q, et al. Coaxial-printed small-diameter polyelectrolyte-based tubes with an electrostatic self-assembly of heparin and YIGSR peptide for antithrombogenicity and endothelialization. Bioact Mater. 2020;6(6):1628-1638. [25] WANG D, WANG X, LI X, et al. Biologically responsive, long-term release nanocoating on an electrospun scaffold for vascular endothelialization and anticoagulation. Mater Sci Eng C Mater Biol Appl. 2020;107:110212. [26] ELNAGGAR MA, SEO SH, GOBAA S, et al. Nitric Oxide Releasing Coronary Stent: A New Approach Using Layer-by-Layer Coating and Liposomal Encapsulation. Small. 2016;12(43):6012-6023. [27] YANG Z, YANG Y, ZHANG L, et al. Mussel-inspired catalytic selenocystamine-dopamine coatings for long-term generation of therapeutic gas on cardiovascular stents. Biomaterials. 2018;178:1-10. [28] ZHANG F, ZHANG Q, LI X, et al. Mussel-inspired dopamine-CuII coatings for sustained in situ generation of nitric oxide for prevention of stent thrombosis and restenosis. Biomaterials. 2019;194:117-129. [29] LI C, DU H, YANG AZ, et al. Thrombosis-Responsive Thrombolytic Coating Based on Thrombin-Degradable Tissue Plasminogen Activator (t-PA) Nanocapsules. Advanced Functional Materials, 2017;27(45): 1703934.1-1703934.11. [30] 黄佳磊,郁李胤,王境鸿,等.可持续抗非特异性蛋白质吸附的凝血酶响应型水凝胶涂层[J].高分子学报,2021,52(9):1118-1128. [31] BENITO P, NELSON GJ, KELLEY DS, et al. The effect of conjugated linoleic acid on platelet function, platelet fatty acid composition, and blood coagulation in humans. Lipids. 2001;36(3):221-227. [32] LI G, BUTZ D, DONG B, et al. Selective conjugated fatty acids inhibit guinea pig platelet aggregation. Eur J Pharmacol. 2006;545(2-3):93-99. [33] MINH HH, HIEP NT, HAI ND, et al. Fabrication of Polycaprolactone/Polyurethane Loading Conjugated Linoleic Acid and Its Antiplatelet Adhesion. Int J Biomater. 2017;2017:5690625. [34] TRAN N, LE A, HO M, et al. Polyurethane/polycaprolactone membrane grafted with conjugated linoleic acid for artificial vascular graft application. Sci Technol Adv Mater. 2020;21(1):56-66. [35] BREYMANN C, SCHMIDT D, HOERSTRUP SP. Umbilical cord cells as a source of cardiovascular tissue engineering. Stem Cell Rev. 2006;2(2): 87-92. [36] WANG K, LIN RZ, MELERO-MARTIN JM. Bioengineering human vascular networks: trends and directions in endothelial and perivascular cell sources. Cell Mol Life Sci. 2019;76(3):421-439. [37] TAKAHASHI K, YAMANAKA S. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell. 2006;126(4):663-676. [38] FREIMAN A, SHANDALOV Y, ROZENFELD D, et al. Adipose-derived endothelial and mesenchymal stem cells enhance vascular network formation on three-dimensional constructs in vitro. Stem Cell Res Ther. 2016;7:5. [39] LIN RZ, MORENO-LUNA R, LI D, et al. Human endothelial colony-forming cells serve as trophic mediators for mesenchymal stem cell engraftment via paracrine signaling. Proc Natl Acad Sci U S A. 2014;111(28):10137-10142. [40] CHEN W, ZENG W, SUN J, et al. Construction of an Aptamer-SiRNA Chimera-Modified Tissue-Engineered Blood Vessel for Cell-Type-Specific Capture and Delivery. ACS Nano. 2015;9(6):6069-6076. [41] DUAN Y, YU S, XU P, et al. Co-immobilization of CD133 antibodies, vascular endothelial growth factors, and REDV peptide promotes capture, proliferation, and differentiation of endothelial progenitor cells. Acta Biomater. 2019;96:137-148. [42] HAO D, FAN Y, XIAO W, et al. Rapid endothelialization of small diameter vascular grafts by a bioactive integrin-binding ligand specifically targeting endothelial progenitor cells and endothelial cells. Acta Biomater. 2020;108:178-193. [43] INGRAM DA, MEAD LE, TANAKA H, et al. Identification of a novel hierarchy of endothelial progenitor cells using human peripheral and umbilical cord blood. Blood. 2004;104(9):2752-2760. [44] LUO J, SHI X, LIN Y, et al. Efficient Differentiation of Human Induced Pluripotent Stem Cells into Endothelial Cells under Xenogeneic-free Conditions for Vascular Tissue Engineering. Acta Biomater. 2021;119: 184-196. [45] GENERALI M, CASANOVA EA, KEHL D, et al. Autologous endothelialized small-caliber vascular grafts engineered from blood-derived induced pluripotent stem cells. Acta Biomater. 2019;97:333-343. [46] STEVENS KR, MURRY CE. Human Pluripotent Stem Cell-Derived Engineered Tissues: Clinical Considerations. Cell Stem Cell. 2018;22(3): 294-297. [47] XING Y, GU Y, GUO L, et al. Gelatin coating promotes in situ endothelialization of electrospun polycaprolactone vascular grafts. J Biomater Sci Polym Ed. 2021;32(9):1161-1181. [48] ANTONOVA LV, SILNIKOV VN, SEVOSTYANOVA VV, et al. Biocompatibility of Small-Diameter Vascular Grafts in Different Modes of RGD Modification. Polymers (Basel). 2019;11(1):174. [49] 明华伟,何芸,夏德林,等.VEGF165基因转染HUVEC促进大鼠血管生成的实验研究[J].口腔颌面外科杂志,2017,27(3):161-165. [50] 刘仕琪,慈红波,雷鹏,等.磁压榨吻合技术实现犬腹主动脉人工血管置换快速无缝线吻合[J].器官移植,2021,12(2):191-196. [51] 李飞,贾国良,张荣庆,等.弱恒磁场对人脐静脉及兔主动脉内皮细胞增殖的影响[J].中国病理生理杂志,2003,19(6):772,777. [52] 李春梅,杨佐森,解学魁,等.钕铁硼磁片对小鼠微循环影响的观察实验[J].中国公共卫生,2001,17(10):913. [53] 王泽,刘佩,杨志凯,等.下肢动脉人工血管旁路移植术后闭塞的治疗效果研究[J].影像研究与医学应用,2017,1(1):138-139. [54] MINGA LOWAMPA E, HOLEMANS C, STIENNON L, et al. Late Fate of Cryopreserved Arterial Allografts. Eur J Vasc Endovasc Surg. 2016; 52(5):696-702. [55] 任章勇,吕少诚,贺强.同种异体血管在肝胆胰手术中的应用现状[J].解放军医学院学报,2020,41(7):724-727. [56] JASHARI R, VAN HOECK B, NGAKAM R, et al. Banking of cryopreserved arterial allografts in Europe: 20 years of operation in the European Homograft Bank (EHB) in Brussels. Cell Tissue Bank. 2013;14(4):589-599. [57] DIMITRIEVSKA S, NIKLASON LE. Historical Perspective and Future Direction of Blood Vessel Developments. Cold Spring Harb Perspect Med. 2018;8(2):a025742. |
| [1] | Sun Kexin, Zeng Jinshi, Li Jia, Jiang Haiyue, Liu Xia. Mechanical stimulation enhances matrix formation of three-dimensional bioprinted cartilage constructs [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-7. |
| [2] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [3] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [4] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [5] | Zhang Tingting, Liu Juan, Zhang Xu. Bioactivity of phase-transition lysozyme for surface modification of zirconia all-ceramic implant material mediating hydroxyapatite coating [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1043-1049. |
| [6] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [7] | Yang Yitian, Wang Lu, Yao Wei, Zhao Bin. Application of the interaction between biological scaffolds and macrophages in bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1071-1079. |
| [8] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [9] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [10] | Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109. |
| [11] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [12] | Xu Yan, Li Ping, Lai Chunhua, Zhu Peijun, Yang Shuo, Xu Shulan. Piezoelectric materials for vascularized bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1126-1132. |
| [13] | Tao Xin, Xu Yi, Song Zhiwen, Liu Jinbo. Hippo signaling pathway in the regulation of spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(4): 619-625. |
| [14] | Li Shihao, Li Qi, Li Zhen, Zhang Yuanyuan, Liu Miaomiao, Ouyang Yi, Xu Weiguo. Plantar pressure and gait analysis in patients with anterior cruciate ligament injury and reconstruction [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(4): 626-631. |
| [15] | Li Rui, Liu Zhen, Guo Zige, Lu Ruijie, Wang Chen. Aspirin-loaded chitosan nanoparticles and polydopamine modified titanium sheets improve osteogenic differentiation [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 374-379. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

