Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (7): 1103-1109.doi: 10.12307/2023.030
Previous Articles Next Articles
Osteoinductive properties of calcium phosphate ceramic bone repair materials
Lu Di1, Zhang Cheng1, Duan Rongquan1, Liu Zongxiang1, 2
- 1School of Stomatology, Xuzhou Medical University, Xuzhou 221004, Jiangsu Province, China; 2Affiliated Stomatological Hospital of Xuzhou Medical University, Xuzhou 221002, Jiangsu Province, China
-
Received:2021-12-09Online:2023-03-08Published:2022-07-19 -
Contact:Liu Zongxiang, Chief physician, Professor, School of Stomatology, Xuzhou Medical University, Xuzhou 221004, Jiangsu Province, China; Affiliated Stomatological Hospital of Xuzhou Medical University, Xuzhou 221002, Jiangsu Province, China Duan Rongquan, MD, Associate professor, School of Stomatology, Xuzhou Medical University, Xuzhou 221004, Jiangsu Province, China -
About author:Lu Di, Master candidate, Physician, School of Stomatology, Xuzhou Medical University, Xuzhou 221004, Jiangsu Province, China
CLC Number:
Cite this article
Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
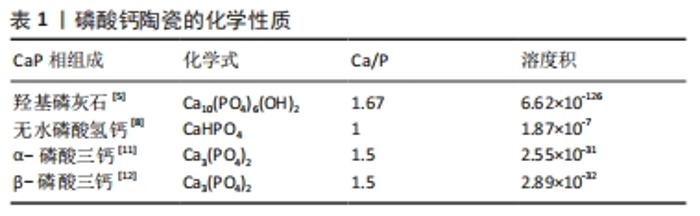
2.1 磷酸钙陶瓷的常见形式 磷酸钙陶瓷是一种具有良好生物活性、骨传导性能的生物陶瓷,受到了广泛的关注[4]。根据钙磷比例不同,磷酸钙陶瓷分为羟基磷灰石、磷酸三钙和双相磷酸钙。 2.1.1 羟基磷灰石 羟基磷灰石是钙磷灰石的天然矿化物质,分子式为Ca10(PO4)6(OH)2,钙磷比1.67,是人体骨骼中主要的无机成分,约占骨骼质量的50%,具有良好的骨传导性[5]。羟基磷灰石在磷酸钙陶瓷各种组成中的稳定性最高,溶解度较小[6]。羟基磷灰石和松质骨相似,初期的机械强度较低,在拉伸和剪切的作用下更加脆弱,但抗压强度可达到100 MPa,且具有比骨更高的弹性系数[7],羟基磷灰石虽然具有较好的强度和细胞吸附能力,但其较差的降解能力不利于材料的吸收和自体骨的长入[2]。 有实验证实,将同样直径为3 mm的羟基磷灰石和磷酸三钙圆柱体植入兔松质骨6个月后,磷酸三钙的降解率高达85.4%,而相同情况下的羟基磷灰石降解率仅为5.4%[5]。为了进一步提高羟基磷灰石的临床应用,材料特性成为研究的热点,其中羟基磷灰石的多孔结构和晶体是高度考虑因素[8]。MATSUO等[9]观察成骨细胞在不同孔隙直径的羟基磷灰石中的增殖分化情况,直径大于150 μm的孔为骨组织提供了理想的生长空间,但过大的孔径会降低植入物的机械强度,无法起到初期支撑作用。为了同时满足理想的生长效果和初期稳定性,目前将大孔直径控制在250 μm左右,孔隙率维持在40%-80%[10]。此外,由于人体内骨骼中的羟基磷灰石为纳米级,研究人员发现纳米级羟基磷灰石较传统的羟基磷灰石具有更优秀的生物性能,具体表现在纳米级羟基磷灰石有很强的诱导细胞增殖分化能力,在新生血管重建上也优于普通羟基磷灰石。 2.1.2 磷酸三钙 磷酸三钙的分子式为Ca3(PO4)2,钙磷比为1.5,磷酸三钙的钙磷比低于羟基磷灰石,则水溶性高于羟基磷灰石[11]。根据烧结温度的不同可将磷酸三钙分为高温相α-磷酸三钙和低温相β-磷酸三钙,α-磷酸三钙通常由β-磷酸三钙在1 120 ℃以上淬火制备,故α-磷酸三钙可以被认为是β-磷酸三钙的高温阶段[12]。两者的化学成分虽然相同,但在溶解度和晶体结构上各有差异。在25 ℃的液体环境中,α-磷酸三钙的沉淀平衡常数(Ksp)为10×10-32-25.5×10-32,β-磷酸三钙的沉淀平衡常数(Ksp)为10×10-32-28.9×10-32。就晶体结构而言,β-磷酸三钙晶体稳定性超过了α-磷酸三钙,因此,α-磷酸三钙在水溶液中更容易发生反应[13]。磷酸三钙具有良好的成骨和降解能力,但降解速度难以与新生骨相匹配,强度相对较差[14]。磷酸三钙与羟基磷灰石相似,虽然多孔的结构有益于新生血管重建但缺少初期稳定性,已有实验证实磷酸三钙植入后经过多种因素作用部分会转化成羟基磷灰石,进而影响磷酸三钙的降解,大部分能在6-24个月后被吞噬吸收,小部分能留存数年[15]。 2.1.3 双相磷酸钙 双相磷酸钙是由不同比例的高度稳定性的羟基磷灰石和溶解度更高的β-磷酸三钙组成[16]。β-磷酸三钙的钙磷比为1.5-1.67,溶解度和降解能力介于羟基磷灰石和磷酸三钙之间[17]。通过调整羟基磷灰石/β-磷酸三钙的比例,结合两者的优点即高度稳定性和易降解性,达到合适的吸收降解速度同时促进骨骼向内生长,此外还具有和骨骼相似的化学组成,常用于口腔科和整形外科的临床应用[18]。上述各类磷酸钙的化学性质已总结在表1中。 "

磷酸钙陶瓷材料的骨传导性已得到公认。近年来的研究揭示了磷酸钙材料还具有一定的骨诱导性[19],早期研究认为磷酸钙材料仅具有骨传导性,WELLS于1911年最早发现钙盐对成骨有促进作用,URIST于1965年正式提出骨诱导现象,同时发现骨形态发生蛋白具有骨诱导能力,可诱导异位成骨,随后,大量的实验也证实未添加生长因子的单纯磷酸钙材料也具有一定的骨诱导性:1988年HEUGHEBAERT等报道羟基磷灰石诱导仓鼠软组织中出现骨样结构[20];1990年YAMASAKI等发现将多孔羟基磷灰石植入狗皮下有新骨形成[21];RIPAMONTI[22]于实验动物非骨部位植入多孔羟基磷灰石有新骨形成,此后,磷酸钙材料的固有骨诱导性基本被认可。但单纯的磷酸钙材料还不足以满足理想骨移植材料标准[19],研究人员着力于优化生物材料特性来提高磷酸钙材料的骨诱导性。 目前应用的骨移植材料中,由于磷酸钙陶瓷化学成分与骨矿物质的相似性以及其优异的生物相容性、骨传导性和骨诱导性,磷酸钙陶瓷最有希望发展成真正的骨替代物[23],大量的研究发现磷酸钙陶瓷的骨诱导性能与其在制造过程中进行优化的材料因素紧密相关[24]。骨诱导生物材料的理化和结构特性可能直接或间接地触发异位成骨过程。微纳米结构特性有利于与骨形态发生蛋白和其他内源性蛋白质相互作用,进而触发骨髓间充质干细胞分化为成骨细胞,从而形成骨组织。表面形貌和无机离子释放(以磷酸钙陶瓷为例)也可能是成骨分化和骨形成过程的直接触发因素。研究结果显示具有骨状磷灰石表层的三维多孔结构和磷酸钙陶瓷固有的某些结构特征对新骨诱导至关重要[25]。 2.2.1 骨修复材料特性与骨诱导性能 磷酸钙陶瓷的固有骨诱导性与其多种材料特性紧密相关。为此,研究人员分别从化学组成、孔隙结构、离子环境、表面粗造度、骨样磷灰石形成、纳米结构等方面深入探究以期提高人工替代骨的骨诱导性[26]。DUAN等[27]分别将具有针状表面形貌的亚微米、微米双相磷酸钙及具有颗粒状表面形貌的亚微米、微米磷酸三钙植入比格犬背肌中,12周后诱导的骨量大致相等,但在相同亚微米大小下,针状表面形貌明显比颗粒状形貌磷酸三钙较早形成新骨,实验数据表明,对骨诱导性影响最大的是材料结构,其次为表面形貌、化学组成。在其他实验组中,亚微米结构的双相磷酸钙表现为出色的骨诱导性,为后续研究提供基础,见表2。 "

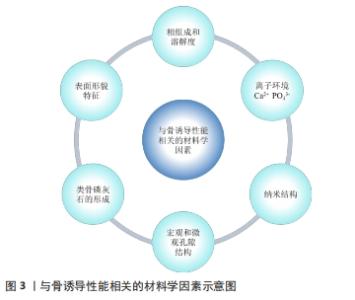
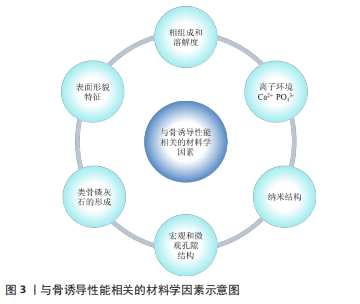
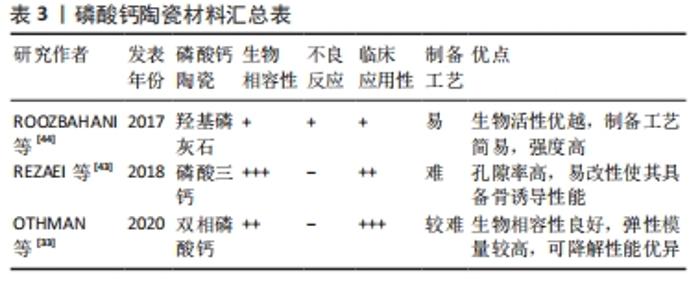
2.2.2 孔隙率与骨诱导性能 实验证实,致密的骨陶瓷不能诱导成骨,而多孔钙陶瓷能显著诱导体内成骨[15]。孔隙的基本功能是容纳细胞生长,提供通道有利于血管的生长,同时充分交换氧气和营养[28]。材料表面形貌改变的同时影响间充质干细胞或基质细胞的显著变化,此外,多孔磷灰石与骨状层或能够形成骨状层的磷酸钙陶瓷在体外形成较强的成骨能力。从仿生学的角度来看,纳米级晶体尺寸可能会改善磷酸钙陶瓷的生物学特性,许多体外实验已经证实这一猜测。骨形成细胞倾向于与生物材料的纳米级表面相互作用,有助于促进干细胞的黏附、增殖和分化[29]。 2.2.3 溶解度与骨诱导性能 磷酸钙陶瓷的溶解度还可以影响材料表面的离子浓度来影响蛋白质的吸附,Ca2+是一种重要的归巢信号,促进细胞迁移和定向生长[24]。高浓度的Ca2+刺激前成骨细胞向骨吸收部位趋化,激活成骨细胞增殖,促进间充质干细胞的分化[30]。因此溶解度更高的磷酸三钙释放出更多的Ca2+和PO43-,吸附更多的纤维蛋白原等,表现出更好的骨诱导性。一般情况下,磷酸钙陶瓷材料较高的溶解度意味着具有较高的骨诱导性,如双相磷酸钙的骨诱导性大于羟基磷灰石。然而,双相磷酸钙可以通过调节羟基磷灰石/β-磷酸三钙的比例达到最适合的表面溶解度,从而使蛋白质的吸附能力达到最优,使骨诱导性能增强[31]。基于大量实验数据,磷酸钙陶瓷材料骨诱导性的排序如下:双相磷酸钙 >β-磷酸三钙> 羟基磷灰石> α-磷酸三钙[27]。在双相磷酸钙不同的比例中发现30%的羟基磷灰石和70%的β-磷酸三钙能够促进骨形态发生蛋白2的高表达[32]。 2.2.4 宏观和微观多孔结构与骨诱导性能 研究证实,骨诱导材料都具有相互连接的多孔结构,除了Ca2+/ PO43-的影响之外,在离子环境下,多孔结构在磷酸钙陶瓷的成骨率中起重要作用。相关实验证实了多孔磷酸钙陶瓷可以诱导骨形成,而致密磷酸钙陶瓷则不能[33]。多孔支架结构的基本功能是使向内生长的细胞与其相适应,而相互连通孔隙的通道是体液、血管和细胞培养支架的中心,为细胞提供充足的氧气和营养交换。在单纯应用骨诱导材料的情况下,可诱导其携带的细胞分化为成骨细胞[34]。 支架的多孔结构参数包括孔隙率、孔径大小、孔径形状和孔径连通性[35]。高孔隙率被认为在促进成骨方面具有显著的积极作用,但这种积极作用并不一定会发生,因为过高孔隙率导致的低强度往往会使植入支架过早坍塌[36]。因此,对于生物活性陶瓷支架,根据植入部位的不同,40%-80%的孔隙率可用于骨缺损修复。此外,开放孔隙的数量也与骨形成直接相关。相互连通的孔看起来像“内部通道”,允许物质运输、细胞黏附和骨长入[37]。有研究在山羊肌肉中放置含有相互连通孔隙的大块无水磷酸氢钙骨水泥后,骨主要形成于外侧孔隙通道的内部,靠近通道开口的方向[20]。当孔隙度为40%-80%时,最佳孔径一般在200-500 μm范围内,孔隙连通通道尺寸在100-200 μm范围内。 此外,微孔(孔径<10 μm)在促进成骨中起着至关重要的作用。大孔壁上的微孔不仅有利于渗透体液,而且孔壁的粗糙表面有利于细胞附着和成骨表型的表达[34]。内部的孔隙限制了体液的流动,从而保持了Ca2+和PO43-浓度水平,降低了吸附在大孔表面的细胞和蛋白质所受的剪切应力。相关研究发现高孔隙率和/或更多孔隙>20 nm的羟基磷灰石和双相磷酸钙颗粒比低孔隙率颗粒吸附更多的纤维蛋白原和胰岛素[38]。 2.2.5 磷酸钙陶瓷的表面形貌与骨诱导性能 材料表面形貌对其成骨诱导能力尤为重要,许多报道探索了材料表面形貌对细胞黏附和分化行为的影响[39]。MCMURRAY等[40]制作了不同表面纳米形貌的材料,发现纳米形貌显著促进间充质干细胞特异性分化;进一步的研究表明,对称和随机的纳米阵列均不能诱导成骨分化,而无序的纳米阵列可诱导成骨分化,即材料表面形貌调节骨的形成[41]。 WANG等[42]在不同孔径和不同孔径形貌的羟基磷灰石圆盘状微球上制备了几种表面形貌,研究发现羟基磷灰石表面的宏观孔结构有利于细胞增殖,而微孔结构上调了早期成骨细胞分化过程。这种表面孔隙结构可以看作是表面形貌,因此不同的细胞反应反映了形貌对细胞生物功能甚至成骨潜能的影响。这些研究揭示了表面形貌对细胞行为甚至细胞成骨分化的可能性。在磷酸钙陶瓷中,由于烧结温度不同、晶粒尺寸不同,其表面形貌也可能反映在表面微观结构的变化上[43]。 2.2.6 磷酸钙陶瓷的纳米结构与骨诱导性能 骨磷灰石由纳米级碳酸钙磷晶体组成,传统的磷酸钙陶瓷虽然在一定程度上模仿了骨性成分和多孔结构,但在微观尺度上存在较大的钙磷颗粒,这可能会降低多孔磷酸钙陶瓷的生物性能[42]。从生物仿生的角度来看,纳米级的晶体尺寸可以改善磷酸钙陶瓷的生物性能,骨形成细胞倾向于与生物材料的纳米级表面相互作用,促进黏附、增殖和分化[44]。 LI等[45]成功地使用改性共沉淀法和微波烧结制备了多孔钙磷纳米陶瓷,这些钙磷纳米陶瓷吸收了更多的骨相关蛋白,并对包括骨生长因子在内的某些特定蛋白表现出选择性吸附作用。在不同表面微观结构的影响下,尺寸< 100 nm的双相磷酸钙陶瓷表面对蛋白质吸附的促进作用强于尺寸> 100 nm的双相磷酸钙陶瓷表面。此外,由于钙磷纳米陶瓷具有高比表面积、纳米级表面形貌以及微孔丰富的大孔相互连接等特点,可以有效地启动和调节细胞活动,从而获得比传统磷酸钙陶瓷更高的体内骨传导率和骨诱导率。 由此可见,通过优化材料的离子环境、宏微孔结构、形貌特征和纳米结构等特性,可以使磷酸钙陶瓷具有骨诱导性能。这些材料的特性可以直接或间接地影响成骨诱导过程。基于这些结果,通过优化材料的物理化学性能,可以进一步提高磷酸钙陶瓷的成骨率,有助于更深入和更广泛地了解材料的成骨机制,见图3。 "
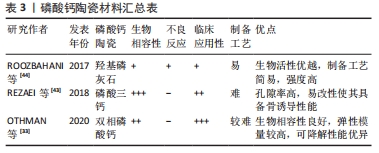
2.3.1 钙磷释放与骨诱导性能 由于成骨诱导现象通常在磷酸钙陶瓷中观察到,而且随着钙磷相组成和溶解性的变化,成骨诱导率不同,Ca2+和PO43-被认为对材料的成骨诱导非常重要。在体内骨吸收过程中,破骨细胞可能会释放Ca2+和PO43-,这导致局部离子浓度增加到过饱和水平,这对成骨细胞的增殖和分化以及随后的骨形成过程有显著影响[46]。 事实上,在许多细胞外微环境中可以观察到Ca2+变化趋势,并被认为是细胞迁移和定向生长的有利化学信号。此外,Ca2+是一个重要的归巢信号,它汇集了骨重塑启动所需的不同类型的细胞,如高浓度的Ca2+能刺激前成骨细胞向骨吸收部位趋化,并促使其成熟为生成新骨的细胞[47]。另一方面,细胞外Ca2+的释放对骨吸收部位附近成骨细胞的增殖和分化也有重要的控制作用。同样PO43-在骨诱导中也起着重要作用,在生理性骨基质矿化中起关键作用[48]。此外,离子环境可能通过影响蛋白质吸附而引发骨诱导。ZHU等[49]研究发现β-磷酸三钙释放Ca2+、PO43-,引起离子浓度的局部增加,从而导致更多的钙磷沉淀,促进蛋白质更好地吸收,进而促进成骨。此外,这些研究也可以解释了为什么由高可溶性(双相磷酸钙)和低可溶性(双相磷酸钙)相混合而成的双相磷酸钙陶瓷在促进成骨细胞分化方面比羟基磷灰石或磷酸三钙表现得更好,见表3。 "
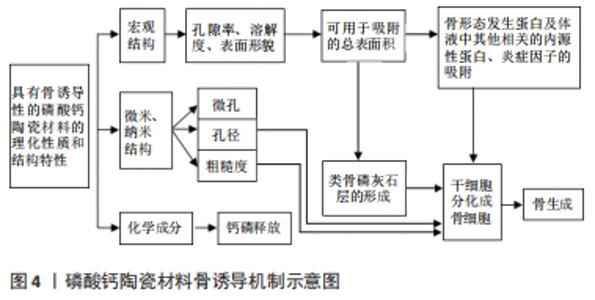
2.3.2 蛋白吸附与骨诱导性能 钙磷对蛋白质具有较高的亲和力,通过提供较高的表面能量[10],并为带负电荷的蛋白质提供带正电荷的Ca2+结合位点。因此,蛋白质的吸附是磷酸钙陶瓷植入体内成骨的首要条件。因为磷酸钙陶瓷的一些物理或化学特性,如表面形貌等强烈影响着蛋白质吸附数量和特异性吸附蛋白质,现已被证明能够影响钙磷骨结合,这个过程可能与骨结合相关,可能是钙磷诱导成骨的原因。 虽然对于骨形态发生蛋白吸附或共沉淀对钙磷成骨作用的理论是合理的,但骨形态发生蛋白与钙磷生物材料的成骨作用仍然存在明显差异。如钙磷诱导的异位骨形成通常通过膜内骨化发生,而骨形态发生蛋白诱导的异位骨形成多通过软骨内骨化发生[50]。除了骨形态发生蛋白,其他蛋白质也可被钙磷吸附,其中纤维连接蛋白、玻璃体结合蛋白等细胞黏附蛋白可以与细胞膜上的特异性整合素结合,为细胞生成锚点,并启动细胞-细胞外基质相互作用,这些作用已经被证明影响不同类型的细胞行为,如黏附、增殖甚至成骨分化[51]。这种特异性的结合和相关的细胞行为是由不同类型的整合素所主导的,它们与细胞信号网络的关联启动了下游信号级联,如黏着斑激酶、蛋白激酶C和丝裂原活化蛋白激酶途径[52]。 研究发现,在磷酸三钙表面培养人脂肪干细胞可观察到磷酸化黏着斑激酶存在和分化的证据,随后,SALASZNYK等[53]研究发现,在Ⅰ型胶原和玻连蛋白涂层表面上的骨髓间充质干细胞通过黏着斑激酶的磷酸化向成骨细胞分化,导致Runt相关转录因子2的激活。因此,磷酸钙吸附的细胞黏附蛋白,可能通过随后的黏着斑激酶磷酸化和细胞外信号调节激酶1/2通路的激活来调节成骨细胞的分化。最新研究发现a2b1整合素和MAPK/ERK信号通路参与骨形态发生蛋白2自分泌环路对磷酸三钙骨传导的调控[54]。 2.3.3 生物矿化与骨诱导性能 许多研究表明,磷酸钙陶瓷表面形成的类骨磷灰石在骨诱导中起重要作用。类骨磷灰石由碳酸钙羟基磷灰石组成,在组成和结构上与天然骨的主要无机相基本一致。磷酸钙陶瓷材料通过溶解、再沉淀或通过体液聚集在其表面的方式形成具有类骨磷灰石层的能力,这是迄今为止骨诱导材料显示出的唯一特性[55]。在磷酸钙陶瓷上的类骨磷灰石形成过程包括磷酸钙的聚集、生长和结晶,这一过程主要取决于Ca2+和PO43-浓度、pH值、温度和表面形貌。类骨磷灰石层的沉积伴随着成骨蛋白等有机因子的共沉淀,这可能触发相关细胞的成骨分化;尽管成骨蛋白可能吸附在材料表面,但如果类骨磷灰石不发生沉积,就也不会发生成骨诱导[56]。这一现象可能与骨诱导发生所需的蛋白质积累量有关。类骨磷灰石形成能力的强弱顺序与钙磷陶瓷的诱导成骨能力的强弱顺序相对应。通过对多孔双相磷酸钙陶瓷表面微纳米结构与骨诱导生物学功能关系的研究发现,类骨磷灰石不同微观结构也会影响材料的骨诱导能力。磷酸钙陶瓷的成骨诱导能力需要具有某些特性的类骨磷灰石层的形成。 2.3.4 免疫调剂与骨诱导 磷酸钙陶瓷诱导成骨的机制可能非常复杂,涉及多种细胞、分子机制交联相互作用的生物学进展。作者已经描述了关于磷酸钙陶瓷蛋白吸附机制的现有理论,它不仅涉及骨骼系统,还涉及血管和免疫系统。根据近年来的研究,可以看出微孔磷酸钙陶瓷可能通过可溶性因素(如Ca2+和PO43-)和/或不溶性因素(如其微米级甚至纳米级的形貌特征)与各种蛋白质和细胞相互作用。磷酸钙陶瓷植入后不仅会影响巨噬细胞的活性,还会影响巨噬细胞的表面形态。研究发现,前列腺素E2是炎症期生物材料周围巨噬细胞产生的因子,与在光滑的羟基磷灰石表面培养的细胞相比,巨噬细胞在微粗糙的羟基磷灰石表面可分泌更多的前列腺素E2,这是骨诱导材料所特有的表现[57]。此外,前列腺素E2已被证明对间充质干细胞具有趋化作用,并刺激其成骨分化。CHEN等[58]研究表明,具有不同相组成的磷酸钙陶瓷可通过调节巨噬细胞的极化和功能状态呈现不同的骨诱导能力,具有强骨诱导能力的双相磷酸钙可改善长期炎症并诱导与愈合相关的M2表型以启动骨形成。这些发现不仅有助于深入了解磷酸钙陶瓷参与骨诱导的机制,而且通过赋予生物材料适当的免疫调节能力,有助于组织诱导植入物的设计。因此,微孔磷酸钙陶瓷通过可溶性因素(如Ca2+和PO43-释放)和不溶性因素(如其微米级甚至纳米级的形貌特征)与炎症因子和细胞相互作用,导致相关蛋白(骨形态发生蛋白、细胞黏附蛋白)和炎症因子的吸附,以及各种细胞(单核细胞、间充质干细胞、内皮细胞)的募集,见图4。这一过程可能伴随着磷酸钙的动态溶解/沉淀,以及蛋白质的共沉淀,在磷酸钙表面形成类骨磷灰石层[59]。 "
| [1] BOULER JM, PILET P, GAUTHIER O, et al. Biphasic calcium phosphate ceramics for bone reconstruction: A review of biological response. Acta Biomater. 2017;53:1-12. [2] ZHANG D, ZONG X, GUO X, et al. Influence of different sintering temperatures on mesoporous structure and ectopic osteogenesis of biphasic calcium phosphate ceramic granule materials. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2021;35(1):95-103. [3] HONG Y, FAN H, LI B, et al. Fabrication, biological effects, and medical applications of calcium phosphate nanoceramics. Mater Sci Eng R Rep. 2010;70(3-6):225-242. [4] 刘日旭,吕文波,高文山.磷酸钙骨水泥改性相关研究与临床应用[J].中国组织工程研究,2021,25(34):5537-5543. [5] XIAO D, ZHANG J, ZHANG C, et al. The role of calcium phosphate surface structure in osteogenesis and the mechanisms involved. Acta Biomater. 2020;106:22-33. [6] 周育巧,郭阗廷,许强,等.羟基磷灰石在骨科中应用的研究进展[J].赣南医学院学报,2020,40(10):1068-1072. [7] WU L, ZHOU C, ZHANG B, et al. Construction of Biomimetic Natural Wood Hierarchical Porous-Structure Bioceramic with Micro/Nanowhisker Coating to Modulate Cellular Behavior and Osteoinductive Activity. ACS Appl Mater Interfaces. 2020;12(43):48395-48407. [8] 陈崧,何远丽,谢雯佳,等.磷酸钙纳米颗粒药物递送系统在骨组织工程研究与应用中的优势[J].中国组织工程研究,2021,25(22): 3565-3570. [9] MATSUO A, CHIBA H, TAKAHASHI H, et al. Clinical application of a custom-made bioresorbable raw particulate hydroxyapatite/poly-L-lactide mesh tray for mandibular reconstruction. Odontology. 2010; 98(1):85-88. [10] WANG J, CHEN X, GUO B, et al. A serum protein adsorption profile on BCP ceramics and influence of the elevated adsorption of adhesive proteins on the behaviour of MSCs. J Mater Chem B. 2018;6(45): 7383-7395. [11] LI J, YUAN H, CHANDRAKAR A, et al. 3D porous Ti6Al4V-beta-tricalcium phosphate scaffolds directly fabricated by additive manufacturing. Acta Biomater. 2021;126:496-510. [12] RH OWEN G, DARD M, LARJAVA H. Hydoxyapatite/beta-tricalcium phosphate biphasic ceramics as regenerative material for the repair of complex bone defects. J Biomed Mater Res B Appl Biomater. 2018; 106(6):2493-2512. [13] SAMAVEDI S, WHITTINGTON AR, GOLDSTEIN AS. Calcium phosphate ceramics in bone tissue engineering: a review of properties and their influence on cell behavior. Acta Biomater. 2013;9(9):8037-8045. [14] WANG M, CHEN F, WANG J, et al. Calcium phosphate altered the cytokine secretion of macrophages and influenced the homing of mesenchymal stem cells. J Mater Chem B. 2018;6(29):4765-4774. [15] CHAI YC, CARLIER A, BOLANDER J, et al. Current views on calcium phosphate osteogenicity and the translation into effective bone regeneration strategies. Acta Biomater. 2012;8(11):3876-3887. [16] SANTOS PS, CESTARI TM, PAULIN JB, et al. Osteoinductive porous biphasic calcium phosphate ceramic as an alternative to autogenous bone grafting in the treatment of mandibular bone critical-size defects. J Biomed Mater Res B Appl Biomater. 2018;106(4):1546-1557. [17] MOSHIRI A, TEKYIEH MAROOF N, MOHAMMAD SHARIFI A. Role of organic and ceramic biomaterials on bone healing and regeneration: An experimental study with significant value in translational tissue engineering and regenerative medicine. Iran J Basic Med Sci. 2020; 23(11):1426-1438. [18] 李祖浩,王辰宇,王中汉,等.骨质疏松性骨缺损的治疗进展:支架植入与局部药物递送[J].中国组织工程研究,2018,22(18):2939-2945. [19] JEONG J, KIM JH, SHIM JH, et al. Bioactive calcium phosphate materials and applications in bone regeneration. Biomater Res. 2019;23:4. [20] KIM SE, PARK K. Recent Advances of Biphasic Calcium Phosphate Bioceramics for Bone Tissue Regeneration. Adv Exp Med Biol. 2020; 1250:177-188. [21] LEVINGSTONE TJ, HERBAJ S, DUNNE NJ. Calcium Phosphate Nanoparticles for Therapeutic Applications in Bone Regeneration. Nanomaterials (Basel). 2019;9(11):1570. [22] RIPAMONTI U. Bone induction in nonhuman primates. An experimental study on the baboon. Clin Orthop Relat Res. 1991;(269):284-294. [23] WANG J, CHEN Y, ZHU X, et al. Effect of phase composition on protein adsorption and osteoinduction of porous calcium phosphate ceramics in mice. J Biomed Mater Res A. 2014;102(12):4234-4243. [24] CHEN Y, WANG J, ZHU X, et al. The directional migration and differentiation of mesenchymal stem cells toward vascular endothelial cells stimulated by biphasic calcium phosphate ceramic. Regen Biomater. 2018;5(3):129-139. [25] DENRY I, KUHN LT. Design and characterization of calcium phosphate ceramic scaffolds for bone tissue engineering. Dent Mater. 2016;32(1): 43-53. [26] TANG Z, LI X, TAN Y, et al. The material and biological characteristics of osteoinductive calcium phosphate ceramics. Regen Biomater. 2018; 5(1):43-59. [27] DUAN R, VAN DIJK LA, BARBIERI D, et al. Accelerated bone formation by biphasic calcium phosphate with a novel sub-micron surface topography. Eur Cell Mater. 2019;37:60-73. [28] 陈浩东,姚金凤,梁志刚.磷酸钙的固有骨诱导性及其应用[J].中国组织工程研究,2016,20(25):3785-3792. [29] DIMITRIOU R, JONES E, MCGONAGLE D, et al. Bone regeneration: current concepts and future directions. BMC Med. 2011;9:66. [30] GUO X, JIANG H, ZONG X, et al. The implication of the notch signaling pathway in biphasic calcium phosphate ceramic-induced ectopic bone formation: A preliminary experiment. J Biomed Mater Res A. 2020;108(5):1035-1044. [31] CHEN F, WANG M, WANG J, et al. Effects of hydroxyapatite surface nano/micro-structure on osteoclast formation and activity. J Mater Chem B. 2019;7(47):7574-7587. [32] LUO G, HUANG Y, GU F. rhBMP2-loaded calcium phosphate cements combined with allogenic bone marrow mesenchymal stem cells for bone formation. Biomed Pharmacother. 2017;92:536-543. [33] OTHMAN Z, MOHREN RJC, CILLERO-PASTOR B, et al. Comparative proteomic analysis of human mesenchymal stromal cell behavior on calcium phosphate ceramics with different osteoinductive potential. Mater Today Bio. 2020;7:100066. [34] CHEN Y, WANG J, ZHU XD, et al. Enhanced effect of β-tricalcium phosphate phase on neovascularization of porous calcium phosphate ceramics: in vitro and in vivo evidence. Acta Biomater. 2015;11:435-448. [35] YAO J, LIU Z, MA W, et al. Three-Dimensional Coating of SF/PLGA Coaxial Nanofiber Membranes on Surfaces of Calcium Phosphate Cement for Enhanced Bone Regeneration. ACS Biomater Sci Eng. 2020;6(5):2970-2984. [36] LI Y, JIANG T, ZHENG L, et al. Osteogenic differentiation of mesenchymal stem cells (MSCs) induced by three calcium phosphate ceramic (CaP) powders: A comparative study. Mater Sci Eng C Mater Biol Appl. 2017; 80:296-300. [37] WANG Z, TANG Z, QING F, et al. Applications of calcium phosphate nanoparticles in porous hard tissue engineering scaffolds. NANO. 2012; 7(4):1230004. [38] CHEN Y, SUN Z, LI Y, et al. Preparation and biological effects of apatite nanosheet-constructed porous ceramics. J Mater Chem B. 2017;5(4): 807-816. [39] ZHANG C, ZHANG T, GENG T, et al. Dental Implants Loaded With Bioactive Agents Promote Osseointegration in Osteoporosis: A Review. Front Bioeng Biotechnol. 2021;9:591796. [40] MCMURRAY RJ, GADEGAARD N, TSIMBOURI PM, et al. Nanoscale surfaces for the long-term maintenance of mesenchymal stem cell phenotype and multipotency. Nat Mater. 2011;10(8):637-644. [41] ZAMPARINI F, PRATI C, GENERALI L, et al. Micro-Nano Surface Characterization and Bioactivity of a Calcium Phosphate-Incorporated Titanium Implant Surface. J Funct Biomater. 2021;12(1):3. [42] WANG Z, XIAO Z, FAN H, et al. Fabrication of Micro-grooved Patterns on Hydroxyapatite Ceramics and Observation of Earlier Response of Osteoblasts to the Patterns. J Inorg Mater. 2013;28(1):51-57. [43] REZAEI M, FARHADIAN M, RASHIDI AM, et al. Nano-Biphasic Calcium Phosphate Ceramic for the Repair of Bone Defects. J Craniofac Surg. 2018;29(6):e543-e548. [44] ROOZBAHANI M, ALEHOSSEINI M, KHARAZIHA M, et al. Nano‑calcium phosphate bone cement based on Si-stabilized α-tricalcium phosphate with improved mechanical properties. Mater Sci Eng C Mater Biol Appl. 2017;81:532-541. [45] LI B, CHEN X, GUO B, et al. Fabrication and cellular biocompatibility of porous carbonated biphasic calcium phosphate ceramics with a nanostructure. Acta Biomater. 2009;5(1):134-143. [46] KANG HJ, MAKKAR P, PADALHIN AR, et al. Comparative study on biodegradation and biocompatibility of multichannel calcium phosphate based bone substitutes. Mater Sci Eng C Mater Biol Appl. 2020;110:110694. [47] DOOSTI BA, LOBOVKINA T. Ca2+ Gradient Induces Membrane Bending and Formation of Nanotubes in Giant Lipid Vesicles. Biophys J. 2016; 110(3):584A. [48] MURSHED M, HARMEY D, MILLÁN JL, et al. Unique coexpression in osteoblasts of broadly expressed genes accounts for the spatial restriction of ECM mineralization to bone. Genes Dev. 2005;19(9): 1093-1104. [49] ZHU XD, ZHANG HJ, FAN HS, et al. Effect of phase composition and microstructure of calcium phosphate ceramic particles on protein adsorption. Acta Biomater. 2010;6(4):1536-1541. [50] ZENG J, LIN J, YAO G, et al. Effect of modified compound calcium phosphate cement on the differentiation and osteogenesis of bone mesenchymal stem cells. J Orthop Surg Res. 2017;12(1):102. [51] CHEN X, WANG J, CHEN Y, et al. Roles of calcium phosphate-mediated integrin expression and MAPK signaling pathways in the osteoblastic differentiation of mesenchymal stem cells. J Mater Chem B. 2016;4(13): 2280-2289. [52] SHEKARAN A, GARCÍA AJ. Extracellular matrix-mimetic adhesive biomaterials for bone repair. J Biomed Mater Res A. 2011;96(1):261-272. [53] SALASZNYK RM, KLEES RF, WILLIAMS WA, et al. Focal adhesion kinase signaling pathways regulate the osteogenic differentiation of human mesenchymal stem cells. Exp Cell Res. 2007;313(1):22-37. [54] LU Z, ZREIQAT H. The osteoconductivity of biomaterials is regulated by bone morphogenetic protein 2 autocrine loop involving α2β1 integrin and mitogen-activated protein kinase/extracellular related kinase signaling pathways. Tissue Eng Part A. 2010;16(10):3075-3084. [55] MILLAN C, VIVANCO JF, BENJUMEDA-WIJNHOVEN IM, et al. Mesenchymal Stem Cells and Calcium Phosphate Bioceramics: Implications in Periodontal Bone Regeneration. Adv Exp Med Biol. 2018;1107:91-112. [56] DE MELO PEREIRA D, EISCHEN-LOGES M, BIRGANI ZT, et al. Proliferation and Osteogenic Differentiation of hMSCs on Biomineralized Collagen. Front Bioeng Biotechnol. 2020;8:554565. [57] HUMBERT P, BRENNAN MÁ, DAVISON N, et al. Immune Modulation by Transplanted Calcium Phosphate Biomaterials and Human Mesenchymal Stromal Cells in Bone Regeneration. Front Immunol. 2019;10:663. [58] CHEN X, WANG M, CHEN F, et al. Correlations between macrophage polarization and osteoinduction of porous calcium phosphate ceramics. Acta Biomater. 2020;103:318-332. [59] WANG J, CHEN X, YANG X, et al. Positive role of calcium phosphate ceramics regulated inflammation in the osteogenic differentiation of mesenchymal stem cells. J Biomed Mater Res A. 2020;108(6):1305-1320. |
| [1] | Wen Xinghua, Ding Huanwen, Cheng Kai, Yan Xiaonan, Peng Yuanhao, Wang Yuning, Liu Kang, Zhang Huiwu. Three-dimensional finite element model analysis of intramedullary nailing fixation design for large femoral defects in Beagle dogs [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1371-1376. |
| [2] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [3] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [4] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [5] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [6] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [7] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [8] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| [9] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [10] | Xu Yan, Li Ping, Lai Chunhua, Zhu Peijun, Yang Shuo, Xu Shulan. Piezoelectric materials for vascularized bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1126-1132. |
| [11] | Tao Xin, Xu Yi, Song Zhiwen, Liu Jinbo. Hippo signaling pathway in the regulation of spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(4): 619-625. |
| [12] | Li Shihao, Li Qi, Li Zhen, Zhang Yuanyuan, Liu Miaomiao, Ouyang Yi, Xu Weiguo. Plantar pressure and gait analysis in patients with anterior cruciate ligament injury and reconstruction [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(4): 626-631. |
| [13] | Zhou Jie, Pei Xibo, Wan Qianbing. Advances and biological application of asymmetric dressings [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 434-440. |
| [14] | Chen Jingqiao, Li Ying, Meng Maohua, Xu Xingxing, Wang Qinying, Wang Huan, Lu Jing, Shu Jiayu, Dong Qiang. Research progress in platelet-rich fibrin in stomatology [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 441-446. |
| [15] | Han Tao, Hao Jianqiang, Li Wenbo, Shi Jie, Gao Qiuming. Advantages and problems of antibiotic-loaded bone cements for bone and joint infections [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 470-477. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||