Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (11): 1799-1804.doi: 10.12307/2022.369
Role and mechanism of tetramethylpyrazine in spinal cord injury repair
Jiang Shengyuan, Deng Bowen, Xu Lin, Liu Gang, He Feng, Zhao Yi, Ren Jingpei, Mu Xiaohong
- Dongzhimen Hospital, Beijing University of Chinese Medicine, Beijing 100700, China
-
Received:2021-02-06Revised:2021-02-10Accepted:2021-03-06Online:2022-04-18Published:2021-12-13 -
Contact:Mu Xiaohong, MD, Professor, Chief physician, Doctoral supervisor, Dongzhimen Hospital, Beijing University of Chinese Medicine, Beijing 100700, China -
About author:Jiang Shengyuan, MD candidate, Dongzhimen Hospital, Beijing University of Chinese Medicine, Beijing 100700, China -
Supported by:the National Natural Science Foundation of China, No. 81874467 (to MXH)
CLC Number:
Cite this article
Jiang Shengyuan, Deng Bowen, Xu Lin, Liu Gang, He Feng, Zhao Yi, Ren Jingpei, Mu Xiaohong. Role and mechanism of tetramethylpyrazine in spinal cord injury repair[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(11): 1799-1804.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

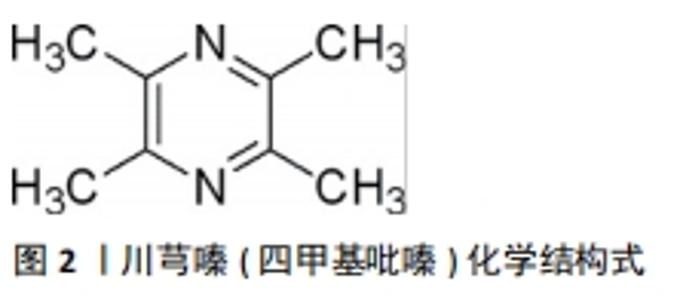
通过结构修饰可与多种化合物结合[18]。盐酸川芎嗪注射液被广泛应用于临床,已被证实具有促进神经再生、诱导神经保护的作用[19]。现代药理学研究证明川芎嗪还具备抗缺血再灌注损伤、抗氧化、抗血栓、抗肿瘤以及镇痛等作用,多用于治疗心脑血管系统、呼吸系统以及肝肾等疾病[20-22]。川芎嗪对于心脏的保护主要体现在其可以抗心肌缺血、保护心肌细胞、抑制心肌收缩、抗心肌肥大等方面[23-24]。QIAN等[25]认为川芎嗪能够通过保护线粒体、改善能量代谢、清除氧自由基以及维持钙离子的动态平衡等多条途径抗心肌缺血再灌注损伤。川芎嗪作为常用的活血化瘀药物,其还具有抑制血小板聚集、扩张血管等作用。CAI等[26]通过实验证明,川芎嗪在病理条件下具有抑制血管纤维化和血栓形成的作用,机制可能与CXCR4表达下调有关。川芎嗪对于多种因素导致的脑和神经损伤亦具有保护作用,TIAN等[27]研究发现,川芎嗪可以通过体外丝裂原活化蛋白激酶途径促进缺氧大鼠脑神经干细胞的增殖和分化。 2.2 川芎嗪在脊髓损伤修复中的临床应用 目前国外文献对川芎嗪在脊髓损伤的临床应用鲜有报道,大多仍停留于动物实验阶段。国内吴贤良等[28]在对72例脊髓损伤患者手术治疗以及常规治疗(甲强龙冲击、甘露醇脱水、神经节苷脂应用)后,给予观察组36例患者连续14 d注射川芎嗪注射液治疗,术后3,6,12个月的运动、感觉功能评分均高于对照组,证明川芎嗪能促进脊髓损伤患者术后运动感觉功能的恢复。黎启福等[29]将56例胸腰段急性脊髓损伤患者分为2组,治疗组术前应用丹参川芎嗪注射液,与对照组相比,治疗组患者术后的神经功能改善有效率大幅提升。俞勇等[30]在治疗脊髓损伤的过程中,术后给予89例患者行高压氧治疗,其中45例患者在此基础上给予丹参川芎嗪注射液治疗,术后2周发现联合组患者脊柱功能恢复指标、凝血指标以及血液流变学等指标均优于对照组,且联合组患者术后早期并发症的发生率明显低于对照组患者,其认为丹参川芎嗪注射液联合高压氧治疗脊髓损伤患者可有效减低术后早期并发症的发生率,对促进患者血液循环、缓解炎症反应均有积极作用。侯建雄等[31]将颈椎骨折合并脊髓损伤的65例患者随机分为2组,治疗组33例患者采用手术联合丹参川芎嗪注射液、甲基泼尼松龙治疗,对照组32例患者仅采用手术联合甲基泼尼松龙治疗,其发现治疗组患者术后不同时间点的运动感觉功能均有明显改善。都芳涛等[32]将90例脊髓损伤非手术患者随机分为2组,分别给予不同剂量川芎嗪注射液治疗后,发现高剂量组患者术后脑脊液中炎性指标(肿瘤坏死因子α、白细胞介素1β)mRNA的表达以及运动感觉功能评分均优于低剂量组,因此其认为川芎嗪可能通过影响脑脊液中的炎症因子的表达促进脊髓损伤的恢复,且与川芎嗪的剂量具有相关性。 上述报道虽一定程度上可以说明川芎嗪在促进脊髓损伤恢复方面有疗效,但也存在局限性:患者脊髓损伤程度、手术方式等均可以影响研究结果,且大多数学者采用丹参川芎嗪注射液,无法单独证明川芎嗪的疗效。目前临床使用川芎嗪单体注射液治疗脊髓损伤的报道较少,究其原因,无外乎于目前的动物实验尚未完全阐明川芎嗪在脊髓损伤修复过程中的机制。因此,川芎嗪的临床疗效仍有待于进一步探究。 2.3 川芎嗪修复脊髓损伤的机制 2.3.1 改善微循环障碍 脊髓损伤后微环境破坏,包括血管变化如出血、血管痉挛、血栓形成、血脑屏障破坏等,这些反应可引起脊髓组织水肿、缺血缺氧和坏死[33-34]。目前发现,缺血是导致继发性脊髓损伤的重要因素。引起脊髓损伤初期持续性缺血的机制主要包括内皮素生成增多、血管内皮细胞凋亡、细胞内钙离子超载等。 (1)抑制内皮素生成:脊髓组织缺乏侧支循环,循环血流量少,对缺血缺氧耐受性差,损伤后极易发生血管痉挛。内皮素存在于脊髓、心脏等多种器官组织中,是目前发现的作用最强、持续最久的缩血管多肽,在脊髓损伤过程中发挥重要作用[35]。有学者认为,内皮素1的下调可改善脊髓组织的缺血反应,从而减少氧化应激和细胞凋亡[36]。PETERS 等[37]发现,阻断脊髓损伤后血管内皮素受体及星形胶质细胞内内皮素的受体,可以降低出血及星形胶质细胞增殖的概率,从而增加神经元的存活率。李洋[38]在研究川芎嗪对脊髓损伤微循环影响的实验中发现,随着时间推移,脊髓损伤大鼠全血低、中、高切黏度均增高,提示微循环障碍;当给予川芎嗪干预后,大鼠的血液流变学、行为学指标均明显改善,受损脊髓组织中内皮素的含量也相应降低;其认为内皮素在继发性脊髓损伤过程中扮演重要角色,川芎嗪可抑制内皮素的产生,从而达到扩张血管、改善微循环的作用。 (2)抑制血管内皮细胞凋亡:正常脊髓组织内的血管管壁成分包括血管内皮细胞、基膜、周细胞及星形胶质细胞足突等,共同构成血脊髓屏障[39]。脊髓损伤会导致血管内皮细胞凋亡,进一步引起血脊髓屏障通透性增加,炎性细胞大量浸润,加剧微血管的继发性损伤[40]。完整的血管结构是血脊髓屏障发挥正常功能的前提,既往研究发现,在脊髓损伤初期,血管内皮细胞数量会暂时性增加,预示着新生血管的生成[41]。虽然这种现象是短暂的,但对于缓解脊髓损伤后血流灌注不足、改善局部代谢仍具有一定的作用。 李东哲[42]通过实验发现,对脊髓损伤大鼠注射川芎嗪后,实验组术后不同时间点的内皮细胞凋亡数目均低于对照组,其认为川芎嗪可抑制急性脊髓损伤后血管内皮细胞的凋亡,同时提高微血管的密度。HU等[43]通过对脊髓损伤大鼠注射川芎嗪后发现血管内皮细胞凋亡明显减少,随后其利用MicroCT扫描发现川芎嗪组脊髓组织内血管数量、血管体积分数、血管连续性等指标均优于对照组,从而证明川芎嗪可通过抑制内皮细胞的凋亡促进新生血管生成。在脑和脊髓损伤中,基质金属蛋白酶尤其是基质金属蛋白酶2和9在维持血脑屏障和血脊髓屏障的完整性方面起主导作用[44]。HU等[45]在随后的研究中发现,川芎嗪可通过下调基质金属蛋白酶2、基质金属蛋白酶9蛋白的表达,抑制血管内皮细胞凋亡,促进血管生成,从而减轻神经损伤。 脊髓损伤通常会导致局部氧代谢异常,缺氧诱导因子1α是缺氧微环境中的关键因子,能有效刺激下游血管内皮生长因子的合成,特异性地促进血管内皮细胞增殖与新生血管形成[46]。吴天定[47]在川芎嗪治疗脊髓损伤的实验过程中发现,缺氧诱导因子1α/血管内皮生长因子低氧代谢途径参与脊髓损伤后的血管修复,川芎嗪能够改善脊髓损伤后的低氧环境,但川芎嗪的促血管再生作用与缺氧诱导因子1α介导的血管内皮生长因子增高无关,可能存在其他通路。有学者认为川芎嗪可通过Fas-FasL途径增强小鼠微血管细胞系中血管内皮生长因子与碱性成纤维细胞生长因子的表达[48],同时调控缺氧诱导因子1α蛋白[49],诱导内皮细胞增殖与血管新生。YANG等[50]认为川芎嗪可抑制Rho/ROCK信号通路,下调RhoA与Racl表达,调控内皮型一氧化氮合酶与活性氧,减少对脑微血管内皮细胞的损伤。但上述两种机制是否存在于脊髓损伤的修复过程中尚未可知,仍需进一步的研究加以证明。 (3)拮抗钙离子内流:脊髓损伤后,血清中Ca2+浓度升高致使细胞内外Ca2+浓度梯度增大,进一步导致Ca2+内流。细胞内Ca2+不仅可与线粒体结合影响能量代谢,还能够激活细胞膜上的蛋白酶,产生大量病理性自由基参与脂质过氧化,进而引起血管痉挛、闭塞,导致微循环障碍[51]。蔡卫华等[52]研究发现,脊髓损伤后内皮素1与细胞内Ca2+浓度均维持在较高的水平,其认为二者共同参与了继发性脊髓损伤,内皮素1可通过多种途径促进Ca2+的内流。川芎嗪抑制脊髓损伤后内皮素的生成已在前文描述,既往的研究还发现,川芎嗪还可以通过调节Ca2+ /钙调蛋白/钙调蛋白激酶Ⅱβ抑制Ca2+ 内流,进而起到舒张血管的作用[53]。李洋[38]认为,川芎嗪可拮抗钙离子的内流,可防止细胞内Ca2+超载,对血管平滑肌有松弛效应。孙海燕等[54]研究发现,给予脊髓损伤大鼠注射川芎嗪后,脊髓组织内Ca2+浓度升高,进而印证川芎嗪可拮抗Ca2+内流,阻止细胞内钙超载所引起的一系列病理反应。 综上所述,急性脊髓损伤所引发局部微循环障碍是导致脊髓继发性损伤的重要原因,川芎嗪具有活血行气之功效,被广泛用于心脑血管等缺血性疾病的治疗。川芎嗪改善脊髓损伤微循环障碍的机制主要可以归纳为以下几点:①抑制内皮素产生,防止血小板聚集,降低血液黏度,扩张血管,改善缺血区域的血液供应;②促进血管内皮生长因子等血管新生蛋白表达,抑制血管内皮细胞凋亡,调控血脊髓屏障通透性;③调控细胞内外Ca2+浓度,防止血管收缩痉挛。 2.3.2 调控炎症反应 脊髓损伤后的炎症反应属于一把“双刃剑”,其益害取决于时间点和免疫细胞的激活状态[55]。脊髓损伤后的炎症反应主要涉及神经及免疫两大系统[56],多由浸润至损伤部位的中性粒细胞、巨噬细胞、小胶质细胞、星形胶质细胞等启动[57]。炎症反应的急性期以中性粒细胞、单核细胞浸润至损伤区域为特征,慢性期主要为淋巴细胞介导,神经胶质细胞对脊髓损伤反应迅速,在数小时内即可上调炎性因子表达[58-59]。其中介导脊髓损伤的炎性细胞因子主要包括肿瘤坏死因子α、白细胞介素、一氧化氮以及趋化因子等[60]。目前对于川芎嗪调控脊髓损伤后炎症反应的研究主要集中于相关信号通路及炎性细胞因子的表达。 (1)调节白细胞介素:白细胞介素在传递信息、激活与调节免疫细胞、介导T、B淋巴细胞活化以及在炎症反应中作用显著。李晓明[61]研究发现,脊髓损伤大鼠注射川芎嗪后,体内白细胞介素10、白细胞介素18的表达量分别增加和减少,其认为川芎嗪可通过抑制促炎细胞因子、促进抑炎因子表达而恢复脊髓损伤后的神经功能。WANG等[62]研究发现,川芎嗪可通过Akt/Nrf2/HO-1通路改善脊髓损伤大鼠运动功能,同时可降低促炎细胞因子白细胞介素1β、白细胞介素18以及肿瘤坏死因子α的表达。信号转导与转录激活因子3(signal transducer and activator of transcription 3,STAT3)的异常激活能够促进白细胞介素17的分泌[63]。张男等[64]通过实验发现,川芎嗪可有效抑制脊髓损伤后STAT3磷酸化及白细胞介素17的表达,其认为这可能是促进脊髓恢复的机制之一。SHIN等[65]通过夹压法制作脊髓损伤小鼠模型,术前30 min给予实验组川芎嗪注射,发现川芎嗪治疗可降低脊髓损伤4 h后脊髓组织中白细胞介素1β mRNA的上调,同时川芎嗪对脊髓损伤48 h后的小胶质细胞激活和中性粒细胞浸润也有明显的抑制作用。 (2)抑制核因子κB(nuclear factor kappa-B,NF-κB) 信号通路:IKK/NF-кB通路参与脊髓损伤后炎症反应及细胞凋亡的调控,神经元和胶质细胞中NF-κB的异常激活,可使NF-κB 依赖的促炎细胞因子和趋化因子上调,导致炎症细胞浸润、神经元凋亡和胶质瘢痕形成,加重继发性损伤[66]。IκB 激酶抑制剂(IKK) 是NF-κB 的激活物,由IKKα、IKKβ和IKKγ组成[67]。HU等[68]认为川芎嗪不仅能够调控脊髓损伤后白细胞介素10、白细胞介素18的表达,还可促进I-κBα的表达,抑制巨噬细胞移动抑制因子(MIF)、NF-κB的表达,并且其认为川芎嗪降低NF-κB转录活性的机制可能是通过抑制巨噬细胞移动抑制因子表达而增加I-κBα的表达。ZHANG等[69]在进行自身免疫性脑脊髓膜炎的实验中发现,川芎嗪通过激活STAT3/SOCS3和抑制NF-кB信号通路来调节小胶质细胞从M1表型向M2表型的极化,从而保护血脊髓屏障的完整性,此外,川芎嗪减少了BV2小胶质细胞的促炎细胞因子(肿瘤坏死因子α,白细胞介素1β)的分泌,增加了抗炎细胞因子(白细胞介素4,白细胞介素10)的分泌。基于上述研究,作者推测:川芎嗪调节炎症反应的机制主要是通过抑制NF-кB信号通路进而抑制促炎细胞因子的表达。 (3)抑制中性粒细胞浸润:中性粒细胞在脊髓损伤24 h内即可迅速浸润至损伤部位,进而介导炎症反应[70]。髓过氧化物酶是一种血红素蛋白,外界刺激可导致中性粒细胞聚集,从而释放髓过氧化物酶。FAN等[71]在进行脊髓缺血再灌注的实验中发现,川芎嗪可抑制NF-κB、上调白细胞介素10等抗炎因子以及下调白细胞介素1β等促炎因子,还发现脊髓组织中的髓过氧化物酶活性在缺血再灌注损伤的反应中显著增加,而川芎嗪治疗明显降低了损伤区域髓过氧化物酶的活性,这表明川芎嗪在缺血再灌注损伤过程中可保护脊髓免受中性粒细胞的浸润。中性粒细胞释放的中性粒细胞弹性蛋白酶(NE)参与了中性粒细胞的迁移,促进白细胞介素2、白细胞介素6的表达,加重炎症反应。黎俊豪[72]发现,川芎嗪能够减少大鼠急性脊髓损伤后损伤部位中性粒细胞弹性蛋白酶的含量,其认为中性粒细胞弹性蛋白酶可上调促炎因子如肿瘤坏死因子α、NF-κB的表达,抑制中性粒细胞弹性蛋白酶可减轻炎症反应所带来的继发性损伤。 综上所述,炎症反应在脊髓继发性损伤中起重要作用。免疫细胞和神经胶质细胞所分泌的细胞因子具有浓度低、活性高、与特异性受体结合介导炎症反应等特点,如何调控抗炎细胞因子与促炎细胞因子的比例是治疗脊髓损伤的关键。基于以往的研究结果,川芎嗪对于脊髓损伤后炎症反应的调控,主要是通过NF-кB信号通路来调节白细胞介素、肿瘤坏死因子等相关炎症因子完成的,至于其他信号通路是否参与了炎症反应的发生与发展,尚需进一步的实验来验证。 2.3.3 抑制神经细胞凋亡 脊髓损伤后组织内部出血、水肿引发神经元细胞凋亡,神经轴突断裂致使神经传导中断,神经系统功能受到不同程度破坏,此为脊髓损伤后主要的病理改变。如何有效减少神经细胞凋亡的数量及速度,成为修复脊髓损伤待解决的问题之一[73]。近年来研究发现,川芎嗪在脊髓损伤后可通过不同途径抑制神经细胞的凋亡。 天冬氨酸特异性半胱氨酸蛋白酶(Caspase)为Ca2+依赖性蛋白酶,目前的研究已证明急性脊髓损伤后Caspase可诱导神经细胞凋亡[74]。Caspase-3的激活在脊髓损伤后诱导神经细胞凋亡的执行过程中起重要作用,是多种凋亡途径的共同下游效应部分[75]。沈正祥等[76]发现经川芎嗪治疗的脊髓损伤大鼠术后各个时间点Caspase-3表达均下降,在术后第7天达到最低值;同时,神经丝蛋白作为神经元细胞的结构蛋白表达增加,且与Caspase-3的表达呈负相关,因此,其认为川芎嗪可通过调节Caspase-3的表达量抑制神经细胞凋亡。王圣轩[77]在脊髓损伤的实验中发现,川芎嗪注射组术后不同时间点Caspase-8酶活力单位浓度以及Fas相关死亡域蛋白(Fas-associated death domin protein,FADD)的表达均低于对照组,其认为川芎嗪可通过抑制相关促细胞凋亡基因修复脊髓损伤。王健等[78]通过流式细胞术发现大鼠脊髓损伤后6 h内即出现神经细胞凋亡,损伤区域Caspase-3 mRNA的水平明显升高,且与细胞凋亡的比例、细胞超微结构的变化具有一定相关性,其认为早期使用川芎嗪可通过抑制Caspase-3的表达而抑制神经细胞的凋亡。 bcl-2基因家族与细胞凋亡进程联系密切,研究发现Bcl-2蛋白有抑制细胞凋亡的作用,而Bax蛋白与其拮抗,形成了细胞凋亡的正负控制[79]。孙海燕[80]研究发现川芎嗪可促进脊髓损伤后bcl-2基因的表达以及蛋白产物的增加,抑制Bax蛋白,同时存活神经元细胞的数量与Bcl-2蛋白的变化成正相关。FAN等[81]在脊髓缺血再灌注损伤的研究中发现,川芎嗪对兔模型脊髓缺血再灌注损伤具有较强的保护作用,并通过上调Bcl-2水平与下调Bax水平降低凋亡细胞的比例。这一结论与孙海燕等的研究结果相一致。研究通过川芎嗪联合骨髓间充质干细胞治疗脊髓损伤大鼠发现,与单纯骨髓间充质干细胞移植组相比,实验组Bcl-2、碱性成纤维细胞生长因子的基因表达量明显升高,神经椎体细胞数目亦明显增加,其认为川芎嗪可产生抑制损伤区神经细胞凋亡的有利微环境。有学者认为miR-214-3p是脊髓损伤中的促凋亡因子,它直接靶向bcl-2 mRNA,导致Bcl-2蛋白降解,进而加速脊髓内神经元细胞凋亡,川芎嗪可通过抑制MiR-214-3p水平、增加Bcl-2的表达水平抑制神经细胞凋亡[82]。 除上述机制外,川芎嗪亦可通过其他途径调控细胞凋亡相关基因。神经营养因子包括脑源性神经营养因子、神经生长因子、神经营养素3等,此类蛋白质分子不仅能够促进神经细胞增殖分化,还能够保护神经元细胞,维持其正常功 能[83]。周赟等[84]的实验证明川芎嗪干预脊髓损伤大鼠后,术后神经元细胞存活数量明显增多,相关神经营养因子的表达也增多,其认为川芎嗪对神经元细胞的保护作用是通过提高神经营养因子的表达而实现的。黄江湖[85]通过实验发现,大鼠急性脊髓损伤后miRNA的表达谱发生变化,其中miRNA-21在损伤3 d时表达量异常升高,且miRNA-21具有抗凋亡作用。miRNA可以单项调节上百种mRNA的表达,通过调节单个miRNA可以达到“单击多靶”的效果。其进一步验证了神经细胞的凋亡与miRNA-21下游促凋亡靶基因FasL、PTEN、PDCD4等有关,故而得出结论:川芎嗪可通过提高miRNA-21的表达、降低相关促凋亡基因表达抑制神经细胞凋亡。 综上所述,脊髓损伤后抑制神经细胞凋亡、促进内源性神经干细胞向神经元分化是恢复神经功能的关键。川芎嗪可通过保护线粒体功能、提高细胞膜Na+-K+-ATP酶的活性、降低脂质过氧化反应、抑制有害蛋白在基因转录水平的表达,在亚细胞水平抑制神经细胞凋亡。除此之外,其还能够促进相关神经营养因子的表达,促进神经细胞增殖分化,进而使得轴突再生,恢复神经功能。"

| [1] ASHAMMAKHI N, KIM HJ, EHSANIPOUR A, et al. Regenerative Therapies for Spinal Cord Injury. Tissue Eng Part B Rev. 2019;25(6):471-491. [2] COWAN H, LAKRA C, DESAI M. Autonomic dysreflexia in spinal cord injury. BMJ. 2020;371:m3596. [3] Karsy M, Hawryluk G. Modern Medical Management of Spinal Cord Injury. Curr Neurol Neurosci Rep. 2019;19(9):65. [4] OYINBO CA. Secondary injury mechanisms in traumatic spinal cord injury: a nugget of this multiply cascade. Acta Neurobiol Exp (Wars). 2011;71(2):281-299. [5] ALIZADEH A, DYCK SM, KARIMI-ABDOLREZAEE S. Traumatic Spinal Cord Injury: An Overview of Pathophysiology, Models and Acute Injury Mechanisms. Front Neurol. 2019;10:282. [6] ANWAR MA, AL SHEHABI TS, EID AH. Inflammogenesis of Secondary Spinal Cord Injury. Front Cell Neurosci. 2016;10:98. [7] SHIMIZU EN, SEIFERT JL, JOHNSON KJ, et al. Prophylactic Riluzole Attenuates Oxidative Stress Damage in Spinal Cord Distraction. J Neurotrauma. 2018;35(12):1319-1328. [8] DYCK S, KATARIA H, ALIZADEH A, et al. Perturbing chondroitin sulfate proteoglycan signaling through LAR and PTPσ receptors promotes a beneficial inflammatory response following spinal cord injury. J Neuroinflammation. 2018;15(1):90. [9] SODERBLOM C, LUO X, BLUMENTHAL E, et al. Perivascular fibroblasts form the fibrotic scar after contusive spinal cord injury. J Neurosci. 2013;33(34):13882-13887. [10] SANDEAN D. Management of acute spinal cord injury: A summary of the evidence pertaining to the acute management, operative and non-operative management. World J Orthop. 2020;11(12):573-583. [11] LI J, LIU G, ZHENG Y, et al. The epidemiological survey of acute traumatic spinal cord injury (ATSCI) of 2002 in Beijing municipality. Spinal Cord. 2011;49(7):777-782. [12] YANG R, GUO L, HUANG L, et al. Epidemiological Characteristics of Traumatic Spinal Cord Injury in Guangdong, China. Spine. 2017; 42(9):E555-E561. [13] ZHENG Y, QI S, WU F, et al. Chinese Herbal Medicine in Treatment of Spinal Cord Injury: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Am J Chin Med. 2020;48(7):1593-1616. [14] LU Y, YANG J, WANG X, et al. Research progress in use of traditional Chinese medicine for treatment of spinal cord injury. Biomed Pharmacother. 2020;127:110136. [15] 韩炜.川芎的化学成分与药理作用研究进展[J].中国现代中药, 2017,19(9):1341-1349. [16] KOUSHKI D, LATIFI S, NOROUZI JAVIDAN A, et al. Efficacy of some non-conventional herbal medications (sulforaphane, tanshinone IIA, and tetramethylpyrazine) in inducing neuroprotection in comparison with interleukin-10 after spinal cord injury: A meta-analysis. J Spinal Cord Med. 2015;38(1):13-22. [17] HU JZ, WANG XK, CAO Y, et al. Tetramethylpyrazine Facilitates Functional Recovery after Spinal Cord Injury by Inhibiting MMP2, MMP9, and Vascular Endothelial Cell Apoptosis. Curr Neurovasc Res. 2017;14(2):110-116. [18] 姜宇懋,王丹巧.川芎嗪药理作用研究进展[J].中国现代中药, 2016,18(10):1364-1370. [19] ZHAO Y, LIU Y, CHEN K. Mechanisms and Clinical Application of Tetramethylpyrazine (an Interesting Natural Compound Isolated from Ligusticum Wallichii): Current Status and Perspective. Oxid Med Cell Longev. 2016;2016:2124638. [20] DING Y, DU J, CUI F, et al. The protective effect of ligustrazine on rats with cerebral ischemia-reperfusion injury via activating PI3K/Akt pathway. Hum Exp Toxicol. 2019;38(10):1168-1177. [21] ZHANG H, DING S, XIA L. Ligustrazine inhibits the proliferation and migration of ovarian cancer cells via regulating miR-211. Biosci Rep. 2021;41(1):BSR20200199. [22] JIANG G, XIN R, YUAN W, et al. Ligustrazine ameliorates acute kidney injury through downregulation of NOD2 mediated inflammation. Int J Mol Med. 2020;45(3):731-742. [23] REN Z, MA J, ZHANG P, et al. The effect of ligustrazine on L-type calcium current, calcium transient and contractility in rabbit ventricular myocytes. J Ethnopharmacol. 2012;144(3):555-561. [24] YU L, SHE T, LI M, et al. Tetramethylpyrazine inhibits angiotensin II-induced cardiomyocyte hypertrophy and tumor necrosis factor-α secretion through an NF-κB-dependent mechanism. Int J Mol Med. 2013;32(3):717-722. [25] QIAN W, XIONG X, FANG Z, et al. Protective effect of tetramethylpyrazine on myocardial ischemia-reperfusion injury. Evid Based Complement Alternat Med. 2014;2014:107501. [26] CAI X, CHEN Z, PAN X, et al. Inhibition of angiogenesis, fibrosis and thrombosis by tetramethylpyrazine: mechanisms contributing to the SDF-1/CXCR4 axis. PLoS One. 2014;9(2):e88176. [27] TIAN Y, LIU Y, CHEN X, et al. Tetramethylpyrazine promotes proliferation and differentiation of neural stem cells from rat brain in hypoxic condition via mitogen-activated protein kinases pathway in vitro. Neurosci Lett. 2010;474(1):26-31. [28] 吴贤良,王小勇,黄建军.川芎嗪对急性脊髓损伤患者术后神经功能恢复的影响[J].山东医药,2019,59(29):67-69. [29] 黎启福,赵金平,王宏新,等.丹参川芎嗪注射液联合甲基泼尼松龙治疗胸腰段急性脊髓损伤[J].齐齐哈尔医学院学报,2012,33(4): 450-451. [30] 俞勇,陈明,彭爱明,等.丹参川芎嗪注射液联合高压氧对急性脊髓损伤早期并发症的预防作用[J].中国药房,2018,29(2):244-247. [31] 侯建雄,马海燕,李莉.手术配合丹参川芎嗪、甲基泼尼松龙治疗颈椎骨折伴脊髓损伤的临床观察[J].河北医药,2013,35(14):2110-2112. [32] 都芳涛,方继峰,李兴晶,等.不同剂量川芎嗪治疗脊髓损伤的临床效果比较[J].中国医药,2019,14(10):1511-1514. [33] TRAN AP, WARREN PM, SILVER J. The Biology of Regeneration Failure and Success After Spinal Cord Injury. Physiol Rev. 2018;98(2):881-917. [34] FAN B, WEI Z, YAO X, et al. Microenvironment Imbalance of Spinal Cord Injury. Cell Transplant. 2018;27(6):853-866. [35] GUO J, LI Y, HE Z, et al. Targeting endothelin receptors A and B attenuates the inflammatory response and improves locomotor function following spinal cord injury in mice. Int J Mol Med. 2014;34(1):74-82. [36] A JC, LI ZY, LONG QF, et al. MiR-379-5p improved locomotor function recovery after spinal cord injury in rats by reducing endothelin 1 and inhibiting astrocytes expression. Eur Rev Med Pharmacol Sci. 2019; 23(22):9738-9745. [37] PETERS CM , ROGERS SD , POMONIS JD, et al. Endothelin receptor expression in the normal and injured spinal cord: potential involvement in injury-induced ischemia and gliosis.Exp Neurol. 2003;180(1):1-13. [38] 李洋. 川芎嗪对大鼠脊髓急性损伤段微循环影响的实验性研究[D].长沙:中南大学,2007. [39] BARTANUSZ V, JEZOVA D, ALAJAJIAN B, et al. The blood-spinal cord barrier: morphology and clinical implications. Ann Neurol. 2011;70(2): 194-206. [40] JIN LY, LI J, WANG KF, et al. The blood-spinal cord barrier in spinal cord injury: a review. J Neurotrauma. 2021 Feb 16. doi: 10.1089/neu. 2020.7413. [41] 魏正军,朱涛,江荣才,等.脊髓损伤大鼠内皮祖细胞与脊髓血管新生[J].中国组织工程研究,2012,16(36):6774-6778. [42] 李东哲.川芎嗪对大鼠急性脊髓损伤后微血管及胶原成分的影响[D].长沙:中南大学,2014. [43] HU J, CAO Y, WU T, et al. Micro-CT as a Tool to Investigate the Efficacy of Tetramethylpyrazine in a Rat Spinal Cord Injury Model. Spine. 2016; 41(16):1272-1278. [44] REMPE RG, HARTZ AMS, BAUER B. Matrix metalloproteinases in the brain and blood-brain barrier: Versatile breakers and makers. J Cereb Blood Flow Metab. 2016;36(9):1481-1507. [45] HU JZ, WANG XK, CAO Y, et al. Tetramethylpyrazine Facilitates Functional Recovery after Spinal Cord Injury by Inhibiting MMP2, MMP9, and Vascular Endothelial Cell Apoptosis. Curr Neurovasc Res. 2017;14(2):110-116. [46] APTE RS, CHEN DS, FERRARA N. VEGF in Signaling and Disease: Beyond Discovery and Development. Cell. 2019;176(6):1248-1264. [47] 吴天定. 川芎嗪对大鼠急性脊髓损伤后血管再生的作用及相关机制的研究[D].长沙:中南大学,2012. [48] ZHANG M, GAO F, TENG F, et al. Tetramethylpyrazine promotes the proliferation and migration of brain endothelial cells. Mol Med Rep. 2014;10(1):29-32. [49] LIANG X, ZHOU H, DING Y, et al. TMP prevents retinal neovascularization and imparts neuroprotection in an oxygen-induced retinopathy model. Invest Ophthalmol Vis Sci. 2012;53(4):2157-2169. [50] YANG G, QIAN C, WANG N, et al. Tetramethylpyrazine Protects Against Oxygen-Glucose Deprivation-Induced Brain Microvascular Endothelial Cells Injury via Rho/Rho-kinase Signaling Pathway. Cell Mol Neurobiol. 2017;37(4):619-633. [51] 刘如春. 电针对急性脊髓损伤大鼠差异表达基因及钙离子作用的实验研究[D].北京:北京中医药大学,2007. [52] 蔡卫华,叶晓健,谭炳毅,等.急性脊髓损伤后内皮素-1与Ca~ (2+)含量的变化关系的研究[J].中国矫形外科杂志,2004,12(20):1568-1570. [53] LU D, SHAO HT, GE WP, et al. Ginsenoside-Rb1 and tetramethylpyrazine phosphate act synergistically to prevent dilated cardiomyopathy in cTnTR141W transgenic mice. J Cardiovasc Pharmacol. 2012;59(5):426-433. [54] 孙海燕,贾连顺,陈宣维,等.川芎嗪对大鼠脊髓损伤段电解质、水含量改变的保护作用[J].中国中医骨伤科杂志,2005,13(2):4-6. [55] MIRON VE, FRANKLIN RJ. Macrophages and CNS remyelination. J Neurochem. 2014;130(2):165-171. [56] 王涛丽,顾兵,李华南,等.急性脊髓损伤后的炎症反应及其抗炎治疗[J].中国药理学通报,2015,31(4):452-457. [57] DONNELLY DJ, POPOVICH PG. Inflammation and its role in neuroprotection, axonal regeneration and functional recovery after spinal cord injury. Exp Neurol. 2008;209(2):378-388. [58] 王明,陈铁戈,杨新乐,等.脊髓损伤炎症反应的研究进展[J].解放军医学院学报,2018,39(8):723-726. [59] JONES TB, MCDANIEL EE, POPOVICH PG. Inflammatory-mediated injury and repair in the traumatically injured spinal cord. Curr Pharm Des. 2005;11(10):1223-1236. [60] ULNDREAJ A, CHIO JC, AHUJA CS, et al. Modulating the immune response in spinal cord injury. Expert Rev Neurother. 2016;16(10): 1127-1129. [61] 李晓明. 川芎嗪对大鼠急性脊髓损伤模型IL-10、IL-18表达的影响[D].长沙:中南大学,2008. [62] WANG C, WANG P, ZENG W, et al. Tetramethylpyrazine improves the recovery of spinal cord injury via Akt/Nrf2/HO-1 pathway. Bioorg Med Chem Lett. 2016;26(4):1287-1291. [63] SU X, YE J, HSUEH EC, et al. Tumor microenvironments direct the recruitment and expansion of human Th17 cells. J Immunol. 2010; 184(3):1630-1641. [64] 张男,赵茗,孙亚澎.川芎嗪对大鼠脊髓损伤后运动功能恢复的影响及机制[J].中国医科大学学报,2015,44(1):60-63. [65] SHIN JW, MOON JY, SEONG JW, et al. Effects of tetramethylpyrazine on microglia activation in spinal cord compression injury of mice. Am J Chin Med. 2013;41(6):1361-1376. [66] HAN X, LU M, WANG S, et al. Targeting IKK/NF-κB pathway reduces infiltration of inflammatory cells and apoptosis after spinal cord injury in rats. Neurosci Lett. 2012;511(1):28-32. [67] 周小珏,赵小华,张安仁.脊髓损伤炎症中的NF-кB信号通路[J].中国生物化学与分子生物学报,2020,36(10):1159-1164. [68] HU JZ, HUANG JH, XIAO ZM, et al. Tetramethylpyrazine accelerates the function recovery of traumatic spinal cord in rat model by attenuating inflammation. J Neurol Sci. 2013;324(1-2):94-99. [69] ZHANG L, LU X, GONG L, et al. Tetramethylpyrazine Protects Blood-Spinal Cord Barrier Integrity by Modulating Microglia Polarization Through Activation of STAT3/SOCS3 and Inhibition of NF-кB Signaling Pathways in Experimental Autoimmune Encephalomyelitis Mice. Cell Mol Neurobiol. 2020;10.1007/s10571-020-00878-3. [70] NEIRINCKX V, COSTE C, FRANZEN R, et al. Neutrophil contribution to spinal cord injury and repair. J Neuroinflammation. 2014;11:150. [71] FAN L, WANG K, SHI Z, et al. Tetramethylpyrazine protects spinal cord and reduces inflammation in a rat model of spinal cord ischemia-reperfusion injury. J Vasc Surg. 2011;54(1):192-200. [72] 黎俊豪. 川芎嗪对大鼠急性脊髓损伤模型P-选择素、中性粒细胞弹性蛋白酶表达的影响[D].长沙:中南大学,2009. [73] 刘建敏,王福川,周亚净,等.电针刺激对脊髓挫伤模型大鼠神经细胞凋亡的影响[J].中国组织工程研究,2016,20(5):616-621. [74] 孙正义,赵斌,洪光祥,等.大鼠脊髓慢性压迫及减压后神经细胞凋亡及其相关基因的表达[J].中国脊柱脊髓杂志,2003,13(3):33-36+63. [75] Wu B, Liang J. Pectolinarigenin promotes functional recovery and inhibits apoptosis in rats following spinal cord injuries. Exp Ther Med. 2019;17(5):3877-3882. [76] 沈正祥,吕红斌,李小明,等.川芎嗪对大鼠急性脊髓损伤模型caspase-3和NF表达的影响[J].中南大学学报(医学版),2008, 33(8):693-699. [77] 王圣轩. 川芎嗪对大鼠急性脊髓损伤模型中FADD表达及Caspase-8活性的影响[D].长沙:中南大学,2009. [78] 王健,贾玉柱,郑纯威,等.川芎嗪对急性脊髓损伤大鼠神经细胞早期凋亡和Caspase-3mRNA表达的影响[J].中华中医药学刊, 2011,29(12):2662-2668. [79] ZHU N, RUAN J, YANG X, et al. Triptolide improves spinal cord injury by promoting autophagy and inhibiting apoptosis. Cell Biol Int. 2020; 44(3):785-794. [80] 孙海燕. 川芎嗪对大鼠脊髓继发性损伤神经保护作用及机制的研究[D].上海:第二军医大学,2004. [81] FAN LH, WANG KZ, CHENG B, et al. Anti-apoptotic and neuroprotective effects of Tetramethylpyrazine following spinal cord ischemia in rabbits. BMC Neurosci. 2006;7:48. [82] Fan Y, Wu Y. Tetramethylpyrazine alleviates neural apoptosis in injured spinal cord via the downregulation of miR-214-3p. Biomed Pharmacother. 2017;94:827-833. [83] Bhattacharyya S, Dinda A, Vishnubhatla S, et al. A combinatorial approach to modulate microenvironment toward regeneration and repair after spinal cord injury in rats. Neurosci Lett. 2021;741:135500. [84] 周赟,胡建中,吕红斌,等.川芎嗪对脊髓急性损伤大鼠神经营养因子表达的影响[J].现代中西医结合杂志,2010,19(9):1058-1060. [85] 黄江湖. MicroRNA-21在急性脊髓损伤中的作用及川芎嗪的抗凋亡作用机制研究[D].长沙:中南大学,2013. |
| [1] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhou Qian, Zhang Qiang, Chen Qiu. Human salivary components and osteoporosis/osteopenia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1439-1444. |
| [2] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| [3] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| [4] | Li Zhiyi, He Pengcheng, Bian Tianyue, Xiao Yuxia, Gao Lu, Liu Huasheng. Bibliometric and visualized analysis of ferroptosis mechanism research [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1202-1209. |
| [5] | Yang Shenglin, Pu Xingwei, Luo Chunshan, Yang Jianwen. Neuroprotective effects of tetrandrine preconditioning in rabbits with spinal cord ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1223-1227. |
| [6] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [7] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [8] | Tang Wenjing, Wu Siyuan, Yang Chen, Tao Xi. Inflammatory responses in post-stroke depression [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1278-1285. |
| [9] | Kan Houming, Fan Lijun, Chen Xuetai, Shen Wen. Application of platelet-rich plasma in neuropathic pain [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1286-1292. |
| [10] | Guo Jia, Ding Qionghua, Liu Ze, Lü Siyi, Zhou Quancheng, Gao Yuhua, Bai Chunyu. Biological characteristics and immunoregulation of exosomes derived from mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1093-1101. |
| [11] | Wu Weiyue, Guo Xiaodong, Bao Chongyun. Application of engineered exosomes in bone repair and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1102-1106. |
| [12] | Zhou Hongqin, Wu Dandan, Yang Kun, Liu Qi. Exosomes that deliver specific miRNAs can regulate osteogenesis and promote angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1107-1112. |
| [13] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [14] | Huang Chenwei, Fei Yankang, Zhu Mengmei, Li Penghao, Yu Bing. Important role of glutathione in stemness and regulation of stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1119-1124. |
| [15] | Hui Xiaoshan, Bai Jing, Zhou Siyuan, Wang Jie, Zhang Jinsheng, He Qingyong, Meng Peipei. Theoretical mechanism of traditional Chinese medicine theory on stem cell induced differentiation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1125-1129. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||