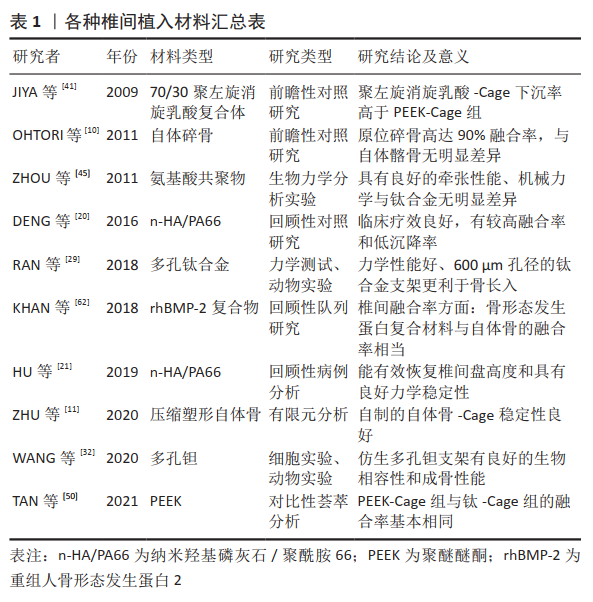
Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (10): 1597-1603.doi: 10.12307/2022.209
Previous Articles Next Articles
Advantages and disadvantages of interbody implant materials in lumbar fusion
Chen Zhengyu1, 2, Tong Jie3, Li Xuelin1, 2, Yan Yiguo1, 2
- 1Department of Spine Surgery, 2Orthopedic Research Center, 3Department of Rehabilitation Medicine, First Affiliated Hospital of University of South China, Hengyang 421001, Hunan Province, China
-
Received:2021-05-06Revised:2021-05-11Accepted:2021-06-01Online:2022-04-08Published:2021-10-27 -
Contact:Yan Yiguo, MD, Chief physician, Department of Spine Surgery, and Orthopedic Research Center, First Affiliated Hospital of University of South China, Hengyang 421001, Hunan Province, China -
About author:Chen Zhengyu, Master candidate, physician, Department of Spine Surgery, and Orthopaedic Research Center, First Affiliated Hospital of University of South China, Hengyang 421001, Hunan Province, China -
Supported by:Hunan Natural Science Foundation, No. 2020JJ4549 (to YYG); Key Laboratory Project of Research and Development of Orthopaedic Plants in Hengyang, No. 2018KJ115 (to YYG); Hunan Natural Science Foundation/Provincial and Municipal Joint Fund Project, No. 2019JJ60032 (to LXL)
CLC Number:
Cite this article
Chen Zhengyu, Tong Jie, Li Xuelin, Yan Yiguo. Advantages and disadvantages of interbody implant materials in lumbar fusion[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(10): 1597-1603.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
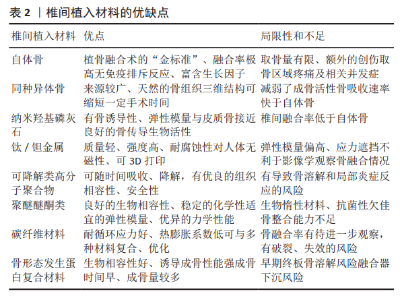
2.1 自体骨 椎体间自体骨移植一直被公认为是植骨手术的黄金标准[5]。在腰椎椎间融合术中特别是取三面骨皮质自体髂骨移植的融合率极高,因为它几乎没有感染源性或免疫排斥反应、降低了疾病传播的风险,而且富含成骨所需的各种生长因子,具有天然的骨诱导活性,见表2。然而,自体骨的使用存在显著局限性和不足[6]:包括取骨量有限、手术整体时间延长、额外的创伤至供区部位持续性疼痛等并发症;部分患者伴有骨质硬化、疏松或其他全身性代谢性疾病等,导致植骨质量不满意以及腰椎融合术后骨不连[7-9]。 临床腰椎椎间融合术中自体骨的主要来源有两方面:一是自身的双侧髂骨(沿髂前上棘向上保留3 cm以上,作骨膜下剥离后取三面皮质骨为佳),二是手术减压过程中收集的棘突、部分椎板、关节突关节等碎骨块。部分学者认为减压收集所得碎骨块以皮质骨占多数,而皮质骨与松质骨相比,其成骨细胞及干细胞含量少,组织更为致密,骨生成和骨诱导特性相对较差,并不利于椎间融合。也有持相反意见,OHTORI等[10]在一项前瞻性随机对照试验中,发现采用术中收集的棘突、椎板等原位碎骨块与取自体髂骨植骨相比,原位碎骨组术后平均融合时间约8.5个月,可高达90%的骨融合率,与自体髂骨组的融合比较无显著差异,且手术时间更短。 现阶段,有研究者希望保持自体骨的优良特性又能维持植入物的力学强度;ZHU等[11]团队研发了一种自体骨成型装置,可将术中收集的棘突和椎板等碎骨块经压缩塑形后制作成“自体骨椎间融合器(Cage)”,经有限元力学分析研究,该自体骨Cage可以达到接近传统钛合金或者聚醚醚酮 (polyetheretherketone,PEEK)融合器的稳定性,且自体骨Cage模型在终板界面的最大应力较低,理论上降低了融合器下沉的风险。KOEHLER等[12]进行了一项队列研究,在94例腰椎后路减压+植骨融合术中,目标椎间隙分别植入了填充自体骨的Cage(57例)和仅填充减压所得自体骨(37例),结果表明,两组患者在临床表现和影像学上均有显著改善,且两组术后的骨融合率和椎间隙高度方面无显著差异。 2.2 同种异体骨 异体骨可分为同种异体骨和异种骨两大类,随着医疗产业的发展,现阶段临床上最常用以同种异体骨居多(包括同种松质骨和皮质骨)。它取材来源相对广泛,通常在合法供者死亡1 d内获取,经灭菌、干燥及冷冻等深加工后真空包装保存。目前仍是自体骨常用的替代品。研究发现同种异体松质骨具有天然骨组织的三维多孔结构,可通过骨诱导和骨传导的优势促进植骨区域的新骨组织生成,能为新骨形成提供良好的成骨空间,且随着融合时间推移,移植骨可逐步吸收降解,并被新生骨组织替代达到融合效果。符合多数骨科学者认同的骨“爬行替代”理论。临床上应用异体骨还可缩短一定手术时间、减少术后并发症等优势[13]。 但据文献报道,同种异体骨也存在诸多不足[14]:经灭菌消毒加工处理后的同种异体骨,降低了移植免疫原性的同时也明显减弱了本身的成骨活性;其次,在有效的支撑力学强度时限内,骨融合率要次于自体骨,且骨吸收降解速率显著快于自体骨。为避免上述不足,临床上脊柱外科医师常将同种异体骨与自体骨混合应用[15],既保证充足植骨量的同时又维持了一定成骨活性,来达到良好的椎间融合效果。 2.3 纳米羟基磷灰石(nano-hydroxyapatile,n-HA) 羟基磷灰石是一种活性生物陶瓷,是人和动物骨骼的主要无机成分,对骨代谢过程中钙盐沉积起到支架作用,同时有一定诱导新骨形成的能力。早期文献报道:在20世纪90年代初学者HIROSHI和RIPAMONTI分别用犬和灵长类动物体内植入实验,验证了植入的多孔羟基磷灰石在皮下和肌肉中均有异位骨化现象发生,提示多孔羟基磷灰石具有骨诱导成骨性可能[16-17]。ZHANG等团队[18],在羟基磷灰石陶瓷材质上培养小鼠成骨样细胞,并通过基因表达微阵列分析表明,多孔羟基磷灰石陶瓷对基因表达谱有很大影响,具有较高的成骨细胞成熟分化潜能。多数研究者也认同,三维多孔结构和羟基磷灰石表面形成的纳米级类骨磷灰石层对于骨诱导性具有重要意义[19]。 近10年来纳米羟基磷灰石/聚酰胺66(nano-hydroxyapatile polyamide,n-HA/PA66)材质Cage研究较常见,该材料是将纳米级羟基磷灰石晶体颗粒均匀分散在聚酰胺66中复合而成,该Cage弹性模量(3-30 GPa)与人皮质骨相近,具有良好的骨传导生物活性及满意的力学性能。现临床上n-HA/PA66材质Cage成功用于腰椎间融合术,且获得了较满意的临床疗效。DENG等[20]进行了一项回顾性病例对照研究,对124例应用n-HA/PA66材质Cage组的患者和142例应用PEEK材质Cage组的患者进行经椎间孔入路腰椎间融合术治疗,平均随访2年结果表明,n-HA/PA66和PEEK材质Cage在治疗退行性腰椎疾病方面,都能有效改善影像学结果和达到满意的临床疗效,术后有较高融合率和低沉降率,表明n-HA/PA66椎间融合器是腰椎重建的理想选择之一。HU等[21]经过回顾性分析,采用n-HA/PA66椎间融合器治疗退变性腰椎侧凸患者43例(其中单节段融合18例、双节段融合25例),随访时间18-62个月(平均30.9个月),研究表明n-HA/PA66 Cage能有效恢复和维持融合节段的椎间盘高度和力学稳定性,对退变性腰椎侧凸也有良好治疗效果。在保持融合节段椎间高度方面,双节段融合效果优于单节段融合。尽管多数研究者报道了纳米羟基磷灰石植骨材料的优良疗效,但仍有少数学者持反对观点。日本学者KUSHIOKA等[22]构思新奇,为了便于对比,在腰椎椎间融合术中将同一个腰椎Cage内2个单独的植骨孔内,一孔植入自体髂骨,另一孔填充羟基磷灰石/胶原复合材料,通过计算机断层扫描评估术后骨融合效果,最终发现Cage内自体骨孔融合率要明显高于羟基磷灰石/胶原填充孔。 2.4 钛合金及钽金属类 钛及其合金仍是目前脊柱椎间融合器制造的主流材料之一。自从20世纪80年代KUSLICH等研制出BAK钛合金融合器并成功用于人腰椎腰椎椎间融合术后,便开启了金属类椎间植入物的研发热潮。众所周知,钛合金材料具有质量轻、强度高、优良的耐腐蚀性、抗疲劳性且对人体无毒、无磁性等优点,同时可通过金属表面修饰后来改善细胞黏附和骨整合能力,是较理想的体内植入物材料。但随着临床应用,钛合金材质Cage的相关缺点显露:一是钛金属弹性模量偏高(弹性模量约110 GPa),术后易出现邻近椎体内植物下沉及应力遮挡等相关问题;二是不利于影像学观察骨融合情况。为改善以上不足,经优化后制作成的多孔结构钛合金内植入物问世,并相继应用于临床医疗。 特别在近年来,随着3D打印增材制造工业水平的蓬勃发展,个性化的缺损修复、可预控孔隙率的多孔结构合金内植材料出现了飞跃式的变革。现阶段以TC4(Ti6Al4V)双相合金材料为主力军,3D打印制造的多孔结构Cage取得了良好的临床疗效。多孔结构的椎间植入物有以下特点[23-24]:①具有良好生物相容性;②相互贯通的微孔结构利于细胞黏附和骨组织生长长入、便于营养物质运输及代谢等;③在维持生物力学刚度需求的同时,进一步减轻了整体质量,减少了自身的应力遮挡效应,并满足解剖学负荷要求。 据文献报道,通过细胞增殖等多项体内外研究表明多孔钛合金具有良好的生物相容性和骨整合能力[25-26],但不同的孔径和孔隙率又对骨结合能力、细胞侵袭和血管生成至关重要。因此,设计出既满足力学性能要求又利于骨组织长入的孔隙结构对于多孔骨替代材料尤为关键。ZHENG等[27]采用选择性激光熔融技术(SLM),成功制备了4种不同孔径且孔隙率均在70%以上的钛合金支架,通过对多孔支架的体外表征、体内动物实验得出,平均孔径约202 μm的钛合金支架的骨整合能力最强,对周围骨组织的稳固效果最佳。PENG等[28]研究发现,孔隙率维持在60%-80%,孔径大小为480-685 μm的多孔钛合金植入体,通过有限元分析证实具备适宜弹性模量和满意的机械力学性能。RAN等[29]为了解多孔Ti6Al4V支架孔径大小对其生物学性能的影响,通过SLM技术制备出实际孔径分别约为401,607,801 μm钛合金支架,经力学性能测试,结果表明其力学性能与正常骨组织相当;并行兔股骨缺损再生实验研究表明,孔径约600 μm 的多孔钛合金生物学性能较优,有利于内植体孔内的骨生长和骨/内植体之间的稳定性。总而言之,多数研究提示3D打印的孔隙率维持在70%-90%、孔径为202-600 μm的多孔钛合金支架机械和生物学性能更优。但如需在材料力学性能和生物相容性之间探索到最佳平衡点,仍需要进行更精细和更大样本量的系统研究。 从21世纪初开始,钽作为一种新型骨科内植材料进入了人们的视野,钽是一种生物相容性好、对细胞增殖无毒性且相对惰性的过渡金属。多孔钽是一种开放式的金属结构,类似于人松质骨的外观,该材料所具有的高孔隙率是吸引多数研究者的优势之一[30]。多孔钽的总孔隙率可达到80%以上,且相邻之间的通孔率极高,因此具有一些独特的机械力学性能。有文献指出,多孔钽支架的弹性模量为3-25 GPa,与人类松质骨和皮质骨的弹性模量相近,可以更好地传递载荷,最大限度的减少应力遮挡现象[31]。 而近几年对于多孔钽的骨科内植物研究报道具有一定热点。WANG等[32]将新型多孔钽粉与骨髓间充质干细胞复合培养、并建立犬股骨干骨缺损模型,用新型多孔钽棒填充骨缺损,通过扫描电子显微镜和硬组织切片等研究,从体外细胞实验和体内动物实验2方面,验证了新型仿生多孔钽支架具有良好的生物相容性和成骨性能。同样另有研究者用多孔钽材料检验成骨性实验结果观察到,培养在多孔钽上的成骨细胞在第3天开始黏附在钽表面和孔壁上,到第12周时,钽表面和孔隙内已完全被交织的骨组织覆盖、且骨小梁已成熟并与钽支架稳定相连,再次表明钽是一种理想的成骨黏附、增殖和营养物质渗透交换的材料[33]。多孔钽Cage在腰椎疾病中也取得了不错的临床疗效。美国捷迈公司生产的金属骨小梁椎间系列产品是目前最具代表性的多孔钽Cage。 MATEJKA等[34]的一项前瞻性研究采用后外侧和前路腰椎间融合术对40例腰椎间盘突出患者使用金属骨小梁椎间融合器,超过1年的随访发现68%的患者获得了高质量的骨性融合,71%的患者诊断为良好的后外侧融合,且术后腰腿痛的目测类比评分明显降低。LEQUIN等[35]通过临床资料行回顾性分析研究:患者26例经单纯后路腰椎间融合放置金属骨小梁椎间融合器,在治疗满意度方面,约69%患者对术后疗效满意,85%的患者随访时工作状态较前有明显改善。但单独使用金属骨小梁椎间融合器的疗效与并发症还需更大的样本量和更长的周期随访观察。 2.5 高分子聚合物类 2.5.1 可降解类高分子聚合物 聚酯类聚合物(聚乳酸):近年来可吸收聚合物融合器逐渐受到众多研究者的重视与关注。大多数可吸收材料有着极优的组织相容性,在体内随着时间改变能被逐渐分解成无毒性的小分子物质,可再次被组织吸收、利用或参与体内物质代谢[36]。在脊柱外科方面,其中最为常用、研究较多的主要是聚乳酸及其衍生物材质制作而成的可吸收降解型椎间融合器。聚乳酸作为一种可降解的半晶体聚合物,在理想情况下,植入椎间2个月后便会开始缓慢降解,一般在12-18个月逐渐代谢,最终分解成二氧化碳和水[37],其降解速率与正常情况下骨组织重建修复时间大致相适应,在体内Cage的降解与脊柱融合过程相互交叉、同时进行,使再生的骨组织逐渐爬行替代聚乳酸材质融合器,直到最终实现骨性融合。聚乳酸具有3种异构聚合物,分别为左旋多聚乳酸(PLLA)、右旋多聚乳酸(PDLA)和无定形的消旋多聚乳酸(PDLLA);其中左旋多聚乳酸的弹性模量与人皮质骨最相似,临床使用最为普遍。 在3D打印支架中添加生物活性物质后,可优化增强支架的生物学特性,这对于获得良好的骨整合效果非常重要[38]。 HAN等[39]采用3D打印技术制备了一种新型多孔结构聚乳酸材质支架,并将人骨形态发生蛋白2和间充干细胞与制备的多孔聚乳酸支架相结合,经体外细胞实验和体内动物实验对该新型复合聚乳酸支架的成骨效果进行评价。通过micro-CT观察和组织学分析研究得出,以人骨形态发生蛋白2为载体构建的多孔聚乳酸复合支架具有优良的生物相容性,在动物骨缺损区域显示出了良好且均匀的新生骨组织分布。 当将70%的左旋多聚乳酸与30%右旋多聚乳酸经比例混合特制后,可得到70/30的聚左旋消旋乳酸复合多聚体。美国学者COUTURE和BRANCH[40]进行了一项前瞻性研究,对27例患者行双侧腰椎后路椎间融合术,共计48个椎体节段植入70/30聚左旋消旋乳酸复合椎间融合器(Cage内填充自体骨),平均26个月的规律随访得出:最终腰椎间融合率高达95.5%,且治疗节段增多对整体融合率呈负相关影响。JIYA等[41]将可吸收的70/30聚左旋消旋乳酸椎间融合器和PEEK椎间融合器经后路椎间融合术式分别各植入13例腰椎疾病患者(共26例),前瞻性随机对照试验结果发现,聚左旋消旋乳酸Cage组下沉率明显高于PEEK材质Cage,且聚左旋消旋乳酸组中发生了2例骨溶解的不良反应。无独有偶,FROST等[42]在病例报道中汇报,曾有9例患者在后路椎间融合术式下植入可吸收聚左旋消旋乳酸(PLDLLA)椎间融合器治疗,经1年以上随访,通过高分辨CT扫描发现有4例椎间融合器周围发生了骨溶解现象,可见发生骨溶解是 聚左旋消旋乳酸椎间融合器的较严重的弊端之一。配比出关键参数对于聚左旋消旋乳酸融合器的力学强度、吸收降解速率和生物相容性有重要影响,因此,探索出最优的黄金比例参数仍是该领域面临的一项重大挑战。 氨基酸共聚物:因聚乳酸材质降解后会降低局部的pH值从而改变细胞内环境,有研究者推测这可能是导致炎性反应和骨溶解的因素之一。而多元氨基酸共聚物(Multi-AACP,MAACP)作为另一种可吸收降解医用高分子材料具有同样良好的生物活性,且该材料降解后不会形成低pH值环境[43],得到了研究者们的认可。其MAACP中含有的6-氨基己酸具有良好的极性与刚性,是构成氨基酸共聚物高分子骨架的主要成分,且赋予了支架良好力学性能;其余多种天然氨基酸(甘氨酸、脯氨酸、丙氨酸和苯丙氨酸等)则参与调节该材料的亲/疏水性、降解速率等生物学性能。 在动物实验上,REN等[44]在24只活体山羊椎间盘切除模型上,分别植入可吸收氨基酸共聚物/纳米羟基磷灰石/硫酸钙(MAACP/n-HA/CS)-Cage、钛合金Cage、羊自体髂骨块3种内植物作对比研究,通过生物力学评估椎体活动度,经组织学切片分析评估骨融合效果,并检测可吸收融合器的相关异物反应,结果表明:MAACP/n-HA/CS椎间融合器具有良好的融合效果,生物力学稳定性好,且与周围骨组织结合紧密。 有研究利用15具离体的山羊脊柱模型,测试了多元氨基酸共聚物/磷酸钙(MAACP/TCP)-Cage的生物力学性能[45]。研究表明,新型MAACP/TCP-Cage具有良好的牵张性能,且在机械力学方面与钛合金Cage无明显差异;但值得注意的是,从融合周期角度考虑,需保证MAACP/TCP融合器植入体内后至少能维持6个月以上有效强度。 2.5.2 不可降解类高分子聚合物 聚醚醚酮(PEEK):是一种人工合成的、线性芳香族半结晶高分子聚合物,也是目前脊柱外科应用最广的椎间融合器材料之一。PEEK不仅具有可靠的生物相容性和稳定的化学性,同时优异的力学性能与人体皮质骨最为相似的弹性模量,在一定程度上能够有效减少应力遮挡,降低融合器下沉的概率,及其可兼容X射线和磁共振(MRI)等诸多特性[46],使之能在众多医用骨科生物材料中独具一格,引起广大研究者的探索与研究。 20世纪90年代末,在骨科领域方面,PEEK材料已发展成为金属内植物的替代候选材料之一[47],并逐渐开始在脊柱外科领域得到研究应用。早期在2002年,法国学者SéNéGAS 等[48]通过研究表明:采用PEEK材质制作的非刚性稳定系统对退行性不稳定型腰椎疾病引起的下腰痛症状有效,且未发现严重并发症。YAO等[49]通过一项回顾性对照分析研究,54例行微创经椎间孔入路腰椎间融合(MI-TLIF)患者,分别植入了钛Ti-PEEK复合Cage与标准PEEK材质Cage行对比研究,经长达2年时间随访得出:钛Ti-PEEK复合Cage在MI-TLIF中的应用与单纯PEEK-Cage一样均安全、有效,两组在骨融合率(6个月椎间融合率约88.9%)、Cage沉降率及并发症发生率方面无显著差异,且术后临床疗效也大致相当。TAN等[50]系统回顾和荟萃分析比较了钛和PEEK椎间融合器在脊柱融合术中的临床和放射学结果,经客观鉴定得出,接受腰椎融合术的两组患者,在最终随访时钛Cage组与PEEK-Cage组的融合率基本相当。 同时,随着临床中PEEK材质的广泛应用,也暴露出些许不足[46]:①由于PEEK表面较光滑且亲水基团较少,无法为细胞黏附提供理想的成骨环境,可能导致骨整合能力欠 佳;②PEEK作为一种生物惰性材料,其抗菌性能欠佳。为优化上述不足,提高有效椎间融合率。目前有研究者通过对PEEK材料进行仿生学加工处理,添加碳纤维、纳米羟基磷灰石、钛涂层等修饰方法进行表面改性研究[51-53],以进一步优化提高PEEK融合器的机械力学性能和诱导成骨的能力。 碳纤维材料:碳纤维椎间融合器在脊柱外科中的应用已有20余年。据文献报道,早在1991年美国学者BRANTIGAN等[54]便研究制作出碳纤维椎间融合器并成功在腰椎后路融合术中得到应用。碳纤维是一种含碳量在90%以上的高模量纤维,其微结构的化学性质非常稳定。碳纤维材料具有以下优点:①耐循环应力好,有着极低的热膨胀系数,应用于脊柱支撑内植物能较好的维持椎间隙高度[55];②可作为增强材料与钛金属、生物陶瓷、PEEK等材料进行兼容复合[56-57],制造出优于原料的新型复合材料,达到“1+1 > 2”的效果;③能透视X射线,便于术后骨组织融合情况的观察与评估。 因上述特性,目前在脊柱外科方面碳纤维多以改性材料复合在生物力学欠佳的树脂类材料中使用,使其优化提高机械学性能。BONNHEIM等[56]对碳纤维增强复合PEEK材质(CFR/PEEK)的骨科内植物进行了单调载荷和疲劳裂纹扩展实验,研究发现,在循环载荷下CFR/PEEK表现出更优秀的抗疲劳性能,并且这种表现在经退火工艺后进一步加强。王二平等[58]对不同碳纤维含量的PEEK复合材料(CF/PEEK)进行拉伸、弯曲、摩擦磨损等性能测试,结果得出,经碳纤维增强的PEEK复合材料力学性能较前明显提升,强度和弹性模量均提高2倍以上,且在显微镜下观察发现碳纤维与PEEK结合有着优良的融合性。然而,也有临床研究者报道了碳纤维增强融合器失败及不良并发症的案例:SARDAR和JARZEM[59]回顾了一例49岁患者,经后路椎间融合术式于L4/5、L5/S1双节段融合术后失败再次翻修,并发现碳纤维增强Cage断裂现象。提示如融合节段出现骨不连和机械不稳等征象,植入碳纤维增强Cage也有破裂失效的风险;并强调重视医疗管理和提高手术操作技巧来实现节段稳定至关重要。 2.6 骨形态发生蛋白复合材料 骨形态发生蛋白是具有骨诱导活性的细胞因子,属于转化生长因子β超家族成员之一,在促进细胞聚集、诱导成骨方面有着极大的潜能。而重组人骨形态发生蛋白2具有生物相容好、诱导成骨能力强、成骨时间早及成骨量较多等优点,其复合材料近年来倍受众多骨科研究者关注与青睐。自从2002年美国食品药品监督管理局(FDA)批准人骨形态发生蛋白2可在腰椎前路椎间融合术中合法使用,便开启了人骨形态发生蛋白2复合材料的医学探索之旅。 临床研究报道,人骨形态发生蛋白2复合材料作为椎间融合内植物可有效提高脊柱融合率和融合强度[60-61]。美国脊柱外科医师KHAN等[62]进行一项回顾性队列研究,分析对比187例成年人经椎间孔入路腰椎间融合术式腰椎融合者,其中植入人骨形态发生蛋白2融合器患者83例、自体骨移植者104例,历经2年以上时间的放射学和临床随访,分析得出,使用人骨形态发生蛋白2椎间植入材料在骨融合率方面可达到与自体骨相似效果,且两组并发症的发生率也大致接近。翁汭等[63]对纳入标准的68例已行椎间融合术的胸腰椎结核患者行回顾性分析研究,椎间植入支撑体分为人骨形态发生蛋白2联合自体骨组(试验组)和单纯自体骨植入组(对照组),术后经1年以上临床随访,结果表明人骨形态发生蛋白2联合自体骨行腰椎椎间融合术治疗胸腰椎结核,在具有相对安全性的同时,相比单纯植入自体骨可在短期内加速骨融合(术后6个月内),且后期临床疗效确切。在使用骨形态发生蛋白2的最佳剂量方面,LYTLE等[64]经系统回顾研究,从客观角度分析得出,在有效减少并发症同时维持最佳融合率的基础上,其骨形态发生蛋白2最低有效剂量约为1.28 mg/水平。 然而,在临床应用中人骨形态发生蛋白2材料也存在些许不足,其中在椎间融合术早期终板骨溶解较明显的问题突出,易导致椎间融合器的下沉或位移。LI等[65]提出,锶(Sr)元素既能促进骨形成也能抑制骨吸收,具有双重作用,锶可能是解决人骨形态发生蛋白2材料在腰椎椎间融合术后引起早期骨溶解的一种方法,但这种协同效应是否会导致新的代谢途径激活还有待进一步研究。其次的弊端是异位骨化问题,在腰椎腰椎椎间融合术中不恰当的使用人骨形态发生蛋白2可能会引起新骨过度生长,产生异位骨化导致脊髓、神经根受压等不良风险[66]。"
| [1] RAVINDRA VM, SENGLAUB SS, RATTANI A, et al. Degenerative lumbar spine disease: estimating global incidence and worldwide volume. Global Spine J. 2018;8(8):784-794. [2] MOBBS RJ, PHAN K, MALHAM G, et al. Lumbar interbody fusion: techniques, indications and comparison of interbody fusion options including PLIF, TLIF, MI-TLIF, OLIF/ATP, LLIF and ALIF. J Spine Surg. 2015; 1(1):2-18. [3] LEE CK, LANGRANA NA. A review of spinal fusion for degenerative disc disease: need for alternative treatment approach of disc arthroplasty? Spine J. 2004;4(6 Suppl):173s-176s. [4] HERRERA A, YÁNEZ A, MARTEL O, et al. Computational study and experimental validation of porous structures fabricated by electron beam melting: a challenge to avoid stress shielding. Mater Sci Eng C Mater Biol Appl. 2014;45:89-93. [5] AGARWAL R, WILLIAMS K, UMSCHEID CA, et al. Osteoinductive bone graft substitutes for lumbar fusion: a systematic review. J Neurosurg Spine. 2009;11(6):729-740. [6] KAISER MG, GROFF MW, WATTERS WC, 3RD, et al. Guideline update for the performance of fusion procedures for degenerative disease of the lumbar spine. Part 16: bone graft extenders and substitutes as an adjunct for lumbar fusion. J Neurosurg Spine. 2014;21(1):106-132. [7] ZOU D, JIANG S, ZHOU S, et al. Prevalence of osteoporosis in patients undergoing lumbar fusion for lumbar degenerative diseases: a combination of dxa and hounsfield units. Spine (Phila Pa 1976). 2020; 45(7):E406-E410. [8] ALPANTAKI K, KAMPOUROGLOU A, KOUTSERIMPAS C, et al. Diabetes mellitus as a risk factor for intervertebral disc degeneration: a critical review. Eur Spine J. 2019;28(9):2129-2144. [9] GUZMAN JZ, IATRIDIS JC, SKOVRLJ B, et al. Outcomes and complications of diabetes mellitus on patients undergoing degenerative lumbar spine surgery. Spine (Phila Pa 1976). 2014;39(19):1596-1604. [10] OHTORI S, SUZUKI M, KOSHI T, et al. Single-level instrumented posterolateral fusion of the lumbar spine with a local bone graft versus an iliac crest bone graft: a prospective, randomized study with a 2-year follow-up. Eur Spine J. 2011;20(4):635-639. [11] ZHU H, ZHONG W, ZHANG P, et al. Biomechanical evaluation of autologous bone-cage in posterior lumbar interbody fusion: a finite element analysis. BMC Musculoskelet Disord. 2020;21(1):379. [12] KOEHLER S, HELD C, STETTER C, et al. Alloplastic or autologous? Bone chips versus peek cage for lumbar interbody fusion in degenerative spondylolisthesis. J Neurol Surg A Cent Eur Neurosurg. 2021. doi:10.1055/s-0040-1718770. [13] Ehrler DM, Vaccaro AR. The use of allograft bone in lumbar spine surgery. Clin Orthop Relat Res. 2000;(371):38-45. [14] GARCÍA DE FRUTOS A, GONZÁLEZ-TARTIÈRE P, COLL BONET R, et al. Randomized clinical trial: expanded autologous bone marrow mesenchymal cells combined with allogeneic bone tissue, compared with autologous iliac crest graft in lumbar fusion surgery. Spine J. 2020; 20(12):1899-1910. [15] BUSER Z, BRODKE DS, YOUSSEF JA, et al. Synthetic bone graft versus autograft or allograft for spinal fusion: a systematic review. J Neurosurg Spine. 2016;25(4):509-516. [16] HIROSHI Y. Heterotopic bone formation around porous hydroxyapatite ceramics in the subcutis of dogs. J Oral Biosci. 1990;32(2):190-192. [17] RIPAMONTI U. The morphogenesis of bone in replicas of porous hydroxyapatite obtained from conversion of calcium carbonate exoskeletons of coral. J Bone Joint Surg Am. 1991;73(5):692-703. [18] ZHANG L, HANAGATA N, MAEDA M, et al. Porous hydroxyapatite and biphasic calcium phosphate ceramics promote ectopic osteoblast differentiation from mesenchymal stem cells. Sci Technol Adv Mater. 2009;10(2):025003. [19] DAVISON NL, SU J, YUAN H, et al. Influence of surface microstructure and chemistry on osteoinduction and osteoclastogenesis by biphasic calcium phosphate discs. Eur Cell Mater. 2015;29:314-329. [20] DENG QX, OU YS, ZHU Y, et al. Clinical outcomes of two types of cages used in transforaminal lumbar interbody fusion for the treatment of degenerative lumbar diseases: n-HA/PA66 cages versus PEEK cages. J Mater Sci Mater Med. 2016;27(6):102. [21] HU J, OU Y, ZHU Y, et al. Effectiveness of nano-hydroxyapatite/polyamide-66 Cage in interbody fusion for degenerative lumbar scoliosis. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2019;33(3):287-295. [22] KUSHIOKA J, KAITO T, MAKINO T, et al. Difference in the fusion rate and bone formation between artificial bone and iliac autograft inside an inter-body fusion cage - A comparison between porous hydroxyapatite/type 1 collagen composite and autologous iliac bone. J Orthop Sci. 2018;23(4):622-626. [23] MCGILVRAY KC, EASLEY J, SEIM HB, et al. Bony ingrowth potential of 3D-printed porous titanium alloy: a direct comparison of interbody cage materials in an in vivo ovine lumbar fusion model. Spine J. 2018; 18(7):1250-1260. [24] VLAD MD, FERNÁNDEZ AGUADO E, GÓMEZ GONZÁLEZ S, et al. Novel titanium-apatite hybrid scaffolds with spongy bone-like micro architecture intended for spinal application: in vitro and in vivo study. Mater Sci Eng C Mater Biol Appl. 2020;110:110658. [25] ICHIOKA Y, ASA’AD F, MALEKZADEH B, et al. Epigenetic changes of osteoblasts in response to titanium surface characteristics. J Biomed Mater Res A. 2021;109(2):170-180. [26] LOTZ EM, BERGER MB, SCHWARTZ Z, et al. Regulation of osteoclasts by osteoblast lineage cells depends on titanium implant surface properties. Acta Biomater. 2018;68:296-307. [27] ZHENG Y, HAN Q, WANG J, et al. Promotion of osseointegration between implant and bone interface by titanium alloy porous scaffolds prepared by 3D printing. ACS Biomater Sci Eng. 2020;6(9):5181-5190. [28] PENG WM, LIU YF, JIANG XF, et al. Bionic mechanical design and 3D printing of novel porous Ti6Al4V implants for biomedical applications. J Zhejiang Univ Sci B. 2019;20(8):647-659. [29] RAN Q, YANG W, HU Y, et al. Osteogenesis of 3D printed porous Ti6Al4V implants with different pore sizes. J Mech Behav Biomed Mater. 2018; 84:1-11. [30] LU M, XU S, LEI ZX, et al. Application of a novel porous tantalum implant in rabbit anterior lumbar spine fusion model: in vitro and in vivo experiments. Chin Med J (Engl). 2019;132(1):51-62. [31] PATEL MS, MCCORMICK JR, GHASEM A, et al. Tantalum: the next biomaterial in spine surgery? J Spine Surg. 2020;6(1):72-86. [32] WANG X, ZHU Z, XIAO H, et al. Three-dimensional, multiscale, and interconnected trabecular bone mimic porous tantalum scaffold for bone tissue engineering. ACS Omega. 2020;5(35):22520-22528. [33] WANG Q, ZHANG H, LI Q, et al. Biocompatibility and osteogenic properties of porous tantalum. Exp Ther Med. 2015;9(3):780-786. [34] MATEJKA J, ZEMAN J, BELATKA J. Mid-term results of 360-degree lumbar spondylodesis with the use of a tantalum implant for disc replacement. Acta Chir Orthop Traumatol Cech. 2009;76(5):388-393. [35] LEQUIN MB, VERBAAN D, BOUMA GJ. Posterior lumbar interbody fusion with stand-alone Trabecular Metal cages for repeatedly recurrent lumbar disc herniation and back pain. J Neurosurg Spine. 2014;20(6):617-622. [36] HOJO Y, KOTANI Y, ITO M, et al. A biomechanical and histological evaluation of a bioresorbable lumbar interbody fusion cage. Biomaterials. 2005;26(15):2643-2651. [37] LOWE TG, COE JD. Resorbable polymer implants in unilateral transforaminal lumbar interbody fusion. J Neurosurg. 2002;97(4 Suppl): 464-467. [38] MAIA-PINTO MOC, BROCHADO ACB, TEIXEIRA BN, et al. Biomimetic mineralization on 3D printed pla scaffolds: on the response of human primary osteoblasts spheroids and in vivo implantation. Polymers (Basel). 2020. doi:10.3390/polym13010074. [39] HAN SH, CHA M, JIN YZ, et al. BMP-2 and hMSC dual delivery onto 3D printed PLA-Biogel scaffold for critical-size bone defect regeneration in rabbit tibia. Biomed Mater. 2020;16(1):015019. [40] COUTURE DE, BRANCH CL JR. Posterior lumbar interbody fusion with bioabsorbable spacers and local autograft in a series of 27 patients. Neurosurg Focus. 2004;16(3):E8. [41] JIYA T, SMIT T, DEDDENS J, et al. Posterior lumbar interbody fusion using nonresorbable poly-ether-ether-ketone versus resorbable poly-L-lactide-co-D, L-lactide fusion devices: a prospective, randomized study to assess fusion and clinical outcome. Spine (Phila Pa 1976). 2009; 34(3):233-237. [42] FROST A, BAGOURI E, BROWN M, et al. Osteolysis following resorbable poly-L-lactide-co-D, L-lactide PLIF cage use: a review of cases. Eur Spine J. 2012;21(3):449-454. [43] 邵洪波.新型氨基酸共聚物/磷酸钙复合骨修复材料的相关研究[D].石家庄:河北医科大学,2015. [44] REN C, SONG Y, XUE Y, et al. Evaluation of bioabsorbable multiamino acid copolymer/nanohydroxyapatite/calcium sulfate cage in a goat spine model. World Neurosurg. 2017;103:341-347. [45] CHUNGUANG Z, YUEMING S, CHONGQI T, et al. Evaluation of bioabsorbable multiamino acid copolymer/α-tri-calcium phosphate interbody fusion cages in a goat model. Spine (Phila Pa 1976). 2011; 36(25):E1615-E1622. [46] 毛誉蓉,孙佳敏,周雄,等.医用特种高分子聚醚醚酮植入体及其表面界面工程[J].功能高分子学报,2021,34(2):144-160. [47] KURTZ SM, DEVINE JN. PEEK biomaterials in trauma, orthopedic, and spinal implants. Biomaterials. 2007;28(32):4845-4869. [48] SÉNÉGAS J. Mechanical supplementation by non-rigid fixation in degenerative intervertebral lumbar segments: the Wallis system. Eur Spine J. 2002;11 Suppl 2(Suppl 2):S164-S169. [49] YAO YC, CHOU PH, LIN HH, et al. Outcome of Ti/PEEK Versus PEEK cages in minimally invasive transforaminal lumbar interbody fusion. Global Spine J. 2021. doi:10.1177/21925682211000323. [50] TAN JH, CHEONG CK, HEY HWD. Titanium (Ti) cages may be superior to polyetheretherketone (PEEK) cages in lumbar interbody fusion: a systematic review and meta-analysis of clinical and radiological outcomes of spinal interbody fusions using Ti versus PEEK cages. Eur Spine J. 2021. doi:10.1007/s00586-021-06748-w. [51] KASHII M, KITAGUCHI K, MAKINO T, et al. Comparison in the same intervertebral space between titanium-coated and uncoated PEEK cages in lumbar interbody fusion surgery. J Orthop Sci. 2020;25(4): 565-570. [52] WANG S, DENG Y, YANG L, et al. Enhanced antibacterial property and osteo-differentiation activity on plasma treated porous polyetheretherketone with hierarchical micro/nano-topography. J Biomater Sci Polym Ed. 2018;29(5):520-542. [53] XUE Z, WANG Z, SUN A, et al. Rapid construction of polyetheretherketone (PEEK) biological implants incorporated with brushite (CaHPO(4)·2H(2)O) and antibiotics for anti-infection and enhanced osseointegration. Mater Sci Eng C Mater Biol Appl. 2020; 111:110782. [54] BRANTIGAN JW, STEFFEE AD, GEIGER JM. A carbon fiber implant to aid interbody lumbar fusion. Mechanical testing. Spine (Phila Pa 1976). 1991;16(6 Suppl):S277-S282. [55] 宋成哲,金红旭.碳纤维椎间融合器与钛网椎间融合器修复腰椎退行性变:生物相容性比较[J].中国组织工程研究,2015,19(12): 1909-1913. [56] BONNHEIM N, ANSARI F, REGIS M, et al. Effect of carbon fiber type on monotonic and fatigue properties of orthopedic grade PEEK. J Mech Behav Biomed Mater. 2019;90:484-492. [57] HEARY RF, PARVATHREDDY NK, QAYUMI ZS, et al. Suitability of carbon fiber-reinforced polyetheretherketone cages for use as anterior struts following corpectomy. J Neurosurg Spine. 2016;25(2):248-255. [58] 王二平,朱姝,谭宗尚,等.CF/PEEK复合材料的性能研究[J].纤维复合材料,2020,37(4):35-38. [59] SARDAR Z, JARZEM P. Failure of a carbon fiber-reinforced polymer implant used for transforaminal lumbar interbody fusion. Global Spine J. 2013;3(4):253-256. [60] NOURIAN AA, HARRINGTON J, PULIDO PA, et al. Fusion rates of lateral lumbar interbody fusion using recombinant human bone morphogenetic protein-2. Global Spine J. 2019;9(4):398-402. [61] VINCENTELLI AF, SZADKOWSKI M, VARDON D, et al. rhBMP-2 (Recombinant Human Bone Morphogenetic Protein-2) in real world spine surgery. A phase IV, National, multicentre, retrospective study collecting data from patient medical files in French spinal centres. Orthop Traumatol Surg Res. 2019;105(6):1157-1163. [62] KHAN TR, PEARCE KR, MCANANY SJ, et al. Comparison of transforaminal lumbar interbody fusion outcomes in patients receiving rhBMP-2 versus autograft. Spine J. 2018;18(3):439-446. [63] 翁汭,叶林强,黄学成,等.重组人骨形态发生蛋白2联合自体骨行椎间植骨融合治疗胸腰椎结核[J].中国组织工程研究,2020, 24(23):3609-3614. [64] LYTLE EJ, LAWLESS MH, PAIK G, et al. The minimally effective dose of bone morphogenetic protein in posterior lumbar interbody fusion: a systematic review and meta-analysis. Spine J. 2020;20(8):1286-1304. [65] LI Z, WANG S, XU G, et al. Synergy effect of Sr and rhBMP-2: a potential solution to osteolysis caused by rhBMP-2. Med Hypotheses. 2020;144:109895. [66] ROSEN CD, KIESTER PD, LEE TQ. Pseudo-pedicle heterotopic ossification from use of recombinant human bone morphogenetic protein 2 (rhBMP-2) in transforaminal lumbar interbody fusion cages. Am J Orthop (Belle Mead NJ). 2018. doi:10.12788/ajo.2018.0003. |
| [1] | Jiang Haifang, Liu Rong, Hu Peng, Chen Wei, Wei Zairong, Yang Chenglan, Nie Kaiyu. Application of 3D printing technology in the precise and personalized treatment of cleft lip and palate [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 413-419. |
| [2] | Zhai Hongjie, Han Guanda, Li Lei, Dong Xiaohui, Jiang Zhiquan, Lou Feiyun. 3D printed polyetheretherketone material for skull defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 380-384. |
| [3] | Pan Baoshun, Fang Zhen, Gao Mingjie, Fang Guiming, Chen Jinshui. Design for posterior atlantoaxial internal fixation system with fusion cage based on imaging data [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1372-1376. |
| [4] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [5] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhou Qian, Zhang Qiang, Chen Qiu. Human salivary components and osteoporosis/osteopenia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1439-1444. |
| [6] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| [7] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| [8] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [9] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [10] | Guo Jia, Ding Qionghua, Liu Ze, Lü Siyi, Zhou Quancheng, Gao Yuhua, Bai Chunyu. Biological characteristics and immunoregulation of exosomes derived from mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1093-1101. |
| [11] | Wu Weiyue, Guo Xiaodong, Bao Chongyun. Application of engineered exosomes in bone repair and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1102-1106. |
| [12] | Zhou Hongqin, Wu Dandan, Yang Kun, Liu Qi. Exosomes that deliver specific miRNAs can regulate osteogenesis and promote angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1107-1112. |
| [13] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [14] | Huang Chenwei, Fei Yankang, Zhu Mengmei, Li Penghao, Yu Bing. Important role of glutathione in stemness and regulation of stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1119-1124. |
| [15] | Hui Xiaoshan, Bai Jing, Zhou Siyuan, Wang Jie, Zhang Jinsheng, He Qingyong, Meng Peipei. Theoretical mechanism of traditional Chinese medicine theory on stem cell induced differentiation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1125-1129. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||