Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (25): 4070-4075.doi: 10.12307/2021.022
Previous Articles Next Articles
Research, application and development of human amniotic epithelial cells in the field of obstetrics and gynecology
Wang Xuan, Zhou Chao, Zhang Yingzi
- Department of Gynecology, Binzhou Medical University Hospital, Binzhou 256603, Shandong Province, China
-
Received:2020-06-23Revised:2020-07-01Accepted:2020-07-31Online:2021-09-08Published:2021-03-30 -
Contact:Zhang Yingzi, Master, Chief physician, Department of Gynecology, Binzhou Medical University Hospital, Binzhou 256603, Shandong Province, China -
About author:Wang Xuan, Master candidate, Department of Gynecology, Binzhou Medical University Hospital, Binzhou 256603, Shandong Province, China
CLC Number:
Cite this article
Wang Xuan, Zhou Chao, Zhang Yingzi. Research, application and development of human amniotic epithelial cells in the field of obstetrics and gynecology[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 4070-4075.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
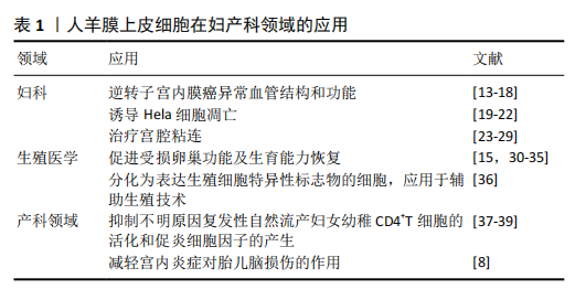
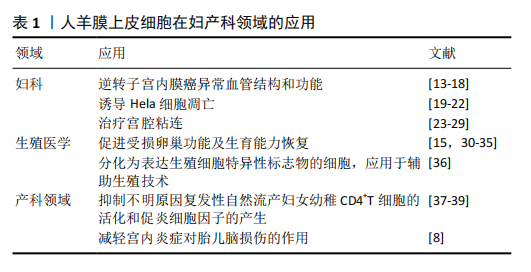
2.1 人羊膜上皮细胞的生物学特性 2.1.1 人羊膜上皮细胞的组织及形态学特点 人羊膜上皮细胞是从足月胎盘的羊膜中分离出来的,羊膜是胎盘最内层的无血管组织,它由5层组成:上皮细胞层、基底层、致密层、间充质细胞层和贴近绒毛膜的海绵层[1],对胎儿起保护作用,并参与调节母体、胎儿和羊水之间的液体平衡。人羊膜上皮细胞为中等大小的细胞,呈圆形,有1个中心核或偏心核,一两个核仁,细胞质丰富,通常呈空泡状[2]。人羊膜上皮细胞源于受精第8天的上胚层细胞,分化发生早于原肠时期,因此,人羊膜上皮细胞维持原肠胚时期上胚层细胞的可塑性。 2.1.2 干细胞性 人羊膜上皮细胞是由多能上皮细胞衍生而来的,原肠形成是早期胚胎发育中决定细胞命运的一个阶段,使这些羊膜细胞成为最早的功能细胞类型之一[3]。研究发现,胚胎干细胞表面标志物TRA1-60、TRA1-81、SSEA3和SSEA4在第2阶段早期胎儿羊水上皮细胞中大部分表达[4],其中一些干细胞标记物阳性的细胞会保留在足月胎盘羊膜上皮中,干细胞表面标记阳性的细胞比阴性细胞表现出更高的干细胞标记基因表达[5]。此外,人羊膜上皮细胞还表达多潜能干细胞特定的转录因子Oct-4和Nanog,具有明显的可塑性和多向分化潜能,在不同生长因子的调节下,人羊膜上皮细胞具有向外胚层细胞(如神经细胞)、中胚层细胞(如心肌细胞)和内胚层细胞(如肝细胞和胰腺细胞)分化的潜能[3]。与成体干细胞相比,其分化能力更强,与胚胎干细胞相比,不但避免了伦理学的限制,还在应用上减少了成瘤的风险[6]。 2.1.3 免疫特性 胎盘的作用之一是在整个妊娠过程中保护胎儿免受母体免疫识别。胎儿细胞在妊娠完成后很久才从母体血液和组织中清除出来[7],显示了某些胎儿细胞的免疫优势。MIKI等[7]指出包括人羊膜上皮细胞在内的许多胎盘细胞类型都表现出免疫豁免性,能减少免疫排斥反应的发生,这是由于人羊膜上皮细胞只表达主要组织相容性复合体(MHC)Ⅰ类抗原HLA-A、-B、-C,不表达MHC Ⅱ类抗原和HLA-DR、共刺激分子CD80B7-1、CD86B7-2、CD40或CD40配体,它们既不表达程序性细胞死亡受体1,也不表达程序性死亡配体1和2 [8]。人羊膜上皮细胞的独特特征之一是表面组织限制性的非经典人类白细胞抗原G(HLA-G)的表达,被认为是诱导耐受的机制之一。HLA-G分子的表达可以保护胎儿免受母体自然杀伤细胞的排斥[9],HLA-G通过结合调节性T细胞、髓系细胞和自然杀伤细胞表面的特异性受体,调节这些免疫细胞的免疫应答[7]。 2.1.4 抗炎性 目前对人羊膜上皮细胞的主流观点认为它们是免疫调节细胞,表达或分泌可溶性免疫反应分子,其中一些分子也可以影响中性粒细胞,因此,人羊膜上皮细胞有望修饰中性粒细胞活性[10]。人羊膜上皮细胞还可分泌抗炎因子,对激活的炎症细胞具有抑制能力,可以防止移植后炎性反应的发生。人羊膜上皮细胞的抗炎活性已经被证实,YAWNO等[11]研究认为人羊膜上皮细胞通过减少炎症细胞因子来减轻胎儿肺部炎症;人羊膜上皮细胞移植可抑制肿瘤坏死因子α介导的细胞凋亡,减轻化疗所致卵巢损伤的炎症反应;移植的人羊膜上皮细胞还可能通过旁分泌途径分泌抗炎因子,促进生长因子的分泌,形成更有利于卵泡生长发育的局部微环境[12]。 2.2 人羊膜上皮细胞在妇科领域的应用 2.2.1 人羊膜上皮细胞逆转子宫内膜癌异常血管结构和功能 子宫内膜癌是女性生殖系统最常见的恶性肿瘤之一,发病逐渐呈年轻化趋势[13]。目前子宫内膜癌的主要治疗手段是手术治疗,必要时辅以放、化疗,抗血管治疗被认为是与手术和化疗同样重要的肿瘤治疗方法,但抗血管治疗的效果并不满意,这是由于肿瘤血管内皮细胞排列紊乱,易渗漏,血流灌注低,肿瘤细胞容易侵袭、逃离肿瘤血管并抵抗肿瘤治疗[14]。临床试验发现,抗血管治疗后化疗可以帮助癌症患者延长生存期,其原因是抗血管药物改善了肿瘤的血管结构和灌注功能,使抗肿瘤药物在治疗过程中能够更有效地杀死肿瘤细胞,人羊膜上皮细胞用于组织工程可以增加血液灌注和促进伤口愈合[15]。GUAN等[14]通过建立裸鼠子宫内膜原位癌模型,发现人羊膜上皮细胞可分化为肿瘤血管内皮细胞,增加肿瘤血管的完整性;它还可使血管内皮生长因子A表达降低,抑制异常的肿瘤血管增生,证实了人羊膜上皮细胞具有增加血液灌注率、纠正肿瘤组织缺氧、减少血管渗漏、提高肿瘤血管灌注效率、增强顺铂对子宫内膜癌的细胞毒作用等特征,为抗肿瘤血管治疗提供了新的方向。 目前的治疗目标已经转变为在化疗或放疗后修复肿瘤血管和增强血管灌注。肿瘤血管重建被认为是肿瘤治疗的另一种选择,用来改善肿瘤血管结构和功能的方法被称为“血管正常化”,现已有多种抑制肿瘤血管生成的方法问世。例如,来那度胺通过免疫调节和抗血管生成活性使肿瘤血管正常 化[16],曲妥珠单抗通过阻断血管内皮生长因子A的表达使肿瘤血管正常[17],三焦磷酸肌醇通过PTEN-PI3K-AKT信号通路使肿瘤血管正常化[18],这些药物只能在短时间内重塑肿瘤血管,但不能诱导血管稳态,其影响是有限的。血管组织工程可能为肿瘤血管修复提供新的契机,其中一个途径是利用血管生成生长因子的释放,结合细胞外基质、生物化学和机械信号来刺激血管生成;另一种方法是使用组织工程化血管结构,这种结构由单独的内皮细胞或镶嵌在细胞外基质聚合物支架上的血管周围细胞中的内皮细胞组成,血管周围细胞通过与内皮细胞沟通来促进血管稳定,并将其与宿主循环结 合[18]。然而,人羊膜上皮细胞定位于肿瘤组织并分化为血管成分的详细机制仍需进一步探讨。 2.2.2 人羊膜上皮细胞诱导Hela癌细胞凋亡 癌症治疗领域出现了许多新思路,许多研究集中探讨干细胞在癌症中的作用,如靶向肿瘤干细胞、分化治疗、干细胞移植等。人羊膜上皮细胞通过诱导凋亡来抗血管生成和抗癌的特性,以及其免疫调节作用,使得人羊膜上皮细胞有可能成为控制癌细胞生长和转移的候选治疗细胞。NIKNEJAD等[19]通过实验检测人羊膜上皮细胞对Hela癌细胞凋亡的影响,发现人羊膜上皮细胞条件培养基处理后,Hela癌细胞活力和增殖能力下降,癌细胞中caspase-8和caspase-3的表达显著增加,证明了人羊膜上皮细胞可诱导癌细胞凋亡,提示人羊膜上皮细胞是羊膜分泌促凋亡物质的关键因素。 羊膜被认为具有抗血管生成的特性[20],在人羊膜上皮细胞中已检测到抗血管生成因子如血小板反应素1、白细胞介素1受体拮抗剂、白细胞介素10和金属蛋白酶组织抑制因子(TIMP-1、TIMP-2、TIMP-3和TIMP-4)[21]。 MAGATTI等[22]报道羊膜上皮细胞的抗增殖作用与未知的可溶性因子诱导细胞周期阻滞于G0/G1期有关。这些研究表明,羊膜细胞可以下调与细胞周期进程相关的癌细胞基因的表达,如细胞周期素(cyclin D2,cyclin E1和cyclin H)和细胞周期蛋白依赖性激酶(CDK2,CDK4和CDK6)的表达。 针对这些发现,作者认为羊膜介导的肿瘤细胞凋亡、血管生成抑制和细胞周期阻滞是通过抑制热休克蛋白90实现的。热休克蛋白90是一种依赖三磷酸腺苷的分子伴侣,可通过抑制细胞周期阻滞、凋亡以及促进血管生成来保护肿瘤细胞。综上所述,羊膜上皮细胞具有抗血管生成和诱导凋亡的作用,有望成为肿瘤治疗药物的候选细胞。 2.2.3 人羊膜上皮细胞可以治疗宫腔粘连 宫腔粘连也被称为Asherman综合征,是一种难治性纤维性疾病,其特征是纤维线连接子宫的对侧壁,部分或完全阻塞宫腔。子宫内膜基底层的任何损伤都可能导致宫腔粘连,从而导致月经过少、闭经、异常慢性疼痛、不孕和反复流产等[23]。一般来说,宫腔粘连的常见原因是手术过程中对宫腔的人为损伤,如刮宫、剖宫产和子宫肌瘤切除术,这可能会损伤子宫内膜基底层,此外,先天性苗勒氏管畸形如子宫纵隔,会增加宫腔粘连的发生率,创伤、感染和遗传易感性导致子宫内膜自发性恢复和血管生成丧失,可引发子宫内膜粘连[23-24]。宫腔镜粘连松解术虽被广泛推荐用于诊断和治疗,但重度宫腔粘连患者预后较差,复发率仍较高(高达20.0%-62.5%)。为了降低高复发率,应用了许多防粘连治疗,例如激素治疗、放置宫内节育器或防粘连凝胶,但还没有一致的结果,而且在粘连松解后,由于子宫内膜的新陈代谢和血管生成受损,患者容易发生妊娠并发症,如早产和胎盘发育异常。CERVELLó等[25]研究发现原位注射诱导多能干细胞可以挽救由机械损伤或细菌脂多糖诱导的小鼠宫腔粘连,从而减轻炎症并提高生育力。目前,以干细胞治疗为基础的再生医学工程为纤维化子宫内膜提供了一种新的治疗方法,如骨髓间充质干细胞、月经血间充质基质细胞,已成功植入重度难治性宫腔粘连患者体内,虽然这些临床试验的患者数量有限,但子宫内膜厚度明显增加,预后良好[26-28]。受试者招募和干细胞收集是一个有创且昂贵的过程[29],这些限制了研究的进展。 为了研究人羊膜上皮细胞对宫腔粘连的潜在作用,BAI等[24]采用机械损伤方法建立了宫腔粘连大鼠模型,模拟宫腔粘连患者的发病机制,并将原代培养的人羊膜上皮细胞注射到大鼠子宫内,结果表明,人羊膜上皮细胞移植后子宫内膜增厚,子宫内膜腺体增生,减少了纤维化面积;人羊膜上皮细胞治疗过程中,促纤维化分子转化生长因子β的表达受到抑制,胶原沉积明显减少;在受损子宫内膜修复过程中,血管内皮生长因子上调,促进了子宫内膜血管生成和增殖。雌激素受体是一种核转录因子,与雌激素联合作用可促进子宫内膜细胞的新陈代谢和增殖,人羊膜上皮细胞还能促进子宫内膜雌激素受体的表达,上调胰岛素样生长因子和白细胞介素4的表达,参与子宫内膜微环境和炎症反应的调节。此外,LI等[23]将人羊膜上皮细胞移植到宫腔粘连小鼠体内,改善了子宫内膜的形态,恢复了宫腔粘连小鼠的生育能力,提高了妊娠率和胎数。综上所述,人羊膜上皮细胞移植可抑制宫腔粘连模型大鼠纤维化的进展,促进其增殖和血管生成,是治疗重度宫腔粘连的一种新的候选细胞[24],也是再生医学中治疗纤维化疾病的候选干细胞。 2.2.4 人羊膜上皮细胞促进受损卵巢功能及生育能力恢复 人羊膜上皮细胞可抑制化疗诱导的卵巢颗粒细胞凋亡。化疗后卵巢组织经常表现为卵泡闭锁、皮质纤维化和血管损伤,导致年轻女性患者生育能力下降。随着年轻癌症患者增多,预防化疗引起的医源性不孕将是更重要的工作之一[30]。干细胞移植通过分泌营养和免疫调节因子来修复受损伤的细胞和组织,YAO等[31]研究发现有109种细胞因子参与了细胞凋亡、血管生成和免疫应答等生物学过程,人羊膜上皮细胞分泌细胞因子可改善受损的卵巢微环境,有效促进卵巢损伤后卵泡的发育和存活,增加化疗损伤卵巢中次级卵泡和成熟卵泡的数量,上调卵泡生长相关基因的表达[32]。研究表明,卵巢可以表达肿瘤坏死因子受体,对肿瘤坏死因子α介导的细胞凋亡途径敏感,化疗药物诱导卵巢颗粒细胞凋亡,并增加卵巢组织内的炎症反应,而人羊膜上皮细胞以旁分泌的方式有效抑制化疗诱导的颗粒细胞凋亡,减轻卵巢炎症反应[12]。 人羊膜上皮细胞以旁分泌方式促进损伤卵巢血管形成。先前的研究表明,静脉注射人羊膜上皮细胞可以迁移到早发性卵巢功能不全小鼠的受损卵巢组织中,并在卵母细胞周围分化为颗粒细胞,参与卵泡发育。同时,人羊膜上皮细胞分泌的细胞因子促进化疗诱导的卵巢早衰小鼠卵泡发育和血管生成,均证明了人羊膜上皮细胞对卵巢功能减退的潜在影响。人羊膜上皮细胞通过分泌转化生长因子β、生长分化因子9、骨形态发生蛋白15、血管内皮生长因子等细胞因子,构建健康的卵巢微环境,促进卵巢功能恢复。血管内皮生长因子在调节卵巢血管生成中起重要作用,但它也参与排卵周期中的许多关键事件,包括卵泡生长、排卵和黄体发育[15]。YAO等[31]使用Bu/Cy诱导卵巢衰竭小鼠模型,经人羊膜上皮细胞处理后血管内皮生长因子A、血管内皮生长因子受体1和血管内皮生长因子受体2的表达减少,证实人羊膜上皮细胞可能通过调节血管内皮生长因子及其受体的表达来恢复卵巢功能,从而诱导血管生成,促进与旁分泌活性相关的卵泡生长。此外,在大鼠卵巢中注射血管内皮生长因子后,初级和次级卵泡的数量增加。 越来越多的证据表明,人羊膜上皮细胞的治疗潜力与损伤组织的免疫调节功能有关,人羊膜上皮细胞对自身免疫性卵巢疾病小鼠卵巢功能恢复有免疫调节作用。自身免疫性卵巢疾病被认为是卵巢早衰的主要原因,人羊膜上皮细胞的免疫调节特性已在多种疾病模型中得到研究[33]。自身免疫性疾病引起的卵巢功能障碍可能与卵透明带蛋白3(ZP3,一种卵巢特异性糖蛋白)抗原和血清ZP抗原抗体(AZPAb)有关[34],并干扰正常的卵泡发育,导致卵泡耗竭和闭经。因此,可以用ZP3免疫小鼠建立实验性自身免疫性卵巢疾病模型,模拟临床病理变化[35]。ZHANG等[33]研究了人羊膜上皮细胞对注射ZP3的自身免疫性卵巢疾病模型小鼠卵巢功能的影响,结果表明:人羊膜上皮细胞移植可调节注射ZP3所致的动情周期紊乱,恢复血清雌二醇和卵泡生成激素水平,增加原始卵泡和成熟卵泡数量,减轻受损卵巢间质纤维化和细胞凋亡。 2.3 人羊膜上皮细胞在生殖医学领域的应用 人羊膜上皮细胞被诱导分化为表达生殖细胞特异性标志物的细胞。遗传信息通过生殖细胞从一代传到下一代,这些细胞构成了与体细胞截然不同的细胞群体,具有独特的特征,在经历了微妙的减数分裂过程后,显示出单倍体的染色体数目。由于伦理方面的限制,在人类身上研究此过程更加困难。此外,生殖细胞数量有限、生殖细胞在胚胎中的深层位置,以及生殖细胞在发育过程中迁移的事实,都降低了在体内研究配子发生过程的深度。基于人类干细胞的体外培养系统可以为研究生殖细胞发育的某些方面提供一个有价值的平台[36]。EVRON等[36]研究表明新鲜分离的人羊膜上皮细胞表达非常低水平的生殖细胞特异性基因DAZL和VASA,在含血清白蛋白的培养基中培养的人羊膜上皮细胞在蛋白水平上表达生殖细胞特异性标记DAZL和卵母细胞特异性标记ZP3和GDF9,提示人羊膜上皮细胞具有分化为表达生殖细胞特异性标志物的二倍体细胞的潜能,类似的单倍体细胞的可能来源将为人类生殖细胞特性和配子发生研究提供一个合适的体外系统,从而为辅助生殖技术治疗带来新的希望。 2.4 人羊膜上皮细胞在产科领域的应用 2.4.1 人羊膜上皮细胞对妊娠的影响 人羊膜上皮细胞抑制不明原因反复自然流产妇女幼稚CD4+T细胞的活化和促炎细胞因子的产生。复发性自然流产是育龄妇女的一种常见病,其特征是在妊娠20周前连续流产3次或以上。复发性自然流产的病因尚不清楚,但多项研究提出引起这种疾病的原因有遗传、染色体、解剖、内分泌、胎盘异常、同种异体免疫和自身免疫因素、生殖道感染、环境因素等。约50%的复发性自然流产病例被归类为原因不明的复发性自然流产,在很大程度上与母体对胎儿同种异体反应引起的免疫缺陷有关。大量研究提供了令人信服的证据,Th1/Th2细胞因子失衡、调节性T细胞数量或功能缺陷、外周血和蜕膜中Th17细胞和自然杀伤细胞数量的增加,在原因不明的复发性自然流产发病中起着决定性作用[37]。人羊膜上皮细胞具有干细胞样特征,具有调节先天和获得免疫反应的能力。MOTEDAYYEN等[37]通过研究发现人羊膜上皮细胞通过抑制T细胞活化和减少活化T细胞的促炎细胞因子的产生,对原因不明的复发性自然流产患者的初始CD4+T细胞具有免疫调节作用。 人羊膜上皮细胞Toll样受体4活化是妊娠失败的危险因素。母胎界面的免疫耐受在植入和维持妊娠中起着不可或缺的作用。据报道,辅助性T细胞2和调节性T细胞分泌白细胞介素4、白细胞介素5、转化生长因子β和白细胞介素10等免疫抑制介质抑制母体免疫系统,增强母胎耐受性。怀孕期间,孕妇可能受到病原体的威胁,而宫内感染被认为是妊娠失败的重要危险因素,包括胎膜早破、早产和反复流产。大量研究表明,宫内病原体刺激先天免疫系统和后天免疫系统的细胞,通过在母胎界面产生促炎细胞因子,导致胎膜的弱化和破裂;促炎细胞因子上调前列腺素和基质金属蛋白酶的产生,从而促进子宫收缩和细胞程序性死亡(凋亡),导致胎膜早破和早产[38]。 阴道穹隆和宫颈的解剖学结构为许多病原体的定植提供了合适的场所,如解脲支原体、链球菌和其他革兰阴性和革兰阳性细菌,它们是妊娠失败的重要原因。女性生殖道中定植微生物的识别是由免疫系统的各种受体介导的,如先天免疫系统的模式识别受体。人羊膜上皮细胞通过表达各种Toll样受体发挥免疫调节作用,并对入侵的病原体做出反应。Toll样受体是表达于免疫系统不同细胞上的模式识别受体,Toll样受体4感知革兰阴性细菌细胞壁的脂多糖,进而触发细胞内信号级联,从而导致核因子κB和激活蛋白1的激活,这两个因子是主要的转录因子,负责启动和增强炎症反应相关基因的表达。MOTEDAYYEN等[39]研究表明脂多糖刺激人羊膜上皮细胞的Toll样受体4表达,通过诱导人羊膜上皮细胞产生肿瘤坏死因子α、白细胞介素1β、前列腺素E2和转化生长因子β1参与母胎界面的母体免疫异常,这些结果提示Toll样受体4激活可能是妊娠失败的潜在危险因素。 2.4.2 人羊膜上皮细胞减轻宫内炎症对胎儿脑损伤的作用 宫内感染如绒毛膜羊膜炎,是早产、神经疾病和脑性瘫痪的主要危险因素。在早产儿中,最常见的神经病理改变是脑白质异常如脑室周围白质软化症。脑室周围白质软化症是早产儿脑损伤的主要形式,60%-100%患有脑室周围白质软化症的早产儿将被诊断为脑性瘫痪。PANG等[40]发现全身给予胎儿或新生儿细菌内毒素脂多糖会导致脑白质脑损伤,包括脑室周围白质软化症。脑室周围白质软化症新生儿脑组织中肿瘤坏死因子α、白细胞介素1β、白细胞介素6水平升高,而羊水中白细胞介素6和白细胞介素1β浓度升高是诊断脑性瘫痪的独立危险因素。人羊膜上皮细胞可通过减少炎症细胞因子等来减轻胎儿炎症。INSAUSTI等[8]实验证明人羊膜上皮细胞具有改善与炎症相关胎儿脑损伤的潜力,这是第一次在早产儿身上观察到人羊膜上皮细胞通过缓和胎儿脑部炎症反应来减轻脑损伤。 人羊膜上皮细胞在妇产科领域的应用汇总,见表1。 "
| [1] 冯小倩.人羊膜上皮细胞的性质研究[D].北京:北京协和医学院, 2010. [2] MAGATTI M, VERTUA E, CARGNONI A, et al. The Immunomodulatory Properties of Amniotic Cells: The Two Sides of the Coin. Cell Transplant. 2018;27(1):31-44. [3] MIKI T, LEHMANN T, CAI H, et al. Stem cell characteristics of amniotic epithelial cells. Stem Cells. 2005;23(10):1549-1559. [4] IZUMI M, PAZIN BJ, MINERVINI CF, et al. Quantitative comparison of stem cell marker-positive cells in fetal and term human amnion. J Reprod Immunol. 2009;81(1):39-43. [5] MIKI T, MITAMURA K, ROSS MA, et al. Identification of stem cell marker-positive cells by immunofluorescence in term human amnion. J Reprod Immunol. 2007;75(2):91-96. [6] 陈宥艺.人足月胎盘羊膜细胞的生物学特性及其治疗肝纤维化的实验研究[D].西安:第四军医大学,2011. [7] MIKI T. Stem cell characteristics and the therapeutic potential of amniotic epithelial cells. Am J Reprod Immunol. 2018;80(4):e13003. [8] INSAUSTI CL, BLANQUER M, GARCÍA-HERNÁNDEZ AM, et al. Amniotic membrane-derived stem cells: immunomodulatory properties and potential clinical application. Stem Cells Cloning. 2014;7:53-63. [9] STROM SC, GRAMIGNOLI R. Human amnion epithelial cells expressing HLA-G as novel cell-based treatment for liver disease. Hum Immunol. 2016;77(9):734-739. [10] ALIPOUR R, MOTEDAYYEN H, SERESHKI N, et al. Human Amniotic Epithelial Cells Affect the Functions of Neutrophils. Int J Stem Cells. 2020;13(2):212-220. [11] YAWNO T, SCHUILWERVE J, MOSS TJ, et al. Human amnion epithelial cells reduce fetal brain injury in response to intrauterine inflammation. Dev Neurosci. 2013;35(2-3):272-282. [12] ZHANG Q, XU M, YAO X, et al. Human amniotic epithelial cells inhibit granulosa cell apoptosis induced by chemotherapy and restore the fertility. Stem Cell Res Ther. 2015;6(1):152. [13] BRAY F, FERLAY J, SOERJOMATARAM I, et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018;68(6):394-424. [14] GUAN L, ZHANG A. Amniotic epithelial cells reverse abnormal vascular structure and function in endometrial carcinoma. Int J Clin Exp Pathol. 2019;12(7):2405-2424. [15] CARRARO G, PERIN L, SEDRAKYAN S, et al. Human amniotic fluid stem cells can integrate and differentiate into epithelial lung lineages. Stem Cells. 2008;26(11):2902-2911. [16] LEUCI V, MAIONE F, ROTOLO R, et al. Lenalidomide normalizes tumor vessels in colorectal cancer improving chemotherapy activity. J Transl Med. 2016;14(1):119. [17] SORACE AG, QUARLES CC, WHISENANT JG, et al. Trastuzumab improves tumor perfusion and vascular delivery of cytotoxic therapy in a murine model of HER2+ breast cancer: preliminary results. Breast Cancer Res Treat. 2016;155(2):273-284. [18] DE GIROLAMO L, LUCARELLI E, ALESSANDRI G, et al. Mesenchymal stem/stromal cells: a new ‘’cells as drugs’’ paradigm. Efficacy and critical aspects in cell therapy. Curr Pharm Des. 2013;19(13): 2459-2473. [19] NIKNEJAD H, KHAYAT-KHOEI M, PEIROVI H, et al. Human amniotic epithelial cells induce apoptosis of cancer cells: a new anti-tumor therapeutic strategy. Cytotherapy. 2014;16(1):33-40. [20] SEO JH, KIM YH, KIM JS. Properties of the amniotic membrane may be applicable in cancer therapy. Med Hypotheses. 2008;70(4):812-814. [21] HAO Y, MA DH, HWANG DG, et al. Identification of antiangiogenic and antiinflammatory proteins in human amniotic membrane. Cornea. 2000;19(3):348-352. [22] MAGATTI M, DE MUNARI S, VERTUA E, et al. Amniotic membrane-derived cells inhibit proliferation of cancer cell lines by inducing cell cycle arrest. J Cell Mol Med. 2012;16(9):2208-2218. [23] LI B, ZHANG Q, SUN J, et al. Human amniotic epithelial cells improve fertility in an intrauterine adhesion mouse model. Stem Cell Res Ther. 2019;10(1):257. [24] BAI X, LIU J, YUAN W, et al. Therapeutic Effect of Human Amniotic Epithelial Cells in Rat Models of Intrauterine Adhesions. Cell Transplant. 2020;29:963689720908495. [25] CERVELLÓ I, GIL-SANCHIS C, SANTAMARÍA X, et al. Human CD133(+) bone marrow-derived stem cells promote endometrial proliferation in a murine model of Asherman syndrome. Fertil Steril. 2015;104(6): 1552-1560. [26] SANTAMARIA X, CABANILLAS S, CERVELLÓ I, et al. Autologous cell therapy with CD133+ bone marrow-derived stem cells for refractory Asherman’s syndrome and endometrial atrophy: a pilot cohort study. Hum Reprod. 2016;31(5):1087-1096. [27] SINGH N, MOHANTY S, SETH T, et al. Autologous stem cell transplantation in refractory Asherman’s syndrome: A novel cell based therapy. J Hum Reprod Sci. 2014;7(2):93-98. [28] NAGORI CB, PANCHAL SY, PATEL H. Endometrial regeneration using autologous adult stem cells followed by conception by in vitro fertilization in a patient of severe Asherman’s syndrome. J Hum Reprod Sci. 2011;4(1):43-48. [29] TAN J, LI P, WANG Q, et al. Autologous menstrual blood-derived stromal cells transplantation for severe Asherman’s syndrome. Hum Reprod. 2016;31(12):2723-2729. [30] WANG F, WANG L, YAO X, et al. Human amniotic epithelial cells can differentiate into granulosa cells and restore folliculogenesis in a mouse model of chemotherapy-induced premature ovarian failure. Stem Cell Res Ther. 2013;4(5):124. [31] YAO X, GUO Y, WANG Q, et al. The Paracrine Effect of Transplanted Human Amniotic Epithelial Cells on Ovarian Function Improvement in a Mouse Model of Chemotherapy-Induced Primary Ovarian Insufficiency. Stem Cells Int. 2016;2016:4148923. [32] ZHANG Q, BU S, SUN J, et al. Paracrine effects of human amniotic epithelial cells protect against chemotherapy-induced ovarian damage. Stem Cell Res Ther. 2017;8(1):270. [33] ZHANG Q, HUANG Y, SUN J, et al. Immunomodulatory effect of human amniotic epithelial cells on restoration of ovarian function in mice with autoimmune ovarian disease. Acta Biochim Biophys Sin (Shanghai). 2019;51(8):845-855. [34] JAGARLAMUDI K, REDDY P, ADHIKARI D, et al. Genetically modified mouse models for premature ovarian failure (POF). Mol Cell Endocrinol. 2010;315(1-2):1-10. [35] SETIADY YY, SAMY ET, TUNG KS. Maternal autoantibody triggers de novo T cell-mediated neonatal autoimmune disease. J Immunol. 2003;170(9):4656-4664. [36] EVRON A, GOLDMAN S, SHALEV E. Human amniotic epithelial cells differentiate into cells expressing germ cell specific markers when cultured in medium containing serum substitute supplement. Reprod Biol Endocrinol. 2012;10:108. [37] MOTEDAYYEN H, ZARNANI AH, TAJIK N, et al. Immunomodulatory effects of human amniotic epithelial cells on naive CD4(+) T cells from women with unexplained recurrent spontaneous abortion. Placenta. 2018;71:31-40. [38] MOTEDAYYEN H, FATHI F, FASIHI-RAMANDI M, et al. Toll-like receptor 4 activation on human amniotic epithelial cells is a risk factor for pregnancy loss. J Res Med Sci. 2019;24:1. [39] MOTEDAYYEN H, FATHI F, FASIHI-RAMANDI M, et al. The effect of lipopolysaccharide on anti-inflammatory and pro-inflammatory cytokines production of human amniotic epithelial cells. Reprod Biol. 2018;18(4):404-409. [40] Pang Y, Fan LW, Zheng B, et al. Role of interleukin-6 in lipopolysaccharide-induced brain injury and behavioral dysfunction in neonatal rats. Neuroscience. 2006;141(2):745-755. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [3] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [4] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [5] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [6] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [7] | Geng Qiudong, Ge Haiya, Wang Heming, Li Nan. Role and mechanism of Guilu Erxianjiao in treatment of osteoarthritis based on network pharmacology [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1229-1236. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||