Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (25): 4076-4081.doi: 10.12307/2021.023
Previous Articles Next Articles
Autologous chondrocyte implantation in the treatment of cartilage defect of knee joint: no significant difference between regenerated and natural cartilages
Li Xiang, Fu Peiliang
- Department of Joint Surgery, Changzheng Hospital of Naval Medical University, Shanghai 200003, China
-
Received:2020-07-22Revised:2020-07-24Accepted:2020-10-29Online:2021-09-08Published:2021-03-30 -
Contact:Fu Peiliang, MD, Associate professor, Associate chief physician, Department of Joint Surgery, Changzheng Hospital of Naval Medical University, Shanghai 200003, China -
About author:Li Xiang, Master, Physician, Department of Joint Surgery, Changzheng Hospital of Naval Medical University, Shanghai 200003, China -
Supported by:the Scientific Research Project of Science and Technology Committee of Shanghai, No. 17411971800 (to FPL)
CLC Number:
Cite this article
Li Xiang, Fu Peiliang. Autologous chondrocyte implantation in the treatment of cartilage defect of knee joint: no significant difference between regenerated and natural cartilages[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 4076-4081.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
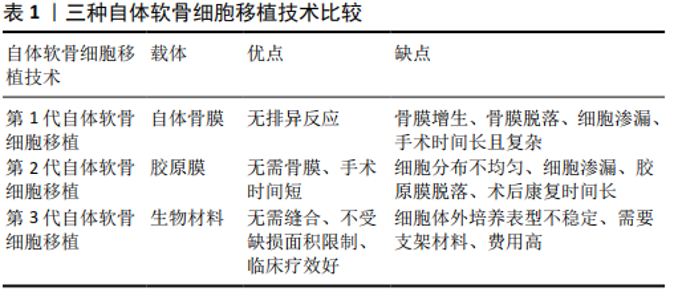
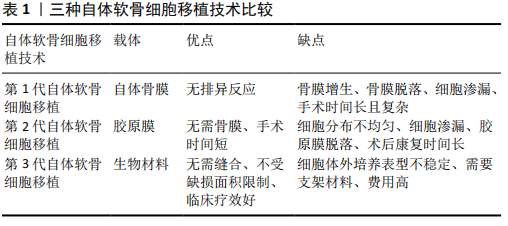
2.1 发展历程 关节软骨缺乏血管、神经、淋巴等结构,其营养主要由关节液提供,再生能力有限[7]。膝关节软骨损伤最常见的部位是髌股关节,包括滑车沟和髌骨,其次是股骨髁和胫骨平台,这些部位损伤后患者通常伴有长期的活动性疼痛和肿胀等症状[8],虽然可给予保守治疗,但保守治疗效果不理想的患者通常需采取手术治疗缓解症状[9-10]。 为了寻求更好的关节软骨修复方法,BRITTBERG在1994年首次报道了应用自体软骨细胞移植修复软骨缺损的临床研究。到目前为止,自体软骨细胞移植发展创新至第3代技术:第1代自体软骨细胞移植(PACI)将人工培养的软骨细胞悬浊液注射到缺损部位,并用取自胫骨近端的自体骨膜对软骨细胞进行封闭固定,但是自体骨膜通常会增生肥大;第2代自体软骨细胞移植(CACI)利用胶原膜替代自体骨膜可以有效解决这个问题;第3代自体软骨细胞移植(MACI)在三维基质中培养软骨细胞,可以有效改善细胞传递质量、维持细胞表型以及允许小关节切口植入[6],见表1,第3代自体软骨细胞移植可以更好地重塑正常软骨结构,提高临床疗效[6]。近年来,已经初步证实自体软骨细胞移植技术具有良好的临床疗效,第3代自体软骨细胞移植已获得美国食品和药物管理局(FDA)批准投入临床使用,但是目前国内尚没有完全开放。软骨修复的目的是再生成熟的软骨细胞,形成与天然软骨结构相似的软骨,继而重新构建关节面。术后组织活检发现再生组织中透明软骨比例越高,临床疗效越好[10],通过对30例自体软骨细胞移植患者的软骨细胞相关基因进行分析,结果显示再生的软骨与天然软骨无明显差异,能够有效维持透明软骨细胞表型和Ⅱ型胶原蛋白高表达[11]。 "
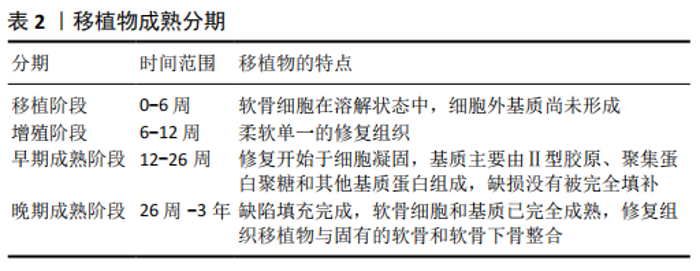
2.2 基础科学 关节软骨细胞外基质由胶原纤维和蛋白多糖组成,蛋白多糖可以维持软骨的弹性功能,高交联的胶原纤维在维持软骨的硬度和剪切强度等方面起重要作用[12]。软骨细胞组织仅占1%-5%,是该区域唯一的细胞类型[13]。此外,细胞外基质还包含特定的糖胺聚糖、硫酸软骨素、硫酸角质素以及透明质酸,其中糖胺聚糖可以固定周围软骨细胞,并能够连接细胞外基质的其他成分与周围骨细胞[12,14]。 软骨修复的目的是再生透明质或类透明质样软骨来重建原有关节面。DIBARTOLA等[10]研究表明,修复组织中透明软骨比例越高,临床疗效越好。最近的一项研究分析自体软骨细胞移植物与天然软骨类似,不仅可以维持软骨细胞表型,而且还可以高表达Ⅱ型胶原蛋白[15]。 自体软骨细胞移植技术再生软骨组织包含4个明确阶 段[16]。第1阶段(植入后0-6周):植入阶段;第2阶段:过渡阶段和增殖阶段( 6-12周),体外培养后植入的软骨细胞开始形成柔软单一的再生组织来填充软骨缺损;第3阶段:早期的成熟阶段(12-26周),软骨细胞开始产生以Ⅱ型胶原、聚集蛋白聚糖等基质蛋白为主的基质,软组织修复移植物开始凝固;第4阶段:成熟期后期(26周-3年),新生组织完全填充病变,软骨细胞和基质完全成熟,形成透明质或类透明质样软骨与固有软骨和软骨下骨整合,见表2。 "

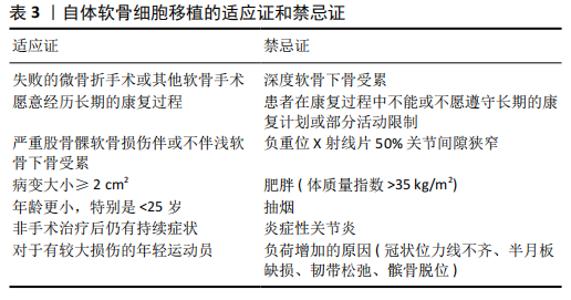
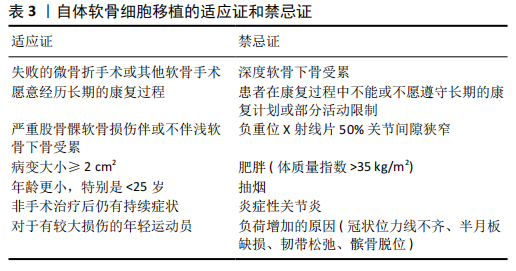
2.3 适应证和禁忌证 2.3.1 适应证 患者必须愿意接受自体软骨细胞移植术后所需要的较长时间恢复过程。由于传统手术成本较低以及术后恢复较快,患者通常更倾向于选择传统手术方法[9]。在初次手术治疗失败后,自体软骨细胞移植是最常用的治疗方法,但需要注意的是,自体软骨细胞移植作为二次手术的失败率要高于自体软骨细胞移植作为初次手术方法[17]。在美国大多数保险公司愿意承担自体软骨细胞移植用于治疗有症状的软骨缺损病变的医疗费用,包括≥2 cm2的股骨髁或髌骨软骨缺损病变。标准的自体软骨细胞移植手术可以应用于没有涉及软骨下骨的病变,也可以运用Sandwich技术联合使用自体软骨细胞移植和自体骨移植来治疗浅层软骨下骨病变[18-19]。 自体软骨细胞移植用于治疗股骨髁缺损,虽然缺损面积大小定义各不相同,但一个被广泛接受的值是≥2.0 cm2 [20]。与同种骨软骨异体移植和微骨折手术相比,自体软骨细胞移植被认为是一个可靠的选择并且有希望提供相对优越的疗效[21],特别适用于寻求恢复体力活动或竞争性活动和专业体育运动的运动员患者[22-23]。年龄小于25岁的患者疗效最好,25-40岁和部分40岁以上的患者也有较好的疗 效[17,24]。出现早期症状的软骨损伤如果能得到及时诊治,疗效会更好,见表3。 2.3.2 禁忌证 患有膝关节退行性病变的患者并不适合该手术,尤其是患者负重位X射线片显示关节间隙狭窄> 50%[25]。基于专家的意见共识,炎症性关节炎也是一种被提出较多的相对禁忌证[26],原因是目前缺乏评估自体软骨细胞移植在这种环境下修复软骨损伤临床疗效的相关研究[25]。体质量指数>35 kg/m2的患者在软骨修复治疗后预后较差。吸烟也与自体软骨细胞移植的疗效不佳有关[27]。自体软骨细胞移植术前或术中,半月板损伤、冠状位力线不齐、髌骨脱位和韧带损伤等疾病都必须提前处理,否则他们都可能会对移植物施加额外的压力负荷,增加手术失败风险[25,28]。自体软骨细胞移植后的完全康复需要较长的时间,通常长达18个月[29],但第3代自体软骨细胞移植之后使用加速康复方案能够在8周内完全承重,4-6个月恢复运动[30-31],因此不能参与必要的康复计划或遵守术后活动部分限制规定的患者都不是自体软骨细胞移植的最佳适应患者。在美国第1代和第2代自体软骨细胞移植治疗髌骨均不符合治疗标准,虽然这类病变在术后都已报告了良好的疗效,但整体效果不如使用自体软骨细胞移植治疗孤立的滑车沟病变好[32-33],但是近年来大部分保险公司都逐渐涵盖了运用第3代自体软骨细胞移植技术治疗髌骨病变的费用,见表3。 2.4 临床技术 自体软骨细胞移植与其他软骨修复手术的主要区别在于,自体软骨细胞移植需要进行2次手术,而其他手术方式仅需1次手术就可以缓解症状。自体软骨细胞移植第1次手术是收集自体软骨细胞,通常是关节镜下从非负重部位收集,最常见的部位是股骨沟远端,收集软骨200- 300 mg,利用胶原酶分离出软骨细胞,然后在液体培养基中培养,运用相关技术维持软骨细胞原始表型和软骨细胞增殖,第2次手术是5-9周后[16,34],把软骨细胞再植入缺损部位,术前应对软骨缺损四周进行适当清理,垂直清理缺损,同时清除钙化软骨,使之达到健康稳定的状态,注意不要侵入软骨下骨,第2次手术通常经小关节切口或关节镜下植入软骨细胞,这2种方法均被报道有良好的临床效果,然而,关节镜下操作会产生过多的干扰,将导致软骨细胞失去活力,增加细胞死亡风险,此外,为准备关节镜下植入而产生的过多操作也会导致软骨细胞失去活力[34-35]。一项小型尸体研究表明,经小关节切口植入后,自体骨膜或生物支架上的存活细胞是关节镜下植入的16倍[34],通过比较开放切口自体软骨细胞移植和关节镜下自体软骨细胞移植,发现开放式自体软骨细胞移植疗效更好[36]。Sandwich技术就是同时运用自体软骨细胞移植和骨移植技术,治疗累及浅层软骨下骨的缺 损[18-19]。 2.5 临床疗效 自体软骨细胞移植技术经过了20多年的应用,已经对缺损大小、年龄、恢复运动、用于翻修手术、失败率、功能结果、影像学和组织学结果等方面进行了长期随访研究,但多数研究仅仅评估了早期第1代自体软骨细胞移植技术,而第2代和第3代自体软骨细胞移植的相关研究较少,由此预测新一代自体软骨细胞移植可以提供更好的长期疗效,但是仍然没有足够的证据说明收益大于风险[37]。 2.5.1 缺损大小 自体软骨细胞移植常用于≥2 cm2的缺损,不适合< 2 cm2的软骨缺损。BENTLEY等[38]通过对100例> 4 cm2缺损患者选择使用自体软骨细胞移植和自体骨软骨移植治疗,术后进行10年随访,结果表明自体软骨细胞移植的疗效更好,失败率显著低于自体骨软骨移植,治疗严重缺损的疗效比微骨折好。ZHANG等[39]对45例高水平运动员的术后疗效分析,提出自体软骨细胞移植技术常用于较大缺损,但是疗效与缺陷大小呈负相关,缺损较小患者的疗效优于缺损较大的患者,高水平运动员术后恢复运动可能性更大。 2.5.2 初次手术失败后的治疗 早期自体软骨细胞移植主要作为翻修手术,用于微骨折等传统手术治疗后症状不能得以缓解的患者[9],然而失败率要高于将自体软骨细胞移植作为初次手术治疗方案。另外一项研究也发现在微骨折术失败后进行自体软骨细胞移植手术的失败率比作为初次手术进行自体软骨细胞移植的失败率高[17]。 2.5.3 恢复运动 运动员经常出现软骨损伤,这使恢复体育运动成为他们治疗的主要期望[40]。研究发现第3代自体软骨细胞移植术后2年Tegner和KOOS评分通常明显改善,尽管只有59%的患者改善较大,但是分别有85%和66%的患者对返回娱乐活动和参加运动的能力感到满意[26]。然而, CAMPBELL等[1]在一篇综述中指出,自体骨软骨移植或自体软骨细胞移植恢复体育运动率比微骨折术高,但二者之间没有显著差异,并且第1代和第2代自体软骨细胞移植之间也没有显著差异。KRYCH等[2]对46例患者进行荟萃分析发现自体骨软骨移植、同种骨软骨异体移植、自体软骨细胞移植和微骨折术后恢复一定程度体育活动的比例分别为93%,88%,88%和 58%,相比较而言,自体骨软骨移植、同种骨软骨异体移植、自体软骨细胞移植术后疗效较好,但并不能恢复到损伤前水平。尽管自体骨软骨移植恢复运动时间需要3.4-6个月,比微骨折、同种骨软骨异体移植和自体软骨细胞移植更快,但第1代和第2代自体软骨细胞移植则要10-18个月,二者对影响小的体育运动员可能会恢复的更早[29], 并且第3代自体软骨细胞移植术后的快速安全恢复方案可让患者在4-6个月内恢复体育运动[30-31]。微骨折或第1代自体软骨细胞移植术后重返赛场的专业和业余足球运动员术后2年期间IKDC评分相似,然而近期随访表明,微骨折组的IKDC评分和运动水平从第2年开始下降,而自体软骨细胞移植组比较稳定[41]。总的来说,年龄小(< 25岁)、术前发病时间短的专业运动员会得到更好的恢复效果。 2.5.4 年龄 自体软骨细胞移植对年龄没有明确的限制,虽然对于40岁以上患者也具有一定的疗效[42],但是年龄小于25岁或小于40岁的患者疗效更为显著[43],手术成功率也明显提高。研究人员对18岁以下的患者术后随访,随访时间平均大于4年,发现第1代自体软骨细胞移植治疗严重软骨缺损的青年患者有明确的疗效,尽管早期失败率高达37.8%,但所有患者术后IKDC、KOOS评分比术前均显著提高[44]。 另一项研究对40例20岁以下经第3代自体软骨细胞移植治疗的患者随访3年,所有患者在6,12,24,36个月的疗效比相匹配的成年人均有所改善[8]。 2.5.5 并发症、失败率和功能性结果 自体软骨细胞移植术后失败通常发生在移植后24个月内,第1代自体软骨细胞移植术后的失败率可能较大,主要原因是骨膜增生肥大,而第2代和第3代自体软骨细胞移植术后的失败率较小[9]。随着时间的推移,自体软骨细胞移植术后疗效显著改善,使这一技术逐渐被广大患者接受。以关节切开为主的自体软骨细胞移植,术后关节纤维化是最常见的并发症,另外不常见的并发症包括移植物分层、细胞渗漏和与软骨细胞移植分布不均匀有关的继发性疾病[9]。 经过长时间随访证实自体软骨细胞移植术后症状可以持续改善,虽然与非运动员相比,有症状损伤的运动员可能会从中获得更大的益处,但短期和中期结果提示均可以改善两者的生活质量。EBERT等[45]在第3代自体软骨细胞移植术后分别评估了97例患者的等速膝关节力量,随访1,2,5年时分别有82.4%,85.6%和85.9%的患者恢复了娱乐活动的能力,并且运动能力和满意度逐年提高。很多研究都证实了自体软骨细胞移植的长期疗效,对100例自体骨软骨移植和自体软骨细胞移植患者进行10年随访,发现自体软骨细胞移植组术后10年的失败率比自体骨软骨移植组显著降低[38]。另一项研究对104例软骨缺损面积平均为4.77 cm2患者进行评估,随访长达10年,结果显示移植失败率为26%,而63%的患者功能恢复较好,25%的患者功能恢复良好,以及98%的受试者表示如果再次患病愿意再次接受相同的手术治疗,但同时结果也表明使用自体软骨细胞移植治疗慢性严重缺损的失败率较高[46]。 2.5.6 MRI检查结果 自体软骨细胞移植的一个可以预测的好处是能够再生类透明或透明样软骨界面,通过自体软骨细胞移植术后二次活检分析揭示再生组织覆盖了大部分的缺损区域以及大多数都有透明软骨层,并且免疫组化染色显示Ⅱ型胶原高表达[6,31,47]。自体软骨细胞移植的优势是可以再生透明软骨,但是修复后的软骨表层也会有纤维软骨的特性[9]。 在DIBARTOLA等[10]的综述中,30.9%的患者在第1代自体软骨细胞移植后显示再生100%透明软骨,23.5%的患者ICRS评分良好;38.3%的患者在第2代自体软骨细胞移植后显示再生100%透明软骨,21.5%的患者ICRS评分良好;29.8%的患者在第3代自体软骨细胞移植后显示再生100%透明软骨,9%的患者ICRS评分良好,尽管早期第3代自体软骨细胞移植修复效果较差,但是随着时间的推移移植物会继续成熟,活检标本也显示了透明质含量逐渐增加。SHARMA等[48]也得出了相同的结论,把修复组织中糖胺聚糖的成分与年龄相匹配的尸体关节软骨进行了比较,发现自体软骨细胞移植术后12个月的修复组织比尸体组织的透明质含量少40%,然而自体软骨细胞移植术后20个月修复组织的透明质含量与尸体标本相当。RUTA等[9]对71例受试者术后10年随访,对自体软骨细胞移植修复部位与健康软骨进行比较,发现成像分数有所下降,但功能结果评分比术前有所改善。此外,还发现了自体软骨细胞移植在修复软骨损伤时也会出现骨髓水肿、软骨下囊肿和内骨赘等并发症[39]。 2.5.7 缺损填充 影像学技术的发展,使监测和评估手术疗效的方法多样化,通过各种影像学技术可以及时评估软骨修复情况,通常可以明显看到软骨缺损面积随时间延长逐渐减小。RIBOH等[49]对运用第3代自体软骨细胞移植技术治疗的软骨缺损填充程度进行了评估,随访时间为2年,采用MRI T2加权扫描,评估软骨缺损填充情况时使用ICRS分级标准,在术后第3-6个月,观察到移植物厚度增长最大为0.3 mm,增长了10.7%,2年后移植物达到最大厚度,平均增长0.44 mm,增长了15.7%,然而长期随访结果显示在术后第3-6个月之间移植物厚度增长小的患者,2年后不完全缺陷填充率较高。研究还发现尽管存在上述差异,但是如果使用IKDC和目测类比评分进行评估,临床结果无差异[49]。 2.6 局限性 相比之下第3代自体软骨细胞移植失败率较小,而第1代和第2代自体软骨细胞移植失败率较高[14]。自体软骨细胞移植术后活检标本显示透明质含量比其他软骨修复方法较高,但是大多数活检标本并非100%再生透明软骨组 织[6,47]。此外,与天然软骨相比,目前尚不清楚再生透明软骨组织的长期存活率。自体软骨细胞移植的一个主要限制是修复组织重塑和成熟的时间长,导致康复时间长达18个月,但是研究发现第3代自体软骨细胞移植术后的快速安全恢复运动方案可让患者在4-6个月内恢复运动[30-31]。各国对医疗产品的监管要求不同,也会限制自体软骨细胞移植在国际上的运用和研究,批准程序的繁琐也会延缓自体软骨细胞移植的运用。此外,成本和保险费用方面的限制,特别是运用第1代和第2代自体软骨细胞移植治疗髌骨缺损疗效较差,通常需同时行截骨术,导致费用较高,美国医疗保险仅将第3代自体软骨细胞移植治疗≥2 cm2的股骨髁或髌骨缺损纳入医保范围[50-52]。目前国内也没有将此种治疗方法纳入医疗保险范围。 "
| [1] CAMPBELL AB, PINEDA M, HARRIS JD, et al. Return to Sport After Articular Cartilage Repair in Athletes’ Knees: A Systematic Review. Arthroscopy. 2016;32(4): 651-668.e1. [2] KRYCH AJ, PAREEK A, KING AH, et al. Return to sport after the surgical management of articular cartilage lesions in the knee: a meta-analysis. Knee Surg Sports Traumatol Arthrosc. 2017;25(10):3186-3196. [3] NIELSEN ES, MCCAULEY JC, PULIDO PA, et al. Return to Sport and Recreational Activity After Osteochondral Allograft Transplantation in the Knee. Am J Sports Med. 2017;45(7):1608-1614. [4] LEPAGE SIM, ROBSON N, GILMORE H, et al. Beyond Cartilage Repair: The Role of the Osteochondral Unit in Joint Health and Disease. Tissue Eng Part B Rev. 2019;25(2):114-125. [5] PIPINO G, RISITANO S, ALVIANO F, et al. Microfractures and hydrogel scaffolds in the treatment of osteochondral knee defects: A clinical and histological evaluation. J Clin Orthop Trauma. 2019;10(1):67-75. [6] GREVENSTEIN D, MAMILOS A, SCHMITT VH, et al. Excellent histological results in terms of articular cartilage regeneration after spheroid-based autologous chondrocyte implantation (ACI). Knee Surg Sports Traumatol Arthrosc. 2020 Apr 10. doi: 10.1007/s00167-020-05976-9. Online ahead of print. [7] DIBARTOLA AC, WRIGHT BM, MAGNUSSEN RA, et al. Clinical Outcomes After Autologous Chondrocyte Implantation in Adolescents’ Knees: A Systematic Review. Arthroscopy. 2016;32(9):1905-1916. [8] NIETHAMMER TR, HOLZGRUBER M, GÜLECYÜZ MF, et al. Matrix based autologous chondrocyte implantation in children and adolescents: a match paired analysis in a follow-up over three years post-operation. Int Orthop. 2017;41(2):343-350. [9] RUTA DJ, VILLARREAL AD, RICHARDSON DR. Orthopedic Surgical Options for Joint Cartilage Repair and Restoration. Phys Med Rehabil Clin N Am. 2016;27(4):1019-1042. [10] DIBARTOLA AC, EVERHART JS, MAGNUSSEN RA, et al. Correlation between histological outcome and surgical cartilage repair technique in the knee: A meta-analysis. Knee. 2016;23(3):344-349. [11] NIETHAMMER TR, LIMBRUNNER K, BETZ OB, et al. Analysis of the autologous chondrocyte quality of matrix-based autologous chondrocyte implantation in the knee joint. Int Orthop. 2016;40(1):205-212. [12] YILMAZ EN, ZEUGOLIS DI. Electrospun Polymers in Cartilage Engineering-State of Play. Front Bioeng Biotechnol. 2020;8:77. [13] CAO C, ZHANG Y, YE Y, et al. Effects of cell phenotype and seeding density on the chondrogenic capacity of human osteoarthritic chondrocytes in type I collagen scaffolds. J Orthop Surg Res. 2020;15(1):120. [14] DAVIES RL, KUIPER NJ. Regenerative Medicine: A Review of the Evolution of Autologous Chondrocyte Implantation (ACI) Therapy. Bioengineering (Basel). 2019;6(1):22. [15] ISLAM A, FOSSUM V, HANSEN AK, et al. In vitro chondrogenic potency of surplus chondrocytes from autologous transplantation procedures does not predict short-term clinical outcomes. BMC Musculoskelet Disord. 2019;20(1):19. [16] EDWARDS PK, ACKLAND T, EBERT JR. Clinical rehabilitation guidelines for matrix-induced autologous chondrocyte implantation on the tibiofemoral joint. J Orthop Sports Phys Ther. 2014;44(2):102-119. [17] MARTINČIČ D, MEKAČ J, DROBNIČ M. Survival Rates of Various Autologous Chondrocyte Grafts and Concomitant Procedures. A Prospective Single-Center Study over 18 Years. Cell Transplant. 2019;28(11):1439-1444. [18] JONES KJ, CASH BM. Matrix-Induced Autologous Chondrocyte Implantation With Autologous Bone Grafting for Osteochondral Lesions of the Femoral Trochlea. Arthrosc Tech. 2019;8(3):e259-e266. [19] MINAS T, OGURA T, HEADRICK J, et al. Autologous Chondrocyte Implantation “Sandwich” Technique Compared With Autologous Bone Grafting for Deep Osteochondral Lesions in the Knee. Am J Sports Med. 2018;46(2):322-332. [20] YOON KH, PARK JY, LEE JY, et al. Costal Chondrocyte-Derived Pellet-Type Autologous Chondrocyte Implantation for Treatment of Articular Cartilage Defect. Am J Sports Med. 2020;48(5):1236-1245. [21] NIEMEYER P, LAUTE V, ZINSER W, et al. A Prospective, Randomized, Open-Label, Multicenter, Phase III Noninferiority Trial to Compare the Clinical Efficacy of Matrix-Associated Autologous Chondrocyte Implantation With Spheroid Technology Versus Arthroscopic Microfracture for Cartilage Defects of the Knee. Orthop J Sports Med. 2019;7(7):2325967119854442. [22] ZARKADIS NJ, KUSNEZOV NA, GARCIA EJ, et al. Return to Preoperative Function After Autologous Cartilage Implantation of the Knee in Active Military Servicemembers. Orthop J Sports Med. 2017;5(5):2325967117706057. [23] NIMKINGRATANA P, BRITTBERG M. Returning to Work After Articular Cartilage Repair Intervention: A Systematic Review. Orthop J Sports Med. 2020;8(3): 2325967120905526. [24] OGURA T, MOSIER BA, BRYANT T, et al. A 20-Year Follow-up After First-Generation Autologous Chondrocyte Implantation. Am J Sports Med. 2017;45(12):2751-2761. [25] ALFORD JW, COLE BJ. Cartilage restoration, part 2: techniques, outcomes, and future directions. Am J Sports Med. 2005;33(3):443-460. [26] EBERT JR, JANES GC, WOOD DJ. Post-operative sport participation and satisfaction with return to activity after matrix-induced autologous chondrocyte implantation in the knee. Int J Sports Phys Ther. 2020;15(1):1-11. [27] CHAHAL J, ROGERS BA, GROSS AE. Surgical Approach to Articular Cartilage Repair // GAHUNIA HK, GROSS AE, PRITZKER KPH, et al. Articular Cartilage of the Knee: Health, Disease and Therapy. New York, NY: Springer, 2020:289-314. [28] ERICKSON BJ, STRICKLAND SM, GOMOLL AH. Indications, Techniques, Outcomes for Matrix-Induced Autologous Chondrocyte Implantation (MACI). Operative Techniques in Sports Medicine. 2018;26(3):175-182. [29] NHO SJ, PENSAK MJ, SEIGERMAN DA, et al. Rehabilitation after autologous chondrocyte implantation in athletes. Clin Sports Med. 2010;29(2):267-282. [30] BUCHER TA, EBERT JR, JANES GC, et al. Arthroscopic Matrix-Induced Autologous Chondrocyte Implantation// FARR J, GOMOLL AH. Cartilage Restoration. New York, NY: Springer, 2018:153-160. [31] HEVESI M, KRYCH AJ, SARIS DBF. Treatment of Cartilage Defects With the Matrix-Induced Autologous Chondrocyte Implantation Cookie Cutter Technique. Arthrosc Tech. 2019;8(6):e591-e596. [32] PASCUAL-GARRIDO C, SLABAUGH MA, L’HEUREUX DR, et al. Recommendations and treatment outcomes for patellofemoral articular cartilage defects with autologous chondrocyte implantation: prospective evaluation at average 4-year follow-up. Am J Sports Med. 2009;37 Suppl 1:33S-41S. [33] FARR J. Autologous chondrocyte implantation improves patellofemoral cartilage treatment outcomes. Clin Orthop Relat Res. 2007;463:187-194. [34] BIANT LC, SIMONS M, GILLESPIE T, et al. Cell Viability in Arthroscopic Versus Open Autologous Chondrocyte Implantation. Am J Sports Med. 2017;45(1):77-81. [35] EBERT JR, FALLON M, WOOD DJ, et al. A Prospective Clinical and Radiological Evaluation at 5 Years After Arthroscopic Matrix-Induced Autologous Chondrocyte Implantation. Am J Sports Med. 2017;45(1):59-69. [36] ERICKSON B, FILLINGHAM Y, HELLMAN M, et al. Surgical management of large talar osteochondral defects using autologous chondrocyte implantation. Foot Ankle Surg. 2018;24(2):131-136. [37] NIXON AJ, SPARKS HD, BEGUM L, et al. Matrix-Induced Autologous Chondrocyte Implantation (MACI) Using a Cell-Seeded Collagen Membrane Improves Cartilage Healing in the Equine Model. J Bone Joint Surg Am. 2017;99(23):1987-1998. [38] BENTLEY G, BIANT LC, VIJAYAN S, et al. Minimum ten-year results of a prospective randomised study of autologous chondrocyte implantation versus mosaicplasty for symptomatic articular cartilage lesions of the knee. J Bone Joint Surg Br. 2012; 94(4):504-509. [39] ZHANG C, CAI YZ, LIN XJ. Autologous chondrocyte implantation: Is it likely to become a saviour of large-sized and full-thickness cartilage defect in young adult knee? Knee Surg Sports Traumatol Arthrosc. 2016;24(5):1643-1650. [40] HIRSCHMÜLLER A, SCHOCH W, BAUR H, et al. Rehabilitation before regenerative cartilage knee surgery: a new prehabilitation guideline based on the best available evidence. Arch Orthop Trauma Surg. 2019;139(2):217-230. [41] KON E, FILARDO G, BERRUTO M, et al. Articular cartilage treatment in high-level male soccer players: a prospective comparative study of arthroscopic second-generation autologous chondrocyte implantation versus microfracture. Am J Sports Med. 2011;39(12):2549-2457. [42] NIEMEYER P, KÖSTLER W, SALZMANN GM, et al. Autologous chondrocyte implantation for treatment of focal cartilage defects in patients age 40 years and older: A matched-pair analysis with 2-year follow-up. Am J Sports Med. 2010;38(12):2410-2416. [43] FARR J, GOMOLL AH. 2016 barriers to cartilage restoration. J Clin Orthop Trauma. 2016;7(3):183-186. [44] CVETANOVICH GL, RIBOH JC, TILTON AK, et al. Autologous Chondrocyte Implantation Improves Knee-Specific Functional Outcomes and Health-Related Quality of Life in Adolescent Patients. Am J Sports Med. 2017;45(1):70-76. [45] EBERT JR, SMITH A, JANES GC, et al. Association Between Isokinetic Knee Strength and Perceived Function and Patient Satisfaction With Sports and Recreational Ability After Matrix-Induced Autologous Chondrocyte Implantation. Orthop J Sports Med. 2019;7(12):2325967119885873. [46] BIANT LC, BENTLEY G, VIJAYAN S, et al. Long-term results of autologous chondrocyte implantation in the knee for chronic chondral and osteochondral defects. Am J Sports Med. 2014;42(9):2178-2183. [47] KIM MK, PARK JS, JEON YM, et al. Clinical, radiological, and histological outcomes after the fibrin-matrix autologous chondrocyte implantation for chondral lesions of the knee in patients more than 50 years old: A prospective case series with minimum 2-year follow-up. J Orthop Surg (Hong Kong). 2020; 28(1):2309499019893509. [48] SHARMA A, REES D, ROBERTS S, et al. A case study: Glycosaminoglycan profiles of autologous chondrocyte implantation (ACI) tissue improve as the tissue matures. Knee. 2017;24(1):149-157. [49] RIBOH JC, CVETANOVICH GL, COLE BJ, et al. Comparative efficacy of cartilage repair procedures in the knee: a network meta-analysis. Knee Surg Sports Traumatol Arthrosc. 2017;25(12):3786-3799. [50] DEKKER TJ, ERICKSON B, ADAMS SB, et al. Topical Review: MACI as an Emerging Technology for the Treatment of Talar Osteochondral Lesions. Foot Ankle Int. 2017;38(9):1045-1048. [51] BASAD E, WISSING FR, FEHRENBACH P, et al. Matrix-induced autologous chondrocyte implantation (MACI) in the knee: clinical outcomes and challenges. Knee Surg Sports Traumatol Arthrosc. 2015;23(12):3729-3735. [52] BOUSHELL MK, HUNG CT, HUNZIKER EB, et al. Current strategies for integrative cartilage repair. Connect Tissue Res. 2017;58(5):393-406. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [3] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [4] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [5] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [6] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [7] | Liu Xiangxiang, Huang Yunmei, Chen Wenlie, Lin Ruhui, Lu Xiaodong, Li Zuanfang, Xu Yaye, Huang Meiya, Li Xihai. Ultrastructural changes of the white zone cells of the meniscus in a rat model of early osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1237-1242. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||