1.1 设计 细胞实验+动物实验。
1.2 时间及地点 实验于2025年4-8月在苏州大学骨科研究所完成。
1.3 材料
1.3.1 实验动物 6-8周龄C57BL/6雌性小鼠24只,SPF级,体质量18-22 g,购自杭州子源实验动物科技有限公司,许可证号:SCXK(浙)2019-0004。18月龄C57BL/6雌性小鼠6只,SPF级,体质量25-30 g,购自杭州子源实验动物科技有限公司,许可证号:SCXK(浙)2019-0004。实验已通过苏州大学动物实验伦理委员会审批(SUDA20250527A06),相关实验操作遵循实验动物管理规定。
1.3.2 实验试剂 α-MEM培养基(Hyclone公司);胎牛血清(东岭生物公司);PBS(赛国生物公司);小鼠髓源性抑制细胞分选试剂盒(Stemcell公司);cDNA合成试剂(Abm公司);抗酒石酸酸性磷酸酶染色试剂盒(Sigma公司);CD11b-BV510抗小鼠流式抗体、Gr1-PE/cy7抗小鼠流式抗体(BioLegend公司);小鼠白细胞介素6 ELISA 试剂盒、小鼠肿瘤坏死因子α ELISA试剂盒(伊莱瑞特生物公司);小鼠巨噬细胞集落刺激因子(近岸蛋白公司);小鼠核因子κB受体活化因子配体(R&D Systems公司)。
1.3.3 实验仪器 流式细胞仪(Thermo公司);荧光定量PCR仪(BIO-RAD公司);Micro-CT(SkyScan公司);光学显微镜(Leica,德国)。
1.4 实验方法
1.4.1 实验分组
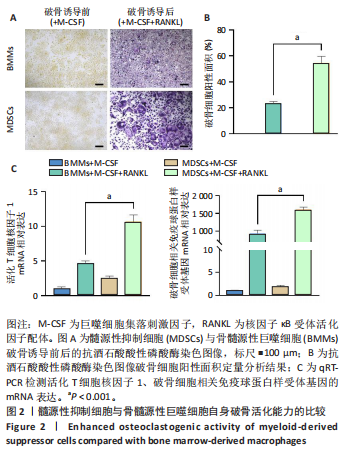
实验1:取6-8周龄雌性C57BL/6小鼠6只,其中3只用于分离提取髓源性抑制细胞,另3只用于分离提取骨髓源性巨噬细胞。将髓源性抑制细胞、骨髓源性巨噬细胞进行破骨诱导分化,破骨诱导5 d后,抗酒石酸酸性磷酸酶染色检测破骨细胞形成;破骨诱导3 d后,qRT-PCR检测活化T细胞核因子1、破骨细胞相关免疫球蛋白样受体基因的mRNA表达。
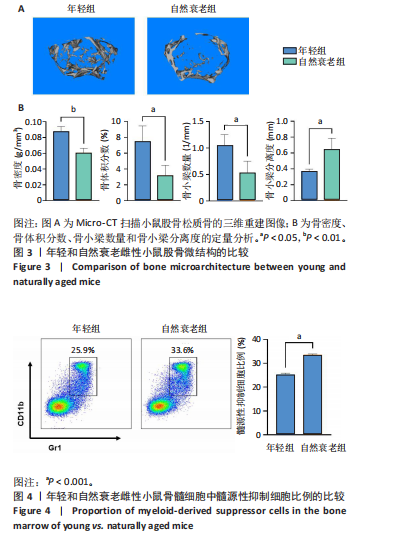
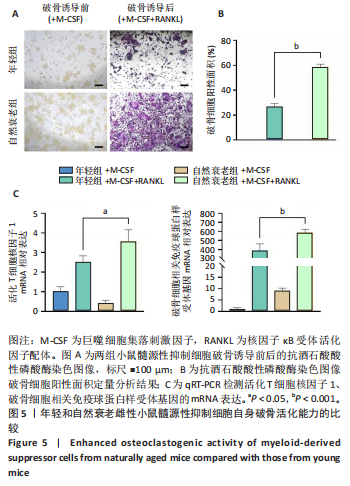
实验2:取6-8周龄雌性C57BL/6小鼠(年轻组,n=6)与18月龄雌性C57BL/6小鼠(自然衰老组,n=6),通过Micro-CT分析股骨远端骨微结构;收集两组小鼠的骨髓细胞,流式细胞术检测髓源性抑制细胞比例;分离提取两组小鼠的髓源性抑制细胞,进行破骨诱导分化,破骨诱导5 d后,抗酒石酸酸性磷酸酶染色检测破骨细胞形成;破骨诱导3 d后,qRT-PCR检测活化T细胞核因子1、破骨细胞相关免疫球蛋白样受体基因的mRNA表达。
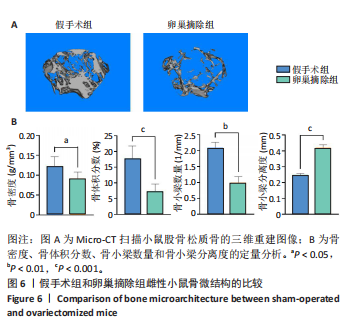
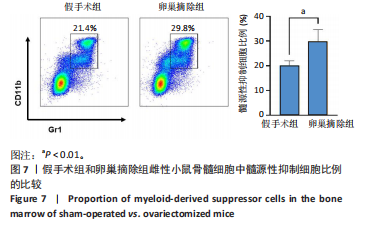
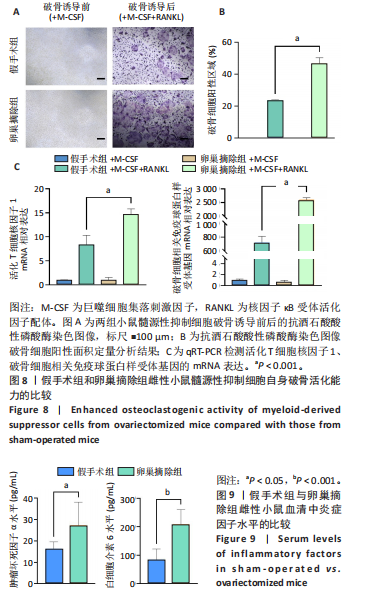
实验3:将12只6-8周龄雌性C57BL/6小鼠随机分为假手术组(n=6)、卵巢摘除组(n=6)。腹腔注射2%戊巴比妥钠(50 mg/kg)麻醉小鼠后固定于鼠板上,无菌条件下开展手术操作,假手术组腹腔切开后查找卵巢后将其复位,缝合腹腔;卵巢摘除组腹腔切开后查找双侧卵巢,实施结扎及卵巢切除术后缝合腹腔。术后连续3 d腹腔注射青霉素钠100 U/g,预防感染。卵巢摘除8周后,通过Micro-CT分析股骨密度降低说明造模成功。验证造模成功后,腹腔注射2%戊巴比妥钠(50 mg/kg)麻醉后处死小鼠,眼眶取血1 mL,分离血清,ELISA法检测血清中肿瘤坏死因子α与白细胞介素6水平;通过Micro-CT分析右侧股骨远端骨微结构;收集两组小鼠左侧股骨骨髓细胞,流式细胞术检测髓源性抑制细胞比例,分离提取髓源性抑制细胞进行破骨诱导分化,破骨诱导5 d后,抗酒石酸酸性磷酸酶染色检测破骨细胞形成;破骨诱导3 d后,qRT-PCR检测活化T细胞核因子1、破骨细胞相关免疫球蛋白样受体基因的mRNA表达。
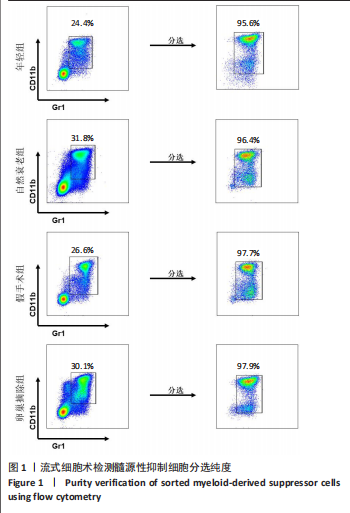
1.4.2 髓源性抑制细胞的提取与分选 腹腔注射2%戊巴比妥钠(50 mg/kg)麻醉后处死小鼠,浸泡于体积分数75%乙醇中消毒10 min,随后转移至超净工作台;使用已灭菌的手术器械取出小鼠后肢,置于体积分数75%乙醇中浸泡1 min以进一步消

毒;剥离后肢肌肉,使胫骨与股骨充分暴露,放入PBS中浸泡2 min;用无菌镊子剪开胫骨和股骨的两端,以无菌注射器吸取含有1%双抗和体积分数10%胎牛血清的α-MEM培养基冲洗骨髓腔,收集骨髓细胞;300×g离心6 min后弃上清,将细胞重悬于含体积分数2%胎牛血清的PBS中。
将细胞转移至5 mL聚苯乙烯圆底管中,加入40 μL FcR阻断剂和50 μL细胞分离混合液,混匀后室温孵育10 min;将快速磁珠涡旋30 s后取75 μL加入细胞中,室温孵育5 min;用含体积分数2%胎牛血清的PBS将细胞体积加满至2 mL,混匀;将试管放入磁柱中并室温孵育3min;拿起磁铁,将分选下来的细胞倒入新试管中,用于后续实验。
1.4.3 骨髓源性巨噬细胞的提取 按照1.4.2中的方法获取骨髓细胞,收集细胞悬液,加入红细胞裂解液裂解红细胞;300×g离心6 min后弃上清,重悬细胞并接种于培养皿中,置于37 ℃、体积分数5% CO2 培养箱中静止培养16 h;吸取上清,300×g离心6 min后弃上清,更换含30 ng/mL巨噬细胞集落刺激因子的培养基[20],置于37 ℃、体积分数5% CO2 培养箱中静止培养3 d,进行后续实验。
1.4.4 流式细胞仪检测小鼠骨髓中髓源性抑制细胞比例 按照1.4.2中的方法获取骨髓细胞,300×g 离心6 min后弃上清,将细胞重悬于含体积分数2%胎牛血清的PBS中,取5×10⁵个细胞转移至1.5 mL EP管中;配制流式抗体工作液,在EP管中加入0.3 μL Gr1-PE-Cy7和0.3 μL CD11b-FITC,混匀后于室温避光孵育30 min;加入400 μL含体积分数2%胎牛血清的PBS清洗细胞,300×g离心6 min后去除上清;用400 μL 含体积分数2%胎牛血清的PBS重悬细胞,上机进行流式细胞术检测,使用FlowJo V10软件进行数据分析。
1.4.5 细胞的破骨活化诱导 计数髓源性抑制细胞(或骨髓源性巨噬细胞),以1×105/孔的密度接种于48孔板中,加入含30 ng/mL巨噬细胞集落刺激因子的培养基;待细胞贴壁后,实验组更换为含50 ng/mL核因子κB受体活化因子配体+30 ng/mL巨噬细胞集落刺激因子的破骨细胞诱导分化培养基[21],对照组更换为新的含30 ng/mL巨噬细胞集落刺激因子的培养基,置于37 ℃、体积分数5% CO2 培养箱中培养,每3 d换液1次;诱导3 d后提取细胞总RNA进行qRT-PCR检测,诱导5 d后进行抗酒石酸酸性磷酸酶染色。
1.4.6 细胞抗酒石酸酸性磷酸酶染色 诱导5 d后弃培养基,用PBS清洗细胞2次,每次5 min;40 g/L多聚甲醛固定细胞15 min;将固红GBC盐溶液与亚硝酸钠溶液加入预热至37 ℃的双蒸水中,混匀后室温静置2 min,按照抗酒石酸酸性磷酸酶染色试剂盒说明书配置染色工作液;将配制好的抗酒石酸酸性磷酸酶染色液滴加至孔板内,置于37 ℃避光孵育30 min;通过光学显微镜观察染色结果并拍照记录,结合Image J软件分析破骨细胞阳性面积。
1.4.7 qRT-PCR检测破骨细胞活化相关基因表达 破骨诱导培养的第3天,弃培养基,用PBS清洗细胞1次;加入1 mL Trizol裂解细胞,使细胞充分裂解;添加200 μL氯仿,轻柔颠倒混匀30 s,置于4 ℃静置10 min;13 000 r/min离心10 min,取上层透明液约400 μL,加入等体积(400 μL)异丙醇,混匀30 s后置于4 ℃孵育10 min;13 000 r/min离心10 min后弃上清,用体积分数75%乙醇洗涤RNA沉淀,13 000 r/min离心10 min后弃上清,此过程重复2次;轻轻晾干RNA沉淀,加入10-20 μL DEPC水,在58 ℃金属浴条件下充分溶解8 min;采用RNA浓度检测仪测量RNA浓度,根据说明书将RNA反转录成cDNA,通过qRT-PCR法检测活化T细胞核因子1、破骨细胞相关免疫球蛋白样受体基因的mRNA表达。基因引物序列见表1。

1.4.8 Micro-CT操作及数据分析 使用SkyScan 1176 微计算机断层扫描仪,启动软件并预热仪器。将股骨样品放置于样品托盘指定位置,关闭扫描舱门,设置扫描参数:X射线电压50 kV,电流200 μA,铝滤片 0.5 mm,扫描分辨率4 000,扫描厚度9 μm,旋转角度70°。进行初步位置校准扫描,确保股骨干骺端位于扫描范围内。重命名样本文件并选择保存路径,启动扫描,完成后取出标本;使用 NRecon软件载入扫描文件,定位预览并选择重建区域。设置数据保存路径并添加至等待队列,点击“Start”启动重建;使用 Dataview 软件打开重建文件,调整视图并保存为数据库格式。通过CTAn软件加载处理后的文件,选择生长板上150层作为分析固定层数,圈定感兴趣区域,设定阈值范围,进行骨密度分析,保存数据并生成Slt 文件格式的三维原始数据。使用Mimics软件加载三维图像,保存固定角度图像,进一步分析骨体积分数、骨小梁数量与骨小梁分离度。
1.4.9 ELISA 法检测小鼠血清中相关炎症因子水平 采集的血样于4 ℃静置12 h后,1 500×g离心20 min,取200 μL血清;将血清加入预包被抗体的96孔板中,加入生物素标记检测抗体、孵育、洗板,加入 Avidin-HRP、显色底物、终止液,检测450 nm
波长处吸光度值,根据标准曲线计算炎性因子肿瘤坏死因子α和白细胞介素6水平。
1.5 主要观察指标 髓源性抑制细胞与骨髓源性巨噬细胞的破骨细胞分化能力,年轻组与自然衰老组小鼠的股骨远端骨微结构、骨髓细胞中髓源性抑制细胞比例、髓源性抑制细胞的破骨细胞分化能力,假手术组与卵巢摘除组小鼠的股骨远端骨微结构、骨髓细胞中髓源性抑制细胞比例、血清中炎症因子水平以及髓源性抑制细胞的破骨细胞分化能力。
1.6 统计学分析 所有数据均以x±s表示,统计学分析采用GraphPad Prism 9.0.0软件进行。两组间比较采用非配对t检验,超过两组数据的比较则采用单因素方差分析(ANOVA)。统计学显著性水平设定为P < 0.05。文章统计学方法已经通过苏州大学生物统计学专家审核。