中国组织工程研究 ›› 2023, Vol. 27 ›› Issue (15): 2356-2362.doi: 10.12307/2023.622
• 干细胞基础实验 basic experiments of stem cells • 上一篇 下一篇
CRISPR/Cas9技术联合脂质体转染子宫内膜癌细胞单质粒基因敲除方法首次编辑免疫相关基因HLA-DRA
蔡 波1,2,李晓晓1,2,张凌寒1,2,刘彦星1,2,毛跟红1,2
- 1郑州大学医学科学院,河南省郑州市 450014;2郑州大学第二附属医院,河南省郑州市 450014
Editing immune-related gene HLA-DRA for the first time by CRISPR/Cas9 technology combined with liposome transfection of endometrial cancer cells with single-plasmid gene knockout method
Cai Bo1, 2, Li Xiaoxiao1, 2, Zhang Linghan1, 2, Liu Yanxing1, 2, Mao Genhong1, 2
- 1Academy of Medical Sciences, Zhengzhou University, Zhengzhou 450014, Henan Province, China; 2Second Affiliated Hospital of Zhengzhou University, Zhengzhou 450014, Henan Province, China
摘要:
文题释义:
CRISPR/Cas9技术:是一种新型的基因编辑技术,具有较强的基因编辑活性,现已被广泛应用于细菌、动物及人类细胞等多领域的科学研究中。
HLA-DRA:HLA-DRA基因在免疫系统中发挥重要功能,此外该基因也被证实是多种肿瘤的独立预后因子,在肿瘤的早期发现和预后评估中起着至关重要的作用。
HEC-1-A细胞株:HEC-1-A细胞是人子宫内膜腺癌细胞,细胞形态为上皮细胞样,在37 ℃、体积分数6%CO2培养条件下贴壁生长。
背景:HLA-DR基因异常表达与多种肿瘤的进展及预后相关,采用CRISPR/Cas9技术编辑子宫内膜癌HLA-DRA基因的研究目前国内外尚未见报道。
目的:利用CRISPR/Cas9技术对HEC-1-A细胞的HLA-DRA基因靶向敲除,检测其敲除效率,并初步探索HLA-DRA基因的功能。
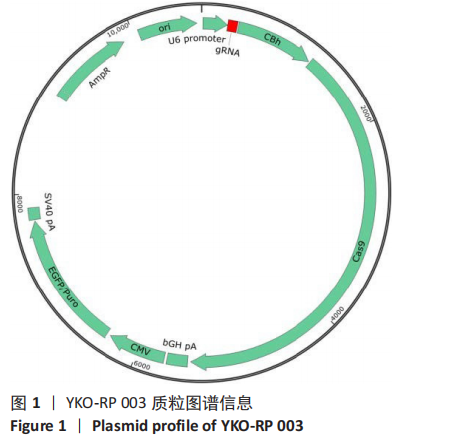
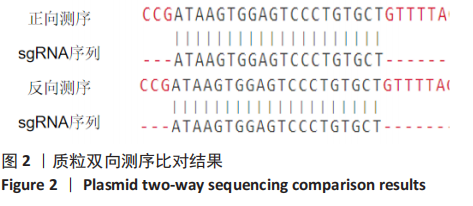
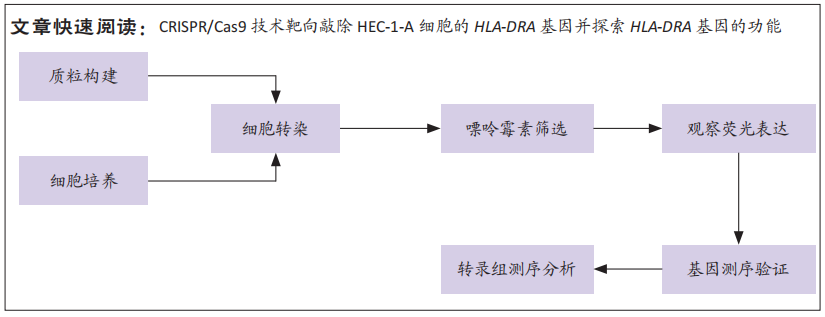
方法:根据HLA-DRA基因序列,针对HLA-DRA外显子设计单链向导RNA(sgRNA),分别将sgRNA、CRISPR/Cas9、增强绿色荧光蛋白和嘌呤霉素抗性克隆至YKO载体中,通过脂质体将sgRNA表达质粒转染到HEC-1-A细胞中。根据荧光表达,观察评估sgRNA敲除效果后,使用表达sgRNA的质粒进行转染,用最佳浓度的嘌呤霉素筛选,获得稳定的绿色荧光蛋白阳性表达细胞后,进行PCR、基因测序、转录组测序。
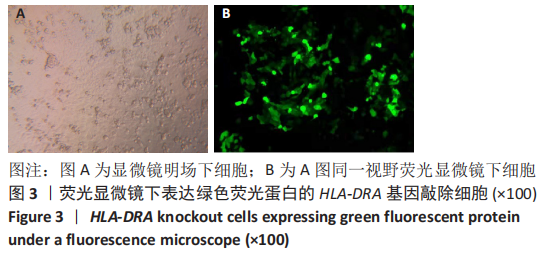
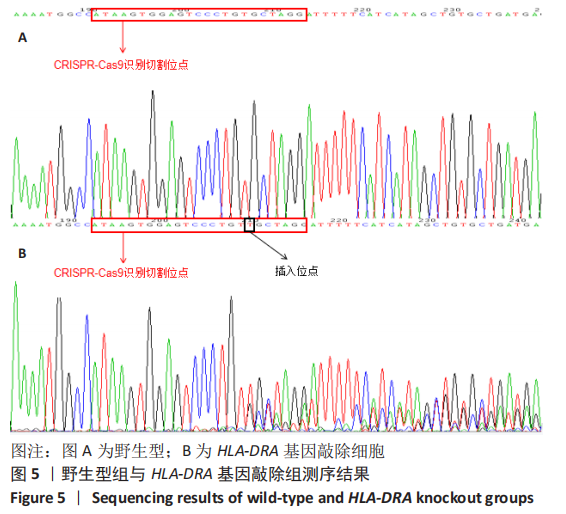
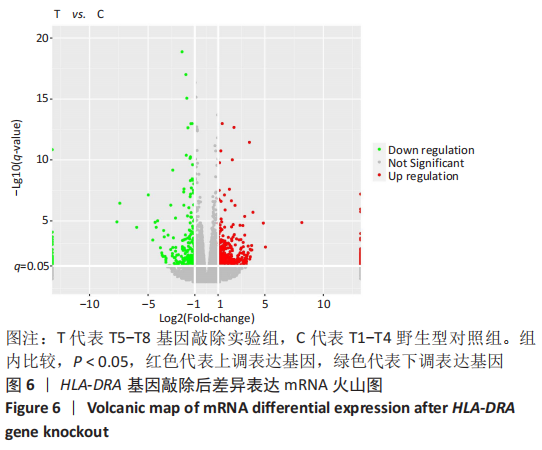
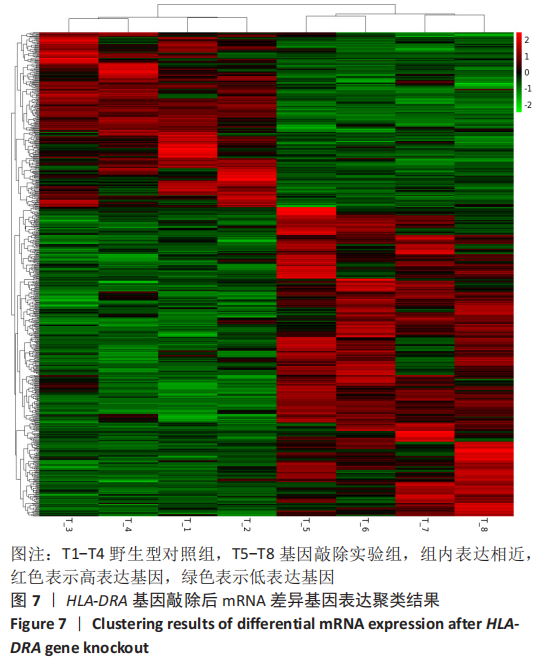
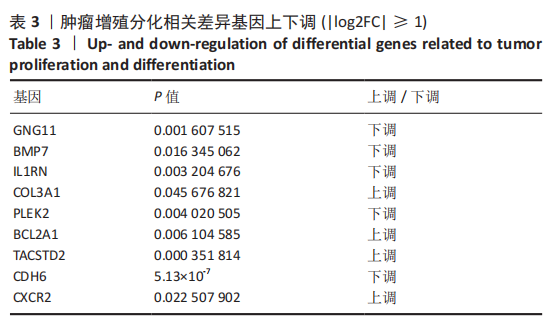
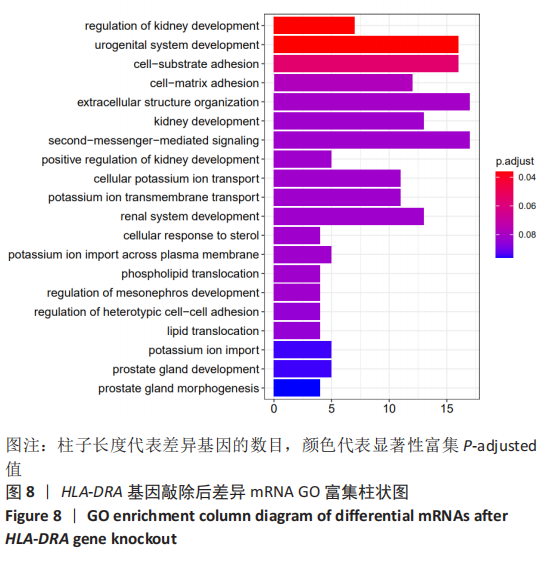
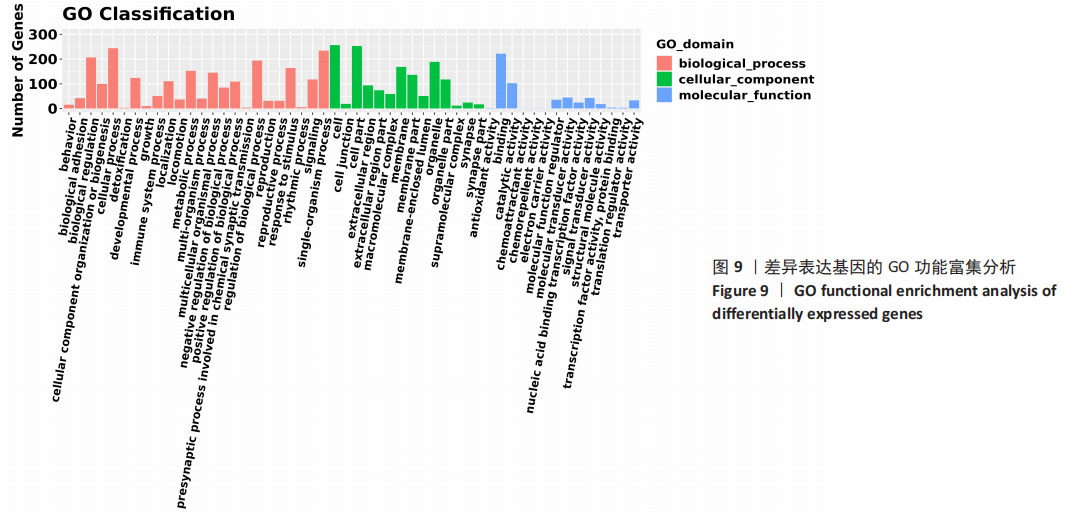
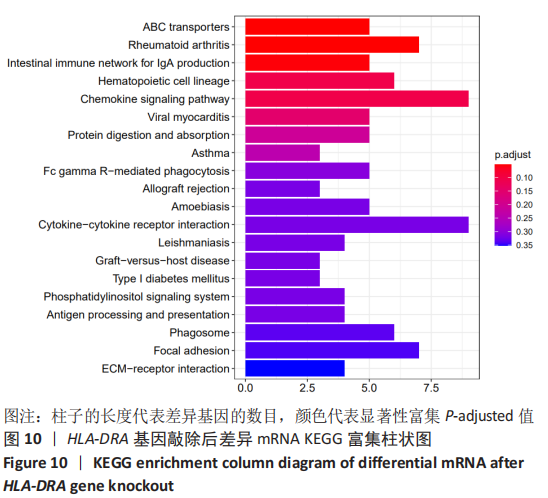
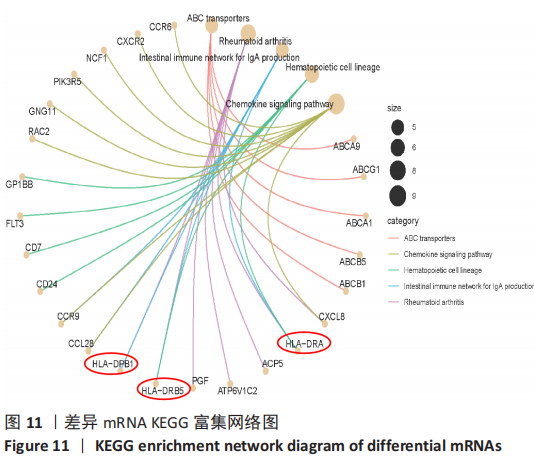
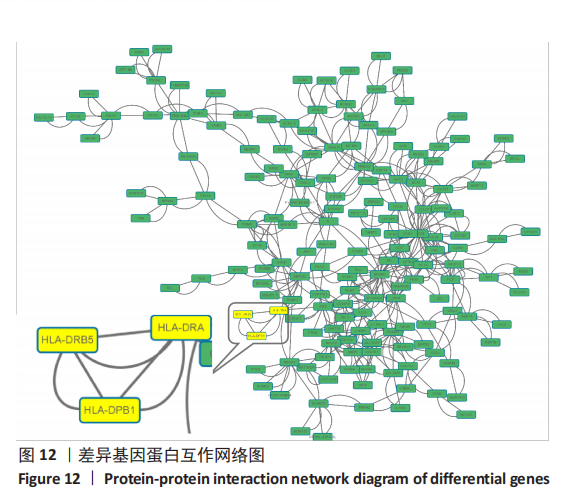
结果与结论:经转染和嘌呤霉素筛选后,获得稳定表达绿色荧光蛋白的HEC-1-A细胞,对其进行Sanger测序分析,结果显示HEC-1-A细胞中HLA-DRA第一号外显子基因被定向敲除,对转录组测序结果进行差异基因筛选,根据筛选所得686个差异表达基因进行GO富集分析和KEGG富集分析,构建蛋白互作网络图,通过对肿瘤增殖分化有关差异基因分析发现COL3A1、BCL2A1、TACSTD2、CXCR2等基因表达上调,GNG11、BMP7、IL1RN、PLEK2、CDH6等基因表达下调。结果可见,HLA-DRA基因参与了多种器官、组织和细胞的功能调控过程。此外,HLA-DRA基因可能通过2种途径(上调/下调)调控子宫内膜腺癌细胞的增殖、分化、迁移及侵袭过程。此研究建立了CRISPR/Cas9技术联合脂质体转染子宫内膜癌细胞的单质粒基因敲除方法,首次敲除子宫内膜癌免疫相关基因HLA-DRA,为子宫内膜癌免疫治疗的研究奠定实验基础。
https://orcid.org/0000-0002-8270-9165 (蔡波)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号: