中国组织工程研究 ›› 2021, Vol. 25 ›› Issue (25): 4032-4037.doi: 10.12307/2021.016
• 干细胞基础实验 basic experiments of stem cells • 上一篇 下一篇
不同诱导极化方式对大鼠骨髓来源巨噬细胞增殖、凋亡及吞噬能力的影响
李 莉1,2,卓 瑾1,2,郑 玲3,周 玲4,王启松1,2,罗 岚2,骆 凯2
- 1福建省口腔疾病研究重点实验室,福建省口腔生物材料工程技术研究中心,福建省高校口腔医学重点实验室,福建省福州市 350002;2福建医科大学口腔医学研究院,福建医科大学口腔组织工程研究中心,福建医科大学附属口腔医院,福建省福州市 350002;3福建武警总队医院,福建省福州市 350003;4福建省级机关医院,福建省福州市 350003
Effects of different induced polarization methods on the proliferation, apoptosis and phagocytosis of rat bone marrow-derived macrophages
Li Li1, 2, Zhuo Jin1, 2, Zheng Ling3, Zhou Ling4, Wang Qisong1, 2, Luo Lan2, Luo Kai2
- 1Fujian Key Laboratory of Oral Diseases & Fujian Provincial Engineering Research Center of Oral Biomaterial & Stomatological Key Laboratory of Fujian College and University, Fuzhou 350002, Fujian Province, China; 2Institute of Stomatology, Fujian Medical University & Center of Oral Tissue Engineering, Fujian Medical University & Hospital of Stomatology, Fujian Medical University, Fuzhou 350002, Fujian Province, China;
摘要:

文题释义:
骨髓源性巨噬细胞:人骨髓来源巨噬细胞分离自骨髓,骨髓细胞中存在未分化的巨噬细胞前体,通过加入巨噬细胞集落刺激因子来分化培养出巨噬细胞。巨噬细胞属免疫细胞,有多种功能,是研究细胞吞噬、细胞免疫和分子免疫学的重要对象。巨噬细胞属不繁殖细胞群,在适宜条件下可生活两三周,多用做原代培养,难以长期生存。
吞噬作用:高等动物具有一些特化的吞噬细胞,包括巨噬细胞和中性粒细胞。它们通过吞噬菌体摄取和消灭感染的细菌、病毒、损伤的细胞、衰老的红细胞。吞噬作用是生物体最古老的,也是最基本的防卫机制之一。对于其要消灭的对象无特异性,在免疫学中称之为非特异性免疫作用。
背景:经典激活巨噬细胞和替代激活巨噬细胞具有不同的表型和功能,目前尚鲜有研究探讨不同诱导方式对骨髓来源巨噬细胞生物学功能的影响。
目的:探讨不同诱导极化方式对大鼠骨髓来源巨噬细胞生物学行为的影响。
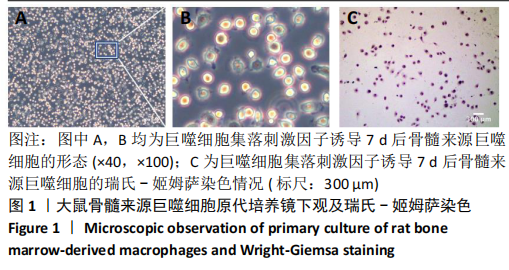
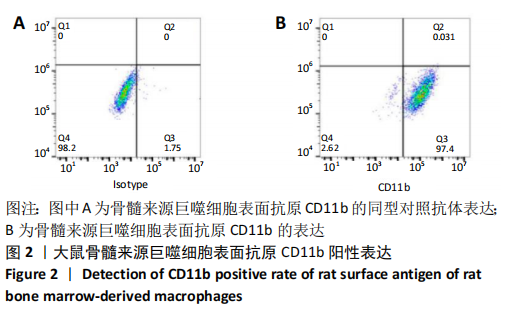
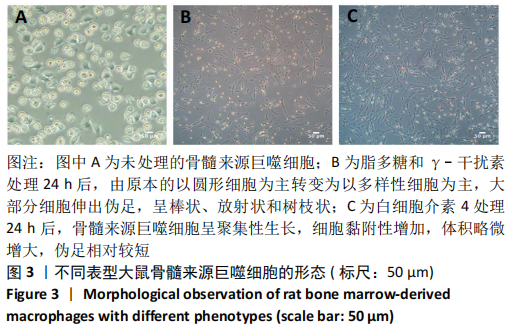
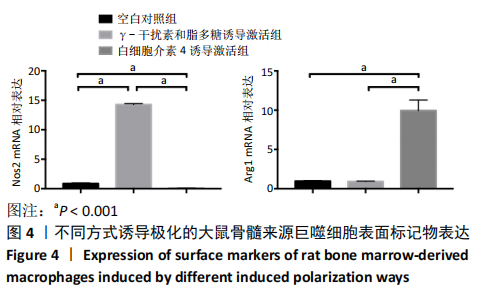
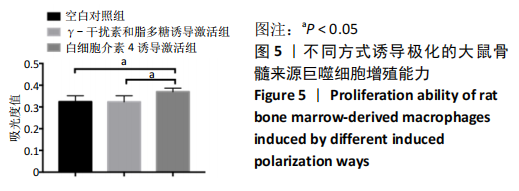
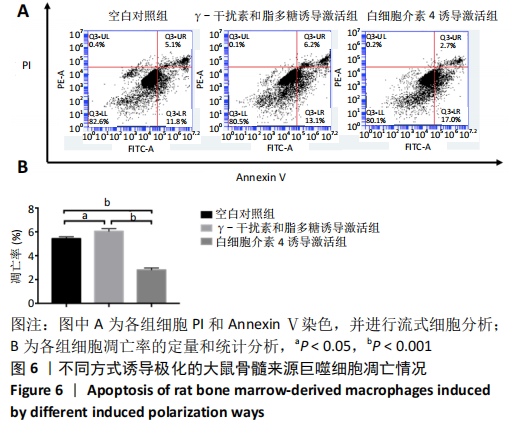
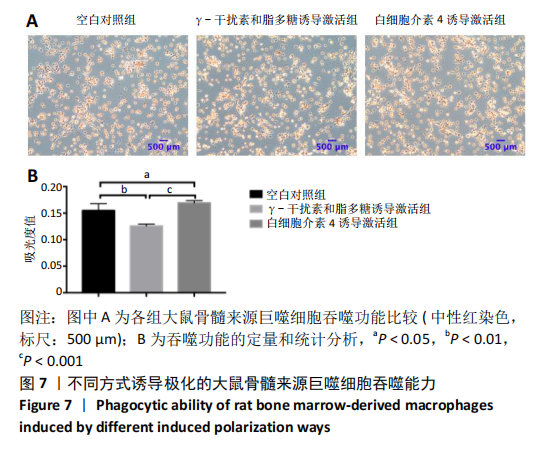
方法:通过原代细胞形态学观察、瑞氏染色和流式细胞术对体外分离培养的大鼠骨髓来源巨噬细胞进行鉴定。经γ-干扰素和脂多糖、白细胞介素4分别诱导激活24 h,倒置显微镜观察细胞形态,Real time-PCR检测细胞表面标记物Nos2和Arg1的表达,CCK-8法检测细胞增殖能力,流式细胞术检测细胞凋亡水平,中性红染色鉴定细胞吞噬功能。
结果与结论:经γ-干扰素和脂多糖联合刺激的骨髓来源巨噬细胞高表达M1型细胞表面标记物Nos2,可促进细胞凋亡并且降低细胞的吞噬功能;而经白细胞介素4刺激的骨髓来源巨噬细胞则高表达M2型细胞表面标记物Arg1,提高细胞增殖和吞噬能力,抑制细胞凋亡。结果表明,不同诱导极化方式可影响骨髓来源巨噬细胞的生物学行为。
https://orcid.org/0000-0003-4940-1203(李莉)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号: