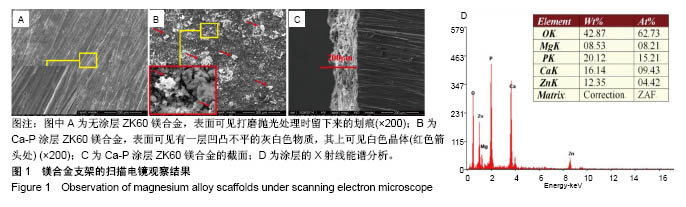
2.1 Ca-P涂层外表观察 电子显微镜下ZK60镁合金样品表面仅可见打磨抛光处理时留下来的划痕,见
图1A。
Ca-P涂层金属表面可见有一层凹凸不平的灰白色物质,其上可见白色晶体(红色箭头处),见图1B。
Ca-P涂层合金的截面图清楚可见涂层膜存在,涂层厚度是80-100 μm,见图1C。
材料X射线能谱仪分析表明该产品主要由O、Mg、P、Ca、Zn组成,Ca、P元素的原子数目比约为0.6,见图1D。
由此可知该产品可能为磷酸二氢钙和无水磷酸钙的混合物[12-13]。以上结果表明,ZK60镁合金表面生成了Ca-P涂层。
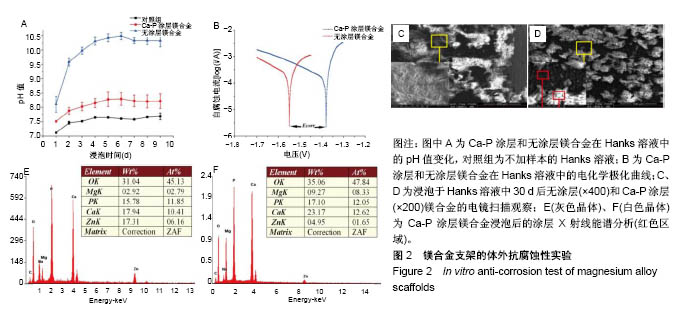
2.2 Ca-P涂层镁合金体外抗腐蚀性实验结果 各材料样本的腐蚀速率通过测量Hanks溶液pH值和电化学腐蚀测试结果确定。各组Hanks溶液pH值随浸泡时间的变化,见
图2A。所有组的pH值都有增加,Ca-P涂层ZK60镁合金溶液
pH值的变化明显低于无涂层ZK60镁合金。前6 d无涂层ZK60镁合金pH值从8.20增加到10.25,Ca-P涂层ZK60镁合金的pH值从7.50增加到8.25。Hanks溶液中pH值的增加主要是由于Mg或其合金的腐蚀,因此涂层合金的腐蚀速率低于无涂层样品的腐蚀速率[14]。此后,所有溶液的pH值保持10.25左右,这是由于此时镁合金表面己形成一定的保护层,且Hanks溶液里离子已达到一定平衡。耐腐蚀是使用镁合金作为骨科生物材料的关键问题,Ca-P涂层ZK60镁合金可满足这一要求,具有更好的耐蚀性。
无涂层和Ca-P涂层ZK60镁合金样本的电化学腐蚀测试结果,见图2B所示。Ca-P涂层后样本自腐蚀电压(Ecorr)值从-1.55 V变成-1.38 V,自腐蚀电流(Icorr)从55.54 μA变为38.19 μA,这表明采用Ca-P涂层改善了ZK60镁合金的耐蚀性。
无涂层和Ca-P涂层ZK60镁合金样品浸泡在Hanks溶液中30 d后的表面形态,见图2C,D所示。可以看出无涂层ZK60合金样本腐蚀严重,表面出现了明显大腐蚀坑,腐蚀产物沉积在Hanks溶液和材料表面上;而Ca-P涂层ZK60的表面仅可见腐蚀裂痕未见腐蚀坑,并且在表面生成了白色晶体。
通过对Ca-P涂层金属表面灰色晶体和白色晶体X射线能谱分析表明,其主要由O、Mg、P、Ca、Zn和C元素组成,如图2E,F;白色晶体相晶体的Ca/P比为1.0,黑色部分约为0.9,都比羟基磷灰石Ca/P比1.67小,接近二水磷酸钙(的Ca/P比1.0。这表明Ca-P涂层ZK60镁合金浸泡在Hanks溶液中后在材料表面上可能产生羟基磷灰石的前体二水磷酸钙[15]。这些都表明,表面上形成了类骨磷灰石[16]。
2.3 动物实验大体观察 术后实验动物情况良好,活动正常,体质量无明显改变,伤口愈合良好,无感染,均为甲级愈合,无意外死亡。正常饲养8周后,大鼠伤口己愈合,皮肤表面正常,没有出现组织结构异常。取股骨进行外表观察,空白组骨缺损部位骨修复比较少;ZK组缺损部位有所修复,但还是可看到有明显的缺损;其他实验组修复较空白组和ZK组好,但各组间看不出明显区别。
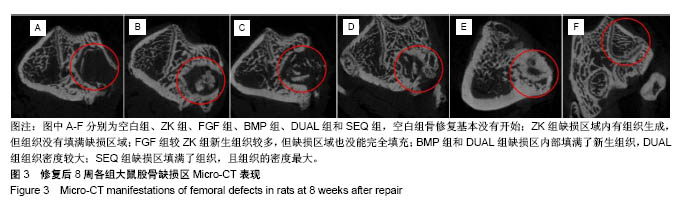
2.4 动物实验Micro-CT结果 空白组外表覆盖了一层软组织,缺损区内部几乎为空的,表明骨修复基本没有开始;ZK组缺损区域内有组织生成,但组织没有填满缺损区域;FGF组较ZK组新生组织较多,但是缺损区域也没能完全填充;BMP组和DUAL组缺损区内部填满了新生组织,DUAL组组织密度较大;SEQ组缺损区填满了组织,且组织的密度最大。通过二维断层扫描成像可清晰地看到缺损区域的内部结构,见图3。
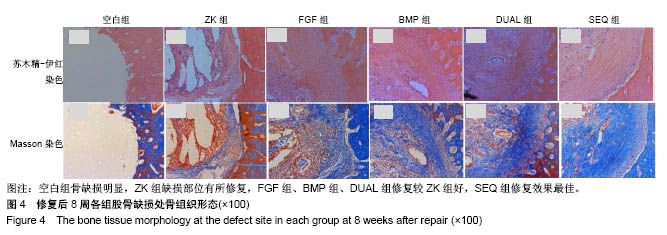
2.5 动物实验组织学观察 组织学观察包括苏木精-伊红和Masson染色,见
图4。苏木精-伊红染色显示,空白组几乎无新组织生成;ZK组在骨缺损区域有组织生成,但组织疏松且填充不充分;FGF组、BMP组、DUAL组、SEQ组骨缺损区域均有新生组织填充满,FGF组新生组织相较疏松,SEQ组可见金属降解后形成的碎渣,在新生组织及周围组织中均未见明显的炎症反应或坏死组织,表明材料在动物体内生物相容性较好。骨缺损区域新生组织组成无法确认,需要进一步染色明确是否为新生成的骨组织。
骨组织主要成分胶原可被Masson染色染成蓝色,不同组新生组织都有被染成蓝色的部分,说明缺损区域均有骨修复,每组被染蓝面积大小的区别说明修复程度区别。空白组未见明显新生组织;ZK组新生组织少部分为蓝色胶原组织,大部分为红色纤维组织;FGF组、BMP组、DUAL组和SEQ组缺损区均比ZK组被染蓝面积大,FGF组缺损区虽基本填充了新生组织,但其中所含胶原相对较少,BMP组和DUAL组相差不大,新生组织中胶原含量均高于FGF组,SEQ组新生组织中被染成蓝色的区域面积最大(图4)。
.jpg)



