中国组织工程研究 ›› 2020, Vol. 24 ›› Issue (22): 3460-3466.doi: 10.3969/j.issn.2095-4344.2299
• 药物控释材料 drug delivery materials • 上一篇 下一篇
水凝胶三维培养对人羊膜间充质干细胞特性及旁分泌效应的影响
王 旗,杨晓双,王达利
- 遵义医科大学附属医院整形外科,贵州省遵义市 563000
Effects of hydrogel three-dimensional culture on the characteristics of human amniotic mesenchymal stem cells and paracrine effect
Wang Qi, Yang Xiaoshuang, Wang Dali
- Department of Plastic Surgery, Affiliated Hospital of Zunyi Medical University, Zunyi 563000, Guizhou Province, China
摘要:

文题释义:
水凝胶三维培养:应用安全稳定的天然或合成聚合物材料为细胞提供一个空间、立体的生存环境,可增强细胞的黏附、增殖及分泌细胞因子能力。
旁分泌效应:以往研究认为干细胞应用于创面治疗的潜能是干细胞归巢分化为损伤组织,后来发现移植的干细胞大多停留在肝、脾,很少能到达损伤创面。目前研究证实间充质干细胞通过分泌某些营养因子作用于临近的靶细胞,起到促进创面愈合的作用。
背景:研究表明间充质干细胞在创面愈合中具有减轻炎症反应、促进创面愈合、减轻瘢痕形成的作用,然而以往的普通二维培养环境由于存在细胞间接触性抑制,可能导致细胞的基因表达、信号传导和形态学存在差异。
目的:观察人羊膜间充质干细胞旁分泌创面愈合相关因子的能力是否受二维培养环境与三维培养环境的影响。
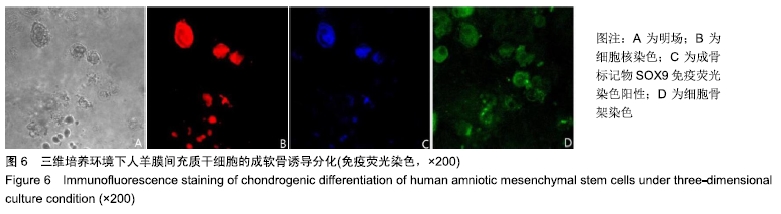
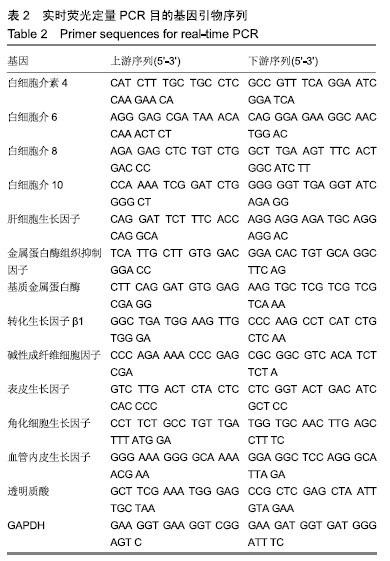
方法:利用传统酶消化法获得人羊膜间充质干细胞后,分别接种于普通细胞培养瓶(二维培养)与ShakeGelTM 3D水凝胶中(三维培养),将水凝胶中的人羊膜间充质干细胞分别进行成脂、成骨、成软骨诱导分化,免疫荧光染色确定细胞分化方向;待两种培养环境中的人羊膜间充质干细胞融合至70%-80%,于倒置相差显微镜和激光共聚焦显微镜下观察细胞的生长特点及形态;培养24 h后,应用RT-qPCR技术测定细胞旁分泌创面愈合相关因子的mRNA相对表达量;培养48 h后,利用ELISA试剂盒检测细胞旁分泌创面愈合相关因子的蛋白表达量。
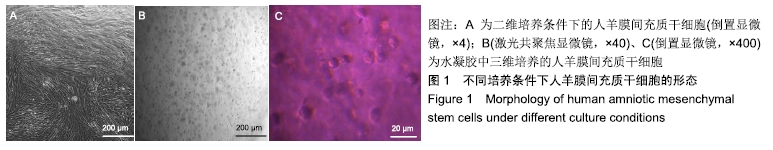
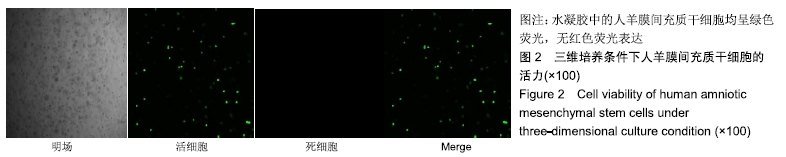
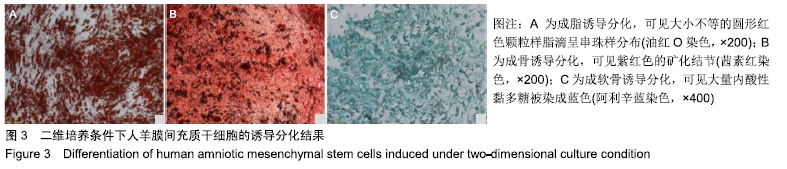
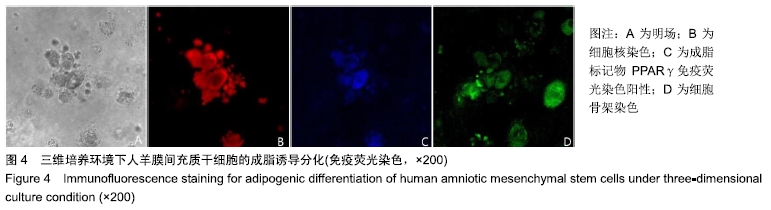
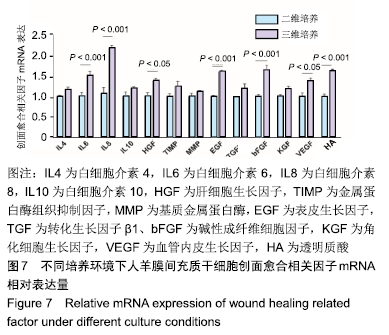
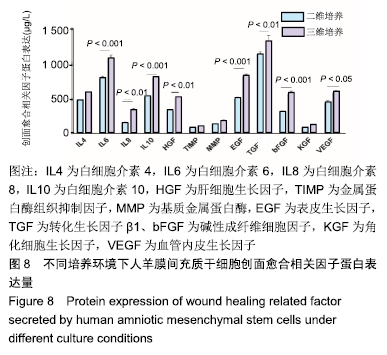
结果与结论:①二维培养组人羊膜间充质干细胞呈扁平状,为典型间充质样细胞形态;三维培养组人羊膜间充质干细胞呈圆形,均匀分散于水凝胶的每一层;②三维培养中的人羊膜间充质干细胞具有3系诱导分化潜能;③三维培养组白细胞介素6、白细胞介素8、表皮生长因子、碱性成纤维细胞因子、透明质酸、肝细胞生长因子、血管内皮生长因子mRNA相对表达量高于二维培养组(P < 0.001,P < 0.05),两组白细胞介素4、白细胞介素10、金属蛋白酶组织抑制因子、基质金属蛋白酶、转化生长因子、角化细胞生长因子mRNA相对表达量比较差异无显著性意义(P > 0.05);④三维培养组白细胞介素6、白细胞介素10、表皮生长因子、碱性成纤维细胞因子、白细胞介素8、肝细胞生长因子、转化生长因子β1、血管内皮生长因子蛋白表达量高于二维培养组(P < 0.001,P < 0.01,P < 0.05),两组白细胞介素4、金属蛋白酶组织抑制因子、基质金属蛋白酶、角化细胞生长因子蛋白表达量比较差异无显著性意义(P > 0.05);⑤结果表明,水凝胶三维培养环境中的人羊膜间充质干细胞可呈现更好的形态及创面修复相关因子旁分泌生物学效应。
ORCID: 0000-0002-9744-2176(王旗)
中国组织工程研究杂志出版内容重点:生物材料;骨生物材料; 口腔生物材料; 纳米材料; 缓释材料; 材料相容性;组织工程
中图分类号: