2.1 软骨损伤的细胞治疗策略 间充质干细胞具有向多种细胞分化潜能,具有跨胚层、跨系统分化特性。在损伤组织修复过程中,间充质干细胞在与微环境相互作用下向相应细胞分化。最早是在2001年成功分离出滑膜间充质干细胞
[16-17]。
Bianco等
[18]认为所有类型的干细胞都应该被其功能检测所定义,应用移植实验来检验干细胞自我更新和多向分化的性能。例如,需要通过形成畸胎瘤、嵌合体来鉴定胚胎干细胞的多能性;造血干细胞的造血功能鉴定需要证明能长期造血重建。
决定组织损伤修复成败的关键:良好的血供、细胞、细胞因子、适当的外界刺激(生化、物理等),以及损伤组织局部稳定的微环境。任何组织损伤后若没有良好的血液循环,损伤组织很难恢复到未损伤以前的自然形态。例如骨组织有良好的再生能力,然而到目前为止还没有一个令人满意的逆转骨缺血性坏死的方法
[19]。与骨不愈合的治疗目标相似
[20],软骨损伤的临床治疗导向也是希望在最短的时间内达到最佳的软骨愈合,尽可能获得最好的功能恢复并且尽量避免并发症的发生。
基于干细胞的软骨组织工程日益受到再生医学领域青睐,软骨组织工程可以从根本上缓解甚至是治愈软骨退行性病变
[12]。国际细胞治疗学会(International Society of Cell Therapy,ISCT)定义多能间充质细胞的最低标准包括3个方面
[21]:①标准培养条件下的塑料贴壁特性。②间充质干细胞必须表达CD73和CD90,CD105,并且不表达CD14,CD45,CD34,或者细胞表达表面分子CD11b,CD79α或CD19和HLA-DR。③具有明确的成骨、成软骨和成脂分化特性。间充质干细胞优先归巢到损伤组织中,提示其细胞治疗潜能
[12,22]。
Ogata等
[23]认为不同来源间充质干细胞的分化方向与其来源组织相似,因此制定应用干细胞治疗组织损伤的治疗策略,其细胞最理想来源应当根据其预期治疗的损伤组织来进行细胞分离纯化。与胚胎干细胞相比,间充质干细胞几乎没有致瘤性
[18,23],且美国食品药品管理局已批准间充质干细胞用于临床试验
[18]。
Yoshimura等
[8]将不同来源间充质干细胞2次传代后,鉴定每个群体细胞表面标记的共同特点为CD11b(-),CD45(-)和CD90(+)。滑膜衍生的有核细胞的集落数比骨髓衍生细胞集落高100倍。滑膜来源的间充质干细胞集落形成率、倍增速率和生长动力学也高于其他组织来源的间充质干细胞。体外软骨形成测定表明从滑膜衍生的软骨颗粒较重,这是因为与来自其他组织的间充质干细胞相比,滑膜间充质干细胞能产生更多的软骨基质,这显示了滑膜间充质干细胞在成软骨方向的优越性。滑膜间充质干细胞在多次传代后仍然保持成软骨特性。滑膜间充质干细胞有更高的成软骨特性和增殖能力
[8-9],这个结果说明滑膜间充质干细胞比骨髓间充质干细胞等其他组织来源的间充质干细胞有更强的成软骨分化能力,能更好地修复损伤软骨组织
[23-24]。
虽然滑膜间充质干细胞有关节修复的潜能。然而,它们在组织中的数量十分稀少,这意味着滑膜间充质干细胞不能被大量分离获得,需要培养扩增后获得一定数量的滑膜间充质干细胞再予以应用
[25]。
2.2 滑膜间充质干细胞分离研究进展 传统间充质干细胞分离方法有胶原酶消化单细胞悬液法。最近,开发了分离干细胞的非酶解移植技术。Lee等
[26]比较了这些技术在功能性骨髓间充质干细胞分离中的应用。干细胞是从骨关节炎患者的纤维和脂肪中分离得到,分别测量滑膜间充质干细胞和骨髓间充质干细胞总数的百分比,并测量扩增的间充质干细胞表面标志表达。用两种分离技术获得的间充质干细胞表现相似,表面标记为CD44、CD90、CD105,并展示相似的成脂、成骨、成软骨分化特性。
酶解技术和直接移植技术获得的间充质干细胞效果相似。移植技术较简单和创伤小,它可能超过酶解技术成为从骨关节炎患者滑膜中分离间充质干细胞的首选方法。
新的证据表明关节软骨和滑膜是从同一前体细胞发育而来,滑膜来源的成软骨细胞有稳定的成软骨活性,使滑膜成为修复关节软骨缺损的新的细胞来源
[15]。但是,成软骨诱导生长因子干预下的成软骨细胞很难生成透明质酸,导致软骨细胞肥大变性,失去成软骨能力。
滑膜间充质干细胞有较高的成骨、成软骨、成脂特性,不同组织来源间充质干细胞的抗原表达大致相同
[9]。体外培养的滑膜间充质干细胞表达如CD44,CD90,CD105和CD166,其也发现于成纤维细胞和间质细胞谱系,并且不表达造血细胞和内皮特异性标志物包括CD45,CD253a和CD31。最近报道的新标志为低亲和力神经生长因子受体(LNGFR)和THY-1。LNGFR
+,THY-1
+细胞为间充质干细胞样细胞,存在于胎盘和脂肪组织
[23]。滑膜间充质干细胞在成软骨分化后有很强的合成分泌浅区蛋白的作用
[7],对降低关节表面摩擦系数有很重要的作用。
2.3 细胞外基质对滑膜间充质干细胞功能的影响 细胞外基质与滑膜间充质干细胞的生物学特性关系密切。最近研究证明,细胞外基质成分对滑膜间充质干细胞的行为影响很大,特别是胎儿供体的脱细胞滑膜源细胞外基质,能使成人滑膜源干细胞恢复活性
[27]。在体外扩增培养滑膜间充质干细胞时,Tateishi等
[28]建议培养基中加用人血清取代胎牛血清,因为研究表明人滑膜间充质干细胞在加入人血清培养基中比在同水平胎牛血清下增殖速度更快,成软骨或成骨分化几乎出现在相同水平,而人血清与胎牛血清相比在人间充质干细胞扩增而不丢失成骨和成软骨分化能力方面更加优越。
滑膜间充质干细胞成骨作用与细胞外基质中的电解质(特别是Ca
2+)之间关系密切。Dry等
[25]研究高浓度Ca
2+促进滑膜间充质干细胞扩增,具体地说,体外培养滑膜间
充质干细胞生长高峰出现在Ca
2+浓度5.0 mmol/L。钙离子通道被阻止后,滑膜间充质干细胞的扩增速度会受到限制。滑膜间充质干细胞对Ca
2+的敏感性以前尚未报道。Dry等
[25]研究结果表明,可以通过补充Ca
2+的培养浓度来上调滑膜间充质干细胞的扩增速率。
2.4 炎性细胞和细胞因子对滑膜间充质干细胞成软骨作用的影响 干细胞疗法联合应用相关细胞因子能提高骨修复作用,Ho等
[29]学者通过研究大鼠骨缺损修复机制,发现骨髓间充质干细胞过表达基质细胞衍生因子1差异显著(
P=0.003)。结果表明,基质细胞衍生因子1通过招募宿主干细胞归巢,并促进成骨分化加速骨折修复。Kim等
[30]认为转化生长因子β1过表达促进人滑膜间充质干细胞增殖和成软骨分化,但不改变滑膜间充质干细胞的细胞表型。
在应用同种异体间充质干细胞移植治疗骨缺损过程中,T细胞也发挥了重要作用,T细胞通过下调干扰素γ诱导的RUNX-2通路和增强肿瘤坏死因子α信号实现介导外源性骨髓间充质干细胞修复骨缺损的过程。
通过核因子κB(NF-κB)的抑制作用,肿瘤坏死因子α转变干扰素γ激活信号,肿瘤坏死因子α受体超家族成员6(Fas)在骨髓间充质干细胞中的非凋亡形式——半胱天冬酶3和半胱天冬酶8相关的凋亡级联反应,导致这些细胞的凋亡
[31]。
最近发现,活化T细胞核因子1(nuclear factor of activated T cells 1,NFAT1)和活化T细胞核因子2 (nuclear factor of activated T cells 2,NFAT2)转录因子抑制软骨细胞肥大,保持关节软骨代谢平衡是在关节软骨修复领域的显著进步。滑膜干细胞调节上游转录过程,有助于保持关节软骨细胞的表型,以改善关节软骨的再生修复效果
[22]。
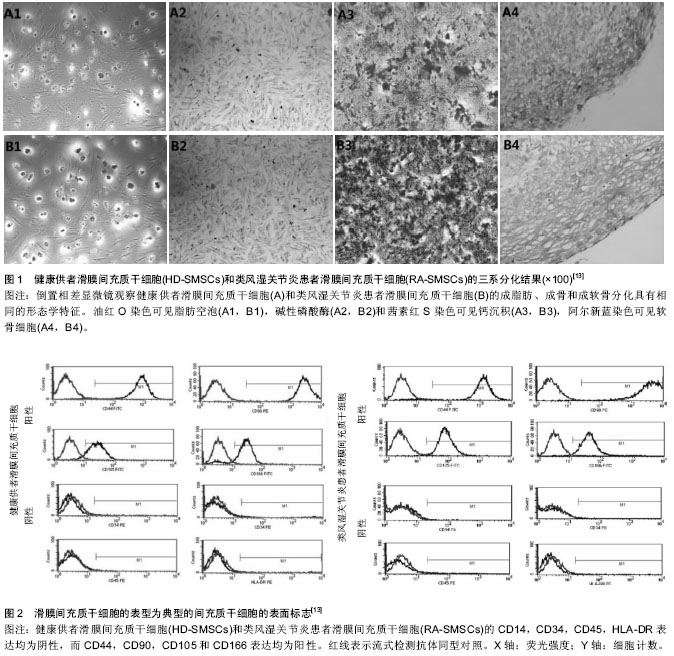
类风湿性关节炎是一种复杂的自身免疫性疾病,涉及多个系统,其特点是由炎性介质递导的软骨和骨的骨质破坏,这些炎症递质涉及白细胞介素17A、肿瘤坏死因子α、干扰素γ。Zhang等
[13]取22例类风湿关节炎患者的滑膜组织和8例半月板损伤(而无其他系统免疫疾病和结缔组织病的健康志愿者)的滑膜组织,比较其成脂、成骨、成软骨作用效果(
图1)。经过分析,两种来自不同组织的滑膜间充质干细胞的生长曲线、细胞活性差异无统计学意义。流式细胞术分析两种来源的滑膜间充质干细胞的细胞表型也完全一致(
图2),即CD14、CD34、CD45、HLA-DR均阴性表达,CD44、CD90、CD105 和CD166均阳性表达,说明滑膜间充质干细胞在类风湿关节炎局部微环境中并无免疫抑制作用。
体外培养时,类风湿关节炎患者滑膜间充质干细胞抑制滑膜T细胞增殖。单独培养滑膜T细胞时,加入白细胞介素17A或肿瘤坏死因子α,滑膜T细胞增殖不受抑制。在白细胞介素17A和肿瘤坏死因子α存在的情况下,健康供体的滑膜间充质干细胞不能抑制滑膜T细胞扩增
[13]。
Hagmann等
[32]认为骨关节炎患者的滑膜间充质干细胞能维持调节性T细胞(Treg)的表型。实验中骨髓间充质干细胞和滑膜间充质干细胞取自骨关节炎患者髋关节,将其分别与取自健康供体的富含CD4
+CD25
+ CD127
-的调节性T淋巴细胞(Treg)共培养。应用流式细胞仪分析调节性T淋巴细胞的比例,分析间充质干细胞的表面标记,结果显示共培养2 d和5 d后,与单独培养淋巴细胞相比,骨髓间充质干细胞和滑膜间充质干细胞能够保持调节性T淋巴细胞的比例。T细胞和间充质干细胞共培养与间充质干细胞单独培养相比,白细胞介素6增长显著。单独培养或与T细胞联合培养,滑膜间充质干细胞与骨髓间充质干细胞相比能产生更高的白细胞介素6。将外源性白细胞介素6加入培养基,能维持调节性T细胞数量的百分比,但是这种现象只能在应用间充质干细胞培养上清液时被观察到。Hagmann最终得到结论,骨关节炎患者的间充质干细胞产生白细胞介素6,介导维持调节性T细胞表型。Hagmann等第一次描述了骨关节炎患者的间充质干细胞与调节性T细胞在异体共培养模型中的相互作用。
骨骼发育和骨折愈合中血小板衍生生长因子发挥着重要的作用,但是目前机制尚未完全了解。血小板衍生生长因子AA可以激活BMP-Smad1/5/8通路,这需要骨形态发生蛋白受体Ⅰ以及血小板衍生生长因子受体α。血小板衍生生长因子AA通过BMP-Smad1/5/ 8-Runx2的OSX轴和经由BMP-Smad1/5/8-TWIST1、ATF4轴的间充质干细胞迁移促进间充质干细胞的成骨分化。血小板衍生生长因子AA激活BMP-Smad1/5/8的信号通过反馈下调骨形态发生蛋白受体α,从而释放骨形态发生蛋白
受体Ⅰ并允许骨形态发生蛋白受体Ⅰ-Ⅱ复合物形成激活BMP-Smad1/5/8
[33]。生长因子中的转化生长因子β1似乎有刺激细胞外基质形成和促进半月板Ⅱ型胶原调节行为。体外研究显示,转化生长因子β1是滑膜间充质干细胞生长和成软骨的关键因子
[24]。碱性成纤维细胞生长因子被发现是软骨基质中另一重要因子,它促进了关节软骨细胞、骨髓间充质干细胞、成骨细胞和脂肪细胞的增殖。此外,碱性成纤维细胞生长因子可保持任何类型细胞分化的能力。组织学显示其能增强细胞的增殖和表达α平滑肌肌动蛋白,但它并没有显着增强细胞外基质的主要成分或促进DNA的合成。但要说明的是,有些研究人员表明碱性成纤维细胞生长因子可以刺激细胞产生细胞外基质和促进组织发育,关于这个问题,尚需进一步研究。骨形态发生蛋白是转化生长因子β超家族的成员之一,其骨诱导潜能在胚胎形成和组织修复中有重要作用
[34]。骨形态发生蛋白7比骨形态发生蛋白2对骨髓间充质干细胞向软骨细胞分化有更强的诱导作用
[35]。联合应用适当的生长因子如转化生长因子β1、胰岛素样生长因子1,碱性成纤维细胞生长因子和骨形态发生蛋白能诱导骨骺修复治疗骨组织缺损
[13]。这些研究结果表明,许多细胞因子对滑膜间充质干细胞成软骨分化有积极的诱导作用。
