中国组织工程研究 ›› 2015, Vol. 19 ›› Issue (19): 3042-3048.doi: 10.3969/j.issn.2095-4344.2015.19.016
• 干细胞移植 stem cell transplantation • 上一篇 下一篇
脂肪干细胞移植对Duchenne型肌营养不良症鼠神经肌肉再生单位的影响
孔 杰1,2,操基清1,杨 娟1,陈 菲1,李亚勤1,黄汝成2,金远林2,张 成1
- 1中山大学第一附属医院神经科,广东省广州市 510080;2广州中医药大学附属宝安区中医院脑病科,广东省深圳市 518133
Effect of adipose stem cell transplantation on the neuromuscular regeneration unit of Duchenne muscular dystrophy mice
Kong Jie1, 2, Cao Ji-qing1, Yang Juan1, Chen Fei1, Li Ya-qin1, Huang Ru-cheng2, Jin Yuan-lin2,Zhang Cheng1
- 1Department of Neurology, First Affiliated Hospital of Sun Yat-sen University, Guangzhou 510080, Guangdong Province, China; 2Department of Encephalopathy, Baoan District Hospital of Traditional Chinese Medicine, Guangzhou University of Chinese Medicine, Shenzhen 518133, Guangdong Province, China
摘要:
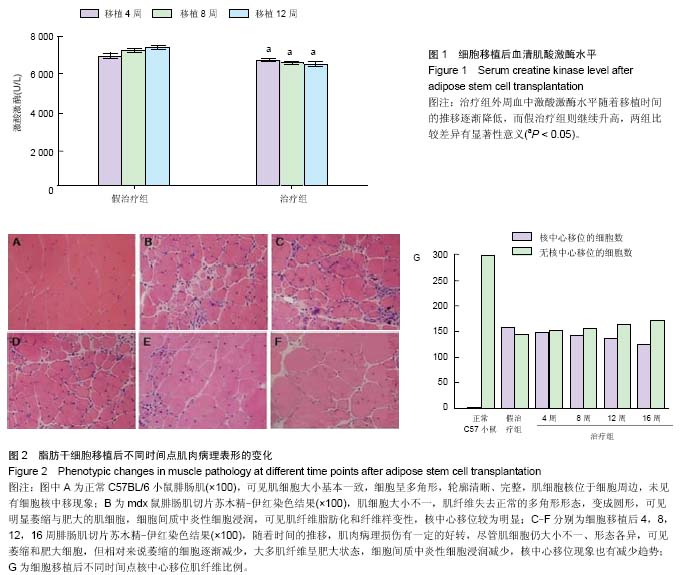
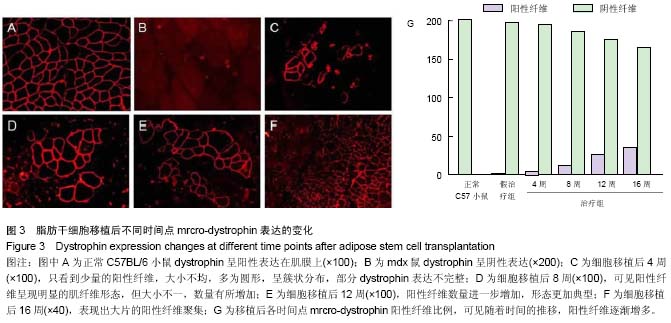
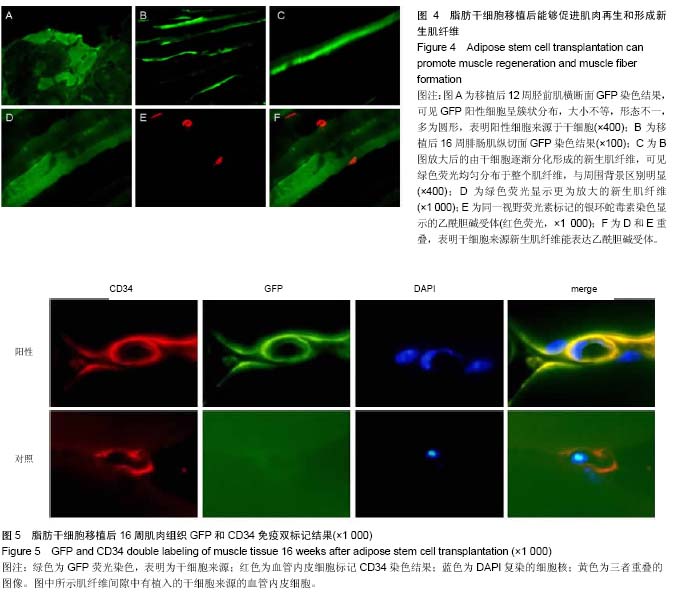
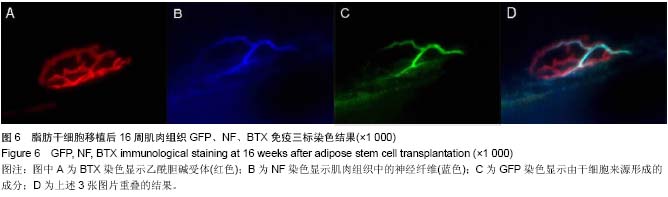
背景:目前,Duchenne型肌营养不良症尚无有效治疗方法,之前的研究表明基因治疗和干细胞移植治疗是可能的“治愈”方法。实验拟将两者结合起来,在动物模型上观察其疗效,并验证之前提出的神经肌肉再生单位的假说。 目的:探讨脂肪干细胞移植治疗Duchenne型肌营养不良症的有效性和可行性,观察细胞移植对肌纤维、新生血管及神经末梢的影响。 方法:体外分离培养mdx鼠脂肪干细胞,经杆状病毒基因载体进行基因修饰,用于移植治疗Duchenne型肌营养不良症模型鼠。移植后检测实验动物的血清肌酸激酶水平、肌肉病理改变及肌肉内dystrophin表达;免疫荧光检测细胞移植后血管、肌肉和神经再生情况。 结果与结论:细胞移植后,能够重建模型鼠的dystrophin表达,一定程度上减轻并逆转肌肉的病理损害,进而降低血清激酸激酶水平;此外,细胞移植后能够形成干细胞来源的肌纤维、血管内皮细胞和神经末梢。这些证据表明,脂肪干细胞移植是有希望治疗Duchenne型肌营养不良症的方法之一。
中图分类号: