中国组织工程研究 ›› 2015, Vol. 19 ›› Issue (14): 2172-2178.doi: 10.3969/j.issn.2095-4344.2015.14.008
• 干细胞移植 stem cell transplantation • 上一篇 下一篇
人脐带间充质干细胞移植治疗系统性红斑狼疮
阮光萍,姚 翔,刘菊芬,王金祥,胡媛媛,李自安,杨建勇,庞荣清,潘兴华
- 解放军成都军区昆明总医院细胞生物治疗中心,云南省昆明市 650032
Transplantation of human umbilical cord mesenchymal stem cells in the treatment of systemic lupus erythematosus
Ruan Guang-ping, Yao Xiang, Liu Ju-fen, Wang Jin-xiang, Hu Yuan-yuan, Li Zi-an, Yang Jian-yong, Pang Rong-qing, Pan Xing-hua
- The Cell Biological Therapy Center, Kunming General Hospital of Chengdu Military Command, Kunming 650032, Yunnan Province, China
摘要:
背景:系统性红斑狼疮是一种以多器官或多系统病变和血清中出现多种自身抗体为特征的自身免疫性疾病,目前缺乏有效的治疗方案,而理论上间充质干细胞可用于治疗系统性红斑狼疮。
目的:观察人脐带间充质干细胞移植治疗系统性红斑狼疮小鼠的疗效。
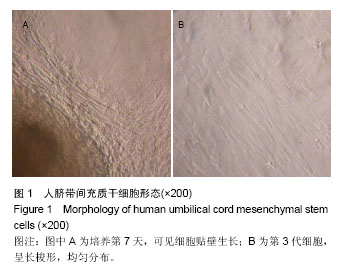
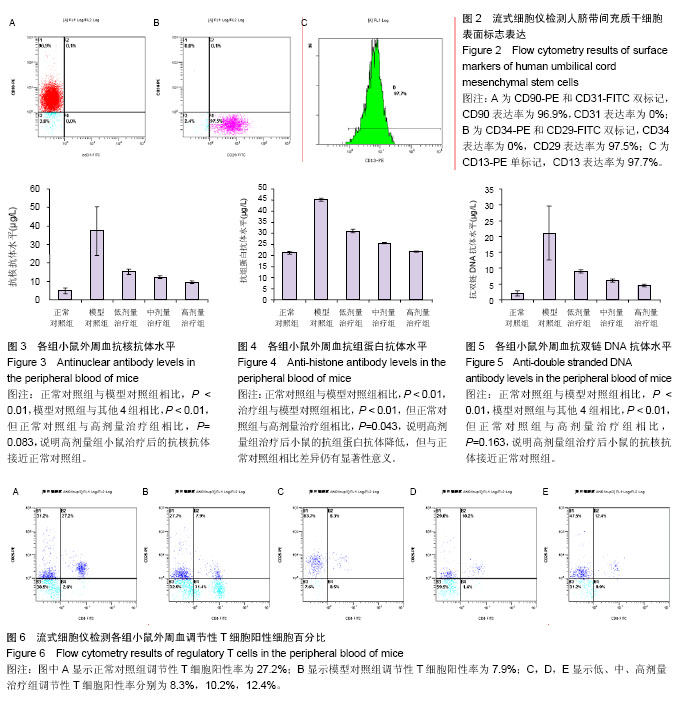
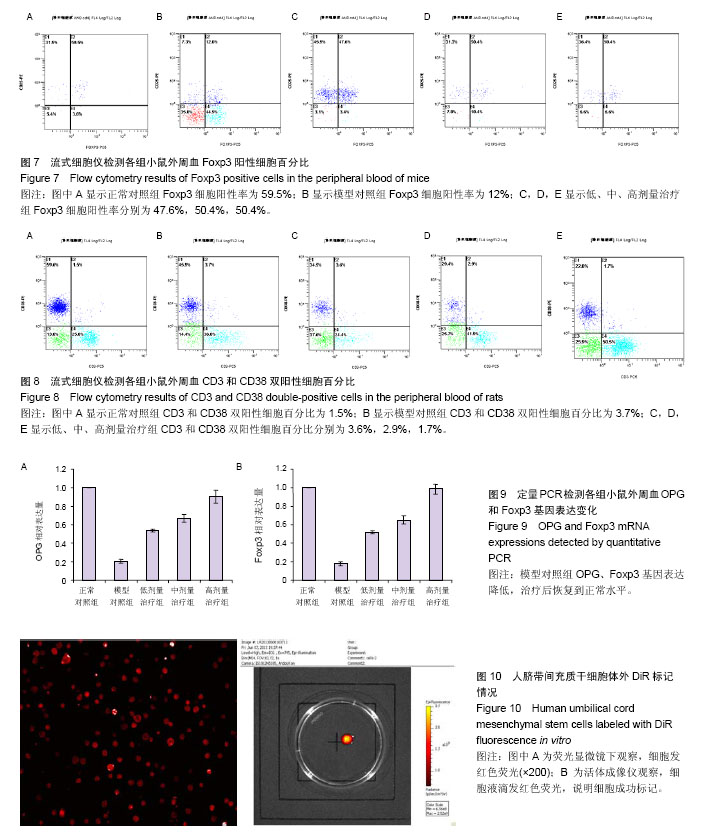
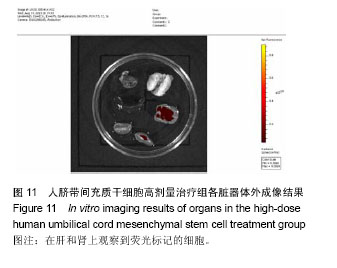
方法:分离培养人脐带间充质干细胞,并用深红色荧光DiR标记细胞。实验小鼠分5组:正常对照组(C57BL小鼠),模型对照组(C57BL/lpr小鼠),低、中、高剂量脐带间充质干细胞治疗组(C57BL/lpr小鼠),每组10只。各治疗组通过尾静脉注射低、中、高剂量(2×106,1×106,0.5×106个)脐带间充质干细胞,每周1次,连续3周,治疗结束采血测抗核抗体、抗组蛋白抗体、抗双链DNA抗体变化,定量PCR检测OPG和Foxp3基因表达的变化。
结果与结论:细胞移植3次后,外周血抗核抗体、抗组蛋白抗体、抗双链DNA抗体均明显下降,CD4+CD25+T细胞明显升高,OPG和Foxp3基因表达也明显升高,接近正常对照组,与模型对照组相比差异均有显著性意义(P < 0.01)。结果表明人脐带间充质干细胞能使C57BL/lpr小鼠的各项相关指标恢复到C57BL正常鼠水平,以高剂量治疗组效果最明显。
中图分类号:
.jpg)
.jpg)