3.1 小鼠胰岛素抵抗模型的建立及其对小肠黏膜通透性的影响 此次结果显示高脂饮食可以成功诱导C57BL/6J小鼠胰岛素抵抗模型,符合人类2型糖尿病的代谢特征。研究发现炎症反应与胰岛素抵抗之间存在相关性,诱导肥胖的小鼠可能因白色脂肪中相关炎症基因的表达增加,从而导致胰岛素分泌量的增加。此外,在组织学中发现,巨噬细胞浸润与炎症反应是肥胖诱导胰岛素抵抗的重要机制[14]。进行为期10周的高脂饮食导致肠道菌群结构改变并使肠道屏障功能受损,肠道内产生的脂多糖进入血液引发炎性因子释放,同时加重了肠道屏障的损伤,形成恶性循环[15]。实验证明,胰岛素抵抗小鼠存在肠黏膜屏障和通透性受损[16]。此次实验认为,脂多糖和右旋乳酸浓度均显著高于正常对照组,且二者呈正相关,表明高脂饮食成功构造了肠黏膜受损病理模型。
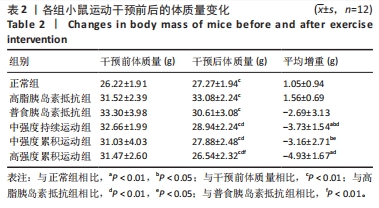
3.2 不同形式的运动对胰岛素抵抗小鼠糖代谢功能的影响 肥胖是导致胰岛素抵抗的重要因素之一,二者相互影响。目前全球肥胖人数在不断增加,研究表明肥胖人群中80%以上存在慢性炎症和胰岛素抵抗。但是,通过运动可以改变体质量,从而控制胰岛素抵抗。研究表明,有氧运动干预可以使高脂饮食诱导的肥胖大鼠的体质量和促炎因子水平显著降低[17]。有氧运动可以通过改变肠道菌群的成分,减轻机体的炎症反应,调节血脂代谢,从而达到减轻体质量和脂肪的目的。此次实验结果表明,运动干预后各胰岛素抵抗运动组小鼠的体质量均有显著降低,胰岛素抵抗的效果也有一定改善。此外,与单独的运动或饮食干预相比,运动结合饮食控制可以获得更好的减肥效果,而高强度的运动干预可以取得更显著的效果。
3.3 不同形式的运动对胰岛素抵抗小鼠肠黏膜屏障功能的影响
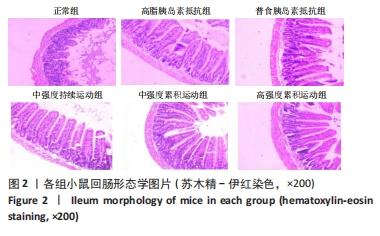
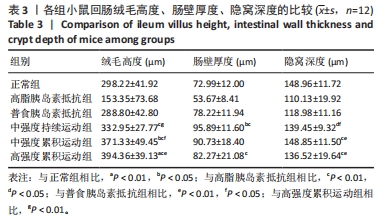
3.3.1 回肠苏木精-伊红染色形态学分析 现代人的饮食结构改变,摄入冰冷刺激食物、高脂高糖食物等对胃肠道造成长期挑战。肠道是人体重要的器官,具有消化、吸收和免疫功能。肠道机械屏障起关键作用,由肠道上皮细胞、细胞间紧密连接和黏膜层组成。内毒素增加、肠腔细菌产生右旋乳酸等会导致炎症因子释放、机体炎症水平改变,最终引起慢性炎症状态和胰岛素抵抗[18]。此次研究显示,累积运动对小鼠肠道起到一定的保护作用,大强度长时间的运动往往是提高运动能力的必要手段。但前人实验说明,过度训练会导致肠黏膜受损,不利于胰岛素抵抗的恢复;且大强度运动的过程中机体血液重新分配,大量的血液供给到运动系统和循环系统,肠道中血液量减少,运动后肠道内易形成缺血再灌注;在漫长的运动过程中,机体肠道内还会产生大量的自由基,破坏肠道上皮细胞。此次实验中强度持续运动对胰岛素抵抗小鼠的肠黏膜起到了一定的保护作用,肠绒毛高度、黏膜厚度以及隐窝深度与高脂胰岛素抵抗组比较均有显著性升高,但均低于累积运动的作用效果,这可能与持续运动的运动时间有关,而8周的累积运动,中强度累积运动对肠黏膜的保护作用最佳,这可能是因为中强度运动每次运动时间短、运动次数多,运动强度相对较小,不会使肠黏膜处于缺血状态,所以更有益于保护肠道上皮细胞不被损坏,保护肠黏膜基本形态。高强度累积运动对肠黏膜的作用结果也是有益的,特别是小肠绒毛高度的作用,但是该运动类型小肠绒毛出现了一定的水肿现象,绒毛基质疏松,这可能与短时间大强度对肠道带来的刺激有关。
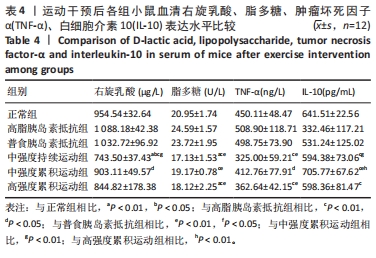
3.3.2 血清脂多糖、右旋乳酸及相关炎症因子的分析 脂多糖是革兰阴性菌细胞壁的主要成分,与类风湿因子样受体结合后会导致炎症因子白细胞介素6、TNF-α等的释放。在单核巨噬细胞表面与单核细胞表面抗原CD14形成复合物并被Toll样受体4识别时,脂多糖会引发骨骼肌细胞和脂肪细胞中Myd88的聚集,激活内毒素相关通路核因子κB途径和丝裂原活化蛋白激酶途径,导致一系列炎症因子,如TNF-α、IL-1β、IL-8、细胞间黏附分子1、诱导型一氧化氮合酶和单核细胞趋化蛋白的大量表达。
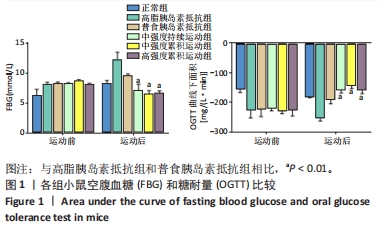
正常情况下,肠道细菌代谢所释放的内毒素可被肠壁吸收进入门静脉并通过肝脏的枯否细胞的吞饮作用被清除[19]。此次研究显示,3组运动组均较高脂胰岛素抵抗组和普食胰岛素抵抗组血清内毒素水平显著性降低,中强度持续运动组较正常组血清脂多糖水平还要低,说明3种运动方式均对血清脂多糖的水平具有下调作用,且3个运动组比较,中强度持续运动组效果最为显著,高强度累积运动组次之,中强度累积运动组与正常组没有差异性。
右旋乳酸是肠道里固有细菌的代谢产物。当肠道遭受紧急缺血等损伤导致肠黏膜通透性增加时,这些细菌会大量产生右旋乳酸,并通过受损的肠黏膜进入血液循环,导致血浆右旋乳酸水平升高。一般情况下,人体内的右旋乳酸含量很低,代谢缓慢,血液中的浓度相对稳定,可以通过检测来进行测量。此次实验结果显示,与高强度累积运动组相比,普食胰岛素抵抗组的血清右旋乳酸浓度都有了不同水平的降低,这说明胰岛素抵抗小鼠通过改善饮食,将高脂改为普通膳食,同样可以缓解肠黏膜的损伤程度,3个运动组较高脂胰岛素抵抗组和普食胰岛素抵抗组右旋乳酸水平也具有不同水平的降低,说明累积运动和持续运动均可降低循环血中的右旋乳酸水平,这可能与它们对肠黏膜屏障的保护作用有关。中强度持续运动组、中强度累积运动组与高强度累积运动组相比,通过运动加饮食的调节与控制,小肠黏膜得到了一定的保护,中强度持续运动效果较中强度累积运动效果好,可能是通过中强度的持续运动可以更好地调动脂肪供能、消耗脂肪,从而调节慢性炎症改善胰岛素抵抗和胃肠道健康。
当机体出现胰岛素抵抗时,会引起炎症因子的分泌改变,如TNF-α,进而影响机体对葡萄糖的代谢和胰岛素的敏感性。而运动可以减少炎症因子的分泌,从而改善胰岛素抵抗和炎症反应[20]。此外,肠道屏障功能障碍也是引起胰岛素抵抗的主要因素之一,高水平的TNF-α表达在其中扮演着重要的角色。TNF-α会影响葡萄糖转运蛋白4的表达,增加胰岛素受体底物1的丝氨酸化水平,扰乱机体组织对葡萄糖的摄取,从而导致胰岛素的敏感性下降。因此,在改善胰岛素抵抗和预防发生胰岛素抵抗方面,减少TNF-α表达和修复肠道屏障功能都具有重要的作用。
此次实验结果显示,中强度持续运动组、高强度累积运动组与高脂胰岛素抵抗组、普食胰岛素抵抗组比较,TNF-α水平均有很大程度降低;与正常组相比,中强度持续运动组、中强度累积运动组、高强度累积运动组TNF-α水平没有统计学意义,说明3组运动可以导致促炎因子TNF-α降低,且8周的运动可以使TNF-α的分泌水平达到正常范围内;与高脂胰岛素抵抗组相比,中强度持续运动组和高强度累积运动组能更好地降低胰岛素抵抗小鼠血清的促炎因子含量,但是与普食胰岛素抵抗组相比,中强度累积运动组无显著变化。此次实验提示中强度持续运动组、高强度累积运动组单纯运动的控制可以通过减少TNF-α的分泌从而改善慢性炎症,作用效果优于中强度累积运动组。
除了分泌促炎因子,机体组织还会释放抗炎因子,其中最具代表性的抗炎因子是IL-10。以往的研究指出,进行中强度的运动可以通过减少肠道促炎因子的分泌来提高抗氧化酶活性,并增加抗炎细胞因子IL-10的分泌。IL-10是机体组织释放的一种重要的抗炎因子,通过阻断核因子κB炎症通路的信号转导,进而抑制TNF-α、IL-6等促炎因子的分泌和表达[21]。这提示通过中强度的运动方式,有助于机体释放抗炎因子IL-10以缓解炎症反应,从而进一步保持身体的健康状态。
此次实验通过对抗炎因子IL-10的研究发现,3个运动组IL-10的血清含量与普食胰岛素抵抗组没有显著性差异,且与高脂胰岛素抵抗组相比显著上升,说明3个运动组分泌IL-10的能力均有相对提高;与普食胰岛素抵抗组相比,只有中强度累积运动组具有显著性差异,而其他两组则无统计学差异;这说明就抗炎因子而言,中强度累积运动对胰岛素抵抗小鼠的改善作用是相对较好的,这可能也与中强度累积运动组小鼠的促炎因子TNF-α水平偏高有一定关系。总之,运动可以通过改善抗炎、促炎因子的相对平衡,从而改善胰岛素抵抗的状态。
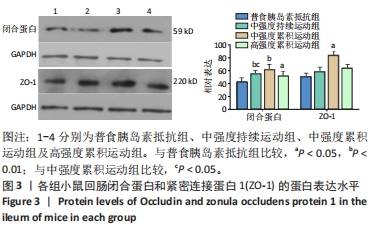
3.3.3 回肠紧密连接蛋白含量的分析 肠黏膜屏障包括机械屏障、生物屏障、化学屏障和免疫屏障,其中机械屏障是维护肠黏膜屏障的核心。肠上皮细胞之间的紧密连接复合体由跨膜蛋白闭合蛋白、claudin-5和胞质附着蛋白ZO-1等蛋白组成,ZO-1在连接跨膜蛋白和细胞骨架蛋白之间起到了桥梁的作用。研究表明,紧密连接蛋白的下调会导致肠黏膜通透性的增加[22]。此次研究显示,持续运动和累积运动两种不同形式运动均可对小鼠肠黏膜的闭合蛋白、ZO-1起到一定的调节作用,对比两种运动,发现累积运动对这2种蛋白的保护作用优于持续运动。这可能与累积运动可以更好地调节抗炎因子IL-10的释放有关,并且累积运动的时间更短,能够更好地保护肠黏膜结构不被破坏。
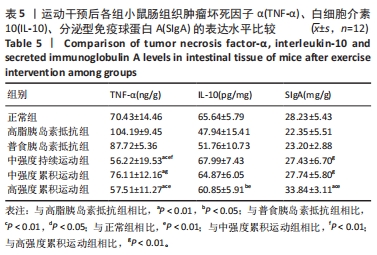
3.3.4 回肠IL-10和TNF-α以及肠黏液SIgA含量的分析 SIgA是黏膜免疫的重要组成部分。黏膜层中存在一种数量很少的微小凹陷细胞,也称为褶皱细胞,主要分布在淋巴小结上。微小凹陷细胞能够选择性地过滤和转运微生物和抗原分子,是黏膜屏障的关键组成部分。SIgA能够通过黏附微小凹陷细胞,特异性、选择性地阻止微生物和抗原分子插入,从而防止细菌入侵。研究指出,过度的力竭性运动训练可能导致大鼠肠道体液免疫功能显著下降,同时谷氨酰胺水平下降和自由基代谢增强[23]。史艳莉等[24]指出,长时间高负荷训练后大鼠肠黏膜的血浆内毒素、肠黏膜通透性和细菌转移率都有所升高,这提示针对过度负荷训练的情况,适当的谷氨酰胺补充可以有效改善肠道体液免疫功能。此次实验显示,高强度累积运动组的小肠黏液SIgA含量明显高于中强度持续运动组和中强度累积运动组,而中强度持续运动组和中强度累积运动组虽然SIgA含量也有所上升,但是与高脂胰岛素抵抗组、普食胰岛素抵抗组相比,并没有统计学差异。分析原因,虽然前人研究表示,高强度的运动会损伤肠黏膜,但是短时间的高强度累积运动可能并不会对损伤肠道通透性导致细菌移位,反而对肠道免疫有一定的增强作用。
代志军等[25]探究了C57BL/6J小鼠运动预适应对溃疡性结肠炎的影响及其可能机制,设置了运动预适应组、模型组和安慰剂对照组,结果显示,经过长期中强度的运动预适应后,能够预防溃疡性结肠炎的发生,并减轻已有疾病的病情,该效应可能与Toll样受体4-核因子κB信号通路的调节以及下游炎症因子基因表达的下调有关。此次研究对胰岛素抵抗小鼠进行了长期的运动干预,并将其与高脂胰岛素抵抗组进行了比较。运动干预组显示出回肠IL-10和TNF-α的明显上调和下降,这表明运动加饮食的干预方案可以改善炎症因子的调节,从而降低促炎因子TNF-α的分泌,提高抗炎因子IL-10的表达水平,相关机制可能与运动干预刺激Toll样受体4-核因子κB信号通路有关。
3.4 不同形式的运动对胰岛素抵抗小鼠肠黏膜屏障功能影响的机制 正常情况下,肠道的微生态结构保持相对的平衡与稳定,这主要依赖于肠道菌群、肠黏膜固有屏障和肠道免疫得以实现。而在病理情况下,肠道环境共生状态出现异常,微生态失调,肠道炎症引发肠道免疫失衡,最终导致肠道黏膜屏障发生病理性变化。研究表明,高强度长时间的运动可能会对肠黏膜屏障和免疫功能造成损伤[26],这种损伤可能是由多种因素引起的,包括过度的训练产生氧化应激、破坏肠道微生物平衡、引发肠道炎症与免疫失衡、导致体温过高和缺血性损伤等。这些因素可能会影响肠道中的自由基和巯基含量、三磷酸腺苷含量、肠道通透性和免疫调节因子的水平,这些变化最终可能导致肠道黏膜屏障发生病理性变化,产生炎症反应且使免疫功能受到破坏。因此,在进行高强度长时间的运动时,需要注意肠道健康状况,避免过度训练,保证足够的营养和水分供给,并及时调整运动强度和时间,以减少可能的肠道损伤。
中小强度的有氧运动有益于肠黏膜屏障。发现长时间中小强度运动降低促炎细胞因子分泌,提高抗氧化酶活性,增加抗炎细胞因子IL-10分泌[27]。长期有氧运动可显著改善胰岛素抵抗,促进脂肪、肌肉等组织细胞对葡萄糖的摄取和利用。有氧运动改善胰岛素抵抗的效果还和运动强度有关。累积运动指一天当中的多次短时运动,即把一段长时间的运动分为多次并分布在全天中完成[28]。累积运动主要适用于长时间久坐人群,是一种打破久坐、促进久坐人群身心健康的运动形式。累积运动一方面具有运动时间短、易执行、不易疲劳等特点,另一方面还可以从心理上给运动者以安慰,减少运动不适带来的心理压力,易被健身者接受和坚持,通过增加累积运动的运动强度,可以达到与持续运动相似的控制体质量的效果,探究累积运动对肠黏膜屏障的作用机制,可能与短时多次的累积运动对机体刺激更加温和,减少肠缺血并能够一定程度地增强免疫调节有关。此次实验结果分析不同形式运动对肠黏膜通透性影响的可能机制是,持续运动可能更好地调动脂肪功能,消耗脂肪,主要通过调节炎症通路来保护肠道健康;累积运动可能经过3 h的时间,适时地给予身体运动刺激,更好地保护肠黏膜结构蛋白ZO-1和闭合蛋白的蛋白表达,促进抗炎因子的表达。
此次研究结果显示,累积运动和持续运动均可不同程度地改善胰岛素抵抗小鼠的胰岛素抵抗状态,并对改善胰岛素抵抗小鼠的肠黏膜屏障起到一定的保护作用,提高肠道免疫功能,持续运动可以更好地保护肠道通透性,抑制促炎因子TNF-α的释放,减轻慢性炎症状态,高强度累积运动则可以更好地保护肠黏膜的结构蛋白,修复肠道损伤,改善胰岛素抵抗状态。中强度累积运动则可以更好地上调抗炎因子IL-10的表达。
3.5 结论 高脂膳食诱导的胰岛素抵抗小鼠伴有体质量增加、血清内毒素和右旋乳酸水平显著升高、血清和小肠组织促炎因子TNF-α含量显著增加等表现。长期规律性的累积运动和持续运动均可降低胰岛素抵抗小鼠的体质量,并明显改善糖代谢功能,纠正或改善胰岛素抵抗症状。长期规律性的累积运动和持续运动均可提高肠黏膜组织中紧密连接蛋白的表达量并增加SIgA分泌量,从而改善肠黏膜通透性,增强肠道免疫功能,降低血清中内毒素脂多糖的含量,进而降低循环血和肠组织中的促炎症因子表达,最终发挥对胰岛素抵抗小鼠肠黏膜屏障的保护作用。等运动量的高强度累积运动与中强度累积运动、中强度持续运动相比,在降低胰岛素抵抗小鼠的体质量、改善胰岛素抵抗症状、保护肠黏膜屏障方面效果更明显。
此次研究结果具有一定的临床转化价值和意义,为运动对肠黏膜通透性和代谢健康的相关探究提供了重要的支持和启示,可以为运动及其在代谢健康和肠道健康中的应用提供理论和实践基础。
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程