1.1 设计 体外细胞实验,采用盲法评估,组间比较采用两样本均数t检验。
1.2 时间及地点 实验于 2021-2022年在新疆医科大学科技楼研究重点实验室完成。
1.3 材料
1.3.1 标本来源 收集2021-2022年新疆医科大学第一临床医学院整形外科提供的增生性瘢痕和正常皮肤。6例增生性瘢痕患者,其中男3例,女3例;6例重睑术后患者,其中男3例,女3例。研究方案的实施符合《赫尔辛基宣言》和新疆医科大学第一临床医学院的相关伦理要求 (伦理批号:20170214-71)。供者对标本的采集完全知情同意,并签署了“知情同意书”。
增生性瘢痕患者纳入标准:①烧烫伤或创伤后增生期增生性瘢痕皮肤;②患者没有任何血液系统及全身性疾病;③只接受过手术治疗。
增生性瘢痕患者排除标准:①瘢痕疙瘩;②供者伴有其他血液系统及全身性疾病;③孕妇及哺乳期妇女;④依从性差者。
正常皮肤供者纳入标准:①正常皮肤;②患者没有血液系统及全身性疾病。
正常皮肤供者排除标准:①供者伴有其他血液系统及全身性疾病;②依从性差者。
1.3.2 主要试剂及仪器 DMEM高糖培养基、PBS (Hyclone,美国);EDTA-胰蛋白酶(Gibico,美国);细胞RIPA裂解液(Solarbio,中国);Ⅰ型胶原多克隆抗体、Ⅲ型胶原单克隆抗体、α-平滑肌肌动蛋白单克隆抗体(Abcam,英国);GAPDH单克隆抗体、辣根过氧化物酶标记的IgG抗体、CCK-8试剂(bioss,美国);miR-2116-3p前向引物、U6前向引物、Ⅰ型胶原野生型(WT)、Ⅰ型胶原突变型(MT)(与miR-2116-3p结合位点的序列突变)及Ⅰ型胶原质粒引物(生工,上海);miR-2116-3p模拟物、miR-2116-3p抑制物、miR-2116-3p阴性对照(锐博,广州);脂质体Lipo8000转染试剂(碧云天,上海);Annexin V-FITC细胞凋亡检测试剂盒、BD FACSCalibur型流式细胞仪(BD,美国);SYBRGreen荧光定量试剂盒-RR820、荧光素酶报告基因检测试剂盒(promega,美国);PCR反转录试剂盒-RR047(Takara,日本);miRNA提取分离试剂盒-DP501、miRNA cDNA第一链合成试剂盒-KR211、miRNA荧光定量检测试剂盒(SYBR Green)-FP411(天根,北京);TRIzol、ThermoScientific™ MultiskanSky型全波长酶标仪(Thermo,美国);CFX96™型实时荧光定量PCR仪、Gel DocTM XR+Western-Blot凝胶成像分析系统(Bio-Rad,美国);Leica DMI4000B/DM5000B型正、倒置荧光显微镜(Leica,日本)。
1.4 实验方法
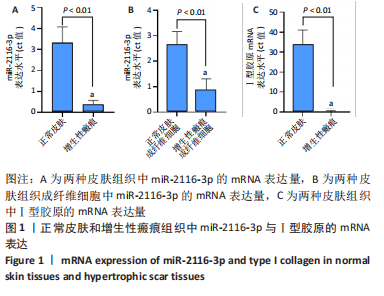
1.4.1 qRT-PCR检测miR-2116-3p、Ⅰ型胶原的mRNA表达 miR-2116-3p的mRNA表达:取正常皮肤组织、增生性瘢痕组织,每50 mg组织加1 mL 裂解液MZ,用匀浆仪进行匀浆处理。按照天根DP501试剂盒提取富集miRNA;按照天根KR211试剂盒反转录cDNA;按SYBRGreen荧光定量试剂盒-FP411说明书,采用实时荧光定量PCR仪进行检测。采用Δ循环阈值(Ct)法处理结果,计算目的基因的相对表达量,即2-ΔΔCt。基因引物序列见表1,扩增条件见表2。

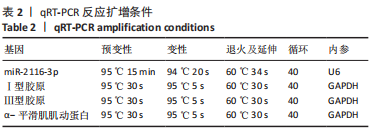
Ⅰ型胶原的mRNA表达:取正常皮肤组织、增生性瘢痕组织,每60-70 mg组织用0.3 mL TRIzol于高速研磨仪匀浆,后加TRIzol试剂至1 mL完全裂解;收集裂解液,加入0.2 mL氯仿,大力振荡15 s,静置2 min;4 ℃下12 000×g离心15 min,取上清液,加入异丙醇0.6 mL,振荡15 s;4 ℃下12 000×g离心10 min,弃上清液,加入等体积的75%无水乙醇洗涤2遍;7 500×g离心5 min,弃上清液,静置风干至啫喱状,用15-30 μL双蒸水溶解RNA沉淀,用nanodrop2000测量总RNA浓度。使用反转录试剂盒将总RNA反转录成cDNA。基因引物序列见表 1,扩增条件见表 2。
1.4.2 增生性瘢痕成纤维细胞的分离及培养 取增生性瘢痕组织,用含3%双抗的PBS漂洗3次,用眼科剪剪为长宽高约0.5 cm×0.5 cm×0.5 cm大小的组织块,放入10 cm培养皿中,加入含体积分数15%胎牛血清的高糖DMEM培养基。待细胞从组织块中爬出,移除组织块,加入含EDTA的胰蛋白酶1.5 mL消化两三分钟;加入3-5 mL含体积分数10%胎牛血清的高糖DMEM培养基终止消化,1 000×g离心5 min,弃上清液,加入前述培养基重新悬浮细胞,置于37 ℃含体积分数5%二氧化碳的培养箱中恒温培养。待细胞生长至80%以上融合时,用EDTA-胰蛋白酶消化,并传代培养。倒置荧光显微镜下观察细胞形态,取第3-6代增生性瘢痕成纤维细胞细胞用于后续实验。同理,分离培养正常皮肤组织成纤维细胞。采用qRT-PCR检测两种皮肤组织成纤维细胞内miR-2116-3p的mRNA表达。

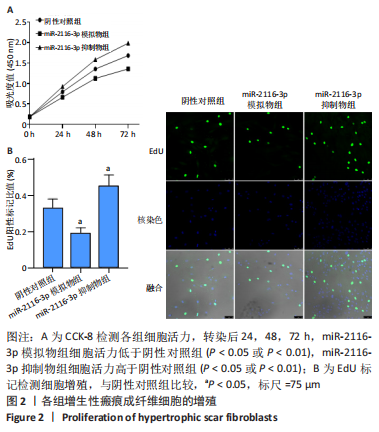
1.4.3 CCK-8法检测成纤维细胞的增殖活力 将成纤维细胞按4×107 L-1的细胞浓度接种于96孔板中,每孔100 μL。将细胞分为阴性对照组、miR-2116-3p模拟物组和miR-2116-3p抑制物组,每组15孔。按照脂质体Lipo8000转染试剂说明书分别转染阴性对照(miR1N0000001-1-5)、miR-2116-3p模拟物(5′-CCU CCC AUG CCA AGA ACU CCC-3′)和miR-2116-3p抑制物(5′-CCU CCC AUG CCA AGA ACU CCC-3′)。转染后0,24,48,72 h,每孔加入10 μL CCK-8溶液,避光置于37 ℃、含体积分数5%CO2的培养箱中恒温培养1-1.5 h,用酶标仪测量450 nm波长处的吸光度值,按照CCK-8试剂说明书计算细胞活力。
1.4.4 EdU检测成纤维细胞的增殖活力 取成纤维细胞,按5×104的细胞密度接种于20 mm共聚焦小皿中。将细胞分为阴性对照组、miR-2116-3p模拟物组和miR-2116-3p抑制物组,每组3皿。转染后48 h,依据 EdU检测说明书进行操作完后用激光共聚焦拍摄,计数绿色的细胞数(处于增殖期的增生性瘢痕成纤维细胞)和蓝色的细胞数(细胞核),用绿色的细胞数/蓝色的细胞数的比值进行统计分析。
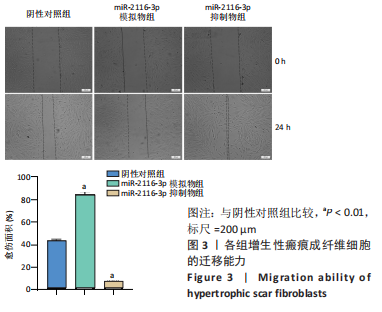
1.4.5 细胞划痕实验检测成纤维细胞迁移能力 将成纤维细胞按1×105/孔的细胞密度接种于6孔板中,待细胞密度达到80%后,取 10 μL枪头在6孔板底垂直划线,用37 ℃预热的 PBS洗涤未贴壁的细胞,加入含有体积分数3%胎牛血清的DMEM高糖培养基,按1.4.3分组转染相应试剂后,立即在倒置相差显微镜下拍摄0 h图像,37 ℃培养箱中培养 24 h后观察并拍摄图像,通过Image J软件计算划痕面积。
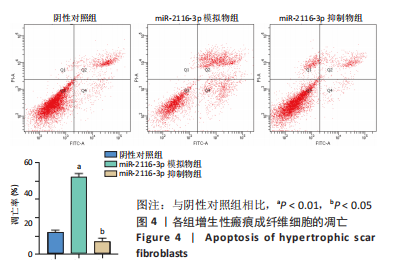
1.4.6 流式细胞术检测成纤维细胞凋亡 将成纤维细胞按1×108 L-1的细胞浓度接种于6孔板,每孔加2 mL完全培养基,按照1.4.3分组及处理。转染后24 h,加入5 μL膜联蛋白AV-FITC混匀后,避光室温孵育15 min,加入400 μL结合缓冲液悬浮细胞。用流式细胞仪分别测细胞凋亡比例,计算细胞凋亡率。
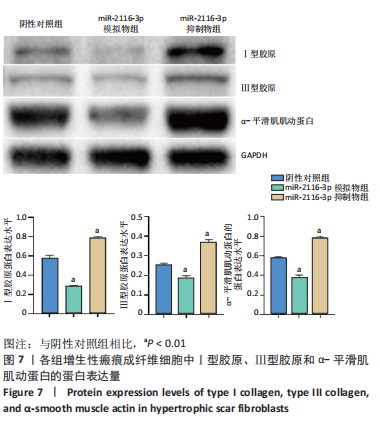
1.4.7 Western blot法检测成纤维细胞中相关蛋白表达 将成纤维细胞按1×108 L-1的细胞浓度接种于6孔板中,每孔加2 mL完全培养基,按照1.4.3分组及处理,每组3孔。转染后24 h,使用细胞RIPA裂解液提取蛋白。取20 μg蛋白样品,Bis-Tris凝胶电泳,湿法转膜,快速封闭液封闭0.5 h。分别加入兔抗人Ⅰ型胶原、α-平滑肌肌动蛋白、Ⅲ型胶原和GAPDH一抗(稀释比:1∶1 000),4 ℃孵育过夜。加入二抗(稀释比:1∶10 000),室温孵育1 h。采用 ECL显影,Biorad凝胶成像分析系统获取图像,采用ImageJ软件行灰度分析,分别计算Ⅰ型胶原、α-平滑肌肌动蛋白、Ⅲ型胶原蛋白灰度值与GAPDH蛋白灰度值的比值,计算各蛋白表达水平。
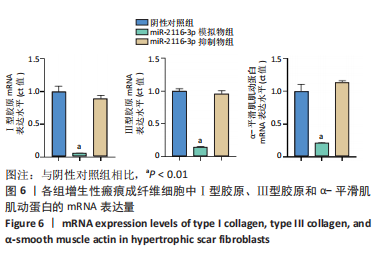
1.4.8 qRT-PCR检测成纤维细胞中相关基因表达 将成纤维细胞按1×108 L-1的细胞浓度接种于6孔板中,每孔加2 mL完全培养基,按照1.4.3分组及处理,每组3孔。转染后24 h,使用细胞RIPA裂解液进行裂解,检测方法同1.4.1中Ⅰ型胶原的mRNA表达检测。引物序列与扩增条件见表1,2。
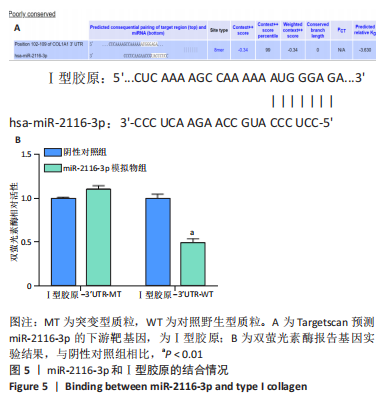
1.4.9 生物信息学网站预测miR-2116-3p与Ⅰ型胶原的靶向关系 应用靶基因预测数据库 Targetscan(www.targetscan.org/vert_80/)预测miR-2116-3p和Ⅰ型胶原的潜在结合位点,选出与增生性瘢痕密切相关的Ⅰ型胶原作为研究对象。
1.4.10 双荧光素酶法检测miR-2116-3p与Ⅰ型胶原的靶向关系 将增生性瘢痕成纤维细胞接种于24孔板上,将含有Ⅰ型胶原的突变型质粒(MT)和对照野生型质粒(WT)分别转染至增生性瘢痕成纤维细胞中,同时分别共转染miR-2116-3p阴性对照物和 miR-2116-3p模拟物。按照Lipo8000转染试剂说明书分别转染。转染后48 h,用荧光素酶报告基因检测试剂盒分别检测并计算荧光素酶和肾荧光素酶的数值,随后计算荧光素酶/肾荧光素酶比值。
1.5 主要观察指标 ①增生性瘢痕组织与正常皮肤组织中miR-2116-3p、Ⅰ型胶原的mRNA表达;②各组成纤维细胞的增殖与凋亡;③各组成纤维细胞中Ⅰ型胶原、Ⅲ型胶原及α-平滑肌肌动蛋白的蛋白与mRNA表达;④Targetscan预测miR-2116-3p的下游靶基因,双荧光素酶验证miR-2116-3p与Ⅰ型胶原的结合情况。
1.6 统计学分析 使用软件 SPSS 25.0进行统计分析,数据均以x±s表示。两组间比较采用t检验,P < 0.05认为差异有显著性意义。文章统计学方法已经新疆医科大学统计学专家审核。