中国组织工程研究 ›› 2022, Vol. 26 ›› Issue (34): 5454-5460.doi: 10.12307/2022.455
• 组织工程软骨材料 tissue-engineered cartilage • 上一篇 下一篇
3D生物打印甲基丙烯酰化明胶水凝胶支架促进软骨下骨缺损的修复
路冬冬1,朱天峰1,张一健1,赵志坚1,刘 洋1,沈 序2,朱雪松1
- 1苏州大学附属第一医院骨科,江苏省苏州市 215006;2苏州市独墅湖医院骨科,江苏省苏州市 215006
3D bio-printing methylacrylated gelatin hydrogel scaffolds promote the repair of subchondral bone defects
Lu Dongdong1, Zhu Tianfeng1, Zhang Yijian1, Zhao Zhijian1, Liu Yang1, Shen Xu2, Zhu Xuesong1
- 1Department of Orthopedics, First Affiliated Hospital of Soochow University, Suzhou 215006, Jiangsu Province, China; 2Department of Orthopedics, Suzhou Dushu Lake Hospital, Suzhou 215006, Jiangsu Province, China
摘要:
文题释义:
3D生物打印:又名快速成型、实体自由成型、增材制造等,它以自体干细胞体外诱导分化出的活细胞为种子细胞和包含生长因子在内的胞外基质与材料作为“生物墨水”,制作出符合细胞增殖分化需要的微环境和空间构架,最终搭建出具有生物活性的人造组织器官。
甲基丙烯酰化明胶水凝胶:为一种常见的光固化水凝胶,兼具天然和合成生物材料的特征,具有优异的生物相容性和细胞反应特性,例如提供合适的细胞黏附位点及具有蛋白水解降解性。此外,该水凝胶具有良好的机械性能,其构建的3D支架具有可调的机械和化学性质。
背景:软骨下骨在关节正常生理活动中发挥着重要作用,一旦损伤就难以修复,而传统的骨水泥和自体骨移植治疗方式存在一定的局限性。
目的:探讨以骨髓间充质干细胞或软骨祖细胞作为种子细胞,利用3D生物打印技术将其包封于甲基丙烯酰化明胶水凝胶支架中修复软骨下骨缺损的有效性。
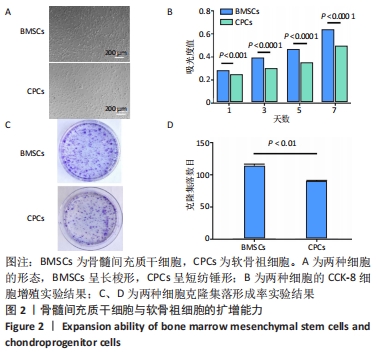
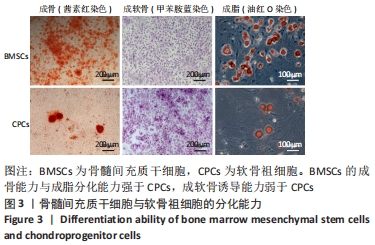
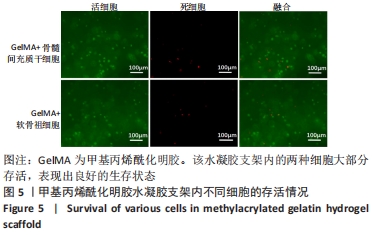
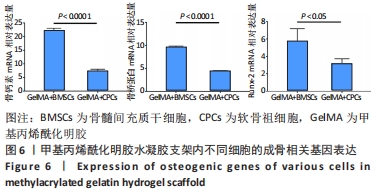
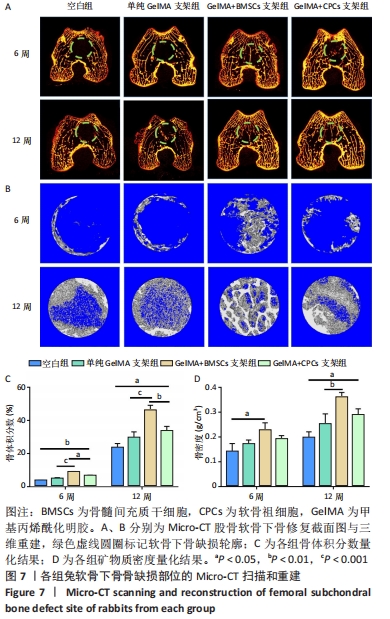
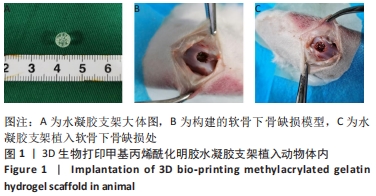
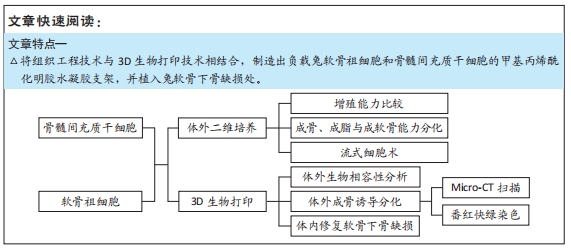
方法:利用纤连蛋白分选获得兔软骨祖细胞,利用全骨髓贴壁法获得兔骨髓间充质干细胞,对比两种细胞的增殖能力及成骨、成软骨、成脂分化能力。通过3D生物打印技术分别制作负载骨髓间充质干细胞与软骨祖细胞的甲基丙烯酰化明胶水凝胶支架,成骨诱导培养后,活死染色分析支架中的细胞存活率,qRT-PCR检测支架的成骨基因表达。在16只新西兰大白兔双侧膝关节处制备直径5 mm、深度5 mm的软骨下骨骨缺损,分4组,A组不做处理,B组植入甲基丙烯酰化明胶水凝胶支架,C组植入负载骨髓间充质干细胞的水凝胶支架,D 组植入负载软骨祖细胞的水凝胶支架,术后6,12周进行骨缺损区Micro-CT扫描与组织学观察。
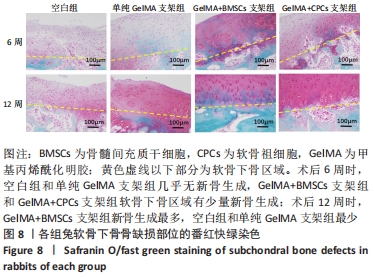
结果与结论:①骨髓间充质干细胞的增殖能力及成骨和成脂分化能力强于软骨祖细胞,成软骨分化能力弱于软骨祖细胞;②水凝胶支架中的两种细胞均表现出良好的生存能力,并且支架中骨髓间充质干细胞的成骨相关基因骨钙素、骨桥蛋白、Runx-2 mRNA表达均高于软骨祖细胞(P < 0.05);③动物体内修复实验Micro-CT扫描显示,C组骨组织形成最多,术后12周可见骨小梁结构形成,新生骨形态与周围的天然松质骨类似;A、B组新生骨组织最少;番红快绿结果显示,术后6周时,仅C、D组软骨下骨区域有少量新骨生成;术后12周时,A、B组开始有骨基质生成,C组显示出软骨下骨的大量修复且新骨生成量多于D组;④结果表明,骨髓间充质干细胞与3D生物打印的甲基丙烯酰化明胶水凝胶是适合于骨组织工程的种子细胞与支架材料。
缩略语:甲基丙烯酰化明胶:methylacrylated gelatin,GelMA;骨髓间充质干细胞:bone marrow mesenchyml stem cells,BMSCs;软骨祖细胞:chondroprogenitor cells,CPCs
https://orcid.org/0000-0003-4856-4270 (路冬冬)
中国组织工程研究杂志出版内容重点:生物材料;骨生物材料; 口腔生物材料; 纳米材料; 缓释材料; 材料相容性;组织工程
中图分类号: