Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (14): 2249-2256.doi: 10.12307/2023.152
Previous Articles Next Articles
Animal models of jaw critical-sized defect in jaw defect repair
Wang Yue, Zhang Xiaoyan, Li Yunlong, Mei Shuang, Li Xiangjun
- Department of Oral and Maxillofacial Surgery, Hebei Key Laboratory of Stomatology, Hebei Provincial Clinical Research Canter for Oral Diseases, School and Hospital of Stomatology, Hebei Medical University, Shijiazhuang 050017, Hebei Province, China
-
Received:2022-04-14Accepted:2022-05-28Online:2023-05-18Published:2022-09-30 -
Contact:Li Xiangjun, MD, Professor, Department of Oral and Maxillofacial Surgery, School and Hospital of Stomatology, Hebei Medical University, Shijiazhuang 050017, Hebei Province, China -
About author:Wang Yue, Master candidate, Department of Oral and Maxillofacial Surgery, School and Hospital of Stomatology, Hebei Medical University, Shijiazhuang 050017, Hebei Province, China -
Supported by:The Key Research & Development Project of Hebei Provincial Department of Science and Technology, No. 21377719D (to LXJ); The Government Funded Medical Talents Project of Hebei Province, No. 361029 (to LXJ)
CLC Number:
Cite this article
Wang Yue, Zhang Xiaoyan, Li Yunlong, Mei Shuang, Li Xiangjun. Animal models of jaw critical-sized defect in jaw defect repair[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(14): 2249-2256.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 建模动物种类及其优缺点 多种哺乳动物被用于骨骼研究,通常用于骨修复和再生研究的哺乳动物要考量骨的大小、形状和内部结构上的差异[5]。以下哺乳动物按照体型及骨量从小到大的顺序依次描述。 2.1.1 啮齿类动物 是最常用的小动物模型之一,主要因为它们生长周期短、饲养条件容易获得、繁殖速度快、价格便宜、易于维护和操作,在测试生物材料作为骨替代品的临床前研究中具有重要作用,被认为是体内骨组织再生实验的首选模型之一[6]。啮齿动物与人类有高度的同源性[7],它们具有与人类非常相似的生物学、遗传学和行为特征,许多人类疾病的症状可以在大鼠身上复制[3]。然而,啮齿动物模型的局限性也是显而易见的,与大动物相比,啮齿类动物的骨骼体积较小、皮质较薄而脆弱[6];此外,啮齿动物模型由一个更原始的骨骼系统组成,该系统不具有哈弗斯系统管式的皮质重塑,故不能完全反映人类的骨愈合情况[8]。 2.1.2 兔 是最常用的动物模型之一,在研究肌肉骨骼的实验动物中排名第一。据报道,兔和人在骨干中段的骨密度和断裂韧性方面有相似之处。兔作为实验动物易得到,也容易饲养和处理,这些特点使兔成为研究人员开发新型颌骨替代生物材料体内实验动物模型的首选。对兔咀嚼模式的分析表明,重负荷与饮食成正比,刚度和力度主要传递到下颌骨牙齿嵌入的骨性部分[9]。但是,对于多种替代生物材料的评价,兔的体积小是骨科植入物研究用实验动物的主要缺点。此外,与灵长类或一些啮齿动物等物种相比,兔子的骨骼变化和转换更快,与人类的颌骨愈合时间存在差异[6]。 2.1.3 犬 一般临床前的测试多在大型的骨骼成熟的动物身上进行,在北美,狗的使用最多,因为狗的骨骼成分和生物学与人类非常相似,被广泛用于各类实验。犬类易于饲养,容易接近,专门饲养用于动物实验的比格犬或浣熊猎犬提供了更多异种混血狗所不具备的繁殖力。一篇对犬类作为动物模型的文献综述表明,在许多科学实验中犬类是优先被选择的实验动物,特别是在骨髓生物学和移植免疫学方面,犬类与人类在生物及免疫学方面的相似性是其他小型哺乳动物无法比拟的。然而,犬类作为人类伴侣动物的社会性使其作为实验动物的使用受到了挑战[5]。 2.1.4 猪 有与人类相似的板层骨结构,在骨解剖、形态学、愈合能力、骨重塑、矿物质密度和浓度等方面被认为是人类骨再生过程中最具代表性的模型,是研究下颌皮质血液供应和骨合成钢板和螺钉设计最为合适的实验动物模型。研究显示,猪与人的骨再生速度较犬类更为相似(犬,1.5-2.0 mm/d;猪,1.2-1.5 mm/d;人,1.0-1.5 mm/d)。此外,在一项关于氟对生长猪皮质骨重建影响的研究中,结果显示猪的皮质骨矿化率与人类相似[10]。然而,猪作为实验动物不仅饲养价格贵、生存要求高,还具有嘈杂、好斗、不容易听话等缺点。解剖结构上猪长骨短而粗,体型大。短骨不易做较大的间隙缺损,因为很难实现充分的固定[5]。此外,人类的牙根和下颌管之间有厚厚的骨组织(智齿有时是例外),而猪的牙根与下颌管直接接触。更为特殊的是,猪的多个颏孔的存在使得局部麻醉比人类更困难,只有进行大范围的局部浸润麻醉,而不能选择性地麻醉特定的神经,因此使麻醉过程变得不精确[10]。研究表明商品猪不适合骨科研究,因为它们的生长速度很快,体质量非常高。为克服这些缺点,培养出小型猪和微型猪[6],小型猪更容易管理,但是遗传的侏儒基因使小型猪在生物学上与人类的相似性低于其他一般家养动物,也使其在实验动物使用上受到限制[5]。 2.1.5 羊 成年绵羊的优势是拥有与成年人类相似的体质量,并且拥有适合测试人类植入物和假肢的长骨,宏观骨结构与人骨相似,可以使用人类临床实践中使用的许多内固定系统,这在兔和犬等物种中是难以实现的。在组织学上,羊的骨结构与人的不同。绵羊的骨骼主要由初级骨骼结构组成,而人类主要是次级骨骼结构。绵羊的次生骨重建直到平均年龄7-9岁才发生,而在三四岁时,它们有一种丛状的骨骼结构,由编织骨和夹杂着血管神经丛的板层骨组成。与人类相比,成熟绵羊的骨小梁密度明显更高,骨强度也更大,但是不同的位置可能会有所不同。一些研究人员认为,尽管存在骨骼结构的差异,绵羊仍然是人类骨骼转换和重塑活动的有价值的模型[6]。绵羊容易获得,性格温顺,但因为是群居动物,单独饲养会表现出胆小易受惊、适应性差、易生病等缺点。绵羊骨密度波动最大,不同季节差异较大,冬季最低[11]。山羊的体型大小和骨骼解剖与绵羊相似,虽被毛较薄,肌肉较少,但对单独饲养导致的压力耐受力更强,因此在美国,山羊作为实验动物越来越普遍,山羊作为骨骼基础研究实验动物成为可行的选择[5]。 2.1.6 非人灵长类动物 在新方法被引入临床试验之前,临床前研究应该在更大的动物模型中进行,非人灵长类动物是一个理想的翻译模型,它们与人类有着惊人相似的遗传、生理和行为特征[12],更接近于具有挑战性的人类临床骨骼缺陷[13]。非人灵长类(NHP)的使用大幅增加了研究成本,并与一些文化和伦理问题有关。非人灵长类动物有时被认为是预测骨修复和再生方法临床表现的首选模型,这一假设是基于进化上的相似性以及相似的结构解剖、内分泌、消化、饮食特征和免疫学的争论。然而,很难证明应该将非人灵长类动物的使用作为骨修复和再生工作的黄金标准的观点是合理的。在3个常见的非人灵长类物种中,只有狒狒接近人类与大型犬、绵羊和山羊共有的骨骼大小范围,缺陷大小是非洲绿猴和恒河猴的一个重要限制因素。非人灵长类物种表现出的深刻的性别二型性(雄性比雌性大)远远大于人类。此外,尽管非人灵长类动物没有同伴动物的地位,但感知进化从属关系的争论引发并增加了在研究中使用它们时的社会和伦理问题。最重要的是,在非人灵长类动物中起作用的方法往往在其他大型动物中也起作用,反之亦然。因此,尽管必须考虑例外情况,但作为一种客观评估植入装置、细胞移植策略或生长因子输送系统之间比较的手段,非人灵长类动物模型缺乏直接证据表明在生物学机制或预测相对或绝对临床表现方面优于其他大型动物模型[5]。 综上所述,临床前的测试一般在骨骼成熟、骨量充足的动物身上进行的,根据以往报道,大鼠、兔、狗、猪是利用最多的实验动物。见表1。 "

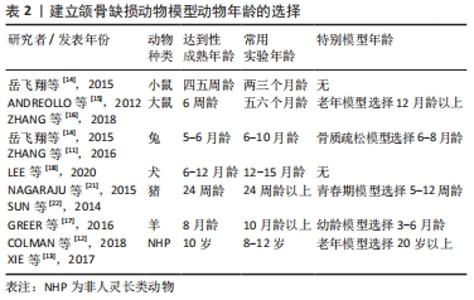
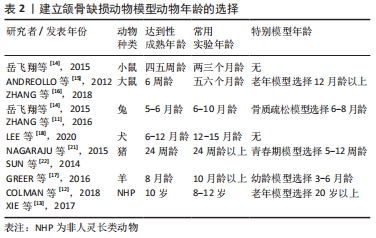
2.2 建模动物年龄的选择 年龄被认为是影响骨骼修复和再生的特征和结果的关键系统变量[5],动物的年龄能够影响实验结果的科学性。实验动物年龄过小,动物自身生长发育旺盛,会影响骨移植材料实验结果的说明性;而且如果动物年龄过小,骨骼强度不够,植骨或内固定后,不易固定牢靠,难以操作管理。相反,如果动物年龄过大,骨骼老化,自身修复能力低下,更不利于实验结果。因此,选择年龄合适的动物,对实验的操作,实验结果的科学性都很重要。 研究通常局限于小动物模型。一般小鼠四五周达到性成熟,通常选择两三个月的小鼠作为模型[14]。以往研究表明,大鼠在童年时期发育迅速,大约6周龄达到性成熟,但在五六个月后达到社会成熟,成年后,大鼠每个月大约相当于人类的2.5岁,12个月后大鼠开始进入老龄期。除成年动物以外,幼年动物作为检测与某些疗法相关的疗效或毒性模型的敏感性是有限的,单独使用幼年动物也可能低估了针对年龄相关缺陷添加辅助方法的增量效应,甚至低估了剂量-反应效应的表征和与某些疗法相关的毒性检测,增加使用老年动物是改进现有动物模型的手段之一[15]。ZHANG等[16]为研究低氧预处理的骨髓间充质干细胞在缺氧诱导因子1α(HIF-1α)表达上调的情况下对老年个体骨愈合过程的影响,报道了21月龄老年SD大鼠下颌骨缺损的动物模型。 一般兔五六个月达到性成熟,所以一般选择6-10个月的兔作为模型[14]。对于骨质疏松模型,兔年龄一般选择6-8个月大,此时已达到性成熟,骨骺板钙化和闭合在性成熟后不久就会发生。与大鼠相比,兔骨骼较大,可以提供更丰富的血清样本,更适合于骨质疏松性骨折治疗的研究[11],而且模型制作手术简单,成模效率高且稳定,在对于组织工程在代谢性疾病的治疗应用研究中被广泛使用。 羊成年较早,一般3-6月龄为幼羊,8月龄达到性成熟,通常选择10月龄以上的羊作为成年模型[17]。不同种类的犬多数在6-12个月之间达到性成熟,一般选择12-15月龄的犬作为模型[18-20]。而猪生长速度快,5-12周即可被视为青少年,一般24周达到成年[21]。在组织工程学研究中,青少年患者和成年患者的要求可能不同,由于青少年患者的生长潜力和骨骼再生能力较强,使用成年临界骨缺损模型是不合适的,因此,与青少年人类密切相关的下颌临界大小缺损(CSD)模型应该位于青少年动物的下颌,其下颌大小与人类相当。猪下颌骨在大小、解剖、形态、功能、新陈代谢和血液供应方面与人类下颌骨相似,猪在骨再生率与人类的相似程度上也超过狗,5-12周大的猪在头面部骨骼成熟方面与青少年人类相当[22],因此在建立青少年颌骨模型方面5-12周龄猪模型是一个很好的选择。 非人灵长类的平均寿命很长,与人类相似,恒河猴与人类基因组有93%的序列同源性,恒河猴的衰老方式与人类相似,是人类的2.5-3倍,它们的寿命以几十年为单位,圈养的平均寿命约为26年,标准饲养下的最长寿命约为40年。恒河猴通常被认为是在大约20岁之后变老。猕猴和其他东半球的猴子是人类骨质疏松症的优秀模型,因为它们的皮质骨有杂乱无章的骨性重塑,而且有类似的生殖内分泌系统影响骨代谢,猕猴在大约10岁时达到骨量峰值[12]。灵长类动物也具有和人类最相似的颌骨结构及牙列,排除其伦理问题及经济成本,10岁左右的猕猴可以作为比较适宜的青年模型,比如,XIE等[13]为探讨抗体介导修复非人灵长类下颌骨连续性缺损骨再生的组织工程研究中,选择了年龄8-12岁的成年雄性猕猴,极好地模拟了人类颌骨节段性缺损,无论从材料组织相容性、骨代谢还是骨修复过程都为人类颌骨修复过程提供了有力证据。 建立颌骨缺损动物模型动物年龄的选择汇总,见表2。 "

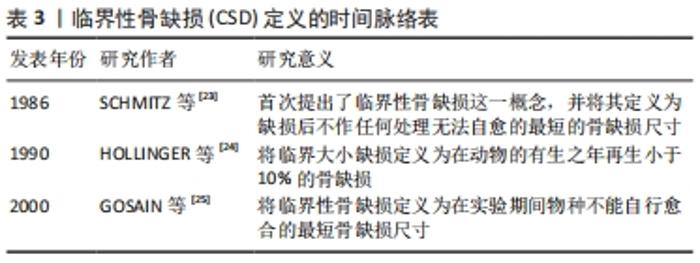
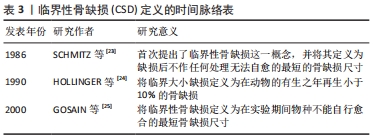
使用动物模型通常是测试新的骨再生材料的重要步骤。从理论上讲,实验性骨缺损应该足够大,以阻止自然愈合,为了达到这一目的,人们在各种动物模型中研究了骨组织的非再生阈值。动物的临界大小的缺损是研究颅颌面骨骼中常见骨缺损的有用模型。1986年,SCHMITZ等[23]研究表明自然状况下骨缺损有一个不能自行愈合的临界值,首次提出了临界性骨缺损(CSD)这一概念,并将其定义为缺损后不作任何处理无法自愈的最短的骨缺损尺寸。随后考虑到观察实验动物完整的生命周期是非常困难的,GOSAIN等[25]将临界性骨缺损值定义为在实验期间物种不能自行愈合的最短骨缺损尺寸。也有学者将临界大小缺损(CSD)定义为在动物的有生之年再生小于10%的骨缺损[24]。 自1979年KABAN等[26]在大鼠下颌骨下颌角区制备了直径为4 mm的圆形骨缺损,经观察24周后发现该缺损未能达到自然完全愈合,故认为直径> 4 mm的圆形骨缺损为大鼠下颌骨的临界骨缺损大小,这一大鼠的下颌骨临界缺损在OZAKI等[27]的研究中得到验证,并在大鼠临界骨缺损的研究中得到认可和应用[28]。DECONDE等[8]在大鼠下颌骨制造长度为0,1,3,5 mm的节段性缺损,得出所有长为5 mm的缺损在micro CT上都不能自发形成骨性愈合的结论,而长为0,1和3 mm的缺损有一定程度的骨愈合和骨形成,提示再生技术研究以使用大鼠5 mm节段性缺损下颌骨模型为宜。因此,在近年来的组织工程学及材料学研究中通常采用4.0-5.0 mm的下颌骨缺损大小作为大鼠的下颌骨临界骨缺损大小[28-32]。DRéNO等[33]在下颌骨放射后遗症模型研究中,在大鼠每个半下颌骨形成不同大小(0,1,3,5 mm)的下颌骨缺损区,得出在照射区域,临界缺陷大小为3 mm的结论。 目前国内外关于兔颌骨缺损模型的临界骨缺损大小尚未达成共识。兔下颌骨是植入组织工程支架材料的理想选择,其前磨牙和磨牙区有足够的牙槽骨高度及厚度(17 mm长,16 mm高,6 mm厚)[34],下前牙远中至前磨牙有长约20 mm的无牙区域,该无牙区牙槽骨宽约5 mm,深约4 mm[35]。这使得兔的下颌骨可以制备一个合适的下颌骨缺损,并且有足够的体积来支撑实验用合成支架,同时还便于手术操作。在早期研究中,有研究表明兔模型中,下颌骨约5 mm的缺损可被认为是临界骨缺损大小[23],超过5 mm的缺损需要支架等材料来引导骨修复[9],但对于该临界骨缺损大小存在争议。ANDERSSON等[36]在兔双侧下颌骨制备直径均为6 mm的圆形全层缺损来探讨牙本质能否作为一种实验性兔骨缺损的移植材料时,缺损中所见到的部分骨形成表明,6 mm对于临界大小的缺损来说是不够的。不少学者于新西兰白兔下颌体部制作直径8 mm的圆形临界大小的缺损,研究提示8 mm可以作为兔下颌骨的临界骨缺损值[37-38]。ASHOUR等[39]在成年雄性新西兰兔双侧下颌骨制备直径10 mm的颊舌侧圆形贯通缺损,研究结果表明直径为10 mm的全厚度下颌骨缺损可以模拟节段性颌骨缺损,并满足兔下颌骨缺损临界大小的要求。OTAGUDDA RANGANATH 等[40]在一只兔体内建立了2个明显不同位置(非承重的顶盖骨和承重的下颌体)共存的双侧临界大小缺损区(CSD)的模型,建立的下颌骨缺损尺寸是直径11 mm,结果分析显示,缺损区具有不可愈合的性质,因此兔的下颌骨临界大小缺损被证实。V等[9,41-42]在新西兰兔颊皮质板,距离侧切牙区15 mm内,形成一个箱状的缺损,缺损槽的长度为10 mm、深度为3 mm、宽度为3 mm,研究结果提示10 mm可以作为兔下颌骨的临界大小缺损值。CARLISLE等[43]选择12 mm×5 mm、12 mm×8 mm、15 mm×10 mm的非节段性骨缺损作为研究对象,发现所有缺损都不能形成完全的骨愈合,但12 mm×5 mm不会影响到颌骨的力学性能,而其他大小的缺损会影响颌骨的抗折强度,在移植骨材料研究中需要慎重选择。还有研究建立了缺损尺寸更大的兔动物模型,MONIR等[44]将兔一侧下颌骨第一前磨牙前方2 mm处至门牙区的骨段移除,形成了一个15 mm长的节段性缺损,并将其作为临界节段性缺损纳入研究。综上所述,目前对于利用新西兰白兔制作颌骨缺损动物模型的临界骨缺损尺寸尚无准确实验证据,对于节段性骨缺损大小和非节段性骨缺损大小均有不同观点。 成年犬为下颌骨不连续缺损的研究提供了一种近乎理想的动物模型,其优点是可以制造出大的双侧骨缺损,并且可以进行配对设计实验。目前为止,只有几项研究记录了犬下颌骨的临界骨缺损大小。ANWAR等[45]为比较双相磷酸钙(BCP)与矿化血浆基质(MPM)和富血小板纤维蛋白(PRF)在犬水平临界大小牙槽骨缺损模型中对骨形成和成熟的质量和数量的影响,在犬下颌第三前磨牙和第四前磨牙拔除基础上建立了7 mm×8 mm×5 mm的缺损模型。LEE等[18]对比格犬实施了包括骨膜去除的20 mm×10 mm×10 mm大小的下颌骨切除术,建立了临界骨缺损动物模型。RAI等[19]建立了18 mm×10 mm×7 mm的犬下颌骨临界骨缺损进行聚己内酯/β-磷酸三钙(PCL/TCP)支架的成骨效果研究,在该研究中使用了与LEE等[18]研究中犬下颌骨临界骨缺损相似的尺寸。KHOJASTEH等[20]在犬下颌骨颊侧皮质板制作了20 mm×10 mm×10 mm的临界骨缺损,报道了复合骨髓间充质干细胞(BMSC)的聚己内酯/β-磷酸三钙支架的骨再生情况。WU等[46]报道了在比格犬下颌体中部成功制备了30 mm长的颌骨节段性缺损的动物模型。MESGARZADEH等[47]在犬下颌第二前磨牙到第一磨牙的牙槽骨至下颌骨下缘建立了长达30 mm的缺损模型。而HUH等[48]的研究结果表明,在成年杂种犬的下颌骨中制造长达60 mm的缺损是可能的,而临界大小的缺损取决于骨膜的存在与否;当有骨膜存在时,临界大小缺损为50 mm,当没有骨膜时,临界大小缺损为15 mm;因此,该结果证明了应根据骨膜是否存在来决定临界缺损的大小,同时显示了骨膜对于骨缺损修复的重要性。 猪下颌骨在大小、解剖学、形态、功能、新陈代谢和血液供应方面与人类下颌骨相似,再生率也在与人类的相似,程度上超过狗。研究发现猪下颌角区无颊侧骨膜的条件下体积5 cm3 缺损是合理的临界缺损模型[22]。DORAFSHAR等[49]在Yorkshire猪的下颌骨制作了6 cm全厚切除的下颌骨缺损模型。VAN OIRSCHOT等[50]在小型猪下颌骨建立了直径8 mm的全层贯穿性缺损。CUI等[51]在小型猪下颌骨中制造了4个圆柱形缺损的模型,每个孔的直径为10 mm,到达髓腔时的深度约为5 mm,他们在符合猪下颌骨临界缺损范围内创建了可以应用于组织工程学的快速骨修复模型。在近年来的组织工程学及材料学研究中通常采用体积大于5 cm3的下颌骨缺损大小作为猪下颌骨合理的临界骨缺损值[52-54]。 在绵羊模型中,SCHLIEPHAKE等[55]以高温牛骨为支架修复长骨缺损,建立了绵羊单侧下颌骨35 mm长的下颌骨节段性缺损。XIE等[13]为了探讨抗体介导的骨修复在非人灵长类下颌骨连续性缺损中的应用,通过手术在食蟹猕猴下颌后牙造成15 mm的连续性缺损,并用钛重建钢板对两段进行了坚固固定,在系统发育上更接近人类的动物模型。周苗等[56]在对于预制个性化骨瓣修复下颌骨缺损的研究中构建了恒河猴下颌骨体长为20 mm的节段性下颌骨缺损模型。但由于羊和灵长类动物的来源及饲养均不易,使用羊或灵长类动物做为骨缺损动物模型的研究很少,迄今未检索到关于羊或灵长类动物颌骨临界缺损的相关研究。 各种动物建立颌骨临界大小缺损的选择汇总,见表4。 "

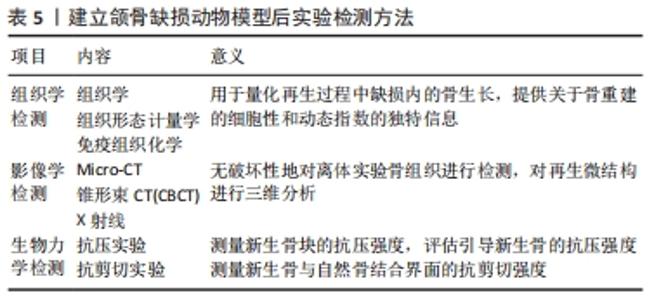
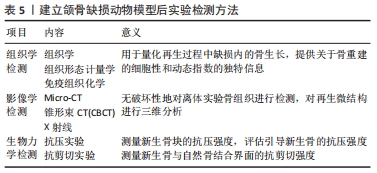
2.4 手术入路及手术部位的选择 从理论上讲,口内伤口会增加感染性并发症的风险,而口腔外操作视野暴露,减少手术难度,易于重复,因此以往研究通常在口腔外制造下颌骨缺损[8]。骨的缺损或间隙易标准化是其突出优点。缺损通常可分为圆柱形或矩形的非节段性骨缺损和节段性骨缺陷,圆柱形或矩形的非节段性骨缺损可使用环钻或钻头制备,节段性骨缺损可使用外科锯制作[5]。制作缺损时注意识别和保留下牙槽神经血管束(NVB),除非它是特定的靶点,有研究表明,大鼠NVB结扎导致同侧及对侧牙齿明显的形态变化,结扎兔单侧NVB 同样影响双侧门牙[57]。 啮齿类动物下颌骨体部充满牙根,骨质稀薄,通常不作为制作下颌骨缺损的部位,而下颌角区域骨质大小适宜,厚度约为2 mm,从下颌角下缘切口入路,抬高全层骨膜瓣,即可充分暴露视野[58]。因此,绝大多数啮齿类下颌骨缺损的动物模型选择在下颌角区域。 如前所述,兔下颌骨体部具有充足的骨质,根据研究要求的不同,可建立多种类型的下颌骨缺损模型,比如,结合磨牙拔除术的牙槽骨缺损模型可以选择在兔下颌骨前磨牙和磨牙区制备缺损[59]。不伤及牙根的颌骨缺损模型可以选择在兔下颌骨磨牙区的下缘[60-61]、以及磨牙区颊侧皮质骨处和前牙区骨质充足处制备[9,37,41,62]。研究表明,相比于兔下颌骨体髓质丰富,下颌角区域仅有薄层皮质,不适宜作为兔下颌骨缺损模型的制备区域[63]。由于兔口腔解剖形态狭窄,增加了口内入路的手术操作难度,存在手术视野暴露不充分的问题,因此,兔磨牙区下颌骨的缺损制作以及下颌骨体前部骨缺损的制作通常均选择在下颌下缘做切口的口外入路的手术方式。 猪的下颌骨体积大骨量充足,现有的研究既有选择在下颌角区域制备圆形或箱状非节段性骨缺损的[22,51],也有的选择在下颌体制备节段性缺损[64],这两种建模方式均适宜用于组织工程相关的实验。 犬的下颌骨体长而且连续,是制作节段性骨缺损的理想模型[48],关于羊和非人灵长类的下颌骨缺损建模的描述少[13,55],据现有的研究报道,与犬一样,也是在下颌骨体部制作节段性骨缺损的合理模型。未来的研究应该调查包含口内伤口以及下颌骨其他部分具有独特解剖学挑战的动物颌骨缺损模型 (例如,联合缺损)[8]。 2.5 建模后实验检测方法 对于新生骨的测定有不同的分析方法,如组织学、组织形态计量学和免疫组织化学,可用于量化再生过程中缺损内的骨生长[30],提供关于骨重建的细胞性和动态指数的独特信息[65]。常规染色切片如苏木精-伊红染色法,显微镜下观察胞核与胞质红蓝染色,可观察成骨细胞数量及分布。特殊染色切片如Goldner 三色法,光镜下可观察到成骨细胞为橘黄色、类骨质为紫红色、成熟骨为绿色、新矿化骨为蓝色,该方法适合区分骨矿化的不同阶段,以及进行相应的骨形态学观察与测量。免疫组织化学观察如骨 γ-羧基谷氨酸蛋白(bone-car-boxyglumatic acid -containing protein,BGP)又称骨钙素,骨的组织形态学参数间及与成骨细胞活性间有明显相关性,骨钙素水平是反映成骨细胞活性的敏感指标,成骨速率越高,骨钙素值越高[66]。迄今为止,定量组织学技术仍是评估骨小梁和皮质骨结构的标准[65]。 然而,传统的组织计量学等方法大多需处死动物固定组织样本,对于再生微结构的三维分析有很大的局限性,因为结构参数是从少数2D切片的体视学分析中得出的,通常假设底层结构是板状的。相比之下,高分辨率三维成像技术,如Micro-CT,直接测量骨微结构,而不依赖于体视学模型。Micro-CT由FELDKAMP及其同事[66]在20世纪80年代末首次提出,Micro-CT现在已成为评估小鼠和其他体外小动物模型骨骼形态和微结构的“金标准”。由于Micro-CT可无破坏性地对体外实验骨组织进行检测,因此,样品可以随后用于其他分析,如组织学或机械测试。使用Micro-CT评估骨形态测量和组织矿物质密度的步骤包括图像采集、图像处理、图像分析和结果报告。定量描述骨结构的标准方法是计算形态计量指数,也称为定量形态计量。基本形态计量学指标包括骨体积(BV)和总体积(TV)的测量,这2项指标的比值称为骨体积分数(BV/TV),另一个基本测量是骨表面积(BS)[65]。用于定义骨微结构和形态的众多参数中,骨体积分数是定义骨愈合过程特征最好的参数之一[67]。Micro-CT主要用于生成有关骨结构的信息,它也可用于估计组织矿物质密度(TMD)。多项研究中,成骨细胞的数量和新形成的骨面积通过组织形态计量学分析来确定,而骨的微结构和骨体积则通过Micro-CT分析来确定。这两种技术在细胞和结构评估中对缺损愈合的有效性方面是相辅相成的[30]。 颌骨组织工程相关研究中新形成的骨通常需要进行生物力学检测,包含抗压实验和抗剪切实验。抗压实验测量新生骨块的抗压强度,评估引导新生骨的抗压强度,将骨块标本置于力学试验机的基座中央,夹具固定,选取合适大小的顶冲头,垂直下降,以0.1-1 mm/s加载速度加压,记录骨块开始形变时的载荷值,单位为N。抗剪切实验测量新生骨与自然骨结合界面的抗剪切强度,将规则形状的骨块标本悬空置于力学试验机的基座上,夹具固定自然骨部分,边缘置于新生骨与自然骨结合界面,配套模具安装于冲顶头,使其作用于新生骨部分,以0.1-1 mm/s 加载速度加压,记录结合界面形变时的载荷值,单位为N[68]。 建立颌骨缺损动物模型后实验检测方法汇总,见表5。 "
| [1] ZHANG Q, WU W, QIAN C, et al. Advanced biomaterials for repairing and reconstruction of mandibular defects. Mater Sci Eng C Mater Biol Appl. 2019;103:109858. [2] 卢嘉蕊,权晶晶.骨缺损动物模型的研究进展[J].口腔医学研究,2021,37(9): 783-786. [3] AWADEEN MA, AL-BELASY FA, AMEEN LE, et al. Early therapeutic effect of platelet-rich fibrin combined with allogeneic bone marrow-derived stem cells on rats’ critical-sized mandibular defects. World J Stem Cells. 2020;12(1):55-69. [4] 陈胡贵,覃建国,李理,等.大动物节段性骨缺损模型的研究进展[J].北京生物医学工程,2021,40(2):203-208. [5] MUSCHLER GF, RAUT VP, PATTERSON TE, et al. The design and use of animal models for translational research in bone tissue engineering and regenerative medicine. Tissue Eng Part B Rev. 2010;16(1):123-45. [6] LI Y, CHEN SK, LI L, et al. Bone defect animal models for testing efficacy of bone substitute biomaterials. J Orthop Translat. 2015;3(3):95-104. [7] HUANG S, XU L, SUN Y, et al. An improved protocol for isolation and culture of mesenchymal stem cells from mouse bone marrow. J Orthop Translat. 2015; 3(1):26-33. [8] DECONDE AS, LEE MK, SIDELL D, et al. Defining the Critical-Sized Defect in a Rat Segmental Mandibulectomy Model. JAMA Otolaryngol Head Neck Surg. 2014;140(1):58. [9] MANJU V, ANITHA A, MENON D, et al. Nanofibrous yarn reinforced HA-gelatin composite scaffolds promote bone formation in critical sized alveolar defects in rabbit model. Biomed Mater. 2018;13(6):065011. [10] ŠTEMBÍREK J, KYLLAR M, PUTNOVÁ I, et al. The pig as an experimental model for clinical craniofacial research. Lab Anim. 2012;46(4):269-279. [11] ZHANG Z, REN H, SHEN G, et al. Animal models for glucocorticoid-induced postmenopausal osteoporosis: An updated review. Biomed Pharmacother. 2016; 84:438-446. [12] COLMAN RJ. Non-human primates as a model for aging. Biochim Biophys Acta Mol Basis Dis. 2018;1864(9):2733-2741. [13] XIE Y, SU Y, MIN S, et al. Collagen Sponge Functionalized with Chimeric Anti-BMP-2 Monoclonal Antibody Mediates Repair of Critical-Size Mandibular Continuity Defects in a Nonhuman Primate Model. Biomed Res Int. 2017;2017:1-11. [14] 岳飞翔,隋海明.骨缺损动物模型的研究进展[J].中国民族民间医药,2015, 24(16):35-36. [15] ANDREOLLO NA, SANTOS EF, ARAÚJO MR, et al. Rat’s age versus human’s age: what is the relationship? Arq Bras Cir Dig. 2012;25(1):49-51. [16] ZHANG J, FENG Z, WEI J, et al. Repair of Critical-Sized Mandible Defects in Aged Rat Using Hypoxia Preconditioned BMSCs with Up-regulation of Hif-1α. Int J Biol Sci. 2018;14(4):449-460. [17] GREER AW, HAMIE JC. Relative maturity and the development of immunity to gastrointestinal nematodes in sheep: an overlooked paradigm? Parasite Immunol. 2016;38(5):263-272. [18] LEE S, CHOI D, SHIM JH, et al. Efficacy of three-dimensionally printed polycaprolactone/beta tricalcium phosphate scaffold on mandibular reconstruction. Sci Rep. 2020;10(1):4979. [19] RAI B, HO KH, LEI Y, et al. Polycaprolactone-20% Tricalcium Phosphate Scaffolds in Combination With Platelet-Rich Plasma for the Treatment of CriticalSized Defects of the Mandible: A Pilot Study. J Oral Maxillofac Surg. 2007;65(11):2195-2205. [20] KHOJASTEH A, BEHNIA H, HOSSEINI FS, et al. The effect of PCL-TCP scaffold loaded with mesenchymal stem cells on vertical bone augmentation in dog mandible: a preliminary report. J Biomed Mater Res B Appl Biomater. 2013;101(5):848-854. [21] NAGARAJU S, BOTTINO R, WIJKSTROM M, et al. Islet xenotransplantation: what is the optimal age of the islet-source pig? Xenotransplantation. 2015;22(1):7-19. [22] SUN Z, KENNEDY KS, TEE BC, et al. Establishing a Critical-Size Mandibular Defect Model in Growing Pigs: Characterization of Spontaneous Healing. J Oral Maxillofac Surg. 2014;72(9):1852-1868. [23] SCHMITZ JP, HOLLINGER JO. The critical size defect as an experimental model for craniomandibulofacial nonunions. Clin Orthop Relat Res. 1986;205(205):299-308. [24] HOLLINGER JO, KLEINSCHMIDT JC. The critical size defect as an experimental model to test bone repair materials. J Craniofac Surg. 1990;1(1):60-68. [25] GOSAIN AK, SONG L, YU P, et al. Osteogenesis in cranial defects: reassessment of the concept of critical size and the expression of TGF-beta isoforms. Plast Reconstr Surg. 2000;106(2):360-371. [26] KABAN LB, GLOWACKI J, MURRAAY JE. Repair of experimental mandibular bony defects in rats. Surg Forum. 1979;30:519-521. [27] OZAKI M, TAKAYAMA T, YAMAMOTO T, et al. A collagen membrane containing osteogenic protein-1 facilitates bone regeneration in a rat mandibular bone defect. Arch Oral Biol. 2017;84:19-28. [28] ZHANG W, SHI W, WU S, et al. 3D printed composite scaffolds with dual small molecule delivery for mandibular bone regeneration. Biofabrication. 2020;12(3): 035020. [29] MIGUEZ PA, TUIN SA, ROBINSON AG, et al. Hesperidin Promotes Osteogenesis and Modulates Collagen Matrix Organization and Mineralization In Vitro and In Vivo. Int J Mol Sci. 2021;22(6):3223. [30] KOCA CG, KÖSEHASANOĞULLAR M. Evaluation of single-dose applied teriparatide effect on bone healing with histomorphometric and micro-ct analysis. J Cranio-Maxillofac Surg. 2021;49(2):98-103. [31] ÖZKAN E, BEREKET MC, ŞENEL E, et al. Effect of Electrohydraulic Extracorporeal Shockwave Therapy on the Repair of Bone Defects Grafted With Particulate Allografts. J Craniofac Surg. 2019;30(4):1298-1302. [32] BARRIENTOS FJ, REDONDO LM, ALBERCA M, et al. Bone regeneration with autologous adipose-derived mesenchymal stem cells: A reliable experimental model in rats. MethodsX. 2020;7:101137. [33] DRÉNO M, BLÉRY P, GUICHEUX J, et al. Development of a Rat Model of Mandibular Irradiation Sequelae for Preclinical Studies of Bone Repair. Tissue Eng Part C Methods. 2020;26(8):447-455. [34] CHENG G, LI Z, WAN Q, et al. A novel animal model treated with tooth extraction to repair the full-thickness defects in the mandible of rabbits. J Surg Res. 2015; 194(2):706-716. [35] 鄂玲玲,王东胜,师占平,等.一种新型的兔牙槽骨缺损模型的建立[J].中华老年口腔医学杂志,2011,9(3):137-140+171. [36] ANDERSSON L, RAMZI A, JOSEPH B. Studies on dentin grafts to bone defects in rabbit tibia and mandible; development of an experimental model. Dent Traumatol. 2009;25(1):78-83. [37] BAI Y, DAI X, YIN Y, et al. Biomimetic piezoelectric nanocomposite membranes synergistically enhance osteogenesis of deproteinized bovine bone grafts. Int J Nanomedicine. 2019;14:3015-3026. [38] LI X, SONG T, CHEN X, et al. Osteoinductivity of Porous Biphasic Calcium Phosphate Ceramic Spheres with Nanocrystalline and Their Efficacy in Guiding Bone Regeneration. ACS Appl Mater Interfaces. 2019;11(4):3722-3736. [39] ASHOUR AA, ZAGHLOUL M, MAHMOUD W, et al. Gelfoam haemostatic agent with or without autologous bone marrow-derived stem cells for the regeneration of critical-size mandibular defects in the rabbit. Int J Oral Maxillofac Surg. 2018; 47(11):1488-1494. [40] KOTAGUDDA RANGANATH S, SCHLUND M, DELATTRE J, et al. Bilateral double site (calvarial and mandibular) critical-size bone defect model in rabbits for evaluation of a craniofacial tissue engineering constructs. Mater Today Bio. 2022;14:100267. [41] V M, IYER S, MENON D, et al. Evaluation of osseointegration of staged or simultaneously placed dental implants with nanocomposite fibrous scaffolds in rabbit mandibular defect. Mater Sci Eng C Mater Biol Appl. 2019;104:109864. [42] PIOTROWSKI SL, WILSON L, MALDONADO KL, et al. Effect of Radiation on DCE-MRI Pharmacokinetic Parameters in a Rabbit Model of Compromised Maxillofacial Wound Healing: A Pilot Study. J Oral Maxillofac Surg. 2020;78(6):1034.e1-1034.e10. [43] CARLISLE PL, GUDA T, SILLIMAN DT, et al. Are critical size bone notch defects possible in the rabbit mandible? J Korean Assoc Oral Maxillofac Surg. 2019;45(2):97. [44] MONIR A, MUKAIBO T, ABD EL-AAL ABM, et al. Local administration of HMGB-1 promotes bone regeneration on the critical-sized mandibular defects in rabbits. Sci Rep. 2021;11(1):8950. [45] ANWAR SK, HAMID HMA. Immuno-histopathologic evaluation of mineralized plasmatic matrix in the management of horizontal ridge defects in a canine model (a split-mouth comparative study). Odontology. 2022;110(3):523-534. [46] WU J, WANG Q, FU X, et al. Influence of Immunogenicity of Allogeneic Bone Marrow Mesenchymal Stem Cells on Bone Tissue Engineering. Cell Transplant. 2016;25(2):229-242. [47] MESGARZADEH AH, NASIRI I, JAROLMASJED S, et al. Evaluation of bone regeneration in mandible large defect using undifferentiated adipose stem cells loaded on gelatin carrier: An animal model case study. J Dent Res Dent Clin Dent Prospects. 2021;15(1):22-29. [48] HUH JY, CHOI BH, KIM BY, et al. Critical size defect in the canine mandible. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2005;100(3):296-301. [49] DORAFSHAR AH, MUNDINGER GS, MOHAN R, et al. Comparison of Free Fibular Flaps With Reamer-Irrigator-Aspirator Bone Grafts for the Reconstruction of Critical-Sized Mandibular Defects. J Craniofac Surg. 2014;25(6):1953-1958. [50] VAN OIRSCHOT BAJA, GEVEN EJW, MIKOS AG, et al. A Mini-Pig Mandibular Defect Model for Evaluation of Craniomaxillofacial Bone Regeneration. Tissue Eng Part C Methods. 2022;28(5):193-201. [51] CUI Y, LU C, CHEN B, et al. Restoration of mandibular bone defects with demineralized bone matrix combined with three-dimensional cultured bone marrow-derived mesenchymal stem cells in minipig models. J Mater Sci Mater Med. 2018;29(9):147. [52] DIENEL K, ABU-SHAHBA A, KORNILOV R, et al. Patient‐Specific Bioimplants and Reconstruction Plates for Mandibular Defects: Production Workflow and In Vivo Large Animal Model Study. Macromol Biosci. 2022;22(4):2100398. [53] UNNIKRISHNAN PS, IYER S, MANJU V, et al. Nanocomposite fibrous scaffold mediated mandible reconstruction and dental rehabilitation: An experimental study in pig model. Mater Sci Eng C Mater Biol Appl. 2021;112631. [54] BOZO IY, DEEV RV, SMIRNOV IV, et al. 3D Printed Gene-activated Octacalcium Phosphate Implants for Large Bone Defects Engineering. Int J Bioprint. 2020;6(3):275. [55] SCHLIEPHAKE H, KNEBEL JW, AIFDERHEIDE M, et al. Use of cultivated osteoprogenitor cells to increase bone formation in segmental mandibular defects: an experimental pilot study in sheep. Int J Oral Maxillofac Surg. 2001; 30(6):531-537. [56] 周苗,彭歆,车月娟,等.构建预制个性化骨瓣修复下颌骨缺损的灵长类动物模型[J].中国组织工程研究,2014,18(18):2812-2817. [57] BASKIN JZ, WHITE BM, VASANJI A, et al. Mandible Biomechanics and Continuously Erupting Teeth: A New Defect Model for Studying Load-Bearing Biomaterials. Biomedicines. 2021;9(7):730. [58] SARGOLZAEI-AVAL F, SABERI EA, ARAB MR, et al. Octacalcium phosphate/gelatin composite facilitates bone regeneration of critical-sized mandibular defects in rats: A quantitative study. J Dent Res Dent Clin Dent Prospects. 2019;13(4):258-266. [59] SHAH SR, YOUNG S, GOLDMAN JL, et al. A composite critical-size rabbit mandibular defect for evaluation of craniofacial tissue regeneration. Nat Protoc. 2016;11(10):1989-2009. [60] ROSKIES MG, FANG D, ABDALLAH MN, et al. Three-dimensionally printed polyetherketoneketone scaffolds with mesenchymal stem cells for the reconstruction of critical-sized mandibular defects. Laryngoscope. 2017;127(11):E392-E398. [61] SCHLUND M, DEPEYRE A, KOTAGUDDA RANGANATH S, et al. Rabbit calvarial and mandibular critical-sized bone defects as an experimental model for the evaluation of craniofacial bone tissue regeneration. J Stomatol Oral Maxillofac Surg. 2021;S2468-7855(21)00268-8. [62] WANG X, WU X, XING H, et al. Porous Nanohydroxyapatite/Collagen Scaffolds Loading Insulin PLGA Particles for Restoration of Critical Size Bone Defect. ACS Appl Mater Interfaces. 2017;9(13):11380-11391. [63] GUO J, MENG Z, CHEN G, et al. Restoration of Critical-Size Defects in the Rabbit Mandible Using Porous Nanohydroxyapatite-Polyamide Scaffolds. Tissue Eng Part A. 2012;18(11-12):1239-1252. [64] DORAFSHAR AH, MOHAN R, MUNDINGER GS, et al. Reconstruction of Porcine Critical-Sized Mandibular Defects with Free Fibular Flaps: The Development of a Craniomaxillofacial Surgery Model. J Reconstr Microsurg. 2014;30(04):241-248. [65] BOUSEIN ML, BOYD SK, CHRISTIANSEN BA, et al. Guidelines for assessment of bone microstructure in rodents using micro-computed tomography. J Bone Miner Res. 2010;25(7):1468-1486. [66] FELDKAMP LA, GOLDSTEIN SA, PARFITT AM, et al. The direct examination of three-dimensional bone architecture in vitro by computed tomography. J Bone Miner Res. 1989;4(1):3-11. [67] MORGAN EF, MASON ZD, CHIEN KB, et al. Micro-computed tomography assessment of fracture healing: relationships among callus structure, composition, and mechanical function. Bone. 2009;44(2):335-344. [68] 杨晓峰,白晓雪,孙勇.引导新生骨质量的检测方法与评价[J].西南国防医药,2013,23(4):445-447. |
| [1] | Nong Fuxiang, Jiang Zhixiong, Li Yinghao, Xu Wencong, Shi Zhilan, Luo Hui, Zhang Qinglang, Zhong Shuang, Tang Meiwen. Bone cement augmented proximal femoral nail antirotation for type A3.3 intertrochanteric femoral fracturalysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-10. |
| [2] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [3] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [4] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [5] | Wang Ji, Zhang Min, Yang Zhongya, Zhang Long. A review of physical activity intervention in type 2 diabetes mellitus with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1272-1277. |
| [6] | Nie Chenchen, Su Kaiqi, Gao Jing, Fan Yongfu, Ruan Xiaodi, Yuan Jie, Duan Zhaoyuan, Feng Xiaodong. The regulatory role of circular RNAs in cerebral ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1286-1291. |
| [7] | Gao Yu, Han Jiahui, Ge Xin. Immunoinflammatory microenvironment after spinal cord ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1300-1305. |
| [8] | Ruan Ling, Wang Guanghua, Wu Rongping, Jin Zhan, Lyu Zhenqing, Zhang Nan, Li Shoubang. Correlation between exercise intensity and lipid metabolism disorder and oxidative stress in a high-diet rat model [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1149-1155. |
| [9] | Zhu Lin, Gu Weiping, Wang Can, Chen Gang. Biomechanical analysis of All-on-Four and pterygomaxillary implants under different maxillary bone conditions [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 985-991. |
| [10] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [11] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [12] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [13] | Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109. |
| [14] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| [15] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||