Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (8): 1300-1305.doi: 10.12307/2023.051
Previous Articles Next Articles
Immunoinflammatory microenvironment after spinal cord ischemia-reperfusion injury
Gao Yu, Han Jiahui, Ge Xin
- Department of Intensive Care Unit, Wuxi Ninth Hospital Affiliated to Soochow University, Wuxi 214000, Jiangsu Province, China
-
Received:2022-01-18Accepted:2022-03-12Online:2023-03-18Published:2022-07-29 -
Contact:Ge Xin, MD, Associate chief physician, Department of Intensive Care Unit, Wuxi Ninth Hospital Affiliated to Soochow University, Wuxi 214000, Jiangsu Province, China -
About author:Gao Yu, Master, Department of Intensive Care Unit, Wuxi Ninth Hospital Affiliated to Soochow University, Wuxi 214000, Jiangsu Province, China -
Supported by:the Precision Medicine Project of Wuxi Municipal Healthy Commission, No. J202007 (to GX)
CLC Number:
Cite this article
Gao Yu, Han Jiahui, Ge Xin. Immunoinflammatory microenvironment after spinal cord ischemia-reperfusion injury[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1300-1305.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
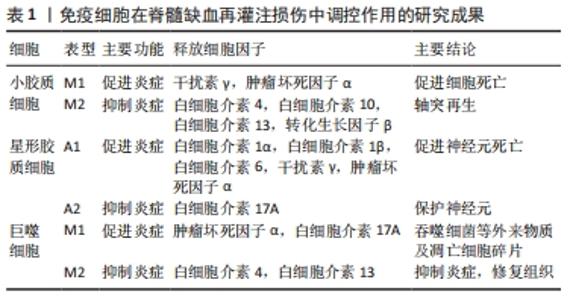
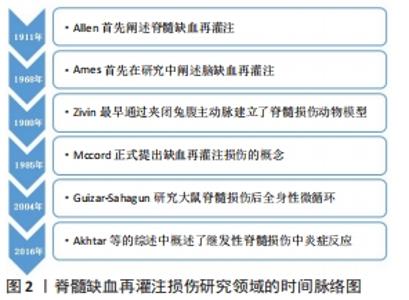
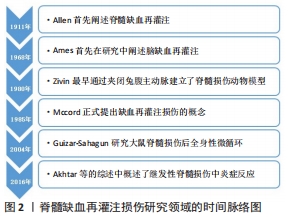
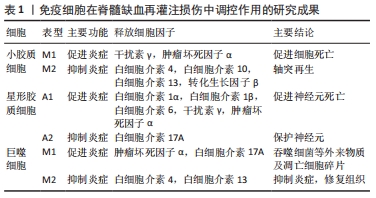
2.1 脊髓缺血再灌注损伤后的免疫炎症反应 脊髓缺血再灌注损伤是在原发性脊髓损伤础上的继发性损伤,再灌注血液不仅加重缺血脊髓组织损伤还会导致神经系统的并发症。脊髓缺血再灌注损伤潜在病理机制较为复杂,其显著的病理学特征就是血管系统以及免疫微环境的紊乱,如脊髓损伤部位浸润性白细胞的活化,再灌注后恢复的血流刺激黏附分子和趋化因子的表达,通过激活小胶质细胞、星形胶质细胞和巨噬细胞等免疫细胞导致免疫炎性微环境的改变[6]。脊髓缺血再灌注损伤的炎性反应以灰质内大量炎性细胞聚集为特征,继发性损伤的级联反应在损伤区域引发了后续的巨大炎症反应,可广泛延伸至邻近组织,最终导致血脊髓屏障的破坏,神经细胞水肿、凋亡和焦亡,并在很大程度上抑制轴突再生和脊髓损伤后的功能恢复[6-8]。在炎症的不同阶段,不同的免疫细胞可以交互影响,免疫微环境的变化在促炎过程和抑炎过程的调节中起着至关重要的作用。 2.2 脊髓缺血再灌注损伤后的免疫细胞活化 免疫细胞在脊髓缺血再灌注损伤中调控作用,见表1。"
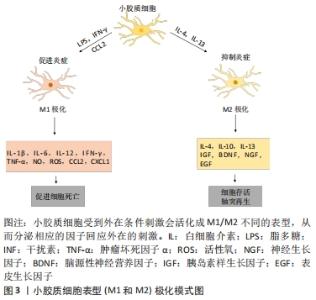
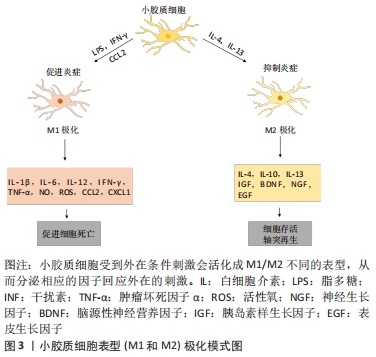
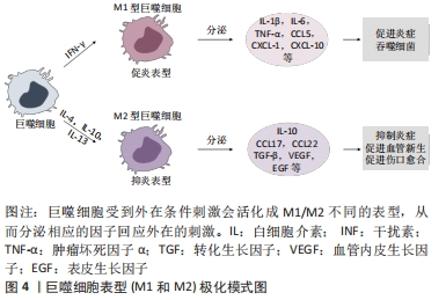
2.2.1 小胶质细胞 神经细胞和胶质细胞是构成中枢神经系统的主要细胞,神经细胞和胶质细胞的比例接近1∶1。神经胶质细胞主要包括星形胶质细胞,少突胶质细胞和小胶质细胞,它们共同起着维持神经系统平衡的作用,支持和保护神经元[6-7]。小胶质细胞是巨噬细胞样细胞,作为中枢神经系统的主要免疫细胞,是免疫微环境变化的主动感受器,负责抵御传染源,清除凋亡和受损细胞,重塑不适当的神经连接,帮助神经系统恢复稳态。它们在正常的中枢神经系统中保持静止,而在神经损伤受到刺激时被迅速激活[9-10]。小胶质细胞可以按照不同的表型进行分化,分为M1型和M2型(见图3),不同的亚型具有不同的特征,影响着后续的神经炎症过程。M1型为促炎表型,与高水平的促炎细胞因子如肿瘤坏死因子α和干扰素γ相关,促进炎症反应进而杀死外源性入侵微生物。但是M1型可以产生高水平的一氧化氮和基质金属蛋白酶造成组织损伤和轴索回缩,产生不良后果。M2型为抑炎表型,可以产生白细胞介素4、白细胞介素10和白细胞介素13等抑炎递质,抑制炎症反应恢复稳态起到神经保护作用,还可以通过吞噬细胞碎片等方式参与后期的组织修复和重塑[6-7]。已有多项研究表明M1/M2小胶质细胞表型的平衡在脊髓损伤中起重要作用,促进M2小胶质细胞的分化可以减轻炎性损伤并改善恢复过程[11-12]。"
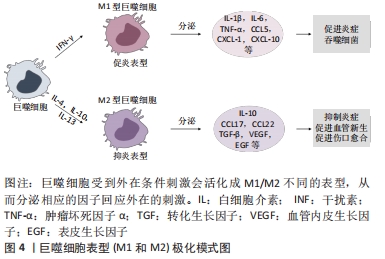
通过检测脊髓缺血再灌注损伤模型大鼠的血浆和脑脊液,有研究发现高级氧化蛋白产物增加,免疫荧光染色提示小胶质细胞过度激活,呈M1促炎表型。脊髓缺血再灌注损伤使活性氧释放增加并诱导了p38MAPK和JNK的磷酸化,随后触发了核因子κB(nuclear factor κB,NF-κB)p65的核转位表达促炎因子。用高级氧化蛋白产物处理小胶质细胞后诱导了核苷酸结合寡聚化样受体蛋白3(nucleotide-binding oligomerization like receptor protein 3,NLRP3)炎性小体的激活和Gasdermin-d(GSDMD)的裂解,出现了细胞焦亡[13]。有研究通过腹主动脉夹闭的方式进行造模,脊髓缺血再灌注损伤后小胶质细胞激活明显增加,而给予右美托咪定后可以抑制小胶质细胞活化。将长链非编码RNA小核仁RNA宿主基因14(small nucleolar RNA host gene 14,SNHG14)转染到小胶质细胞后通过敲低和过表达进行调控处理,发现 SNHG14敲低可以进一步降低ED-1、肿瘤坏死因子α和白细胞介素6的水平,帮助抑制氧糖剥夺/再氧合诱导的小胶质细胞激活的作用,而过表达SNHG14重新激活了小胶质细胞,并加重了神经功能缺陷,消除了右美托咪定的治疗效果,最终证实抑制小胶质细胞活化有利于脊髓缺血再灌注损伤神经功能恢复[14]。电刺激也可以影响小胶质细胞的活化,通过脊髓缺血再灌注损伤造模后于硬膜外放置脊髓电刺激电极,立即给予2 Hz和50 Hz电刺激,结果提示脊髓缺血再灌注损伤后8 h,第1,3,7天小胶质细胞活化明显增加,肿瘤坏死因子α、白细胞介素1β、白细胞介素10和 NF-κB分泌与对照组相比有增加,给予电刺激后可以缓解上述情况;同时发现脊髓刺激对ERK1/2的表达有影响,与对照组相比再灌注后8 h及第1,3,7天p-ERK1/2水平显著升高;与对照组相比,2 Hz组p-ERK1/2水平在再灌注后8 h及1,3,7 d显著下降,而50 Hz组p-ERK1/2水平无差异;该研究首次证实了2 Hz的脊髓电刺激可以抑制小胶质细胞活化起到神经保护作用[15]。 随着研究的深入,学者们发现抑制小胶质细胞会影响脊髓缺血再灌注损伤的神经功能恢复。有研究使用集落刺激因子受体抑制剂PLX3397选择性地消除小胶质细胞来研究小胶质细胞在脊髓中的特定作用,免疫荧光IBA-1染色证实PLX3397喂养,可以成功消除几乎所有的小胶质细胞,但没有影响脊髓中星形胶质细胞和少突胶质细胞等其他类型的细胞。结果提示脊髓损伤7 d后,对照组病变中心周围的小胶质细胞显著减少,小胶质细胞在脊髓损伤部位周围被迅速招募,而集落刺激因子受体减少了脊髓损伤诱导的这种积累,小胶质细胞耗竭的小鼠表现出运动功能恢复受损;而且他们惊奇的发现使用PLX3397耗尽小胶质细胞时,病变核心周围的星形胶质细胞定向是随机的,没有向任何特定方向对齐并形成了较小紧凑的瘢痕;最后作者们认为小胶质细胞消耗使得活化的星形胶质细胞对病变部位的再生明显延迟,在脊髓损伤后活化的星形胶质细胞消融之前,炎症细胞扩散增加;无序的星形胶质细胞瘢痕促进了白细胞在病变核心外的扩散,并伴随着神经元存活率减少,轴突收缩明显增加,致使运动功能恢复减弱[16]。在挫伤性脊髓损伤的小鼠模型中,小胶质细胞也被确定为脊髓损伤后形成瘢痕的关键细胞成分,以保护神经组织 [17]。 2.2.2 巨噬细胞 巨噬细胞是先天免疫的重要细胞组成部分,主要为源于骨髓造血干细胞的单核细胞,其特点是具有较高的可塑性和对不同刺激的多向分化能力[18]。巨噬细胞按其表型分为原始型巨噬细胞(M0),经典活化的巨噬细胞(M1)和选择性活化巨噬细胞(M2)[19](见图4)。M1型巨噬细胞,可以被Toll样受体(Toll-like receptor,TLR)的配体脂多糖或干扰素γ激活,高表达促炎细胞因子白细胞介素12、白细胞介素23和肿瘤坏死因子α等,在功能上可以促进免疫清除外来病原体和肿瘤细胞,也被称为促炎表型[20]。M2型巨噬细胞可以被细胞因子、糖皮质激素、免疫复合物和脂多糖等多种刺激极化,进一步分为M2a、M2b、M2c和M2d亚类,在抗炎、促进新生血管形成和损伤组织修复等方面起重要作用[21]。尽管小胶质细胞和单核细胞来源的巨噬细胞具有相同的细胞标记物和形态,但它们可以通过对特殊环境刺激的极化反应显示出不同的功能。与单核细胞来源的巨噬细胞相比,小胶质细胞产生高水平的白细胞介素10,并显示出更强的髓磷脂吞噬能力[20-21]。 "
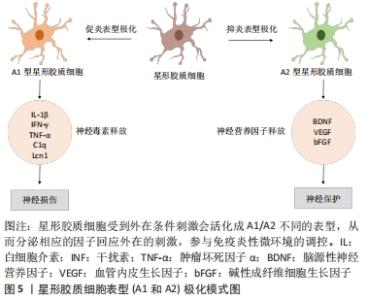
研究表明在脊髓缺血再灌注损伤早期,单核细胞来源的巨噬细胞表现为M1型,其生物标志物iNOS、肿瘤坏死因子α、CD86、CD16的急剧升高,释放有害的促炎细胞因子肿瘤坏死因子α、白细胞介素1β、白细胞介素6和氧化代谢物,形成炎性微环境从而损害轴突的再生,但是短暂的局限于脊髓缺血再灌注损伤后的第1周。1周后,M2生物标志物CD204和CD206升高,释放保护性和神经营养因子、清除细胞碎片和解决局部炎症来限制缺血性损伤。此外,通过氯膦酸脂质体全身给药的方式消耗单核细胞来源的巨噬细胞,小鼠显著保留了神经功能,缓解了脊髓缺血再灌注损伤引起的神经元损伤。而第2周开始消融单核细胞来源的巨噬细胞可能对功能恢复没有影响,因此认为单核细胞来源的巨噬细胞流入脊髓的时间仅限于第1周,主要是促炎的M1型,而小胶质细胞是后期M2型细胞的主要来源。早期单核细胞来源的巨噬细胞会导致脱髓鞘和神经元损伤,后期小胶质细胞则通过清除碎片来保护神经元[22]。最近的脊髓缺血再灌注损伤研究证实活化的小胶质细胞和巨噬细胞使得丛状蛋白B2(Plexin-B2)表达增加,小胶质细胞负责早期同心物理屏障的形成同时影响新生血管的空间方向。新生血管空间方向反过来可能通过引导血源性免疫细胞导向病变核心来促进聚集,从而确保保护屏障内的清除活性和炎症反应。事实上,最初缺乏细胞的坏死核心后来被充满脂质碎片的密集的巨噬细胞所取代。活化的巨噬细胞也可以通过直接的物理相互作用触发轴突顶梢枯死或营养不良轴突收缩。因此,在星形胶质细胞边界内聚集活化的小胶质细胞和巨噬细胞对于减轻它们与轴突的直接接触至关重要[23]。 2.2.3 星形胶质细胞 星形胶质细胞是神经元的支持细胞,是胶质细胞边缘的关键组成部分,维持中枢神经系统稳态和神经元功能。它积极促进血脑屏障的形成和维持,而且可以限制免疫细胞通过血脑屏障进入中枢神经系统实质;它可以分泌神经营养因子来调节突触发生、神经元分化和存活,在局部和适应性免疫反应调节中起着关键作用[24-25]。神经炎症诱导星形胶质细胞活化,表型分类分为A1型和A2型,与小胶质细胞中M1和M2的活化分型平行。A1型为促炎表型,使多个促炎基因上调,并增强促炎细胞因子、趋化因子和生长因子的产生,对突触有破坏性[26]。A2型可以使许多神经营养因子上调,并分泌促进中枢神经系统突触生长的蛋白,具有神经保护和修复功能[27],见图5。 "
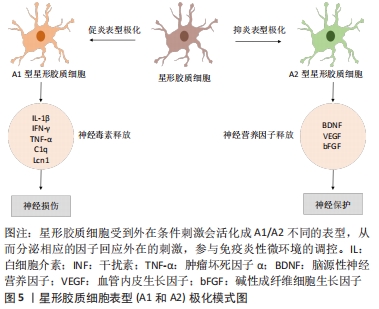

(1)脊髓缺血再灌注损伤后星形胶质细胞中NF-κB通路研究现状:在炎症过程中,星形细胞的信号通路似乎汇聚在共同的下游转录调控因子上,例如,NF-κB异源二聚体的核转位是星形胶质细胞活化的中心步骤。近期研究显示脊髓缺血再灌注损伤后星形胶质细胞活化增强,通过热休克蛋白A8激活NLRP3炎性小体,导致NF-κB的核转位和DNA结合活性增强。将热休克蛋白A8敲低后可以逆转上述状况,使活化的星形胶质细胞表达减少,产生神经保护作用,改善神经功能[6]。热休克蛋白A8的表达,在该研究存在星形胶质细胞和小胶质细胞的共定位,但是热休克蛋白A8和IBA-1之间的相关性弱于热休克蛋白A8和GFAP免疫反应细胞,特别是在再灌注12 h后,因此强调脊髓星形胶质细胞的热休克蛋白A8表达可能在脊髓缺血再灌注损伤损伤的发病机制中发挥重要作用[6]。 (2)脊髓缺血再灌注损伤后脊髓水肿机制研究现状:星形胶质细胞对血脊髓屏障的影响和缺血再灌注后脊髓水肿的机制研究也是主要的研究方向。有研究发现给予脊髓缺血再灌注损伤模型大麻素-2受体(cannabinoid-2 receptor,CB2R)激动剂JWH-133预处理,可减轻模型大鼠后肢运动功能缺陷和血脊髓屏障渗漏,并可防止紧密连接蛋白1下调和基质金属蛋白酶9上调,可降低损伤后血管周围基质金属蛋白酶9和活化星形胶质细胞的表达[5]。该结论也在其他研究中得到证实[28],同时作者还证实了星形胶质细胞的水肿是通过HMGB1/TLR4/MyD88/NF-κB信号通路介导并以白细胞介素6依赖的方式完成的,而使用右美托咪定可以抑制该通路的激活,增加水通道蛋白(aquaporin,AQP)4的表达,抑制炎症反应减轻水肿,改善神经功能[28]。人参皂苷单体具有抗氧化、抗凋亡和神经保护的生物学活性。研究发现AQP4在脊髓缺血再灌注损伤的星形胶质细胞氧糖剥夺/再氧合模型中的表达下调,人参皂苷Rb1治疗显著减弱了AQP4的降低,以保护星形胶质细胞的完整性,上调AQP4可以抑制氧糖剥夺/再氧合诱导的星形胶质细胞水肿[29]。 (3)脊髓缺血再灌注损伤治疗药物研究现状:临床药物对AQP4的影响也有报道,甲强龙(methylprednisolone)和促红细胞生成素(erythropoietin)是目前最常见的用于治疗脊髓缺血再灌注损伤的药物,研究发现它们对AQP4有协同作用增加其表达,减轻损伤后水肿[30]。退行性颈椎病手术减压模型在减压前30 min和术后2周给予30 mg/kg甲强龙,结果发现单剂量甲强龙治疗可在不损害免疫系统的情况下,显著加快运动恢复(P < 0.05),降低围术期运动并发症发生率,且不影响循环白细胞组成。脊髓的组织学评估显示神经元存活增多和实质炎症的减轻[31]。而促红细胞生成素5 000 U/kg的预处理同样改善了兔脊髓缺血再灌注损伤模型的组织损伤和细胞凋亡,改善神经功能获得更高的评分[32]。因此,有国外学者将甲强龙和促红细胞生成素进行了临床研究,将110例脊髓型颈椎病患者随机分为对照组和试验组,两组患者均行颈椎融合内固定和颈前路椎间盘切除术,对照组在脊髓减压前30 min快速注射甲强龙30 mg/kg,而试验组在脊髓减压前30 min静脉注射甲强龙同时还给予促红细胞生成素3 000 U/kg;在术前和治疗后3个月对两组患者进行神经功能评估,治疗后3个月两组患者采用世界卫生组织生活质量评估工具(WHOQOL-100)评估生活质量;术前统计学资料基线数据无差异,治疗3个月后试验组患者白细胞介素1β、白细胞介素8水平低于对照组(P < 0.05),试验组患者在心理、生理、社会关系、独立性、环境和一般生活质量等方面的WHOQOL-100指标均高于对照组(P < 0.05);因此得出结论促红细胞生成素与甲强龙联合治疗脊髓缺血再灌注损伤是有效的,可以降低S-100β、神经特异性烯醇和白细胞介素1β的分泌,保留和改善患者脊髓神经功能和生活质量[33]。最近,维生素D也被用于脊髓缺血再灌注损伤的治疗,有研究将0.5 μg/kg维生素D和30 mg/kg甲强龙进行了单药物治疗比较,结果发现维生素D治疗组在氧化应激产物的生成、病理损伤和神经功能评分方面均优于甲强龙组,提示维生素D是治疗脊髓缺血再灌注损伤的有效药物[34],在未来有一定的前景。 2.2.4 小胶质细胞和星形胶质细胞的交互 小胶质细胞、少突胶质细胞和星形胶质细胞形成一个被高度调控的微环境,它们之间的相互作用对维持中枢神经系统内稳态至关重要。小胶质细胞通常对病理刺激比星形胶质细胞反应更快,诱导星形胶质细胞激活并决定它的命运[24]。星形胶质细胞反馈性影响小胶质细胞激活的能力和细胞功能,形成星形胶质细胞和小胶质细胞交互。细胞因子、趋化因子、生长因子和三磷酸腺苷等多种分子是这种细胞间的交互的主要媒介[35]。高度富集的星形胶质细胞培养物在脂多糖刺激下仅释放少量的肿瘤坏死因子α、一氧化氮和活性氧等炎性因子,这表明至少在炎症条件下星形胶质细胞的免疫反应仍依赖于小胶质细胞,在没有小胶质细胞刺激后,星形胶质细胞不能产生足够水平的促炎因子[36]。通过脂多糖激活的小胶质细胞分泌白细胞介素1α、肿瘤坏死因子α和补体成分1q,诱导星形胶质细胞的转录反应使星形胶质细胞活化,分化为A1表型继而分泌了神经毒性因子,导致星形胶质细胞吞噬活性降低,神经营养因子表达减少。在炎症条件下,小胶质细胞来源的促炎因子损害了星形胶质细胞代谢谷氨酸的能力,这表明中枢神经系统先天免疫中小胶质细胞-星形胶质细胞交互作用是十分关键的[37]。星形胶质细胞反过来通过许多星形胶质细胞衍生的因子来调节小胶质细胞的表型和功能,如细胞因子、趋化因子、Ca2+、补体蛋白和其他炎性递质。在病理损伤或存在炎症刺激的情况下,星形胶质细胞的多种可溶性因子的表达发生变化,通过改变小胶质细胞的激活、迁移和吞噬发挥关键作用。星形胶质细胞在炎症刺激下可以分泌血清类黏蛋白2(orosomucoid-2,ORM2),可以与小胶质细胞C-C趋化因子受体5(C-C chemokine receptor type 5,CCR5)结合,并阻断趋化因子C-X-C配体(C-X-C motif ligand,CXCL)4和CCR5相互作用。星形胶质细胞通过ORM2下调小胶质细胞的激活,在神经炎症过程中发挥抗炎作用[35,38]。1型纤溶酶原激活剂抑制剂(plasminogen activator inhibitor type 1,PAI-1),已被确定为星形胶质细胞-小胶质细胞相互作用的重要介质,它可以通过低密度脂蛋白受体相关蛋白(LRP)1/Janus激酶(JAK)/STAT1通路促进体外小胶质细胞迁移[35]。星形胶质细胞也通过细胞增生对中枢神经系统损伤做出反应,并与包括小胶质细胞在内的其他细胞类型形成胶质细胞瘢痕,有助于轴突的再生[39]。在创伤性脑损伤模型中,小胶质细胞可以通过下调星形胶质细胞P2Y1嘌呤能受体和形成星形胶质细胞瘢痕来诱导星形胶质细胞分化为A2表型[40]。 CXCL10在脊髓中以低水平表达,但在脊髓缺血再灌注损伤后CXCL10在3 d内以时间依赖的方式持续增加,免疫荧光双染证实CXCL10在小胶质细胞和星形胶质细胞中均表达上调。趋化因子受体CXCR3是CXCL10的主要配体,在不同的细胞上表达激活导致不同的细胞活性。小胶质细胞中CXCR3的表达在脊髓缺血再灌注损伤后12 h开始增加,在48 h更加明显。相比之下,星形胶质细胞上CXCR3表达的增加明显延迟,在脊髓缺血再灌注损伤后48 h才被检测到。CXCR3可能早早期给小胶质细胞提供了兴奋性信号并开始扩散,从而导致星形胶质细胞的晚期激活,证实了脊髓缺血再灌注损伤后小胶质细胞和星形胶质细胞的序贯激活[41]。应激诱导磷蛋白1是一种配体蛋白,可以与IκB竞争,与热休克蛋白A8结合形成复合物。研究证实应激诱导磷蛋白1通过抑制NF-κB信号活性改善脊髓缺血再灌注损伤炎症和氧糖剥夺/再氧合诱导的小胶质细胞炎症,表明应激诱导磷蛋白1通过抑制小胶质细胞介导的炎症来抑制脊髓缺血再灌注损伤。而应激诱导磷蛋白1过表达可以使IκB表达增加和NF-κB信号通路失活,使得活化的星形胶质细胞减少缓解了细胞焦亡[42]。 "

| [1] ALLEN AR. Surgery of experimental lesion of spinal cord equivalent to crush injury of fracture dislocation of spinal column. J Am Med Assoc. 1911;57:878-890. [2] CHIANG J, KOWADA M, AMES A, et al. Cerebral ischemia. III. Vascular changes. Am J Pathol. 1968;52(2):455-476. [3] MCCORD JM. Oxygen- derived free radicals in postischemic tissue injury. N Engl J Med. 1985;312(3):159-163. [4] JING N, FANG B, LI Z, et al. Exogenous activation of cannabinoid-2 receptor modulates TLR4/MMP9 expression in a spinal cord ischemia reperfusion rat model. J Neuroinflammation. 2020;17(1):101. [5] AL MAMUN A, WU Y, MONALISA I, et al. Role of pyroptosis in spinal cord injury and its therapeutic implications. J Adv Res. 2021;28:97-109. [6] MI J, YANG Y, YAO H, et al. Inhibition of heat shock protein family A member 8 attenuates spinal cord ischemia-reperfusion injury via astrocyte NF-κB/NLRP3 inflammasome pathway: HSPA8 inhibition protects spinal ischemia-reperfusion injury. J Neuroinflammation. 2021;18(1):170. [7] GU C, LI L, HUANG Y, et al. Salidroside Ameliorates Mitochondria-Dependent Neuronal Apoptosis after Spinal Cord Ischemia-Reperfusion Injury Partially through Inhibiting Oxidative Stress and Promoting Mitophagy. Oxid Med Cell Longev. 2020;2020:3549704. [8] 陈梦吉,叶佳辉,应一博,等.氧调控性神经生长因子基因修饰神经干细胞移植治疗急性脊髓损伤[J].中华骨科杂志,2020,40(10):669-679. [9] ANWAR MA, AL SHEHABI TS, EID AH. Inflammogenesis of Secondary Spinal Cord Injury. Front Cell Neurosci. 2016;10:98. [10] WU J, SUN L, LI H, et al. Roles of programmed death protein 1/programmed death-ligand 1 in secondary brain injury after intracerebral hemorrhage in rats: selective modulation of microglia polarization to anti-inflammatory phenotype. J Neuroinflammation. 2017;14(1):36. [11] TANG Y, LE W. Differential Roles of M1 and M2 Microglia in Neurodegenerative Diseases. Mol Neurobiol. 2016;53(2):1181-1194. [12] GOGOLEVA VS, DRUTSKAYA MS, ATRETKHANY KS. The Role of Microglia in the Homeostasis of the Central Nervous System and Neuroinflammation. Mol Biol (Mosk). 2019;53(5):790-798. [13] LIU Z, YAO X, JIANG W, et al. Advanced oxidation protein products induce microglia-mediated neuroinflammation via MAPKs-NF-κB signaling pathway and pyroptosis after secondary spinal cord injury. J Neuroinflammation. 2020; 17(1):90. [14] TA NA HS, AN M, ZHANG T, et al. Dexmedetomidine inhibits microglial activation through SNHG14/HMGB1 pathway in spinal cord ischemia-reperfusion injury mice. Int J Neurosci. 2020;1:1-12. [15] CHIU C W, HUANG W H, LIN SJ, et al. The immunomodulator decoy receptor 3 improves locomotor functional recovery after spinal cord injury. J Neuroinflammation. 2016;13(1):154. [16] FU H, ZHAO Y, HU D, et al. Depletion of microglia exacerbates injury and impairs function recovery after spinal cord injury in mice. Cell Death Dis. 2020;11(7):528. [17] BELLVER-LANDETE V, BRETHEAU F, MAILHOT B, et al. Microglia are an essential component of the neuroprotective scar that forms after spinal cord injury. Nat Commun. 2019;10(1):518. [18] CHISTIAKOV DA, MYASOEDOVA VA, REVIN VV, et al. The impact of interferon-regulatory factors to macrophage differentiation and polarization into M1 and M2. Immunobiology. 2018;223(1):101-111. [19] SHAPOURI-MOGHADDAM A, MOHAMMADIAN S, VAZINI H, et al. Macrophage plasticity, polarization, and function in health and disease. J Cell Physiol. 2018; 9(233):6425-6440. [20] ARORA S, DEV K, AGARWAL B, et al. Macrophages: their role, activation and polarization in pulmonary diseases. Immunobiology. 2018;223(4-5):383-396. [21] ATRI C, GUERFALI FZ, LAOUINI D. Role of human macrophage polarization in inflammation during infectious diseases. Int J Mol Sci, 2018,19(6):E1801. [22] LI H, WANG P, TANG L, et al. Distinct Polarization Dynamics of Microglia and Infiltrating Macrophages: A Novel Mechanism of Spinal Cord Ischemia/Reperfusion Injury. J Inflamm Res. 2021;14:5227-5239. [23] ZHOU X, WAHANE S, FRIEDL MS, et al. Microglia and macrophages promote corralling, wound compaction and recovery after spinal cord injury via Plexin-B2.Nat Neurosci. 2020;23(3):337-350. [24] LINNERBAUER M, WHEELER MA, QUINTANA FJ. Astrocyte Crosstalk in CNS Inflammation. Neuron. 2020;108(4):608-622. [25] JHA MK, LEE WH, SUK K. Functional polarization of neuroglia: Implications in neuroinflammation and neurological disorders. Biochem Pharmacol. 2016;103:1-16. [26] IIZUMI T, TAKAHASHI S, MASHIMA K, et al. A possible role of microglia-derived nitric oxide by lipopolysaccharide in activation of astroglial pentose-phosphate pathway via the Keap1/Nrf2 system. J Neuroinflammation. 2016;13(1):99. [27] WANG G, WENG YC, CHIANG IC, et al. Neutralization of Lipocalin-2 Diminishes Stroke-Reperfusion Injury. Int J Mol Sci. 2020;21(17):E6235. [28] SUN L, LI M, MA X, et al. Inhibition of HMGB1 reduces rat spinal cord astrocytic swelling and AQP4 expression after oxygen-glucose deprivation and reoxygenation via TLR4 and NF-κB signaling in an IL-6-dependent manner. J Neuroinflammation. 2017;14(1):231. [29] LI Y N, GAO Z W, LI R, et al. Aquaporin 4 regulation by ginsenoside Rb1 intervenes with oxygen-glucose deprivation/reoxygenation-induced astrocyte injury. Medicine (Baltimore). 2019;98(42):e17591. [30] WANG C, XU Y, HUANG Y, et al. Effects of erythropoietin and methylprednisolone on AQP4 expression in astrocytes. Mol Med Rep. 2017;16(5):5924-5930. [31] VIDAL PM, ULNDREAJ A, BADNER A, et al. Methylprednisolone treatment enhances early recovery following surgical decompression for degenerative cervical myelopathy without compromise to the systemic immune system. J Neuroinflammation. 2018;15(1):222. [32] SIMON FH, ERHART P, VCELAR B, et al. Erythropoietin preconditioning improves clinical and histologic outcome in an acute spinal cord ischemia and reperfusion rabbit model. J Vasc Surg. 2016;64(6):1797-1804. [33] ERYILMAZ F, FAROOQUE U. The Efficacy of Combined Medication With Methylprednisolone and Erythropoietin in the Treatment of Ischemia-Reperfusion Injury to the Spinal Cord in Patients With Cervical Spondylotic Myelopathy. Cureus. 2021;13(3):e14018. [34] GüRER B, KARAKOC A, BEKTAşOğLU PK, et al. Comparative effects of vitamin D and methylprednisolone against ischemia/reperfusion injury of rabbit spinal cords. Eur J Pharmacol. 2017;813:50-60. [35] JHA MK, JO M, KIM JH, et al. Microglia-Astrocyte Crosstalk: An Intimate Molecular Conversation. Neuroscientist. 2019;25(3):227-240. [36] IIZUMI T, TAKAHASHI S, MASHIMA K, et al. A possible role of microglia-derived nitric oxide by lipopolysaccharide in activation of stroglial pentose-phosphate pathway via the Keap1/Nrf2 system. J Neuroinflammation. 2016;13(1):99. [37] LIDDELOW SA, GUTTENPLAN KA, CLARKE LE, et al. Neurotoxic reactive astrocytes are induced by activated microglia. Nature. 2017;541(7638):481-487. [38] TRIPATHI P, RODRIGUEZ-MUELA N, KLIM JR, et al. Reactive Astrocytes Promote ALS-like Degeneration and Intracellular Protein Aggregation in Human Motor Neurons by Disrupting Autophagy through TGF-beta1. Stem Cell Reports. 2017; 9(2):667-680. [39] ANDERSON MA, BURDA JE, REN Y, et al. Astrocyte scar formation aids central nervous system axon regeneration. Nature. 2016;532(7598):195-200. [40] SHINOZAKI Y, SHIBATA K, YOSHIDA K, et al. Transformation of Astrocytes to a Neuroprotective Phenotype by Microglia via P2Y(1) Receptor Downregulation. Cell Rep. 2017;19(6):1151-1164. [41] YU Q, TIAN DL, TIAN Y, et al. Elevation of the Chemokine Pair CXCL10/CXCR3 Initiates Sequential Glial Activation and Crosstalk During the Development of Bimodal Inflammatory Pain after Spinal Cord Ischemia Reperfusion. Cell Physiol Biochem. 2018;49(6):2214-2228. [42] JIN H, GE X, HUAN Z, et al. Stress-induced phosphoprotein 1 restrains spinal cord ischaemia-reperfusion injury by modulating NF-kappaB signalling. J Cell Mol Med. 2021;25(24):11075-11084. |
| [1] | Fang Xingyan, Tian Zhenli, Zhao Zheyi, Wen Ping, Xie Tingting. Effects of sodium arsenite on human umbilical vein endothelial cell injury and sphingosine kinases 1/sphingosine 1-phosphate signaling axis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-7. |
| [2] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [3] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [4] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [5] | Tang Liang, Li Xiheng, Niu Ruijuan, Li Xinyue, Zou Xinying, Mao Tianjiao, Li Jiang. Naringin regulates the function of RAW264.7 macrophages to affect the osteogenic differentiation of MC-3T3-E1 cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1205-1210. |
| [6] | Yang Zhishan, Tang Zhenglong. YAP/TAZ, a core factor of the Hippo signaling pathway, is involved in bone formation [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1264-1271. |
| [7] | Wang Ji, Zhang Min, Yang Zhongya, Zhang Long. A review of physical activity intervention in type 2 diabetes mellitus with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1272-1277. |
| [8] | Nie Chenchen, Su Kaiqi, Gao Jing, Fan Yongfu, Ruan Xiaodi, Yuan Jie, Duan Zhaoyuan, Feng Xiaodong. The regulatory role of circular RNAs in cerebral ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1286-1291. |
| [9] | Liang Jiaqi, Liu Hengxu, Yang Jinxin, Yang Yi, Deng Xuhui, Tan Mingjian, Luo Jiong. Health benefit relationship between exercise and intestinal bacteria [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1292-1299. |
| [10] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [11] | Yang Yitian, Wang Lu, Yao Wei, Zhao Bin. Application of the interaction between biological scaffolds and macrophages in bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1071-1079. |
| [12] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [13] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [14] | Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109. |
| [15] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||