Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (14): 2285-2290.doi: 10.12307/2022.496
Previous Articles Next Articles
Macrophage polarization effectively promotes nerve regeneration after peripheral nerve injury through the M2 phenotypic regulation
Hu Taotao, Chang Shusen, Wei Zairong
- Department of Plastic Surgery, Affiliated Hospital of Zunyi Medical University, Zunyi 563003, Guizhou Province, China
-
Received:2021-03-18Revised:2021-03-20Accepted:2021-05-07Online:2022-05-18Published:2021-12-22 -
Contact:Wei Zairong, MD candidate, Master’s supervisor, Chief physician, Department of Plastic Surgery, Affiliated Hospital of Zunyi Medical University, Zunyi 563003, Guizhou Province, China -
About author:Hu Taotao, Master candidate, Physician, Department of Plastic Surgery, Affiliated Hospital of Zunyi Medical University, Zunyi 563003, Guizhou Province, China -
Supported by:Master’s Startup Fund of the Affiliated Hospital of Zunyi Medical University, No. (2016) 35 (to CSS); Guizhou Provincial Innovation Talent Team for Integrated Surgery of Wounds, No. [2020] 5012 (to WZR)
CLC Number:
Cite this article
Hu Taotao, Chang Shusen, Wei Zairong. Macrophage polarization effectively promotes nerve regeneration after peripheral nerve injury through the M2 phenotypic regulation[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(14): 2285-2290.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
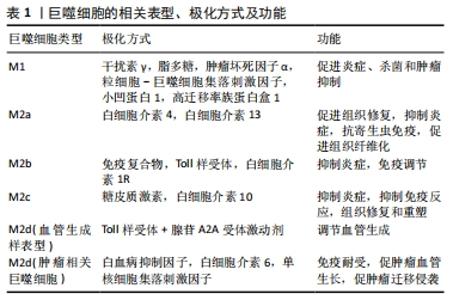
2.1 周围神经中巨噬细胞来源 在神经系统中,巨噬细胞根据其来源的不同可被分为两大类,即常驻巨噬细胞和浸润巨噬细胞,常驻巨噬细胞通常在内环境稳态条件下存在,浸润巨噬细胞响应组织损伤而被激活,浸润相应组织发挥作用[5]。MULLER等[6]使用骨髓嵌合体实验模型发现,坐骨神经损伤后远端神经内膜的常驻巨噬细胞迅速激活,改变其形状,并表达溶酶体巨噬细胞活化抗原ED1,在血源性巨噬细胞流入神经损伤部位之前就快速增殖并最早开始吞噬髓磷脂。该团队的进一步研究发现,通过使用绿色荧光蛋白标记经过血液循环后的神经内巨噬细胞,发现周围神经系统的常驻巨噬细胞大部分来源于血液单核细胞。因此,周围神经损伤后,很可能是神经内膜常驻巨噬细胞最早反应,最后来自循环系统的大量浸润巨噬细胞进入神经损伤部位[7]。虽然常驻巨噬细胞最早识别损伤,开始吞噬髓鞘,但血源性巨噬细胞可能是去除髓磷脂和变性轴突的最主要细胞[8]。因此,神经内膜常驻巨噬细胞可能主要参与周围神经系统的监视,并作为损伤的感受器。由于它们的有利位置,能快速识别损伤,发生反应,可能主要起调节细胞作用,而后来到达的血源性巨噬细胞可能起组织破坏和修复效应细胞的作用。鉴于周围神经内膜常驻巨噬细胞的这种循环补充机制,未来有希望将循环中巨噬细胞作为基因治疗的载体,将其输送到目标神经内膜来治疗相关疾病。但是,目前这些促使常驻巨噬细胞发生循环或是长期驻留的分子机制尚不清楚。值得注意的是,最近一些研究发现,不同组织的周围神经中常驻巨噬细胞也具有不同的亚群,这些常驻巨噬细胞在不同组织进化成不同的亚型可能与神经保护和稳态有关[5]。 2.2 周围神经损伤后巨噬细胞的募集 周围神经损伤后巨噬细胞的及时募集对于神经修复是非常必要的。巨噬细胞的募集需要一些趋化因子或其他信号蛋白的帮助。单核细胞趋化蛋白1 (MCP-1/CCL2)被认为是周围神经损伤后单核细胞/巨噬细胞的主要趋化因子。CCL2可被许多细胞分泌,在神经组织中主要由神经损伤后的许旺细胞产生[9],它能以高亲和力与巨噬细胞表达的受体CCR2结合,产生细胞内信号传导级联的活化,从而产生趋化作用[10]。在敲除CCL2或CCR2基因的小鼠中,坐骨神经损伤后巨噬细胞的募集明显减少,使用阻断CCL2或CCR2功能的抗体也会减少损伤坐骨神经中的巨噬细胞积累[11]。TOFARIS等[12]研究发现许旺细胞条件培养基中趋化性白血病抑制因子的存在,也可在周围神经损伤后募集巨噬细胞。此外,NAMIKAWA等[13]研究发现胰腺炎相关蛋白(PAP-Ⅲ)也能响应神经损伤信号,从损伤神经的许旺细胞释放,作为一种新型巨噬细胞趋化因子募集巨噬细胞,但目前PAP-Ⅲ的具体作用机制仍有待进一步研究。最近,KWON等[14]研究发现,通过直接向第5腰椎背根神经节注射巨噬细胞炎性肽1α(CCL3)也导致背根神经节中的巨噬细胞蓄积。但CCL3是否可以作为一种新型巨噬细胞趋化因子将巨噬细胞募集到背根神经节中仍有待进一步研究。综上所述,周围神经损伤后许旺细胞分泌的CCL2是将血源性巨噬细胞募集到损伤神经的主要因子,但CCL2可能不是将血源性巨噬细胞募集到损伤神经的唯一因子,进一步研究神经损伤后巨噬细胞募集的分子生物学机制将为周围神经损伤治疗提供新的思路。 2.3 巨噬细胞极化成不同表型及极化方式 周围神经损伤后,巨噬细胞会产生不同的表型,发挥不同的功能。根据过去使用的经典Th1/Th2二分法,巨噬细胞可被分为“经典激活”的促炎表型(M1)和“交替激活”的抗炎表型(M2)[15]。M1巨噬细胞主要在促进炎症、杀菌和肿瘤抑制方面有重要作用[16],可被干扰素γ、脂多糖或肿瘤坏死因子α激活[17],此外,其他研究证实粒细胞-巨噬细胞集落刺激因子[18]、小凹蛋白1[19]、高迁移率族蛋白盒1蛋白也可诱导M1极化[20]。M2巨噬细胞通常被认为是一种免疫抑制细胞,可以分泌抑炎因子抑制炎症,促进组织重塑和修复,并在寄生虫清除、免疫调节以及肿瘤血管生成、生长和进展方面具有重要作用[21]。M2巨噬细胞可分为M2a、M2b、M2c、M2d四种类型。M2a型由白细胞介素4或白细胞介素13诱导,主要通过细胞外基质的分泌促进组织修复,也能在抑制炎症反应上发挥作用,可能还参与Th2细胞介导的抗寄生虫免疫反应,促进组织纤维化等[22-23];M2b型可被免疫复合物和Toll样受体或白细胞介素1受体激动剂(IL-1Ra)诱导,主要参与抑制炎症和免疫调节功能;M2c型由糖皮质激素和白细胞介素10诱导,目前研究认为其可参与抑制炎症、抑制免疫反应、组织修复和重塑等功能[23]。关于M2d巨噬细胞,目前有2种不同的定义。FERRANTE等[24-25]研究认为,在Toll样受体激动剂的刺激下,由腺苷A2A受体激动剂诱导促炎性M1产生的一种血管生成表型,以表达高水平的白细胞介素10、诱导型一氧化氮合酶和血管内皮生长因子以及低水平的肿瘤坏死因子α、精氨酸酶1和白细胞介素12为特征,具有调节血管生成和抗炎的作用,因此将这种表型定义为“M2d”。此外,DULUC 等[26]的一项研究发现肿瘤相关巨噬细胞与M2有类似的功能,具有与M2a、M2b、M2c不一样的特性,将其命名为M2d,可在肿瘤微环境中由白血病抑制因子或白细胞介素6与单核细胞集落刺激因子协同作用诱导生成。肿瘤相关巨噬细胞在肿瘤的发生发展中有重要作用,对肿瘤的免疫耐受使其削弱了抗肿瘤免疫疗法的功效,还能促进肿瘤的血管生长和肿瘤的迁移、侵袭[27]。综上所述,不同表型的巨噬细胞具有不同的功能,见表1,鉴于巨噬细胞这种极高的可塑性,通过使巨噬细胞向特定的表型分化来发挥相应的功能可能为周围神经修复提供新的治疗策略。 "


2.4 周围神经损伤后巨噬细胞表型动态变化 在坐骨神经横断后各个时间点通过流式细胞仪对每个巨噬细胞表型标记进行分析,发现在损伤后的所有时间点存在4个带有不同表型标记的巨噬细胞群,包括CD86+/CD206+,CD86+/CD206-,CD86-/CD206+,CD86-/CD206-。CD86也称为B7.2,它提供T细胞活化所必需的共刺激信号,被认为是M1巨噬细胞的细胞表面标记。CD206是与胞吞作用有关的甘露糖受体,它是与M2巨噬细胞特异性相关的标志物。在坐骨神经损伤后第3天,大多数巨噬细胞带有M1表型(CD86+/CD206-)。然而在坐骨神经损伤后第14天此表型优势显著下降,而混合表型(CD86+/CD206+)和M2表型(CD86-/CD206+)增加[28]。此外,NADEAU等[29]使用流式细胞仪和多重免疫荧光标记巨噬细胞发现小鼠坐骨神经损伤后3 h,循环单核细胞即浸润了受损的坐骨神经,M1巨噬细胞在一两天显著增加,在两三天最大浸润,然后在第7天逐渐减少。在第3天,M1巨噬细胞逐渐被M2巨噬细胞替代,这种表型从第3-7天开始一直保持优势。这些数据表明周围神经损伤后首先在损伤部位聚集的是M1巨噬细胞,随后巨噬细胞表型可能在受伤后的前2周内从M1表型逐渐转变为M2表型。 2.5 周围神经损伤后的巨噬细胞功能"


2.5.1 巨噬细胞参与神经损伤后瓦勒变性 周围神经损伤后,远端轴突发生瓦勒变性,及时地清除破碎的髓磷脂和轴突碎片对于神经再生是非常必要的,因为这些来自变性的轴突成分会抑制轴突的再生,巨噬细胞是清除破碎的髓鞘和变性轴突碎片的主要细胞[3]。在小鼠坐骨神经损伤后,用二氧化硅封闭单核细胞可以减少巨噬细胞的浸润,减缓髓鞘的降解[30]。活细胞成像研究还表明,巨噬细胞在轴突碎裂之前很久就到达了损伤部位,轴突碎片可以在斑马鱼模型中被浸润的巨噬细胞所吞噬[31]。除了血源性巨噬细胞的主要作用外,常驻巨噬细胞也参与了瓦勒变性[32]。在神经损伤早期,浸润巨噬细胞进入之前,常驻巨噬细胞就迅速激活,开始增殖和吞噬髓鞘[6]。因此,巨噬细胞在周围神经损伤后的瓦勒变性中起重要作用。但是,NIEMI等[11]敲除Ccr2基因,阻碍神经损伤后巨噬细胞在远端坐骨神经中的蓄积,他们发现这并没有明显抑制髓磷脂的清除。最近,LINDBORG等[33]通过Ccr2-/-小鼠耗竭中性粒细胞发现髓磷脂清除明显受到抑制,证明了中性粒细胞也有清除髓磷脂的作用,确定了巨噬细胞损失后嗜中性粒细胞的补偿作用。此外,GOMEZ-SANCHEZ等[34]研究发现许旺细胞也能通过自噬蛋白促进瓦勒变性期间髓磷脂的清除。 2.5.2 巨噬细胞促进许旺细胞、成纤维细胞迁移和增殖 许旺细胞是周围神经的胶质细胞,是周围神经再生的重要参与者,在神经损伤后独特的去分化,刺激炎症细胞聚集,吞噬破碎的髓磷脂和变性的轴突碎片,参与神经损伤后期的修复再生[35]。巨噬细胞作为促进神经再生的最重要细胞之一,能促进损伤神经的许旺细胞去分化、增殖和迁移[36]。一些巨噬细胞衍生因子也可调节许旺细胞成熟[37]。周围神经横断后,巨噬细胞会进入神经间隙参与神经桥的形成,巨噬细胞主要位于新生神经桥的最外层,表达轴突导向分子Slit3,而位于神经桥内的许旺细胞和成纤维细胞会表达Robo1受体,位于神经桥最外层的巨噬细胞可以利用Slit3-Robo1排斥信号来控制桥内许旺细胞和成纤维细胞迁移的轨迹,从而控制新生轴突的正确延伸[36]。此外,ZHAN等[38]将许旺细胞与M1巨噬细胞或M2巨噬细胞衍生的微泡共同孵育,发现M2巨噬细胞来源微囊泡能显著提高许旺细胞的迁移、增殖、神经生长因子和层粘连蛋白水平,促进轴突生长。miR-223是在微囊泡中表达量最多的miRNA,抑制miR-223可减少与微囊泡共同孵育的许旺细胞的神经生长因子和层粘连蛋白水平,减少许旺细胞的迁移和增殖。将巨噬细胞衍生的微囊泡添加到幼稚的单核细胞时可诱导巨噬细胞分化、成熟,说明巨噬细胞可能通过衍生的微囊泡促进自身的分化、成熟来增强免疫功能,这可能受其表达的miR-223信号分子调控[39]。 2.5.3 巨噬细胞促进损伤神经的血管再生 周围神经横断后,在近端和远端神经之间会形成新的神经桥组织,再生轴突可以使新形成的神经桥穿越神经间隙,尽管新生的神经桥中包含多种细胞类型,但只有巨噬细胞可以感知低氧并通过激活缺氧诱导因子1α来应答低氧条件[36],而缺氧诱导因子1α最终通过血管内皮生长因子激活刺激血管生成[40]。巨噬细胞促进血管生成,而新生的血管内皮细胞可以引导许旺细胞正确迁移,从而促进神经修复和再生[36]。周围神经损伤后,巨噬细胞还能自分泌血管内皮生长因子A来促进血管生成[41]。此外,一些研究发现,巨噬细胞的其他亚型也能通过分泌血管内皮生长因子促进血管生成从而促进周围神经再生。例如GAO 等[42]发现M1、M2巨噬细胞均能响应缺血信号,增殖并高分泌血管内皮生长因子促进小鼠视网膜新生血管生成,且M1和M2巨噬细胞均比M0巨噬细胞分泌更多的血管内皮生长因子。M2d可以分泌高水平的白细胞介素10和血管内皮生长因子来促进血管生成和血管修复[25],白细胞介素4诱导的M2a巨噬细胞和白细胞介素10诱导的M2c巨噬细胞在体内和体外都能促进血管生成。SPILLER等[43-44]在体外分析了M0、M1、M2a和M2c巨噬细胞中血管生成的基因表达和蛋白分泌谱,血管网的生长经历了萌芽、吻合和成熟过程,M1分泌血管内皮生长因子促进血管的萌芽;M2a分泌参与后期阶段的因子,特别是血小板衍生生长因子BB,促进吻合;M2c分泌高水平的基质金属蛋白酶9,参与血管重塑。深入研究巨噬细胞各个亚型在周围神经的血管生成特性,并利用这些特性来控制血管再生将有助于周围神经更好的修复。 2.6 巨噬细胞极化治疗周围神经损伤 "


在周围神经再生过程中,M1巨噬细胞主要参与早期的瓦勒变性,M2巨噬细胞主要参与后期的神经再生过程。如前所述,抑制巨噬细胞在神经损伤部位聚集,并不会明显抑制髓磷脂和轴突碎片的清除,因为中性粒细胞和许旺细胞也会参与这一过程。此外,M1巨噬细胞可能具有一定神经毒性,释放的活性氧、蛋白水解酶、一氧化氮等都可能杀死神经元,相比之下,M2巨噬细胞无神经毒性,且具有强大的促轴突生长作用[45]。SHIMADA等[46]采用慢性压迫性损伤小鼠模型,测定其后肢肌肉质量和总骨密度,巨噬细胞耗竭组和药物抑制M1巨噬细胞组巨噬细胞浸润减少,肌肉质量和总骨密度明显高于未处理组。M1巨噬细胞浸润加剧了周围神经损伤后的肌肉/骨萎缩,通过抑制神经损伤局部的M1巨噬细胞,可以避免肌肉/骨萎缩。此外,在神经导管内添加干扰素γ或白细胞介素4分别诱导M1表型和M2表型,M2表型的诱导明显促进了大鼠坐骨神经长间隙缺损模型中许旺细胞浸润和轴突生长。M1/M2的比例与神经支架远端轴突再生的数量呈线性关系,提示M2的特殊表型优势比巨噬细胞存在的数量能更好地调节周围神经再生[47]。综上所述,与其抑制免疫反应来抑制其毒性作用,不如将巨噬细胞表型更多地极化成抗炎表型,可能是促进周围神经修复更好的治疗策略,周围神经损伤通过诱导巨噬细胞M2表型,触发了一个内在的抗炎的促进组织修复的保护环境。因此,将巨噬细胞更多地极化成M2表型可能是一种重要的治疗周围神经损伤的策略。接下来,将讨论将这种方法作为周围神经损伤治疗靶点的应用进展。 2.6.1 干细胞刺激巨噬细胞极化促进神经再生 牙髓干细胞是一种从牙髓组织中分离出的成纤维状细胞,可通过促进巨噬细胞向M2型极化来促进神经再生,将牙髓干细胞移植到糖尿病大鼠坐骨神经,牙髓干细胞可通过表达白细胞介素10、单核细胞集落刺激因子等M2诱导因子诱导巨噬细胞极化成M2表型,抑制神经局部炎症,恢复神经传导速度、神经血流量和轴突形态[48]。在KANO等[49]的一项研究中显示,移植的牙髓干细胞促进了大鼠周围神经再生,可能是通过其分泌的免疫调节因子MCP-1/Siglec-9刺激了M2巨噬细胞的极化。体外实验也证明MCP-1/Siglec-9增强了许旺细胞的增殖、迁移、分化、血管形成和神经纤维生长。LI等[50]使用由表皮神经嵴干细胞、细胞外基质和聚丙交酯-共-乙交酯(PLGA)组成的人工神经桥接大鼠10 mm坐骨神经缺损,表皮神经嵴干细胞可以显著改变促炎和抗炎细胞因子的表达水平,促进巨噬细胞从M1向M2的极化,调节并提供更合适的炎症微环境,以修复坐骨神经缺损。此外,间充质干细胞也能促进巨噬细胞极化,HOU等[51]通过将骨髓间充质干细胞与巨噬细胞共培养,发现骨髓间充质干细胞可通过释放旁分泌因子抑制脂多糖+干扰素γ诱导的对M1巨噬细胞的极化,并促进对M2巨噬细胞的极化。YIN等[52]将脂肪间充质干细胞和巨噬细胞共培养,发现也能促进巨噬细胞从M1表型极化成M2表型。 2.6.2 信号分子刺激巨噬细胞极化促进神经再生 信号分子是指用来在细胞间和细胞内传递信息的物质,它们能与细胞受体,如激素、局部介质、神经递质等结合,通过激活或灭活特定的信号通路来传递信息,包括细胞因子、生长因子、一些肽类、核苷酸的集合。通过向神经损伤部位传递信号分子,使巨噬细胞极化成M2表型有利于神经的再生,而添加这种信号分子的途径多种多样,例如直接注射到神经损伤部位、从植入的支架中释放、添加到聚合神经导管内,甚至从已经植入的细胞中分泌[47,53]。MOKARRAM等[47]在聚合神经引导通道内局部传递干扰素γ或白细胞介素4 调节损伤神经局部巨噬细胞表型,发现巨噬细胞对M2a和M2c表型的极化明显促进了大鼠坐骨神经间隙模型(15 mm)中许旺细胞浸润和轴突生长。相反,对M1巨噬细胞的极化延缓了轴突生长。POTAS等[54]通过将白细胞介素10吸附并结合在电纺聚ε-己内酯纳米纤维支架上,证实白细胞介素10结合的纳米纤维成功诱导了M2巨噬细胞的极化,并显著促进了轴突生长。血栓调节蛋白是一种包含5个结构域的跨膜糖蛋白,血栓调节蛋白的凝集素样结构域具有抑制炎症反应的能力,HUANG等[55]研究发现经血栓调节蛋白处理的M1巨噬细胞可极化成M2表型,并在大鼠坐骨神经横断模型中也证实了血栓调节蛋白治疗后许旺细胞数量和轴突密度增加,髓鞘形成和神经功能恢复增强。 2.6.3 细胞外基质刺激巨噬细胞极化促进神经再生 细胞外基质是由细胞合成并分泌的生物大分子(如原纤维蛋白、蛋白聚糖、糖胺聚糖和糖蛋白等)在细胞表面或细胞之间形成的三维高分子网络结构[56]。在周围神经系统中,细胞外基质存在于神经内膜和基底膜,围绕轴突-许旺细胞单位排列,主要由层粘连蛋白、纤维连接蛋白、Ⅰ型和Ⅵ型胶原组成[57]。最近,CHEN等[58]通过体外实验和体内实验均证实Ⅵ型胶原可通过促进巨噬细胞聚集和M2型巨噬细胞极化来促进小鼠坐骨神经再生,他们发现Ⅵ型胶原基因缺陷的小鼠损伤神经中的巨噬细胞迁移能力受损,M2型巨噬细胞极化降低,损伤神经再生延迟。消融Ⅵ型胶原可完全抑制受损坐骨神经中AKT和PKA信号通路的激活。体外研究表明,Ⅵ型胶原通过AKT和PKA信号途径促进巨噬细胞迁移和极化。同样,LV等[59]通过将Ⅵ型胶原包裹在RADA16-Ⅰ水凝胶中,与聚ε-己内酯导管组成复合系统来修复大鼠15 mm长坐骨神经缺损,构建了Ⅵ型胶原在神经损伤部位的持续释放模型,再次证明了Ⅵ型胶原能显著促进巨噬细胞募集,使巨噬细胞向M2表型极化,促进神经再生和功能恢复。未来,这种将生物材料与免疫调节结合的复合系统可能成为周围神经再生中很有前途的治疗策略。 2.6.4 电刺激使巨噬细胞极化促进神经再生 过去的一些研究发现在神经修复过程中进行一次短暂的神经电刺激,强度为20 Hz,1 h,可以增强运动、感觉轴突的再生和再髓鞘形成[60-61]。最近,MCLEAN等[62]局部注射1%溶血磷脂酰胆碱于大鼠胫神经周围使其脱髓鞘,5 d后在溶血磷脂酰胆碱注射部位近端接受强度为1 h 20 Hz的神经电刺激,他们发现神经电刺激可以将巨噬细胞的表型从M1表型转变为M2表型。该研究首次证明通过神经电刺激使神经元活性的短暂增加可以诱导巨噬细胞向M2表型极化。神经电刺激还影响趋化因子CCL2的表达,可以诱导巨噬细胞的聚集。这些研究数据表明,在周围神经修复过程中,短暂的局部神经电刺激可以使神经病变处微环境中巨噬细胞迅速极化为促进修复的M2表型,有利于促进轴突和髓鞘再生,这是一个新的有前景的治疗措施,未来也有可能会用于其他与巨噬细胞极化相关疾病的治疗中。 2.6.5 药物刺激巨噬细胞极化促进神经再生 咪康唑是一种常用于治疗皮肤或阴道真菌感染的药物,目前应用十分广泛,是临床上用于抗真菌的重要药物。在以前的研究中,咪康唑只被证实用于真菌感染。然而,最近研究报道咪康唑能促进脊髓损伤的髓鞘形成[63]。ZHANG等[64]建立小鼠周围神经卡压模型,通过PCR分析、Western blot和荧光免疫组织化学进一步研究了咪康唑在周围神经再生中的潜在作用机制,发现咪康唑可能通过核因子κB途径调节巨噬细胞更多极化成M2表型,从而抑制炎症反应,促进周围神经再生。未来咪康唑可能作为治疗周围神经挤压伤的另一种潜在的治疗方案,但关于其作用机制应进一步探究。 2.6.6 生物材料刺激巨噬细胞极化促进神经再生 目前,修复长神经缺损的“金标准”是自体神经移植,但有供体神经发病率、神经组织大小差异、神经瘤形成和低利用率等局限性[65]。目前最有希望能够代替自体神经移植的是神经引导导管[66]。最近的研究集中于不断优化神经引导导管的表面特性以调节细胞的黏附、表型和其他生物学行为从而更好地促进神经再生[67]。SAINO等[68]证明了巨噬细胞的不同表型可以被不同直径的纳米纤维改变,发现炎症反应随着纳米纤维直径减小而减轻。巨噬细胞的表型也可以通过表面沟槽或其他纳米图形直接调节[69]。此外,其他的体内研究也表明,将巨噬细胞的表型更多极化成M2,促进了周围神经再生[70]。纳米纤维是一种降解速率快和力学性能可控的生物材料,最近在神经再生领域研究越来越多,JIA等[71]通过建立小鼠坐骨神经横断模型,利用不同形态的纳米纤维构建神经引导导管,将巨噬细胞接种在这种纳米纤维上,他们发现排列整齐的纳米纤维支架可以诱导巨噬细胞极化为M2表型,促进了许旺细胞的增殖和迁移,显著促进了周围神经再生。DONG等[72]利用纳米纤维鞘和排列整齐的微纤维芯组成的新型神经导管桥接大鼠坐骨神经缺损,研究发现排列整齐的微纤维芯可通过促进巨噬细胞募集和向M2表型极化来促进神经再生,导管植入后3个月,大鼠电生理功能增强,坐骨神经功能指数得到改善,肌肉萎缩得到缓解。未来,纳米纤维支架会被更多地应用到神经引导导管的设计中。然而,更好地优化这种生物材料的所有特性,使其募集、激活促愈合表型巨噬细胞,并且能减少移植物的排斥作用是未来的挑战。如生物材料的不同特性(硬度、形貌、孔径和表面化学)可以诱导不同的巨噬细胞行为[73]。"

| [1] TRICAUD N, PARK HT. Wallerian demyelination: chronicle of a cellular cataclysm. Cell Mol Life Sci. 2017;74(22):4049-4057. [2] FOURNIER AE, STRITTMATTER SM. Repulsive factors and axon regeneration in the CNS. Curr Opin Neurobiol. 2001;11(1):89-94. [3] BOISSONNAS A, LOUBOUTIN F, LAVIRON M, et al. Imaging resident and recruited macrophage contribution to Wallerian degeneration. J Exp Med. 2020;217(11):e20200471. [4] GORDON S, PLÜDDEMANN A, MARTINEZ ESTRADA F. Macrophage heterogeneity in tissues: phenotypic diversity and functions. Immunol Rev. 2014;262(1):36-55. [5] KOLTER J, KIERDORF K, HENNEKE P. Origin and Differentiation of Nerve-Associated Macrophages. J Immunol. 2020;204(2):271-279. [6] MUELLER M, WACKER K, RINGELSTEIN EB, et al. Rapid response of identified resident endoneurial macrophages to nerve injury. Am J Pathol. 2001;159(6): 2187-2197. [7] MÜLLER M, LEONHARD C, KRAUTHAUSEN M, et al. On the longevity of resident endoneurial macrophages in the peripheral nervous system: a study of physiological macrophage turnover in bone marrow chimeric mice. J Peripher Nerv Syst. 2010;15(4):357-365. [8] TASKINEN HS, RöYTTä M. The dynamics of macrophage recruitment after nerve transection. Acta Neuropathol. 1997;93(3):252-259. [9] BAKST RL, XIONG H, CHEN CH, et al. Inflammatory Monocytes Promote Perineural Invasion via CCL2-Mediated Recruitment and Cathepsin B Expression. Cancer Res. 2017;77(22):6400-6414. [10] WANG ZM, GAO W, WANG H, et al. Green tea polyphenol epigallocatechin-3-gallate inhibits TNF-α-induced production of monocyte chemoattractant protein-1 in human umbilical vein endothelial cells. Cell Physiol Biochem. 2014;33(5): 1349-1358. [11] NIEMI JP, DEFRANCESCO-LISOWITZ A, ROLDÁN-HERNÁNDEZ L, et al. A critical role for macrophages near axotomized neuronal cell bodies in stimulating nerve regeneration. J Neurosci. 2013;33(41):16236-16248. [12] TOFARIS GK, PATTERSON PH, JESSEN KR, et al. Denervated Schwann cells attract macrophages by secretion of leukemia inhibitory factor (LIF) and monocyte chemoattractant protein-1 in a process regulated by interleukin-6 and LIF. J Neurosci. 2002;22(15):6696-6703. [13] NAMIKAWA K, OKAMOTO T, SUZUKI A, et al. Pancreatitis-associated protein-III is a novel macrophage chemoattractant implicated in nerve regeneration. J Neurosci. 2006;26(28):7460-7467. [14] KWON MJ, SHIN H Y, CUI Y, et al. CCL2 Mediates Neuron-Macrophage Interactions to Drive Proregenerative Macrophage Activation Following Preconditioning Injury. J Neurosci. 2015;35(48):15934-15947. [15] 唐俭,陈旭昕,韩志海.巨噬细胞极化及极化调控的研究进展[J].转化医学杂志,2019,8(6):373-376. [16] YUNNA C, MENGRU H, LEI W, et al. Macrophage M1/M2 polarization. Eur J Pharmacol. 2020;877:173090. [17] MOSSER DM. The many faces of macrophage activation. J Leukoc Biol. 2003; 73(2):209-212. [18] VERRECK FA, DE BOER T, LANGENBERG DM, et al. Human IL-23-producing type 1 macrophages promote but IL-10-producing type 2 macrophages subvert immunity to (myco)bacteria. Proc Natl Acad Sci U S A. 2004;101(13): 4560-4565. [19] SHIVSHANKAR P, HALADE GV, CALHOUN C, et al. Caveolin-1 deletion exacerbates cardiac interstitial fibrosis by promoting M2 macrophage activation in mice after myocardial infarction. J Mol Cell Cardiol. 2014;76: 84-93. [20] TIAN S, ZHANG L, TANG J, et al. HMGB1 exacerbates renal tubulointerstitial fibrosis through facilitating M1 macrophage phenotype at the early stage of obstructive injury. Am J Physiol Renal Physiol. 2015;308(1):F69-75. [21] CHEN P, BONALDO P. Role of macrophage polarization in tumor angiogenesis and vessel normalization: implications for new anticancer therapies. Int Rev Cell Mol Biol. 2013;301:1-35. [22] MOSSER DM, EDWARDS JP. Exploring the full spectrum of macrophage activation. Nat Rev Immunol. 2008;8(12):958-969. [23] MaNTOVANI A, SICA A, SOZZANI S, et al. The chemokine system in diverse forms of macrophage activation and polarization. Trends Immunol. 2004; 25(12):677-686. [24] FERRANTE CJ, PINHAL-ENFIELD G, ELSON G, et al. The adenosine-dependent angiogenic switch of macrophages to an M2-like phenotype is independent of interleukin-4 receptor alpha (IL-4Rα) signaling. Inflammation. 2013;36(4): 921-931. [25] FERRANTE CJ, LEIBOVICH SJ. Regulation of Macrophage Polarization and Wound Healing. Adv Wound Care (New Rochelle). 2012;1(1):10-16. [26] DULUC D, DELNESTE Y, TAN F, et al. Tumor-associated leukemia inhibitory factor and IL-6 skew monocyte differentiation into tumor-associated macrophage-like cells. Blood. 2007;110(13):4319-4330. [27] 吴从严,楼美清,贾玉,等.肿瘤相关巨噬细胞研究进展[J].现代肿瘤医学,2020,28(3):508-512. [28] LEE S, SHI XQ, FAN A, et al. Targeting macrophage and microglia activation with colony stimulating factor 1 receptor inhibitor is an effective strategy to treat injury-triggered neuropathic pain. Mol Pain. 2018;14: 1744806918764979. [29] NADEAU S, FILALI M, ZHANG J, et al. Functional recovery after peripheral nerve injury is dependent on the pro-inflammatory cytokines IL-1β and TNF: implications for neuropathic pain. J Neurosci. 2011;31(35):12533-12542. [30] BEUCHE W, FRIEDE RL. Myelin phagocytosis in Wallerian degeneration of peripheral nerves depends on silica-sensitive, bg/bg-negative and Fc-positive monocytes. Brain Res. 1986;378(1):97-106. [31] ROSENBERG AF, WOLMAN MA, FRANZINI-ARMSTRONG C, et al. In vivo nerve-macrophage interactions following peripheral nerve injury. J Neurosci. 2012;32(11):3898-3909. [32] DEFRANCESCO-LISOWITZ A, LINDBORG JA, NIEMI JP, et al. The neuroimmunology of degeneration and regeneration in the peripheral nervous system. Neuroscience. 2015;302:174-203. [33] LINDBORG JA, MACK M, ZIGMOND RE. Neutrophils Are Critical for Myelin Removal in a Peripheral Nerve Injury Model of Wallerian Degeneration. J Neurosci. 2017;37(43):10258-10277. [34] GOMEZ-SANCHEZ JA, CARTY L, IRUARRIZAGA-LEJARRETA M, et al. Schwann cell autophagy, myelinophagy, initiates myelin clearance from injured nerves. J Cell Biol. 2015;210(1):153-168. [35] MIRFEIZI L, STRATTON JA, KUMAR R, et al. Serum-free bioprocessing of adult human and rodent skin-derived Schwann cells: implications for cell therapy in nervous system injury. J Tissue Eng Regen Med. 2017;11(12):3385-3397. [36] CATTIN AL, BURDEN JJ, VAN EMMENIS L, et al. Macrophage-Induced Blood Vessels Guide Schwann Cell-Mediated Regeneration of Peripheral Nerves. Cell. 2015;162(5):1127-1139. [37] STRATTON JA, HOLMES A, ROSIN NL, et al. Macrophages Regulate Schwann Cell Maturation after Nerve Injury. Cell Rep. 2018;24(10):2561-2572.e6. [38] ZHAN C, MA CB, YUAN HM, et al. Macrophage-derived microvesicles promote proliferation and migration of Schwann cell on peripheral nerve repair. Biochem Biophys Res Commun. 2015;468(1-2):343-348. [39] ISMAIL N, WANG Y, DAKHLALLAH D, et al. Macrophage microvesicles induce macrophage differentiation and miR-223 transfer. Blood. 2013;121(6):984-995. [40] TAMURA R, TANAKA T, AKASAKI Y, et al. The role of vascular endothelial growth factor in the hypoxic and immunosuppressive tumor microenvironment: perspectives for therapeutic implications. Med Oncol. 2019;37(1):2. [41] LU CY, SANTOSA KB, JABLONKA-SHARIFF A, et al. Macrophage-Derived Vascular Endothelial Growth Factor-A Is Integral to Neuromuscular Junction Reinnervation after Nerve Injury. J Neurosci. 2020;40(50): 9602-9616. [42] GAO X, WANG YS, LI XQ, et al. Macrophages promote vasculogenesis of retinal neovascularization in an oxygen-induced retinopathy model in mice. Cell Tissue Res. 2016;364(3):599-610. [43] SPILLER KL, ANFANG RR, SPILLER KJ, et al. The role of macrophage phenotype in vascularization of tissue engineering scaffolds. Biomaterials. 2014; 35(15):4477-4488. [44] HERBERT SP, STAINIER DY. Molecular control of endothelial cell behaviour during blood vessel morphogenesis. Nat Rev Mol Cell Biol. 2011;12(9):551-564. [45] KIGERL KA, GENSEL JC, ANKENY DP, et al. Identification of two distinct macrophage subsets with divergent effects causing either neurotoxicity or regeneration in the injured mouse spinal cord. J Neurosci. 2009;29(43): 13435-13444. [46] SHIMADA N, SAKATA A, IGARASHI T, et al. M1 macrophage infiltration exacerbate muscle/bone atrophy after peripheral nerve injury. BMC Musculoskelet Disord. 2020;21(1):44. [47] MOKARRAM N, MERCHANT A, MUKHATYAR V, et al. Effect of modulating macrophage phenotype on peripheral nerve repair. Biomaterials. 2012; 33(34):8793-8801. [48] OMI M, HATA M, NAKAMURA N, et al. Transplantation of dental pulp stem cells suppressed inflammation in sciatic nerves by promoting macrophage polarization towards anti-inflammation phenotypes and ameliorated diabetic polyneuropathy. J Diabetes Investig. 2016;7(4):485-496. [49] KANO F, MATSUBARA K, UEDA M, et al. Secreted Ectodomain of Sialic Acid-Binding Ig-Like Lectin-9 and Monocyte Chemoattractant Protein-1 Synergistically Regenerate Transected Rat Peripheral Nerves by Altering Macrophage Polarity. Stem Cells. 2017;35(3):641-653. [50] LI Y, YAO D, ZHANG J, et al. The Effects of Epidermal Neural Crest Stem Cells on Local Inflammation Microenvironment in the Defected Sciatic Nerve of Rats. Front Mol Neurosci. 2017;10:133. [51] HOU Y, ZHOU X, CAI WL, et al. Regulatory effect of bone marrow mesenchymal stem cells on polarization of macrophages. Zhonghua Gan Zang Bing Za Zhi. 2017;25(4):273-278. [52] YIN X, PANG C, BAI L, et al. Adipose-derived stem cells promote the polarization from M1 macrophages to M2 macrophages. Xi Bao Yu Fen Zi Mian Yi Xue Za Zhi. 2016;32(3):332-338. [53] ALVAREZ MM, LIU J C, TRUJILLO-DE SANTIAGO G, et al. Delivery strategies to control inflammatory response: Modulating M1-M2 polarization in tissue engineering applications. J Control Release. 2016;240:349-363. [54] POTAS JR, HAQUE F, MACLEAN FL, et al. Interleukin-10 conjugated electrospun polycaprolactone (PCL) nanofibre scaffolds for promoting alternatively activated (M2) macrophages around the peripheral nerve in vivo. J Immunol Methods. 2015;420:38-49. [55] HUANG TC, WU HL, CHEN SH, et al. Thrombomodulin facilitates peripheral nerve regeneration through regulating M1/M2 switching. J Neuroinflammation. 2020;17(1):240. [56] 罗雅馨,毕浩然,陈晓旭,等.细胞外基质与组织的再生与修复[J].中国组织工程研究,2021,25(11):1785-1790. [57] BYRON A, HUMPHRIES JD, HUMPHRIES MJ. Defining the extracellular matrix using proteomics. Int J Exp Pathol. 2013;94(2):75-92. [58] CHEN P, CESCON M, ZUCCOLOTTO G, et al. Collagen VI regulates peripheral nerve regeneration by modulating macrophage recruitment and polarization. Acta Neuropathol. 2015;129(1):97-113. [59] LV D, ZHOU L, ZHENG X, et al. Sustained release of collagen VI potentiates sciatic nerve regeneration by modulating macrophage phenotype. Eur J Neurosci. 2017;45(10):1258-1267. [60] AL-MAJED AA, NEUMANN CM, BRUSHART TM, et al. Brief electrical stimulation promotes the speed and accuracy of motor axonal regeneration. J Neurosci. 2000;20(7):2602-2608. [61] SINGH B, XU QG, FRANZ CK, et al. Accelerated axon outgrowth, guidance, and target reinnervation across nerve transection gaps following a brief electrical stimulation paradigm. J Neurosurg. 2012;116(3):498-512. [62] MCLEAN NA, VERGE VM. Dynamic impact of brief electrical nerve stimulation on the neural immune axis-polarization of macrophages toward a pro-repair phenotype in demyelinated peripheral nerve. Glia. 2016;64(9): 1546-1561. [63] CULLY M. Neurodegenerative diseases: Repurposing for remyelination. Nat Rev Drug Discov. 2015;14(6):383. [64] ZHANG L, CHEN X, LIU Z, et al. Miconazole alleviates peripheral nerve crush injury by mediating a macrophage phenotype change through the NF-κB pathway. Brain Behav. 2019;9(10):1400. [65] 李兵仓.周围神经损伤的外科学处理[J].创伤外科杂志,2020,22(11): 864-869. [66] GU X, DING F, WILLIAMS DF. Neural tissue engineering options for peripheral nerve regeneration. Biomaterials. 2014;35(24):6143-6156. [67] SIMITZI C, RANELLA A, STRATAKIS E. Controlling the morphology and outgrowth of nerve and neuroglial cells: The effect of surface topography. Acta Biomater. 2017;51:21-52. [68] SAINO E, FOCARETE ML, GUALANDI C, et al. Effect of electrospun fiber diameter and alignment on macrophage activation and secretion of proinflammatory cytokines and chemokines. Biomacromolecules. 2011;12(5):1900-1911. [69] LUU TU, GOTT SC, WOO BW, et al. Micro- and Nanopatterned Topographical Cues for Regulating Macrophage Cell Shape and Phenotype. ACS Appl Mater Interfaces. 2015;7(51):28665-28672. [70] PELUFFO H, SOLARI-SAQUIERES P, NEGRO-DEMONTEL ML, et al. CD300f immunoreceptor contributes to peripheral nerve regeneration by the modulation of macrophage inflammatory phenotype. J Neuroinflammation. 2015;12:145. [71] JIA Y, YANG W, ZHANG K, et al. Nanofiber arrangement regulates peripheral nerve regeneration through differential modulation of macrophage phenotypes. Acta Biomater. 2019;83:291-301. [72] DONG X, LIU S, YANG Y, et al. Aligned microfiber-induced macrophage polarization to guide schwann-cell-enabled peripheral nerve regeneration. Biomaterials.2021;272:120767. [73] SRIDHARAN R, CAMERON AR, KELLY DJ, et al. Biomaterial based modulation of macrophage polarization: a review and suggested design principles. Materials Today. 2015;18(6):313-325. |
| [1] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhou Qian, Zhang Qiang, Chen Qiu. Human salivary components and osteoporosis/osteopenia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1439-1444. |
| [2] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| [3] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| [4] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [5] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [6] | Kong Yamin, Yan Juntao, Ma Bingxiang, Li Huawei. Massage vibration intervenes with MyoD expression and proliferation and differentiation of muscle satellite cells in rats with sciatic nerve injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1160-1166. |
| [7] | Guo Jia, Ding Qionghua, Liu Ze, Lü Siyi, Zhou Quancheng, Gao Yuhua, Bai Chunyu. Biological characteristics and immunoregulation of exosomes derived from mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1093-1101. |
| [8] | Wu Weiyue, Guo Xiaodong, Bao Chongyun. Application of engineered exosomes in bone repair and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1102-1106. |
| [9] | Zhou Hongqin, Wu Dandan, Yang Kun, Liu Qi. Exosomes that deliver specific miRNAs can regulate osteogenesis and promote angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1107-1112. |
| [10] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [11] | Huang Chenwei, Fei Yankang, Zhu Mengmei, Li Penghao, Yu Bing. Important role of glutathione in stemness and regulation of stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1119-1124. |
| [12] | Hui Xiaoshan, Bai Jing, Zhou Siyuan, Wang Jie, Zhang Jinsheng, He Qingyong, Meng Peipei. Theoretical mechanism of traditional Chinese medicine theory on stem cell induced differentiation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1125-1129. |
| [13] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [14] | Fan Yiming, Liu Fangyu, Zhang Hongyu, Li Shuai, Wang Yansong. Serial questions about endogenous neural stem cell response in the ependymal zone after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1137-1142. |
| [15] | Tian Chuan, Zhu Xiangqing, Yang Zailing, Yan Donghai, Li Ye, Wang Yanying, Yang Yukun, He Jie, Lü Guanke, Cai Xuemin, Shu Liping, He Zhixu, Pan Xinghua. Bone marrow mesenchymal stem cells regulate ovarian aging in macaques [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 985-991. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||