Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (30): 4906-4912.doi: 10.3969/j.issn.2095-4344.0992
Previous Articles Next Articles
Review on three-dimensional printing in the biomedical field
Ju Er-nan1, 2, Wu Li2, Li Xin-xin2, Guan Tian-min2, Chen Yong2, Du Yu-huan1
- 1School of Intelligence & Electronic Engineering, Dalian Neusoft University of Information, Dalian 116028, Liaoning Province, China; 2Institute of Mechanical Engineering, Dalian Jiaotong University, Dalian 116028, Liaoning Province, China
-
Received:2018-06-03Online:2018-10-28Published:2018-10-28 -
Contact:Wu Li, PhD, Associate professor, Institute of Mechanical Engineering, Dalian Jiaotong University, Dalian 116028, Liaoning Province, China -
About author:Ju Er-nan, Master, School of Intelligence & Electronic Engineering, Dalian Neusoft University of Information, Dalian 116028, Liaoning Province, China; Institute of Mechanical Engineering, Dalian Jiaotong University, Dalian 116028, Liaoning Province, China -
Supported by:the Project of Liaoning Provincial Education Department, No. JDL2017026; the Open Fund Project for Key Laboratories at Provincial and Ministerial Levels, No. 2016IRS05
CLC Number:
Cite this article
Ju Er-nan, Wu Li, Li Xin-xin, Guan Tian-min, Chen Yong, Du Yu-huan. Review on three-dimensional printing in the biomedical field[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(30): 4906-4912.
share this article

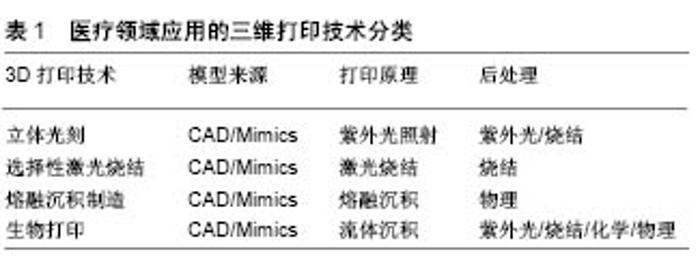
2.1.1 立体光刻技术 立体光刻被认为是第一快速原型制作工艺,并在20世纪80年代后期开发使用[5]。最初的立体光刻在2D模式下通过光栅空间控制HeCd激光对树脂进行聚合[6]。光被投射到容纳液体树脂的平台上,每层固化后,平台降低,附着在平台上的固化结构随之降低,进入储料仓里;未固化的液态树脂散布在顶部,继续下一层图形的固化,其工作空间如图1所示[7]。通过逐层打印完成结构体,排液去除未聚合的液体树脂,取出打印结构体,置于UV烘箱中的固化未反应的基团并强化零件[8]。最后,对结构体去除支撑结构,完成最终打印。目前,由于激光束运动速度较慢,对于大结构体来说成型速率较慢,所以开发遮光技术用来一次固化整层聚合物,提高打印效率。在立体光刻中,应用的材料必须有可交联的光敏基团,目前应用的典型材料包括丙烯酸树脂和环氧树脂。在光聚合的过程中,由于具有生物降解和生物相容向的生物材料较少,所以立体光刻在医疗上应用主要包括制造用于手术规划的解剖模型,以及通过使用立体光刻模型间接制造医疗辅助设备[9-10]。立体光刻的优点是能够打印具有内部结构的复杂性状,而且易于清除未聚合树脂以及分辨率高[11];缺点主要是缺乏与立体光刻打印特性相适应的生物相容性树脂。 2.1.2 选区激光烧结技术 选择性激光烧结由Texas大学在1989年开发的。激光以特定的2D图案扫描粉末状聚合物颗粒的表面,将它们加热至高于玻璃化转变温度来进行烧结。在烧结过程中,分子沿着颗粒的最外表面扩散形成相邻颗粒,在完成一层创建后,包含零件的工作平台降低,一层新的粉末材料滚过顶部表面,随后相与前一层材料结合,其工作空间如图2所示。当部件逐层打印完成后,将未结合的松散粉末去除,进行热处理(以达到粉末颗粒完全结合)及表面处理,提高性能。与立体光刻不同,选择性激光烧结不需要临时支持结构,因为未烧结的固体粉末可支持任何悬臂结构。由于烧结不会使粉末颗粒的完全熔融,因此原始颗粒之间的孔隙可保存。选择性激光烧结有一系列材料可供选择,可以是纯净物或混合物材料,但是纯净物比混合物方便操作,常用的材料有钛粉,不锈钢粉,镁粉,铝粉,聚己内酯和羟基磷灰石[12],聚己内酯和β-磷酸钙[13],Ca-P/PHBV和聚乙烯醇等[14-15]。选择性激光烧结的关键优势是能够直接制造金属植入物,促进骨向内生长和再生,具有高断裂韧性和机械强度,主要缺点是只有少量在激光束下融合而不分解的材料,而且需要移除未固化的粉末。 2.1.3 熔融沉积制造 熔融沉积成型是通过两个含有小孔的加热头,以特定的方式挤出沉积熔融热塑性材 料[16]。一个喷嘴沉积热塑性材料,另一个喷嘴沉积临时材料,用来作为支撑。在熔融沉积中,有一种是融化热塑性聚合物变成半液态,喷嘴将材料挤压到构建平台上,零件以逐层方式将熔合层粘连在一起,打印成型结构体,其工作空间如图3所示[17]。将成型的结构体置于超声波清洗机中将支架材料溶解,进而得到需要的结构体模型,也可对结构体模型进行抛光处理。由于在熔融沉积成型中可使用多个喷嘴,而且每个喷嘴有不同的材料,所以在三维成型过程中,熔融沉积成型在梯度上没有限制。熔融沉积成型选择材料最重要的标准是传热特性和流变性。由于塑料熔融温度低,所以聚氯乙烯、尼龙、ABS树脂和熔模铸造蜡已在熔融沉积中成功使用。而在生物上的应用,由于聚己内酯的熔点低至60 ℃,玻璃化转变温度为-60 ℃,热量高稳定而被经常使 用[18-19]。通过控制挤压头在x-y方向的运动,制造具有不同的孔形态和通道尺寸的生物相容性材料的支架。熔融沉积成型的主要优点是不同沉积模式的高孔隙率和较高的机械强度,主要挑战是需要高黏度的熔融热塑性材料,而且由于较高的挤压力和较高的沉积温度,在材料中不能加入活细胞和温度敏感材料。"


2.1.4 三维生物打印 三维生物打印是在弗莱堡材料研究中心于2000年开发的,用于创建软组织支架,其中一种三维生物打印机如图4所示。三维生物打印是将具有一定匹配密度的黏性液体材料(通常是溶液,糊剂或分散体),通过加压的方式从注射器喷嘴里挤压出来,材料以连续的线条或单点方式进行沉积,从而创建出三维形状[20]。三维生物打印既可在高温条件下也可在低温的条件下进行打印,而低温无菌条件下能够模拟人体环境,可将细胞与材料混合进行打印,而且细胞能够保持活性。目前,生物打印应用的材料包括琼脂、聚氨基葡萄糖、白明胶、壳聚糖[21]、骨胶原、明胶与海藻酸钠、羟基磷灰石复合材料[22]、大豆蛋白[23]、琼脂糖等。生物打印的关键优势在于可室温处理打印材料,打印范围广,可直接加入组织细胞并使细胞均匀分布。其主要缺点是机械刚度有限,需要辅助材料固化方法,复杂结构的多种材料混合成型困难。进一步开发最适于生物因子打印的材料,以及开发下一代可沉积多种生物因子的材料到同一平台上的印刷头,为制造出复杂生物学要求的结构体奠定基础。 2.2 三维打印技术的打印技术流程 3D打印技术的工作原理是通过逐层打印来完成结构体构建的,而且具有相通的打印流程,现通过医疗领域的3D打印技术介绍打印流程,医学领域三维打印技术流程包括前处理、打印过程和后处理3个阶段[24]。下面通过三维生物打印介绍打印步骤。 2.2.1 前处理 前处理阶段包括模型建立、添加支撑、切片分层。建立模型结构是打印的基础,打印结构一般可有两种方式建立:通过计算机辅助设计软件(CAD)直接绘制,基于核磁共振成像(MRI)或计算机断层扫面(CT)技术获取的医学影像,采用mimics、3D.Doctor、VGstudio MAX等三维重建软件建立打印结构模型。对于不同的结构模型,有些形状复杂,受力不均匀,需要添加支撑,以保证在打印中不发生坍塌。添加的支撑与打印结构的接触面积应尽可能的小,而且也不易过多,同时,添加的支撑应容易去除,并且在打印过程中不会造成路径的复杂化。将添加支撑的打印模型保存成STL格式文件,发送生物打印机系统自带的切片软件中,进行分层设置,或者借用其他切片软件也可进行切片,为后期打印作准备。 2.2.2 打印过程 打印阶段包括材料准备、参数优化、打印成型。首先,准备打印材料,因为生物打印机只能够打印具有黏弹性的流体,所以选择材料必须考虑这一特性。将配置成的生物材料或者材料与细胞的混合物注入到点胶针筒内,将点胶筒加载到打印仓中。其次,通过生物打印机的控制软件,对挤压力、打印速度、温度等参数进行优化,选择出适合材料打印的参数。最后,在合适的温度、速度、压力等参数下,将材料沉积在打印平台的打印纸上,逐层沉积,完成结构体打印。 2.2.3 后处理 当生物打印机打印出最终结构模型,并不意味着打印的结束,接下来要对打印模型进行后处理,主要包括固化与去除支撑。由于打印出的结构模型,机械强度较低需要采用一些方法进行固化,主要包括高温烧结、紫外光固化、化学方法等。当固化完成之后,对于添加支撑结构的打印模型,需要去除支撑结构,可采用水溶方法、物理去除等。 2.3 三维打印技术的应用现状 在医疗领域应用的3D打印技术主要是立体光刻技术、激光烧结技术、熔融沉积技术、生物打印技术。不同打印技术在医疗领域应用的范围不同,根据成型材料的生物学性能不同,将生物打印技术分为4个层次的应用:医学术前模型、体内植入物、组织工程支架、细胞结构体。 2.3.1 医学术前模型 通过三维打印技术可在手术前打印出病灶体的个性化模型,借助模型可直观地观察病灶体,为治疗确定最佳方案,提高手术成功率。王峻峰等[25]采用昆明增材佳维科技有限公司3dp-240打印机打印肝脏肿瘤三维模型(图5),用于肝胆外科精准手术的规划及术中引导。Liu等[26]借助选择性激光烧结技术制造出下颌骨实体模型(图6),进行术前模拟。Kong等[27]利用一台高清24位彩色3D打印机Spectrum ZTM 510打印出肝脏模型(图7),用于辅助教学。杨龙等[28]通过3D快速成型机打印出髋关节1∶1实体模型(图8),用于术前模拟和与患者家属交流。Krauel等[29]用Stratasys Connex 500打印机制造出包裹主要血管的肾脏的3D原型肿瘤(图9),进行术前模拟。梁素添等[30]将3D打印技术应用于复杂胫骨平台骨折治疗中,建立模型,实施术前模拟, 进行手术规划。Valverde[31]介绍3D模型在心脏介入手术中用于术前模型和规划。在目前,3D打印技术在骨科、口腔颌面外科、血管外科、神经外科等疾病的诊断、术前评估、手术确定与术后评估得到广泛应用,建立医学模型可为医生提供更加直观的三维信息,与二维的MRI图像相比,更能清楚地显示病变位置,以及确定病变范围,为临床治疗提供可靠依据。同时,医生可基于打印模型进行手术评估、术前模拟,选择最优的手术方案,保证手术顺利进行,降低患者痛苦,缩短手术时间,降低手术风险,提高手术成功率。"


2.3.2 个性化植入物 三维打印技术为患者提供个性化植入物成为可能。Zopf等[32]成功将3D打印的气管支架(图10)植入1例患有支气管软化症的婴儿体内。张庆福等基于钛合金3D打印技术设计和制作的下颌骨(图11)植入体进行个性化修复重建[33]。程文俊等[34]利用3D打印钛合金骨小梁金属臼杯(图12),观察其在全髋关节置换术中应用的效果。2015年11月,澳大利亚医生成功地将3D打印笼状钛金属脊柱(图13)植入到了患者的患处,且术后恢复正常生活[35]。罗婷苑等[36]基于3D打印技术制备的个性化重建钛板在髂骨移植修复下颌骨缺损中。张云绮等[37]应用3D打印技术制作个性化植入体在修复下颌骨缺损中。向梅等[38]介绍并总结种植导板的设计制作及临床应用前景。汪烈等[39]通过3D打印技术制造个性化种植导板,用于多牙种植。张玮航等[40]采用激光打印技术快速成型钛合金牙种植体。Dupret-Bories等[41]利用3D打印技术用于下颌骨模板的个性化制造。目前,3D打印个性化植入物在硬组织领域取得成功,主要包括气管移植物,人体面部颌骨、头颅骨、下肢骨、假牙、义肢和脊柱等部位,随着3D打印技术的发展与新材料的开发,软组织个性化移植物将会被应用,未来将会有更多的个性化移植物用于人体疾病的治疗。 2.3.3 组织工程支架 组织工程支架是用于组织再生与修复的三维结构体,需要具备生物相容性、生物降解性、适当的机械性能、表面化学特性、高孔隙率和互连性。支架不仅提供细胞在体外形成组织的结构基础,而且决定物质运输。支架结构影响单细胞参数(如细胞活力、细胞迁移、细胞分化)和所产生的组织替代物组成。Ariadnaa等[42]采用熔融沉积成型打印机优化聚己内支架参数(图14),打印出适合癌症细胞培养的支架。Ma等[43]通过3DP低温打印,用明胶与海藻酸钠打印出支架,如图15所示。Sapkal等[44]使用熔融沉积成型快速成型技术间接制造患者特异性羟基磷灰石/β-磷酸三钙支架,如图16所示。Cox等[45]采用ZPrinter 310+打印机,用羟基磷灰石打印出适合骨组织生长的支架(图17),并间接处理得到多孔支架。李征宇等[46]采用3D打印技术建立新型复合多层组织工程支架用于体外细胞立体繁育。李佳乐等[47]采用三维打印技术制备由羟基磷灰石/β-磷酸三钙组成的双相磷酸钙陶瓷支架(图18),用于骨组织工程中,为骨组织工程支架提供试验基础。Mouser等[48]通过多种墨水印刷关节软骨组织构建体,为后期植入活体软骨植入物提供可能性。Lee等[49]通过SLA与静电纺丝技术制造神经支架。Rodriguez等[50]利用3D打印技术制造软组织结构体。经过多年的发展,组织工程支架从实验研究向临床应用不断前进,目前,打印的组织工程支架主要应用于临床研究,为细胞提供体外三维环境,进行细胞培养,进行临床试验如抗药性检测,模拟人体环境,以及在动物上进行临床实验。随着新技术与材料的开发,在不久的将来,组织工程支架应用到临床医学中。 2.3.4 细胞结构体 细胞打印是一种在体外构造具有生物活性的三维多细胞体系的先进技术。细胞打印以活细胞及其外基质材料在无菌条件下进行混合,作为墨水进行打印,该技术将快速成形技术和生物制造技术有机结合,可解决传统组织工程难以解决的问题,在生物医学的基础和应用研究中有着广阔的发展前景。与非细胞打印相比,生物打印需要解决额外的复杂问题,比如材料、细胞类型、生长和分化因子、与活细胞敏感性和组织构建相关的技术挑战。解决这些复杂性问题需要整合来自工程、生物材料科学、细胞生物学、物理学和医学领域的技术。Kundu等[51]用聚己内酯-藻酸盐-软骨细胞的混合物,打印出应用于软组织工程的三维支架,如图19所示。Kang等[52]研究光交联水凝胶对含有细胞MEGEL/PEGDA3350/藻酸盐混合物打印的影响,细胞结构体如图20所示。Irvine等通[53]过3D打印技术打印出包含细胞的明胶三维结构体,如图21所示。Billiet等[54]利用3D打印技术制造出具有较高生存能力的明胶甲基丙烯酰胺组织工程结构体。Pati等[55]采用3D打印技术制造出细胞加载的结构体,用于组织再生。Naghieh等[56]采用3D打印技术制造生物材料与细胞混合的支架结构体。目前,生物3D打印技术,机遇与挑战并存,如:单细胞、多种细胞、细胞团簇的受控三维空间输送、精准定位、排列与组装,以及生物制造过程中对细胞的损伤及生物功能的影响等。由于人体复杂的器官结构及功能的多样性,细胞与生物材料的特殊性,材料学、制造学、生物学等多交叉学科的合作及多喷头生物3D打印设备的应用,必将成为学科未来发展的趋势与主流,也是实现复杂器官制造的核心所在。目前,生物打印的细胞结构体,已用于产生和移植几种组织,包括多层皮肤、骨、血管移植物、气管夹板、心脏组织和软骨结构。随着新材料的开发与3D生物打印技术的发展,未来,生物打印的细胞结构体将会在临床上进行应用,最终解决器官移植的难题。 三维打印技术在医学领域应用的4个层次是由简单到复杂,逐步深入的过程。对于术前模型,由于对材料的生物性能要求不高,只需要打印出模型的外形结构,故使用立体光刻、熔融沉积成型技术进行打印即可实现要求;个性化体内植入物不仅要求材料具有生物相容性,而且要求打印结构一定机械性能,通常使用选择性激光烧结技术打印生物材料即能满足要求;组织工程支架打印需要材料具有良好的生物相容性和生物降解性,可采用熔融沉积成型和三维生物打印技术;而对于细胞结构体或者类组织器官则要求支架与细胞同时打印,而且对操作环境要求较高,则采用三维生物打印技术。目前,生物打印研究只限于功能单一的类组织器官打印,实现结构复杂功能完全的器官打印还需探讨新的打印原理和材料。"

| [1] Horvath J,Hoge L,Rich Cameron R,et al.3D printing. Apress, Springer. 2016:161-172.[2] Mironov V,Boland T,Trusk T,et al.Organ printing: computer-aided jet-based 3D tissue engineering.Trends Biotechnol. 2003;21(4): 157-161.[3] Mironovnuno V, Reis N, Derby B.Bioprinting: a beginning. Tissue Eng. 2006;12(4):631-635.[4] Calvert P, Boland T. Materials science: printing cells. Science. 2007; 318(5848):208-209.[5] Dowler CA.Automatic model building cuts design time, costs. Plastic Eng.1989;45:43-45.[6] Fisher JP,Dean D.Photo cross-linking characteristics and mechanical properties of diethyl fumarate / poly (propylene fumarate) biomaterials. Biomaterials.2002;23(22):4333-4343.[7] Melchels FP,Feijen J,Grijpma DW.A review on stereolithography and its applications in biomedical engineering.Biomaterials. 2010;31(24): 6121-6130.[8] Wang WL,Cheah CM,Fuh JYH,et al.Influence of process parameters on stereolithography part shrinkage.Mater Des.1996;17(4):205-213.[9] Kang HW,Cho DW.Development of an Indirect stereolithography technology for scaffold fabrication with a wide range of biomaterial selectivity.Tissue Eng Part C Methods.2012;18(9):719-729.[10] Park JH,Jung JW,Kang HW,et al.Indirect three-dimensional printing of synthetic polymer scaffold based on thermal molding process. Biofabrication.2014;6:025003.[11] Zhang X,Jiang X,Sun C.Micro-stereolithography of polymeric and ceramic microstructures. Sens Actuators A Phys. 1999;77:149-156.[12] Kang H,Hollister SJ,La Marca F,et al.Porous biodegradable lumbar interbody fusion cage design and fabrication using integrated global-Local topology optimization with laser sintering.J Biomech Eng. 2013;135(10): 101013-101018.[13] Liao HT,Lee MY,Tsai WW,et al.Osteogenesis of adipose-derived stem cells on polycaprolactone–β‐tricalcium phosphate scaffoldfabricated via selective laser sintering and surface coating with collagen type I J Tissue Eng Regen Med.2016;10(10):E337-E353.[14] Duan B,Wang M.Customized Ca–P/PHBV nanocomposite scaffolds for bone tissue engineering: design, fabrication, surface modification and sustained release of growth factor. J R Soc Interface. 2010;7:615-629.[15] Shuai CJ,Mao ZZ,Lu HB,et al.Fabrication of porous polyvinyl alcohol caffold for bone tissue engineering via elective laser sintering. Biofabrication.2013;5(1):015014.[16] Zein I,Hutmacher DW,Tan KC,et al.Fused deposition modeling of novel scaffold architectures for tissue engineering applications.Biomaterials. 2002;23(4):1169-1185.[17] van Noort R.The future of dental devices is digital.Dent Mater. 2012; 28(1):3-12.[18] Zein I,Hutmacher DW,Tan KC,et al.Fused deposition modeling of novel scaffold architectures for tissue engineering applications.Biomaterials. 2002;23:1169-1185.[19] Hutmacher DW,Schantz T,Zein I,et al.Mechanical properties and cell cultural response of polycaprolactone scaffolds designedand fabricated via fused deposition modeling.J Biomed Mater Res. 2001; 55:203-216.[20] Landers R,Mülhaupt R.Desktop manufacturing of complex objects, prototypes and biomedical scaffolds by means of computer‐assisted design combined with computer‐guided 3D plotting of polymers and reactive oligomers.Macromol Mater Eng.2015;282(1):17-21.[21] Lim TC,Chian KS,Leong KF.Cryogenic prototyping of chitosan scaffoldswith controlled micro and macro architecture and their effect on in vivo neo‐vascularization and cellular infiltration. J Biomed Mater Res A.2010;94:1303-1311.[22] Lee H,Kim YB, Kim SH,et al.Mineralized biomimetic collagen/alginate/ silica composite scaffolds fabricated by a low-temperature bio-plotting process for hard tissue regeneration: fabrication, characterisation and in vitro cellular activities.J Mater Chem B.2014;2(35):5785-5798.[23] Chien KB,Aguado BA,Bryce PJ, et al.In vivo acute and humoral response to three-dimensional porous soy protein scaffolds.Acta Biomater.2013;9(11):8983-8990.[24] Seedhouse E.Beyond Human, Bioprinting.Science and Fiction, Springer, 2014:65-76. [25] 王峻峰,孙志为,王罡.3D 打印模型在肝脏肿瘤切除手术中的应用[J].中国现代医学杂志,2017,27(3):136-138.[26] Liu YF,Xu LW,Zhu HY,et al.Technical procedures for template-guided surgery for mandibular reconstruction based on digital design and manufacturing.Biomed Eng Online.2014;13:63.[27] Kong X,Nie L,Zhang H,et al.Do 3D Printing Models Improve Anatomical Teaching About Hepatic Segments to Medical Students? A Randomized Controlled Study.World J Surg.2016;40(8):1969-1976. [28] 杨龙,王建吉,刘国勇.3D打印技术在髋臼发育不良髋关节置换中的初步应用[J].中国矫形外科杂志,2016,24(17):1550-1553.[29] Krauel L,Fenollosa F,Riaza L,et al.Use of 3D Prototypes for Complex Surgical Oncologic Cases[J]. World J Surg.2016;40(4):889-894.[30] 梁素添,冯世华,陈定启.复杂胫骨平台骨折治疗中3D 打印技术的应用探析[J].数理医药学杂志,2017,30(11):1688-1689.[31] Valverde I.Three-dimensional Printed Cardiac Models: Applications in the Field of Medical Education, Cardiovascular Surgery, and Structural Heart Interventions.Rev Esp Cardiol(Engl Ed). 2017;70(4):282-291.[32] Zopf DA,Hollister SJ,Nelson ME,et al.Bioresorbable airway splint created with a t hree-dimensional printer.N Engl J Med. 2013;368(21): 2043-2045.[33] 张庆福,刘刚,刘国勤.个体化3D 打印钛合金下颌骨植入体的设计制作与临床应用[J].口腔医学研究, 2015,31(1):48-51.[34] 程文俊,勘武生,李岩,等.3D打印钛合金骨小梁金属臼杯全髋关节置换术的短期疗效[J].中华骨科杂志,2014,34(8):816-823.[35] 王晓易.澳大利亚:首例3D打印钛金属脊柱植入手术[EB/OL].2015-11-20. http://tech.163.com/15/1120/16/B8SKUKQE00094P0U.html.[36] 罗婷苑,张翔,张森林.3D 打印技术在髂骨移植修复下颌骨缺损中的应用研究[J].临床口腔医学杂志,2017,33(4):232-233[37] 张云绮,贾保军,敖建华,等.3D打印技术在下颌骨缺损修复中应用的初步临床研究[J].口腔医学研究,2016,32(5):517-523.[38] 向梅,张宇.种植导板的设计制作及临床应用前景[J].中国组织工程研究, 2015,19(3):448-492.[39] 汪烈,陈智渊,刘融,等.个体化3D打印种植导板在多牙种植中的临床应用[J].上海口腔医学,2017,26(4):453-457.[40] 张玮航,张虎,李英姿,等.3D打印激光快速成型牙种植体的制备及其机械性能分析[J].吉林大学学报,2017,43(1):52-57[41] Dupret-Bories A,Vergez S,Meresse T,et al.Contribution of 3D printing to mandibular reconstruction after cancer.Eur Ann Otorhinolaryngol Head Neck Dis.2018;135(2):133-136.[42] Ariadnaa GP,Marca R,Teresa P,et al.Optimization of Poli (?-caprolactone) scaffolds suitable for 3D cancer cell culture.The Second CIRP Conference on Biomanufacturing. 2016;49:61-66.[43] Ma S,Zheng X, Zhang C,et al.Gelatin-Sodium Alginate Hydrogel Processing by Low-Temperature.3D Printing. 2015:523-532.[44] Sapkal PS,Kuthe AM.Indirect fabrication of hydroxyapatite / b-tricalcium phosphate scaffold for osseous tissue formation using additive manufacturing technology.J Porous Mater. 2016;23: 1567-1574.[45] Cox SC,Thornby JA,Gibbons GJ,et al.3D printing of porous hydroxyapatite scaffolds intended for use in bone tissue engineering applications.Mater Sci Eng C.2015;47:237-247.[46] 李征宇,姬钢,严少荣,等.新型复合多层组织工程支架体外细胞立体繁育系统研究[J].临床医学研究与实践,2017,2(25):1-4.[47] 李佳乐,夏轶超,澈力格尔,等.三维打印双相磷酸钙陶瓷支架在骨组织工程中的应用[J].中国实验诊断学,2017,21(5):878-881[48] Mouser VHM,Levato R, Bonassar LJ,et al.Three-Dimensional Bioprinting and Its Potential in the Field of Articular Cartilage Regeneration.Cartilage.2017;8(4):327-340.[49] Lee SJ,Nowicki M, Harris B,et al.Fabrication of a Highly Aligned Neural Scaffold via a Table Top Stereolithography 3D Printing and Electrospinning.Tissue Eng Part A. 2017;23(11-12):491-502.[50] Rodriguez MJ,Brown J, Giordano J,et al.Silk based bioinks for soft tissue reconstruction using 3-dimensional (3D) printing with in vitro and in vivo assessments. Biomaterials. 2017;117:105-115.[51] Kundu J,Shim JH,Jang J,et al.An additive manufacturing based PCL – alginate – chondrocyte bioprinted scaffold for cartilage tissue engineering.J Tissue Eng Regen Med. 2015;9(11):1286-1297.[52] Kang LH,Armatrong PA,Lee LJ,et al.Optimizing Photo-Encapsulation Viability of Heart Valve Cell Types in 3D Printable Composite Hydrogels. Ann Biomed Eng. 2016;45(2):360-377.[53] Irvine SA,Agrawal A,Lee BH,et al.Printing cell-laden gelatin constructs by free-form fabrication and enzymatic protein crosslinking.Biomed Microdevices.2015;17(1):16.[54] Billiet T,Gevaert E,De Schryver T,et al.The 3D printing of gelatin methacrylamide cell-laden tissue-engineered constructs with high cell viability.Biomaterials.2014;35(1):49-62.[55] Pati F,Shim JH,Lee JS,et al.3D printing of cell-laden constructs for heterogeneous tissue regeneration. Manuf Lett.2013;1:49-53.[56] Naghieh S,Sarker M,Izadifar M,et al.Dispensing-based bioprinting of mechanically-functional hybrid scaffolds with vessel-like channels for tissue engineering applications - A brief review.J Mech Behav Biomed Mater.2018;78:298-314. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [3] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [4] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [5] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [6] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [7] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||