Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (30): 4900-4905.doi: 10.3969/j.issn.2095-4344.0934
Previous Articles Next Articles
Micro-pattern technique and its application in tissue engineering
Qiu Chang-jun1, 2, 3, Hun Ting-ting1, 2, 3, Zhao Ying-tong1, 2, 3, Zhao Feng1, 3, He Jing-wen1, 3, Sun Yan1, 2, 3
- 1Key Laboratory for Biomechanics and Mechanobiology of Ministry of Education, School of Biological Science and Medical Engineering, Beihang University, Beijing 100191, China; 2Beijing Advanced Innovation Centre for Biomedical Engineering, Beihang University, Beijing 102402, China; 3State Key Laboratory of Transducer Technology, Chinese Academy of Sciences, Shanghai 200050, China
-
Received:2018-03-14Online:2018-10-28Published:2018-10-28 -
Contact:Sun Yan, MD, Master’s supervisor, Associate professor, Key Laboratory for Biomechanics and Mechanobiology of Ministry of Education, School of Biological Science and Medical Engineering, Beihang University, Beijing 100191, China; Beijing Advanced Innovation Centre for Biomedical Engineering, Beihang University, Beijing 102402, China; State Key Laboratory of Transducer Technology, Chinese Academy of Sciences, Shanghai 200050, China -
About author:Qiu Chang-jun, Master candidate, Key Laboratory for Biomechanics and Mechanobiology of Ministry of Education, School of Biological Science and Medical Engineering, Beihang University, Beijing 100191, China; Beijing Advanced Innovation Centre for Biomedical Engineering, Beihang University, Beijing 102402, China; State Key Laboratory of Transducer Technology, Chinese Academy of Sciences, Shanghai 200050, China -
Supported by:the National Natural Science Foundation of China, No. 31470942
CLC Number:
Cite this article
Qiu Chang, Hun Ting-ting,Zhao Ying-tong, Zhao Feng, He Jing-wen, Sun Yan. Micro-pattern technique and its application in tissue engineering[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(30): 4900-4905.
share this article

2.1 软骨组织工程 软骨虽然为新陈代谢活跃的组织,但位于间质中的软骨细胞代谢周期却相当长,因为关节软骨为无血管组织,所以自我修复能力相当有限,轻微伤害即有可能导致渐进式的损害与退化。目前的治疗方法均不能实现软骨的生物修复,缺损软骨的修复问题成为临床上较为棘手的问题之一。组织工程学的发展为解决这个问题提供了新思路,使缺损软骨的完全再生成为可能。使用微图案技术解决软骨组织工程中的基本问题,并最终构建血管化的三维软骨组织也是众多研究者关注的热点之一。 Pufe等[12]利用微图案技术在柔性生物相容性多糖凝胶表面上制造微图案特征(宽15-65 μm,深40 μm),将其应用于软骨细胞培养的支架。这些细胞形态呈圆形,在细胞接种10 d后免疫荧光分析整个过程Ⅱ型胶原最大的生成量与对照组在显著差异(P < 0.000 1)。实验证明该支架可有效维持软骨细胞表型。此外,Petersen等[13]进一步通过在单个微图案表面特征中观察到软骨细胞的增殖,并发现在连续微图案表面特征中会形成软骨细胞聚集体,这为体外修复软骨工程的问题提供了一种新方法。同时,Song等[14]通过使用光刻技术在聚苯乙烯板上制备具有不同面积比的聚(乙烯醇)微图案非黏附区域,并将间充质干细胞黏附到微图案化表面,研究细胞密度梯度对增殖和分化等细胞功能的影响。结果表明,以低密度接种的细胞比以高密度接种的细胞增殖更快,尽管以低和高密度接种的间充质干细胞均显示成骨分化,但较高的细胞接种密度可以比低细胞密度更快速地开始成骨分化,并且高细胞密度可更好地诱导软骨分化。以上研究表明,微图案技术可有效控制软骨细胞的排列和细胞密度分布,进而控制软骨细胞的表型、增殖和分化等。 彭荣[15]课题组利用了微图案化技术,于一种细胞接种密度下在不同黏附岛上实现了不同的局部密度,并且可以独立研究细胞尺寸、细胞之间的接触及细胞密度的影响。通过研究不同形状(圆形、方形、三角形、星形及不同长径比的矩形等)上的细胞分化情况发现,细胞形状对干细胞在成骨/成脂分化液中的分化程度有显著影响,如:圆形细胞更易于向成脂肪细胞分化,星形细胞更易于向成骨细胞分化;进一步考察长径比效应时发现,骨髓基质干细胞成脂分化随长径比增加下降,成骨分化随着长径比上升呈现峰值,即存在最佳长径比。彭荣等进一步对细胞尺寸、细胞接触和细胞密度对于干细胞分化的影响进行了研究,结果表明:细胞尺寸和接触都会影响骨髓基质干细胞的成骨分化和成脂分化,而密度效应则是尺寸效应和接触效应的综合结果。随着细胞密度上升,对于成脂分化,细胞尺寸效应和接触效应给出同样的趋势;而对于成骨分化,细胞尺寸效应和细胞接触效应在细胞密度上升时则给出了“竞争”性效应。该研究在利用图案化技术解构细胞密度对干细胞分化影响的内在物理因素基础上,进一步提出了影响干细胞分化细胞密度的两个区段划分概念。虽然细胞聚集被认为能够促进软骨形成,但目前还没有直接证据证实细胞与细胞接触本身会增加干细胞的软骨形成分化,因为细胞与细胞接触的变化通常伴随着其他细胞几何形态和细胞可溶性因子的变化,如O2环境。纳米支架材料与天然细胞外基质的结构最为相似,且其优良的组织相容性及机械性能,使其在软骨组织工程支架的研究及运用中逐渐得到了研究者的重视。 Shi等[16]通过旋涂和微图案化技术的简单组合开发出具有微凹图案的“贴纸状”聚乳酸/聚羟基乙酸共聚体纳米片,得到的微槽化聚乳酸/聚羟基乙酸共聚体纳米片可物理黏附在平坦或多孔表面上,这种聚乳酸/聚羟基乙酸共聚体纳米片在水环境中仍具备优良的稳定性,使其成为用于骨再生应用生物仿生骨膜的新希望。Alshomer等[17]提出了一种使用磷酸盐玻璃纤维微图案化新型纳米复合材料聚合物多面体低聚倍半硅氧烷聚(碳酸酯-脲)聚氨酯(POSS-PCU)模板腱组织工程应用的方法,所制造图案化支架的直径取决于使用的玻璃纤维(15 μm)直径,首次证明了POSS-PCU支持人类肌腱细胞的生长。此外,微图案化聚合物表面上细胞的生物学功能和各种肌腱相关蛋白(例如,scleraxis,Ⅰ型和Ⅲ型胶原蛋白,腱生蛋白C)的表达量显著升高。这项研究提出了一种全新的肌腱修复应用方法。 2.2 肌肉组织工程 人体肌组织包括骨骼肌、平滑肌和心肌,由于功能不同,其结构、组织学也不相同。骨骼肌组织工程替代品在未来可有望治疗各种体内肌肉缺陷和疾病,但是,在体外如何实现功能分化的骨骼肌是组织工程和再生医学研究的主要挑战之一。在骨骼肌肉系统,以骨骼肌的组织工程学研究较为突出[18]。骨骼肌来自体壁中胚层生肌节的间充质细胞增殖,心肌和平滑肌则是由脏壁中胚层间充质细胞分化而来。肌节间充质细胞迁移至肢芽,在胚胎发育期,间充质细胞分化为成肌细胞,再进一步分化为成熟肌细胞[19]。随后肌管融合成肌纤维,继续分化为特定的肌纤维类型。肌管成熟形成的肌纤维是负责肌肉收缩的最小肌肉收缩系统。Li 等[20]将微图案技术和细胞牵引力显微镜技术相结合建立了一种体外模型,首次证明了C2C12细胞可被微图案化为特定的几何形状,并且在聚丙烯酰胺凝胶胶原涂层上保持一致的排列,促进这些细胞向肌管分化。该模型可作为筛选dmd基因治疗的快速且经济方法。利用微图案技术研究肌肉组织工程,可为许多肌肉损伤或者肌肉萎缩疾病(如杜兴肌营养不良症)带来新的希望。 近年来,已采取各种方法通过组织工程来产生功能性肌肉组织。然而,体外生成具有生理结构平滑肌的方法仍然有限。为了模拟平滑肌细胞的体内高度组织化的结构,Nakamoto等[21]使用微图案技术制备了不同宽度梯度(5,10,20,40,60,80,100,200,400,600,800和1 000 μm)的细胞黏附聚苯乙烯平行条带,研究表明,微图案条纹宽度对细胞取向、形态和平滑肌细胞分化有明显影响。当微图案条纹变窄时,细胞显示出更高的取向度。在200 μm到20 μm的狭窄微图案中,观察到钙调蛋白和平滑肌肌动蛋白的表达水平较高,而非图案区域和宽微图案区域表达水平则相似。Zhang等[22]通过微图案化技术将不同亲和力的肽配体微接触印刷到惰性背景上,通过单独的受控生物化学和生物物理学线索来探索间充质干细胞向平滑肌的分化。结果表明,在低纵横比下,配体亲和力是平滑肌分化的主要决定因素,而在高纵横比下,配体亲和力的作用则较小。Huang 等[23]用平行排布的聚丙交酯电喷雾纳米纤维材料对成肌细胞进行排列、培养,结果发现在纳米纤维上的细胞增殖降低,加速退出细胞周期进入分化状态。纳米纤维排列成肌细胞不仅使细胞分化后的肌管定位得到了控制,而且肌管的长度比对照增加了2倍。该研究组发现10 μm微槽也对成肌细胞细胞的分化有明显的促进作用。上述研究结果均表明条带状的细胞排列对成肌细胞分化有促进作用。 Cimetta等[24]利用微图案技术在软材质基板上开发了一项简单通用的体外生产功能化心肌纤维和骨骼肌肌纤维阵列的技术,运用小鼠肌卫星细胞分化出平行肌管,通过微接触印刷技术将细胞外基质蛋白打印在软材质的聚丙烯酰胺基水凝胶上,通过紫外真空等离子技术使其键合在功能化的玻片上。这种方法可简单、重复、有效地获得选择性黏附到软凝胶图案表面的心肌细胞和肌卫星细胞。将心肌细胞诱导形成阵列的心肌纤维,经过2 d的培养后就开始出现收缩行为。该实验首次发现小鼠卫星细胞在一个柔软的水凝胶基质培养7 d后,融合并形成有序排列的肌管。免疫荧光分析证实,细胞的表型、分化标记和肌小节组织均能正确表达。这些结果的获得均来自于研究肌肉萎缩症的野生型和MDX小鼠肌卫星细胞的肌管研究模型。这些阵列的心肌纤维和骨骼肌肌纤维,可用作体外药物筛选实验或单纤维水平的生物研究模型。Zatti等[25]在弹性模量为15 kPa的软凝胶基底表面,研究了宽度为100,300,500 μm的微图案平行条带上早期成肌细胞的增殖和分化,结果表明,随着微图案条带宽度的增加,成肌细胞的增殖降低,而相对的融合系数会增加。Zatti通过分析认为,宽条带微图案有利于内源性分泌因子的积累。有趣的是,Zatti等发现人原代成肌细胞的增殖不受微图案宽度的影响,这可能是由于培养基中的血清含量较高,抑制了分泌因子的作用。目前,微图案技术在肌肉组织工程的研究中得到了极大发展和广泛应用,但是,如何构建三维肌肉组织及如何提高二维下肌管的融合指数和肌管形成率,仍然存在许多疑问。 2.3 血管组织工程 血管移植物必须具有适当的韧性和强度,以承受长期的血液流动所带来的应力和血管壁磨损。天然血管壁是一个结构复杂的组织,其特征在于交替圆周螺旋排列的胶原纤维/细胞和层状弹性蛋白。因此,如何开发出更接近原生血管性质的组织工程替代物,将是糅合材料学和组织工程学的难点问题之一。微图案技术如软光刻技术和3D打印技术,可创造性地模仿天然细胞外基质支架,并对研究细胞在支架上的黏附和行为非常重要[26-30]。 Chiu等[31]将2个血管外植体固定在胶原-壳聚糖水凝胶的相对侧,为了促进血管床的形成,他们嵌入胸腺素β4。另外,它们利用微图案化的硅酮表面来引导来自容器的毛细血管生长。最近有研究表明,200 μm直径的微通道藻酸盐基质与黏附肽和血管生长因子结合,可促进血管样网络的形成[32-33]。Papenburg等[34]采用一种一步法制造了高度多孔微图案的二维支架,具有高葡萄糖扩散特性,表明其对营养物质运输是可行的。人脐带静脉内皮细胞培养证明该支架片适于细胞培养。使用小鼠成肌细胞C2C12和小鼠成骨细胞MC3T3的更广泛培养实验显示,微图案设计影响细胞对齐和组织形成的程度。该研究表明,二维支架非常有希望作为建立三维支架的基础。近年来,有关三维血管支架的研究主要集中在特定端基聚合物上,例如聚甘油癸二酸酯[35],有时与天然聚合物如明胶或胶原蛋白结合。将它们以多种形态进行加工,包括通过静电纺丝制备的纳米纤维支架[36]、通过激光微蚀刻方法与微机电系统制造和封装相结合的3D结构技术[37-38]。这些加工方法的产生对于加工具有显示宿主组织固有各向异性和方向性机械特性的支架是非常重要的。同时,这些方法也各有其优缺点,如下表1所示。 "

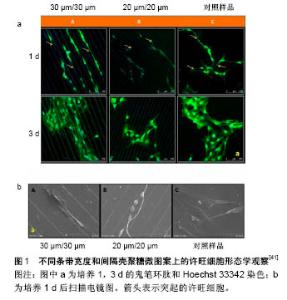
总的来说,目前的方法都无法形成成熟和稳定的血管,所以无法产生足够厚的心脏贴片。然而,血管组织工程的研究已取得了重大进展,这也促进心脏贴片成为治疗现实心脏疾病的未来选择。 2.4 神经组织工程 微图案技术在神经组织工程的研究中也有应用。生物可降解材料,例如聚乳酸和聚乳酸/聚羟基乙酸共聚体是近年来神经组织工程研究的焦点问题。王光林等[39]观察了许旺细胞在聚乳酸及聚乳酸/聚羟基乙酸共聚体材料上的三维生长迁移情况,发现许旺细胞和细胞外基质凝胶混合后再与聚乳酸多孔材料复合,体外培养一段时间后,能够携带大量的许旺细胞和形成类似Bungner’s带状结构的特点,对于构建具有组织工程化的人工神经具有指导意义。 Fozdar等[40]对由一系列微米(约2 μm)或亚微米(约300 nm)孔或具有可变尺寸的线组成的四象限地形网格进行轴突生长测定,将单独大鼠胚胎海马细胞放置在两个并置的形貌图之间,或在并置未图案化光滑表面各个形貌的边界之间,培养24 h。结果表明,在神经导管和其他生物材料支架上设计各种形状和尺寸的表面物理形貌,可帮助刺激轴突再生。Li等[41]使用微模型方法在盖玻片表面上制作了两种尺寸的壳聚糖平行微条带,以研究壳聚糖微图案对神经再生的影响,两种条带的条带宽度和间隔分别是20 μm/20 μm、30 μm/30 μm,并通过扫描电镜观察制备的聚二甲基硅氧烷和壳聚糖微图案形态,使用水接触角测量法评估了微图案的润湿性。通过在壳聚糖微图案上培养许旺细胞来评估壳聚糖微图案对细胞行为的影响,结果表明条带状壳聚糖微图案可在盖玻片表面上成功制备,30 μm/30 μm壳聚糖微图案上的许旺细胞显示出最明显的细胞取向,见图1。 此外,许旺细胞神经生长因子的分泌表明,壳聚糖微图案对细胞的正常生理功能没有负面影响。以上研究进一步证明了壳聚糖微图案可很好地诱导和调节许旺细胞的生长,这可能对体外构建外周神经组织工程具有潜在的应用价值。然而,关于微图案技术在神经组织工程中的应用仍然较少。这主要是由于许旺细胞的纯化仍然是神经组织工程亟待解决难点问题,这同时也极大地制约了微图案技术在神经组织工程研究中的进一步应用。 2.5 肝脏组织工程 肝脏是结构和功能极为精细复杂的生命器官,体外再造肝脏之路注定艰难而漫长。通过科研、临床、产业的紧密协作,在人工肝脏的设计及制备上获得了可喜成果。 通过微图案技术构建人工肝脏类器官,主要是利用高分子材料预先制备生物材料微型模具,为细胞生长提供附着点和微环境支持,以期维持特定的三维形态结构或发挥特定生理功能,形成临床可应用的人工器官。 肝细胞在二维环境中培养时增殖能力有限,且容易失去肝细胞特定的生物学功能,而三维环境培养则能显著提高肝细胞的增殖能力和生理功能[42]。Yamada等[43]在体外构建出了一种三明治结构式肝索样组织凝胶纤维模型,利用微流体装置将与水凝胶混合的肝细胞和3T3细胞分别输入中间和两侧的凝胶微通道,培养后得到一种肝索样组织。与传统的单层单种类细胞培养相比,这种组织随着培养时间进一步延长,表达的肝细胞特异性蛋白更多,分泌白蛋白和合成尿素能力也明显提高。然而,该组织的细胞成分和超微结构与自然的肝索结构之间还是有很大差异。Rennert等[44]设计了一种仿真度更高的肝脏类器官构建方案,通过微流体装置将人类脐静脉内皮细胞与外周血单核细胞按一定比例混合种植到微通道上层,而将HepaRG细胞和星状细胞按一定比例混合后,再种植到微通道的下层,最后得到了与正常肝脏结构和功能更接近的肝脏类器官。 Cho等[45]提出了一种新的方法来,使用微制造的聚二甲基硅氧烷模板在微图案成纤维细胞饲养层上产生肝细胞的分层图案化。作者制造了聚二甲基硅氧烷模板来模拟直径为500 μm的圆形孔,将肝细胞与3T3-J2成纤维细胞以两种图案分别进行共培养以评估和表征共培养系统中的细胞的相互作用。研究结果表明,当通过分层图案化技术增加肝细胞与成纤维细胞之间的异型界面时,肝细胞中的细胞内白蛋白染色均匀,有E-钙黏蛋白表达,肝特异性功能增强和肝糖原合成活跃。这种图案化技术可成为在基础科学、药物筛选、组织工程及生物人工肝设备设计中的有用实验工具。Chen等[46]在进行早期人工肝脏的研究基础上,将人原代肝细胞、成纤维细胞及内皮细胞嵌入可降解的微图案生物支架材料中,在肝脏再生信号的刺激下出现了血管结构及胆管前体结构,并具备人类肝脏相关的分泌及代谢功能[47]。该研究利用微图案技术在肝细胞再生和接种体系方面进行了创新性探索,为肝脏类器官的构建开拓了全新的视野。相信微图案技术在肝脏组织中的应用前景仍然非常巨大,人工肝脏必将成为解决供肝短缺问题的有力武器,为肝脏替代治疗带来新的希望[48]。"
| [1] Mcalear JH,Wehrung JM.MICRODEVICE SUBSTRATE AND METHOD FOR MAKING MICROPATTERN DEVICES: US,CA 1066209 A1[P].[2] Fink J,Théry M,Azioune A,et al.Comparative study and improvement of current cell micro-patterning techniques.Lab Chip.2007;7(6):672-680.[3] Li Y,Jiang X,Zhong H,et al.Hierarchical Patterning of Cells with a Microeraser and Electrospun Nanofibers.Small.2015;12(9):1230-1239.[4] Ali S,Cuchiara ML,West JL.Chapter 8-Micropatterning of Poly(ethylene glycol) Diacrylate Hydrogels// Methods in Cell Biology.Elsevier Science & Technology,2014:105-119.[5] Yap FL,Zhang Y.Protein and cell micropatterning and its integration with micro/nanoparticles assembly.Biosens Bioelectron. 2007;22(6):775.[6] Li Y,Huang G,Zhang X,et al.Engineering cell alignment in vitro. Biotechnol Adv.2014;32(2):347.[7] Staple DB,Farhadifar R,Röper JC,et al.Mechanics and remodelling of cell packings in epithelia. Eur Phys J E Soft Matter. 2010;33(2):117-127.[8] 丁冉,吴志宏,邱贵兴,等.选择性激光烧结技术的多孔钛合金支架的骨组织工程学观察[J].中华医学杂志, 2014,94(19):1499-1502.[9] Tarafder S,Balla VK,Davies NM,et al.Microwave-sintered 3D printed tricalcium phosphate scaffolds for bone tissue engineering.J Tissue Eng Regen Med.2013;7(8):631-641.[10] Pati F,Song TH,Rijal G,et al.Ornamenting 3D printed scaffolds with cell-laid extracellular matrix for bone tissue regeneration.Biomaterials. 2015;37:230-241.[11] Tarafder S,Dernell WS,Bandyopadhyay A,et al.SrO- and MgO-doped microwave sintered 3D printed tricalcium phosphate scaffolds: mechanical properties and in vivo osteogenesis in a rabbit model. J Biomed Mater Res B Appl Biomater.2015;103(3):679-690.[12] Pufe T,Petersen W,Fändrich F,et al.Programmable cells of monocytic origin (PCMO): A source of peripheral blood stem cells that generate collagen type II‐producing chondrocytes.J Orthop Res. 2008;26(3): 304-313.[13] Petersen EF,Spencer RG,McFarland EW.Microengineering neocartilage scaffolds.Biotechnol Bioeng. 2002;78(7):801-804.[14] Song W,Lu H, Kawazoe N,et al.Gradient patterning and differentiation of mesenchymal stem cells on micropatterned polymer surface.J Bioact Compat Polym.2011;26(3):242-256.[15] 彭荣.高分子表面微图案技术研究干细胞形状、尺寸和密度对其分化的影响[D]. 上海: 复旦大学,2012.[16] Shi X,Fujie T,Saito A,et al.Periosteum-mimetic structures made from freestanding microgrooved nanosheets.Adv Mater. 2014;26(20): 3290-3296.[17] Alshomer F,Chaves C,Serra T,et al.Micropatterning of nanocomposite polymer scaffolds using sacrificial phosphate glass fibers for tendon tissue engineering applications.Nanomedicine. 2017;13(3):1267-1277. [18] 杨志明.骨骼肌肉系统组织工程学研究与临床应用[J].现代康复, 2001, 5(16):8-10.[19] Brockett CL,Morgan DL,Proske U.Human hamstring muscles adapt to eccentric exercise by changing optimum length.Med Sci Sports Exerc. 2001;33(5):783-790.[20] Li B,Lin M,Tang Y,et al.A novel functional assessment of the differentiation of micropatterned muscle cells.J Biomech. 2008;41(16): 3349-3353.[21] Nakamoto T,Wang X,Kawazoe N,et al.Influence of micropattern width on differentiation of human mesenchymal stem cells to vascular smooth muscle cells.Colloids Surf B Biointerfaces.2014; 122:316.[22] Zhang D,Sun MB,Lee J,et al.Cell shape and the presentation of adhesion ligands guide smooth muscle myogenesis.J Biomed Mater Res A.2016;104(5):1212-1220.[23] Huang NF,Patel S,Thakar RG,et al.Myotube assembly on nanofibrous and micropatterned polymers. Nano Lett.2006;6(3):537-542.[24] Cimetta E,Pizzato S,Bollini S,et al.Production of arrays of cardiac and skeletal muscle myofibers by micropatterning techniques on a soft substrate.Biomed Microdevices.2009;11(2):389-400.[25] Zatti S,Zoso A,Serena E,et al.Micropatterning Topology on Soft Substrates Affects Myoblast Proliferation and Differentiation.Langmuir. 2012;28(5):2718-2726.[26] Bian W,Jackman CP,Bursac N.Controlling the structural and functional anisotropy of engineered cardiac tissues.Biofabrication. 2014;6:024109. [27] Engelmayr GC Jr,Cheng M,Bettinger CJ,et al.Accordion-like honeycombs for tissue engineering of cardiac anisotropy.Nat Mater. 2008;7:1003-1010.[28] Ravichandran R,Venugopal JR,Sundarrajan S,et al.Poly(Glycerol sebacate)/gelatin core/shell fibrous structure for regeneration of myocardial infarction.Tissue Eng Part A. 2011;17:1363-1373.[29] Madden LR,Mortisen DJ,Sussman EM,et al.Proangiogenic scaffolds as functional templates for cardiac tissue engineering.Proc Natl Acad Sci USA.2010;107:15211-15216.[30] Patra C,Boccaccini AR,Engel FB.Vascularisation for cardiac tissue engineering: the extracellular matrix.Thromb Haemost. 2015;114(3): 532-547.[31] Chiu LL,Montgomery M,Liang Y,et al.Perfusable branching microvessel bed for vascularisation of engineered tissues.Proc Natl Acad Sci USA. 2012;109:E3414-3423.[32] Zieber L,Or S,Ruvinov E,et al.Microfabrication of channel arrays promotes vessel-like network formation in cardiac cell construct and vascularisation in vivo. Biofabrication. 2014;6:024102. [33] Ito Y,Hasuda H,Terai H,et al.Culture of human umbilical vein endothelial cells on immobilized vascular endothelial growth factor.J Biomed Mater Res A.2010;74A(4):659-665.[34] Papenburg BJ,Vogelaar L,Bolhuisversteeg LA,et al.One-step fabrication of porous micropatterned scaffolds to control cell behavior. Biomaterials. 2007;28(11):1998.[35] Chen QZ,Ishii H,Thouas GA,et al.An elastomeric patch derived from poly(glycerol sebacate) for delivery of embryonic stem cells to the heart. Biomaterials.2010;31:3885-3893.[36] Uttayarat P,Perets A,Li M,et al.Micropatterning of three-dimensional electrospun polyurethane vascular grafts.Acta Biomaterialia. 2010;6(11): 4229-4237.[37] Engelmayr GC Jr,Cheng M,Bettinger CJ,et al.Accordion-like honeycombs for tissue engineering of cardiac anisotropy.Nat Mater. 2008;7:1003-1010.[38] Kolewe ME,Park H,Gray C,et al.3D structural patterns in scalable, elastomeric scaffolds guide engineered tissue architecture.Adv Mater. 2013;25:4459-4465.[39] 王光林,林卫,杨志明,等.许旺细胞在支架材料中的三维生长与迁移的研究[J].中华显微外科杂志,2003, 26(1):42-44.[40] Fozdar DY,Lee JY,Schmidt CE,et al.Selective axonal growth of embryonic hippocampal neurons according to topographic features of various sizes and shapes.Int J Nanomedicine. 2010;6:45-57. [41] Li G,Zhao X,Zhang L,et al.Regulating Schwann cells growth by chitosan micropatterning for peripheral nerve regeneration in vitro.Macromol Biosci.2014;14(8):1067.[42] Wang Y,Nicolas CT,Chen HS,et al.Recent advances in decellularization and recellularization for tissueengineered liver grafts.Cells Tissues Organs.2017;203(4):203-214.[43] Yamada M,Utoh R,Ohashi K,et al.Controlled formation of heterotypic hepatic micro-organoids in anisotropic hydrogel microfibers for long-term preservation of liver-specific functions. Biomaterials. 2012;33(33): 8304-8315.[44] Rennert K,Steinborn S,Gröger M,et al.A microfluidically perfused three dimensional human liver model.Biomaterials.2015;71:119-131.[45] Cho CH,Park J,Tilles AW,et al.Layered patterning of hepatocytes in co-culture systems using microfabricated stencils.Biotechniques. 2010; 48(1):47-52.[46] Chen AA,Thomas DK,Ong LL,et al.Humanized mice with ectopic artificial liver tissues.Proc Natl Acad Sci USA. 2011;108(29):11842-11847.[47] Stevens KR,Scull MA,Ramanan V,et al.In situ expansion of engineered human liver tissue in a mouse model of chronic liver disease.Sci Transl Med.2017;9(399):eaah5505.[48] 杨扬,王励.肝脏组织工程研究进展[J].器官移植, 2017,8(5):337-343. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Li Cai, Zhao Ting, Tan Ge, Zheng Yulin, Zhang Ruonan, Wu Yan, Tang Junming. Platelet-derived growth factor-BB promotes proliferation, differentiation and migration of skeletal muscle myoblast [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1050-1055. |
| [3] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [4] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [5] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [6] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [7] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [8] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [9] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [10] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [11] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [12] | Zhou Wu, Wang Binping, Wang Yawen, Cheng Yanan, Huang Xieshan. Transforming growth factor beta combined with bone morphogenetic protein-2 induces the proliferation and differentiation of mouse MC3T3-E1 cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3630-3635. |
| [13] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [14] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [15] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||