Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (5): 768-773.doi: 10.12307/2022.125
Previous Articles Next Articles
Hyaluronic acid around articular chondrocytes: production, transformation and function characteristics
Xu Lei1, Han Xiaoqiang2, Zhang Jintao1, Sun Haibiao2
- 1The First Clinical College of Shanxi Medical University, Taiyuan 030001, Shanxi Province, China; 2Department of Orthopedics, The First Hospital of Shanxi Medical University, Taiyuan 030001, Shanxi Province, China
-
Received:2020-11-19Revised:2020-11-21Accepted:2020-12-25Online:2022-02-18Published:2021-12-01 -
Contact:Sun Haibiao, MD, Chief physician, Department of Orthopedics, The First Hospital of Shanxi Medical University, Taiyuan 030001, Shanxi Province, China -
About author:Xu Lei, Master candidate, Physician, The First Clinical College of Shanxi Medical University, Taiyuan 030001, Shanxi Province, China -
Supported by:Special Professorship Support Program for Young Scholars, No. (2016)128-2 (to SHB)
CLC Number:
Cite this article
Xu Lei, Han Xiaoqiang, Zhang Jintao, Sun Haibiao. Hyaluronic acid around articular chondrocytes: production, transformation and function characteristics[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 768-773.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
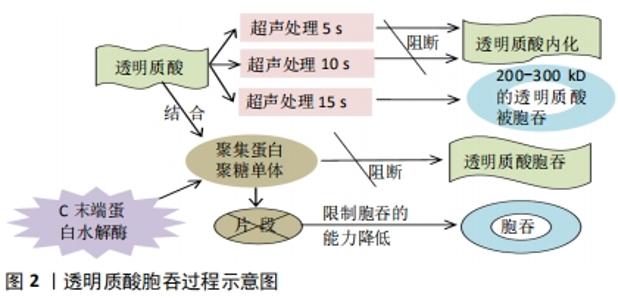
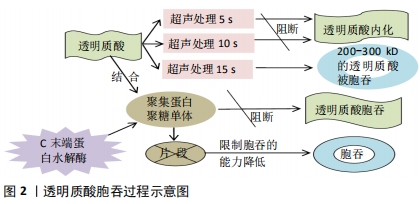
2.1 透明质酸在软骨细胞中的合成、周转及降解 2.1.1 透明质酸的合成 20世纪30年代,Meyer首先从牛眼玻璃体液中发现了透明质酸,随后Meyer团队将其认定为一种内源性非硫酸化糖胺聚糖。透明质酸通常以钠盐形式存在,称为透明质酸钠或玻璃酸钠。与高尔基体中合成的其他糖胺聚糖分子不同,透明质酸是由一组高度专一的膜蛋白透明质酸合酶(hyaluronate synthase,HAS)在质膜上合成的[5]。研究表明,哺乳动物中存在HAS1、HAS2和HAS3三种同工酶,其中HAS2是参与牛和人软骨透明质酸合成的主要同工酶[6]。NISHIDA等[7]将人关节软骨细胞和软骨切片用含有HAS2 mRNA反义序列的硫代磷酸酯寡核苷酸处理,结果表明正常人关节软骨细胞仅表达HAS2及HAS3 mRNA,但HAS2 mRNA的表达水平远高于HAS3。MATSUMOTO等[8]通过敲入Prx1-Cre基因使小鼠胚层肢芽中的HAS2失活,发现HAS2缺陷小鼠出现骨骼畸形和肢体缩短,聚集蛋白聚糖的沉积减少且软骨细胞之间的结构关系被破坏,其研究结果表明,透明质酸在肢体骨骼生长、软骨细胞成熟和滑膜关节形成中具有重要作用。最近数项敲除HAS2基因的动物实验共同表明软骨细胞周围基质中的透明质酸和聚集蛋白聚糖对维持软骨细胞间距极为重要[9-10]。 2.1.2 透明质酸与聚集蛋白聚糖的关系 在关节内软骨细胞周围基质中,软骨细胞合成的透明质酸与聚集蛋白聚糖和连接蛋白相结合形成蛋白多糖集聚体,其间以强大的非共价键结合。当软骨细胞在体外进行单层培养时,可以直接观察到软骨细胞周围被膜出现,而在活细胞中使用颗粒排除测定法方能看到[11],该区域经历洗涤和离心处理后依然稳定[12],但用透明质酸酶处理后被膜溶解,表明这层被膜的支架主要是透明质酸。早期研究发现,单独添加透明质酸或聚集蛋白聚糖单体不足以体外培养软骨细胞周围被膜,只有透明质酸和聚集蛋白聚糖同时存在才可以重建[11]。透明质酸和聚集蛋白聚糖通过CD44(一种跨膜糖蛋白)与软骨细胞结合[13]。这些结果表明,透明质酸与聚集蛋白聚糖共同形成完整的软骨细胞周围被膜。此外,一些研究发现透明质酸和聚集蛋白聚糖在整个生命中持续进行合成与转换[14-15]。 2.1.3 透明质酸在软骨中的周转及降解 多数情况下,软骨细胞周围基质的透明质酸更新与组织细胞周围基质中的透明质酸不同,机体处于稳态时透明质酸更新与软骨细胞代谢发生改变时(骨关节炎、创伤、衰老)的透明质酸也不同。 新合成的透明质酸周转率为其半衰期,软骨中透明质酸的速度与聚集蛋白聚糖合成的速度非常接近。Hyaluronidase 1 (HYAL1) 是一种细胞内的溶酶体透明质酸酶,在不表达HYAL1软骨的软骨细胞中可以观察到大量的透明质酸在细胞周围和细胞内积累。HYAL2是一种细胞表面及细胞内的溶酶体透明质酸酶,最近一项条件性(Col2a-Cre) 抑制HYAL2表达的研究报道了软骨细胞周围基质中透明质酸大小及数量增加[16]。研究发现许多透明质酸酶和受体均是透明质酸转换的关键参与者,包括HYAL1-3、CD44、PH-20、KIAA和TMEM。 软骨细胞依赖CD44结合和胞吞透明质酸,其活性可通过细胞因子上调,如白细胞介素1α或白细胞介素β[17],从而促进分解代谢及增加细胞内透明质酸成倍的积累。透明质酸的大小在胞吞过程中尤为重要,有学者认为透明质酸被胞吞之前会先在软骨细胞周围基质内预切割成小片段[18],较小长度的透明质酸可以更有效地被软骨细胞内化[19]。使用超声预处理荧光标记的透明质酸来观察透明质酸被的胞吞过程,发现超声处理5 s和10 s后可以完全阻断透明质酸内化作用,而超声处理15 s后大小在200-300 kD的透明质酸则被胞吞;结果还观察到完整的聚集蛋白聚糖单体与透明质酸结合可几乎完全阻断透明质酸胞吞的过程,这表明在透明质酸胞吞之前,聚集蛋白聚糖可能先要进行某种程度的加工。为了验证这个观点,使用不影响聚集蛋白聚糖与透明质酸结合的C末端蛋白水解酶将聚集蛋白聚糖预先切割成尺寸较小的片段,结果发现随着聚集蛋白聚糖单体尺寸的减小,其限制透明质酸胞吞的能力逐渐降低。透明质酸胞吞过程示意图,见图2。"

HOLMES等[20]在分析人正常软骨中的透明质酸后发现关节内组织周围间隙的透明质酸随年龄增长而减小。儿童和年轻人的透明质酸约1 000 kD,中年成人组织透明质酸约750 kD,而老年人约500 kD。在长达近百年的生命中,一条1 000 kD的透明质酸可能发生了一两次的裂解,这也表明透明质酸周转降解过程的缓慢性。然而,人体软骨代谢的病理性改变将会对透明质酸的转化代谢过程产生较大的影响。骨关节炎是最常见的关节内疾病,许多研究通过添加促炎性细胞因子模拟人骨关节炎,发现透明质酸从软骨中大量释放,且这种现象与聚集蛋白聚糖的降解密切相关[21-23]。CHUBINSKAYA等[24]提出软骨内透明质酸和聚集蛋白聚糖聚集体的明显丢失是早期骨关节炎的关键机制。 2.2 透明质酸在关节软骨中的功能 2.2.1 透明质酸的生物力学作用 软骨细胞周围基质具有重要的生物力学功能,该区域富含蛋白多糖集聚体(聚集蛋白聚糖、透明质酸和连接蛋白)、胶原蛋白(Ⅱ,Ⅵ和Ⅸ型)和纤维连接蛋白。先前研究表明,软骨细胞通过Ⅵ型胶原蛋白锚定在细胞周围基质上,因此Ⅵ型胶原蛋白被认为是负责维持关节软骨承重能力(占20%-30%)的主要物质[25]。除胶原蛋白外,透明质酸作为基本支架所形成的蛋白多糖集聚体大约占软骨承重能力的10%[26]。聚集蛋白聚糖是关节内一种带负电荷呈刷状的蛋白聚糖大分子,其与透明质酸和连接蛋白形成的蛋白多糖集聚体具有一些软骨的重要特性,如抗压缩、抗剪切变形和液压渗透性等。早期骨关节炎由于蛋白多糖集聚体的降解和损失可导致软骨生物力学功能的改变,造成软骨承重能力的下降和连续关节负荷下进一步的关节损坏。大量透明质酸存在于软骨组织之间的滑液中,参与滑液黏度和流体动力及边界润滑等过程,发挥润滑软骨生物的作用[26]。因此透明质酸直接或间接参与了软骨生物力学功能的维持,是软骨细胞周围基质区域中不可或缺的重要成分。另有研究表明,虽然蛋白多糖集聚体的水力渗透性不会随年龄而变化,但是来自成人软骨的蛋白多糖集聚体比新生儿的蛋白多糖集聚体更坚硬[27]。 2.2.2 透明质酸的信号传导作用 透明质酸在软骨细胞信号传导中同样发挥重要作用。有学者提出软骨细胞周围基质刚度的变化和透明质酸共同组成了机械转导的功能性微环境[28],这种信号传导通过跨膜受体CD44或者透明质酸结合受体进行。信号传导传递的信息包括软骨细胞周围基质中与透明质酸组成或状态相关的变化,例如聚集蛋白聚糖的丢失或缩短、透明质酸的丢失或与其结合的其他物质的丢失[29]。当透明质酸、聚集蛋白聚糖和连接蛋白状态稳定时,信号通路能够及时传递信息,从而使软骨细胞周围基质所需的生物合成减少或分解代谢降低。但当三者之间的状态因为软骨负载或剪切力而改变时,信号会通过跨膜蛋白CD44或其他机械感受器传导至软骨细胞中,引发一系列生理改变。有研究显示,体内低分子量透明质酸具有促炎作用,而高分子量透明质酸具有抗炎特性[30],此阶段中涉及不同的生化途径,例如整联蛋白、Toll样受体及CD44等。 高剂量的透明质酸寡糖已被作为启动软骨细胞信号传导的治疗方式,透明质酸与CD44之间的相互作用可以类比为整联蛋白与细胞周围基质的相互作用。这些过程涉及受体聚集和解聚引起的通路开关的变化,以及基础细胞骨架和各种衔接蛋白的相互作用。与其他细胞不同,软骨细胞对透明质酸包被的基质没有强大的附着力,相反,将突出的富含透明质酸的细胞周围基质从软骨细胞中置换出来比置换弱黏附在透明质酸基质上的软骨细胞更有效。有研究将透明质酸寡糖转化为十糖(HA6-HA10)后成功干扰HA-CD44相互作用。在HA6向HA10转化过程中产生的HA2和HA4并没有置换基质的能力[31]。透明质酸低聚糖的优点是可以区分通过透明质酸合酶固定在细胞表面(不可置换透明质酸)和通过结合受体固定的透明质酸(可置换透明质酸)。因此,透明质酸低聚糖可以从CD44之类的受体中取代高分子量透明质酸并诱导信号传导。 软骨细胞中透明质酸介导的细胞信号传导过程激活了多种下游事件。锚定在胞膜上的蛋白多糖集聚体和细胞周围被膜的细胞共同保持了软骨细胞的静止状态,这种状态的典型体外表现是允许软骨细胞从海藻盐珠粒的酶促分离中恢复1周[32]。使用透明质酸寡糖或链霉菌透明质酸酶干预后,细胞信号传导迅速发生,与白细胞介素1α或白细胞介素1β处理后的情况不同,透明质酸寡糖处理不会导致CD44活性增强[33]。有研究证明透明质酸寡糖可以通过Toll样受体2/Toll样受体4/MyD88依赖性途径激活巨噬细胞[34]。随后其他研究也证明了Toll样受体4存在于软骨细胞上并参与了透明质酸寡糖介导的代谢途径,这种途径可以通过添加高分子量透明质酸来阻止。尽管之前提到透明质酸寡糖具有通过CD44受体取代软骨细胞表面上透明质酸和蛋白多糖集聚体的能力,但上述结果表明透明质酸寡糖诱发的信号传导不仅通过CD44途径,并且指出透明质酸酶活性在软骨细胞中透明质酸降解过程中同样发挥重要作用。 内源性或外源性透明质酸寡糖是否激活软骨中固有免疫途径仍存在争议,一个常见的问题是软骨细胞Toll样受体4途径的激活是由于实验室透明质酸寡糖制剂污染还是内源性透明质酸的降解引起的[35]。这个问题突出了透明质酸相关研究中试剂纯度的重要性,因为确实有一些药用级透明质酸寡糖在治疗中引起了软骨细胞的信号传导反应。有研究将实验室产生的透明质酸寡糖与药用级寡糖对比测试后观察到两种制剂均能刺激软骨细胞诱导型一氧化氮合酶和一氧化氮的释放[36]。另一个争议是尽管Toll样受体2和Toll样受体4在小鼠软骨中存在且具有活性,但人类软骨细胞是否表达Toll样受体4蛋白尚未明确。一些研究者用白细胞介素1β处理后未在人类软骨细胞中观察到Toll样受体2和Toll样受体4[37]。 除透明质酸直接介导的信号传导途径外,其他间接信号传导途径也可能由软骨细胞中HA-CD44相互作用所驱动。在其他系统如CD44可以与肾、乳腺和视网膜上皮细胞上的信号传导受体一起作为共受体。HA-CD44可以和SMAD1蛋白和骨形态发生蛋白7途径的转录调节剂相互作用,LUO等[38]为了明确 CD44-SMAD1和透明质酸之间的相互作用,通过Western免疫印迹检测SMAD1磷酸化和聚集蛋白聚糖信使RNA(mRNA)的表达来评估软骨细胞对骨形态发生蛋白7刺激反应的变化,发现软骨细胞周围基质对骨形态发生蛋白7信号传导至关重要,而CD44的表达则促进了细胞对低浓度骨形态发生蛋白7的反应。还有研究发现在与视网膜色素上皮细胞相关的肿瘤坏死因子α诱导上皮细胞-间充质转化过程中,CD44与2型转化生长因子受体发生免疫共沉淀并导致增殖性玻璃体视网膜病变,可能由CD44结合的转化生长因子β受体内吞进入隔室导致。软骨细胞与视网膜色素上皮细胞的差异在于CD44内吞作用受到更多的限制,例如完整的聚集蛋白聚糖结合的透明质酸不能被内吞而部分降解的聚集蛋白聚糖却可以内吞,通过这种方式,富含透明质酸的细胞周围基质改变可以通过CD44与其他受体形成的通路来进行信号传导。 2.3 透明质酸制剂用于治疗的研究进展 由于透明质酸出色的物理化学特性如高黏度、良好的生物相容性、无毒性和非免疫原性,基于透明质酸的制剂具有广泛的应用,在最近的众多研究中透明质酸是一个热门话题,并在骨关节炎治疗应用中具有显著功效。 2.3.1 抗氧化、抗炎和抗骨关节炎 骨关节炎的特征是关节产生疼痛和僵硬的同时会伴有残疾和生活质量的下降。骨关节炎会影响关节内所有的组织包括滑膜、韧带、半月板、骨骼和软骨等,累及的关节软骨退化并逐渐消失,从而导致骨与骨的直接接触。骨关节炎发生时的病理生理学改变非常复杂,数十年的研究仍未完全明确其途径和机制,普遍认为炎症和氧化应激是骨关节炎发生的主要因素,各种蛋白酶水解酶的比例失衡,氧化(超氧化物和过氧化氢)和亚硝化(一氧化氮和过氧亚硝酸盐)的产生,炎性细胞因子(白细胞介素1β、肿瘤坏死因子α和瘦素)的增加,其他物质(前列腺素E2,cAMP,NF-Κb,Toll样受体)也直接或间接参与骨关节炎进程[39]。TAKAHASHI等[40]在观察透明质酸干预兔骨关节炎模型的研究中发现,透明质酸治疗组的半月板和滑膜中一氧化氮的产生显著低于对照组,表明抑制关节内一氧化氮的产生可能是透明质酸治疗骨关节炎机制的部分原因。还有研究证明除了一氧化氮,透明质酸也可以抑制过氧化物和羟基的产生。在一项体外研究中SASAKI等[41]证明了白细胞介素1β可以诱导基质金属蛋白酶1 mRNA和基质金属蛋白酶3 mRNA的表达,透明质酸可以通过抑制白细胞介素1β与其受体结合从而显著减少基质金属蛋白酶1和基质金属蛋白酶3的产生,以此来发挥其抗炎的作用。 在骨关节炎的发展过程中,关节中内源性透明质酸可从高分子量裂解为较低分子量从而降低了其润滑和结合聚集蛋白聚糖的能力[42],因此临床透明质酸制剂注射是治疗骨关节炎患者内源性透明质酸裂解的常用方法。尽管透明质酸制剂并不能拥有内源性透明质酸的全部特性和活性,但它仍可通过前述的多种途径和机制使骨关节炎患者受益。透明质酸制剂主要有口服和局部注射两种方式,二者在之前的报道中均未观察到统计学上有显著差异的不良反应[43-44]。还有学者发现,当两种治疗方法结合使用时,口服透明质酸可以对透明质酸注射治疗产生增益效果[45]。透明质酸制剂的分子质量不同对临床治疗的影响尚存争议,2005年CUBUKCU等[46]发现在晚期膝关节骨关节炎患者中,关节内注射高分子量和低分子量透明质酸制剂后临床表现均有显著改善但无统计学意义。随后有研究发现高分子量透明质酸制剂在病程超过6个月的膝关节骨关节炎患者中疗效优于低分子量透明质酸制剂[47]。 虽然先前很多试验和荟萃分析已经评估并证明透明质酸制剂相较于安慰剂组在缓解骨关节炎患者症状中具有显著优势[48],但透明质酸制剂相较于其他治疗方法(类固醇激素、富血小板血浆和骨髓间充质干细胞等)是否更有效仍是当前研究的重点。有研究报道关节内注射类固醇激素也可减轻膝关节疼痛[49],但二者之间孰优孰劣仍存争议。最近一项前瞻性临床试验随机将 6 mL透明质酸制剂或曲安奈德溶液一次性注射于有症状的膝关节骨关节炎患者[50],观察的结果指标是6个月内膝关节疼痛的缓解程度及膝关节功能、运动范围等,研究发现注射曲安奈德的患者在24 h至1周内疼痛改善更有效,且2周内膝关节功能评分更高,但6个月后两组的疼痛评分、膝关节功能及运动范围表现出类似的疗效。注射富血小板血浆为膝关节退行性病变保守治疗提供了新的选择,富血小板血浆可以缓解症状及延迟手术干预的时间,最新的一项研究比较了关节内注射透明质酸制剂或富血小板血浆治疗膝关节骨关节炎的临床疗效[51],长期随访(2-5年)后发现二者在骨关节炎患者中均有效改善了膝关节功能和症状但并未有统计学差异。过去的20年中,细胞疗法和组织工程学方法飞速发展,间充质干细胞也成为治疗膝关节骨关节炎时一种极具发展前景的选择,其比软骨细胞治疗更有优势,间充质干细胞具有自我更新的能力并且可以保持人关节内软骨组织的正常更新和维护[52],最近有一项临床研究评估了关节内注射自体骨髓间充质干细胞联合透明质酸制剂治疗膝关节骨关节炎的安全性、可行性和有效性[53],其结果表明骨髓间充质干细胞与透明质酸联合使用比单独使用透明质酸制剂显著缓解了骨关节炎疼痛症状,并且只有大剂量骨髓间充质干细胞联合透明质酸制剂组才会在磁共振成像评分中表现优异。 2.3.2 镇痛 软骨下病变和关节内炎症及纤维化是骨关节炎诱发疼痛的主要原因[54]。关节内注射透明质酸治疗是当前非类固醇抗炎药或其他姑息性止痛治疗的主要替代治疗,有荟萃分析得出结论,透明质酸对骨关节炎的症状改善比其他治疗方式能保持更长的时间[55]。透明质酸减轻骨关节炎关节痛的机制尚未完全明确。HASHIZUME等[56]通过切除兔部分半月板建立了兔骨关节炎模型,且以后爪产生的质量分布来评估兔膝关节的疼痛情况,结果表明透明质酸和洛索洛芬给药后兔后爪质量分布较空白组分布正常,并且透明质酸和洛索洛芬均能抑制关节内前列腺素E2的产生,其中透明质酸还能显著抑制基质金属蛋白酶的产生和软骨退行性病变[56]。早期的一些研究观察到高浓度的透明质酸可以通过改变动物(大鼠、猫、狗、马和绵羊等)机械感受器活性来减轻疼痛。也有人观察不同弹性黏度的透明质酸处理非洲爪蟾卵母细胞的结果后发现,关节内注射透明质酸制剂的镇痛作用是由于关节机械感受器膜拉伸激活通道对机械力的敏感性降低[57]。有研究使用口服的透明质酸制剂来干预肥胖患者骨关节炎,结果显示透明质酸制剂组的大多数炎性细胞因子、瘦素和缓激肽生成均下降,且透明质酸的周转率和滑液流变性明显增加[58]。 2.3.3 保护、修复关节软骨及组织工程中相关应用 关节软骨是由5%的软骨细胞和95%的细胞周围基质组成[59]。在骨关节炎和类风湿性关节炎中,软骨细胞充当机械传感器和渗透传感器并与细胞周围基质互相影响,最终导致软骨的损伤。FRIZZIERO等[60]在一项40例骨关节炎患者的临床试验中,评估了透明质酸治疗后滑膜和软骨的结构变化,发现透明质酸制剂治疗后软骨细胞密度和活力显著改善,并且关节疼痛和活动度也得到了显著且持久的改善。有研究报道关节内注射透明质酸制剂可以直接影响软骨细胞、滑膜细胞及转化生长因子、成纤维细胞衍生生长因子和胰岛素样生长因子,有组织学证据证明透明质酸可防止软骨降解并促进其再生。GHOSH等[61]也发现透明质酸制剂治疗可以减轻滑膜肥大并增加滑膜成纤维样细胞的数量,同时减少巨噬细胞、淋巴细胞、肥大细胞和脂肪细胞的数量,透明质酸似乎可以通过下调细胞因子、自由基和蛋白水解酶来保护软骨。还有一项体外研究从膝关节骨关节炎患者软骨中分离软骨细胞,评估了透明质酸对自发和抗Fas诱导细胞凋亡的影响,发现透明质酸制剂可显著降低抗Fas诱导的软骨病[62]。 关节软骨内主要的蛋白多糖是蛋白多糖集聚体,透明质酸制剂可增加其合成[63],此外透明质酸还可通过细胞表面的CD44受体来增强软骨中软骨细胞增殖和基质合成,由于无血管的软骨自愈能力有限,关节外伤后可能发生严重的软骨缺损,从而显著增加骨关节炎发展的风险,透明质酸因其良好的生物相容性和生物可降解性成为软骨修复的研究重点。天然的透明质酸分子易在生物体内降解和扩散,导致停留时间极短而限制了其应用,所以通常需要将透明质酸进行化学或物理改性以改变其机械性能、生物降解性及停留时间等。有研究对透明质酸进行化学改性后制得透明质酸凝胶[64],将其应用于软骨缺损的兔模型上,8周后观察到缺损软骨得到明显改善且关节表面较光滑。最新一项研究表明透明质酸水凝胶制剂会因为无孔网格限制细胞增殖,而冰冻凝胶作为水凝胶在冷冻温度下结晶形成的一个子类具有高度连通的大孔结构以及足够的机械强度,这些特性对促进软骨修复具有重要意义[65]。除单纯应用透明质酸制剂外,近年来不同治疗方法联合透明质酸制剂的组织工程研究大量开展。有学者以负载软骨细胞的透明质酸可注射材料为载体材料来修复软骨缺损[66],结果显示这种复合材料不但具有取材方便和制备工艺简单的优点,且相较于对照组(单纯应用透明质酸制剂)和空白对照组(自然修复)明显提高了软骨修复能力,有望成为未来软骨修复的理想材料。淫羊藿是中国临床常用中药,具有促进成骨细胞分化和成熟的作用,同时淫羊藿也是一种安全而强大的软骨细胞合成代谢剂,可以增加软骨细胞增殖并减少细胞外基质的降解[67]。将淫羊藿与透明质酸制备的生物材料应用于软骨损伤严重的兔模型中,观察到淫羊藿与透明质酸制剂联合使用可促进软骨细胞的增殖及软骨下骨形成,并成为未来关节软骨修复的潜在治疗方式。除上述研究外,低强度脉冲超声、间充质干细胞等与透明质酸的复合治疗经证实也在软骨修复中具有广泛的应用前景[68-69]。 2.3.4 骨转移癌的治疗 许多癌症例如乳腺癌和前列腺癌等常常会转移到骨骼,骨骼是一种代谢活跃的组织,产生大量的细胞因子和蛋白质,为转移性癌细胞提供了独特的结构和分子微环境。其特征包括透明质酸在内的细胞周围基质的过度产生,其与细胞表面的CD44相互作用从而间接激活Rho蛋白、丝裂原活化蛋白激酶(MAPK)和胞内磷脂酰肌醇激酶(PI3K)信号级联,促进癌细胞生长、增殖、迁移、侵袭和癌前基因的转录,这些信号传导与透明质酸和其细胞表面受体结合有关。当前研究中,一种治疗方法是使用透明质酸低聚糖抑制体内转移癌的生长,透明质酸低聚糖通过与内源性透明质酸竞争对肿瘤生长具有抑制作用[70],例如破坏HA-CD44之间的相互作用。有研究发现注射透明质酸十糖制剂可以抑制体内骨肿瘤的生长,不仅可通过人乳腺癌细胞(MDA-MB-231)直接抑制,而且可对宿主基质细胞直接抑制来介导透明质酸十糖对骨转移病灶的抑制作用[71]。 "

| [1] MEYER K, PALMER JW. The polysaccharide of the vitreous humor. J Biol Chem. 1934;107:629-634. [2] IANNITTI T, LODI D, PALMIERI B. Intra-articular injections for the treatment of osteoarthritis: focus on the clinical use of hyaluronic acid. Drugs R D. 2011; 11(1):13-27. [3] Poole CA. Articular cartilage chondrons: form, function and failure. J Anat. 1997;191(Pt 1):1-13. [4] 胥少汀,葛宝丰,许印坎. 实用骨科学[M].4版.北京:人民军医出版社, 2012:48. [5] LAURENT TC, FRASER JR. Hyaluronan. FASEB J. 1992;6(7):2397-2404. [6] ONO Y, SAKAI T, HIRAIWA H, et al. Chondrogenic capacity and alterations in hyaluronan synthesis of cultured human osteoarthritic chondrocytes. Biochem Biophys Res Commun. 2013;435(4):733-739. [7] NISHIDA Y, KNUDSON CB, NIETFELD JJ, et al. Antisense inhibition of hyaluronan synthase-2 in human articular chondrocytes inhibits proteoglycan retention and matrix assembly. J Biol Chem. 1999;274(31):21893-21899. [8] MATSUMOTO K, LI Y, JAKUBA C, et al. Conditional inactivation of Has2 reveals a crucial role for hyaluronan in skeletal growth, patterning, chondrocyte maturation and joint formation in the developing limb. Development. 2009;136(16):2825-2835. [9] HUANG Y, ASKEW EB, KNUDSON CB, et al. CRISPR/Cas9 knockout of HAS2 in rat chondrosarcoma chondrocytes demonstrates the requirement of hyaluronan for aggrecan retention. Matrix Biol. 2016;56:74-94. [10] KAROUSOU E, MISRA S, GHATAK S, et al. Roles and targeting of the HAS/hyaluronan/CD44 molecular system in cancer. Matrix Biol. 2017;59:3-22. [11] KNUDSON CB. Hyaluronan receptor-directed assembly of chondrocyte pericellular matrix.J Cell Biol. 1993;120(3):825-834. [12] KNUDSON CB, NOFAL GA, PAMINTUAN L, et al. The chondrocyte pericellular matrix: a model for hyaluronan-mediated cell-matrix interactions. Biochem Soc Trans. 1999;27(2):142-147. [13] KNUDSON W, AGUIAR DJ, HUA Q, et al. CD44-anchored hyaluronan-rich pericellular matrices: an ultrastructural and biochemical analysis. Exp Cell Res. 1996;228(2):216-228. [14] MAROUDAS A, BAYLISS MT, UCHITEL-KAUSHANSKY N, et al. Aggrecan turnover in human articular cartilage: use of aspartic acid racemization as a marker of molecular age. Arch Biochem Biophys. 1998;350(1):61-71. [15] Morales TI, Hascall VC. Correlated metabolism of proteoglycans and hyaluronic acid in bovine cartilage organ cultures. J Biol Chem. 1988;263(8):3632-3628. [16] HIGUCHI Y, NISHIDA Y, KOZAWA E, et al. Conditional knockdown of hyaluronidase 2 in articular cartilage stimulates osteoarthritic progression in a mice model. Scientific reports. 2017;7(1):7028. [17] EMBRY JJ, KNUDSON W. G1 domain of aggrecan cointernalizes with hyaluronan via a CD44-mediated mechanism in bovine articular chondrocytes. Arthritis and rheumatism. 2003;48(12):3431-3441. [18] STERN R. Devising a pathway for hyaluronan catabolism: are we there yet? Glycobiology. 2003;13(12):105R-15R. [19] MCGUIRE PG, CASTELLOT JJ JR, ORKIN RW. Size-dependent hyaluronate degradation by cultured cells. J Cell Physiol. 1987;133(2):267-276. [20] HOLMES MW, BAYLISS MT, MUIR H. Hyaluronic acid in human articular cartilage. Age-related changes in content and size. Biochem J. 1988;250(2):435-441. [21] DURIGOVA M, ROUGHLEY PJ, MORT JS. Mechanism of proteoglycan aggregate degradation in cartilage stimulated with oncostatin M. Osteoarthritis Cartilage. 2008;16(1):98-104. [22] DURIGOVA M, TROEBERG L, NAGASE H, et al. Involvement of ADAMTS5 and hyaluronidase in aggrecan degradation and release from OSM-stimulated cartilage. Eur Cell Mater. 2011;21:31-45. [23] FOSANG AJ, TYLER JA, HARDINGHAM TE. Effect of interleukin-1 and insulin like growth factor-1 on the release of proteoglycan components and hyaluronan from pig articular cartilage in explant culture. Matrix. 1991;11(1):17-24. [24] CHUBINSKAYA S, CS-SZABO G, KUETTNER KE. ADAM-10 message is expressed in human articular cartilage. J Histochem Cytochem. 1998;46(6):723-729. [25] GUILAK F, ALEXOPOULOS LG, UPTON ML, et al. The pericellular matrix as a transducer of biomechanical and biochemical signals in articular cartilage. Ann N Y Acad Sci. 2006;1068:498-512. [26] HAN L, GRODZINSKY AJ, ORTIZ C. Nanomechanics of the Cartilage Extracellular Matrix. Annu Rev Mater Res. 2011;41:133-168. [27] NIA HT, HAN L, BOZCHALOOI IS, et al. Aggrecan nanoscale solid-fluid interactions are a primary determinant of cartilage dynamic mechanical properties. ACS Nano. 2015;9(3):2614-29625. [28] PREIN C, WARMBOLD N, FARKAS Z, et al. Structural and mechanical properties of the proliferative zone of the developing murine growth plate cartilage assessed by atomic force microscopy. Matrix Biol. 2016;50:1-15. [29] TOOLE BP, WIGHT TN, TAMMI MI. Hyaluronan-cell interactions in cancer and vascular disease.J Biol Chem. 2002;277(7):4593-4596. [30] AVENOSO A, D’ASCOLA A, SCURUCHI M, et al. Hyaluronan in the experimental injury of the cartilage: biochemical action and protective effects. Inflamm Res. 2018;67(1):5-20. [31] ARIYOSHI W, TAKAHASHI N, HIDA D, et al. Mechanisms involved in enhancement of the expression and function of aggrecanases by hyaluronan oligosaccharides. Arthritis and rheumatism. 2012;64(1):187-197. [32] NISHIDA Y, KNUDSON CB, KUETTNER KE, et al. Osteogenic protein-1 promotes the synthesis and retention of extracellular matrix within bovine articular cartilage and chondrocyte cultures. Osteoarthritis Cartilage. 2000;8(2):127-136. [33] OHNO S, IM HJ, KNUDSON CB, et al. Hyaluronan oligosaccharides induce matrix metalloproteinase 13 via transcriptional activation of NFkappaB and p38 MAP kinase in articular chondrocytes. J Biol Chem. 2006;281(26):17952-17960. [34] JIANG D, LIANG J, FAN J, et al. Regulation of lung injury and repair by Toll-like receptors and hyaluronan. Nat Med. 2005;11(11):1173-1139. [35] DONG Y, ARIF A, OLSSON M, et al. Endotoxin free hyaluronan and hyaluronan fragments do not stimulate TNF-alpha, interleukin-12 or upregulate co-stimulatory molecules in dendritic cells or macrophages. Scientific reports. 2016;6:36928. [36] IACOB S, KNUDSON CB. Hyaluronan fragments activate nitric oxide synthase and the production of nitric oxide by articular chondrocytes. Int J Biochem Cell Biol. 2006;38(1):123-133. [37] LIU-BRYAN R, PRITZKER K, FIRESTEIN GS, et al. TLR2 signaling in chondrocytes drives calcium pyrophosphate dihydrate and monosodium urate crystal-induced nitric oxide generation. J Immunol. 2005;174(8):5016-5023. [38] LUO N, KNUDSON W, ASKEW EB, et al. CD44 and hyaluronan promote the bone morphogenetic protein 7 signaling response in murine chondrocytes. Arthritis Rheumatol. 2014;66(6):1547-1558. [39] GUPTA RC, LALL R, SRIVASTAVA A, et al. Hyaluronic Acid: Molecular Mechanisms and Therapeutic Trajectory. Front Vet Sci. 2019;6:192. [40] TAKAHASHI K, HASHIMOTO S, KUBO T, et al. Hyaluronan suppressed nitric oxide production in the meniscus and synovium of rabbit osteoarthritis model.J Orthop Res. 2001;19(3):500-503. [41] SASAKI A, SASAKI K, KONTTINEN YT, et al. Hyaluronate inhibits the interleukin-1beta-induced expression of matrix metalloproteinase (MMP)-1 and MMP-3 in human synovial cells. Tohoku J Exp Med. 2004;204(2):99-107. [42] ALTMAN RD, MANJOO A, FIERLINGER A, et al. The mechanism of action for hyaluronic acid treatment in the osteoarthritic knee: a systematic review. BMC musculoskeletal disorders. 2015;16:321. [43] NGUYEN C, RANNOU F. The safety of intra-articular injections for the treatment of knee osteoarthritis: a critical narrative review. Expert Opin Drug Saf. 2017; 16(8):897-902. [44] XU X, JHA AK, HARRINGTON DA,et al. Hyaluronic Acid-Based Hydrogels: from a Natural Polysaccharide to Complex Networks. Soft Matter. 2012;8(12):3280-3294. [45] BURDICK JA, PRESTWICH GD. Hyaluronic acid hydrogels for biomedical applications. Adv Mater. 2011;23(12):H41-56. [46] CUBUKCU D, ARDIC F, KARABULUT N, et al. Hylan G-F 20 efficacy on articular cartilage quality in patients with knee osteoarthritis: clinical and MRI assessment. Clin Rheumatol. 2005;24(4):336-341. [47] Berenbaum F. Osteoarthritis as an inflammatory disease (osteoarthritis is not osteoarthrosis!). Osteoarthritis Cartilage. 2013;21(1):16-21. [48] PETRELLA RJ, PETRELLA M. A prospective, randomized, double-blind, placebo controlled study to evaluate the efficacy of intraarticular hyaluronic acid for osteoarthritis of the knee. J Rheumatol. 2006;33(5):951-956. [49] HEPPER CT, HALVORSON JJ, DUNCAN ST, et al. The efficacy and duration of intra-articular corticosteroid injection for knee osteoarthritis: a systematic review of level I studies. J Am Acad Orthop Surg. 2009;17(10):638-646. [50] TAMMACHOTE N, KANITNATE S, YAKUMPOR T, et al. Intra-Articular, Single-Shot Hylan G-F 20 Hyaluronic Acid Injection Compared with Corticosteroid in Knee Osteoarthritis: A Double-Blind, Randomized Controlled Trial. J Bone Joint Surg Am. 2016;98(11):885-892. [51] DI MARTINO A, DI MATTEO B, PAPIO T, et al. Platelet-Rich Plasma Versus Hyaluronic Acid Injections for the Treatment of Knee Osteoarthritis: Results at 5 Years of a Double-Blind, Randomized Controlled Trial. Am J Sports Med. 2019; 47(2):347-354. [52] JO CH, LEE YG, SHIN WH, et al. Intra-articular injection of mesenchymal stem cells for the treatment of osteoarthritis of the knee: a proof-of-concept clinical trial. Stem cells (Dayton, Ohio). 2014;32(5):1254-1266. [53] LAMO-ESPINOSA JM, MORA G, BLANCO JF, et al. Intra-articular injection of two different doses of autologous bone marrow mesenchymal stem cells versus hyaluronic acid in the treatment of knee osteoarthritis: multicenter randomized controlled clinical trial (phase I/II). J Transl Med. 2016;14(1):246. [54] FELSON DT. Developments in the clinical understanding of osteoarthritis. Arthritis Res Ther. 2009;11(1):203. [55] BANNURU RR, NATOV NS, DASI UR, et al. Therapeutic trajectory following intra-articular hyaluronic acid injection in knee osteoarthritis--meta-analysis. Osteoarthritis Cartilage. 2011;19(6):611-619. [56] HASHIZUME M, KOIKE N, YOSHIDA H, et al. High molecular weight hyaluronic acid relieved joint pain and prevented the progression of cartilage degeneration in a rabbit osteoarthritis model after onset of arthritis.Mod Rheumatol. 2010;20(5):432-438. [57] PENA EDE L, SALA S, ROVIRA JC, et al. Elastoviscous substances with analgesic effects on joint pain reduce stretch-activated ion channel activity in vitro. Pain. 2002;99(3):501-508. [58] NELSON FR, ZVIRBULIS RA, ZONCA B, et al. The effects of an oral preparation containing hyaluronic acid (Oralvisc(R)) on obese knee osteoarthritis patients determined by pain, function, bradykinin, leptin, inflammatory cytokines, and heavy water analyses. Rheumatol Int. 2015;35(1):43-52. [59] ALTMAN R, BEDI A, MANJOO A, et al. Anti-Inflammatory Effects of Intra-Articular Hyaluronic Acid: A Systematic Review. Cartilage. 2019;10(1):43-52. [60] FRIZZIERO L, GOVONI E, BACCHINI P. Intra-articular hyaluronic acid in the treatment of osteoarthritis of the knee: clinical and morphological study. Clin Exp Rheumatol. 1998;16(4):441-449. [61] GHOSH P, GUIDOLIN D. Potential mechanism of action of intra-articular hyaluronan therapy in osteoarthritis: are the effects molecular weight dependent? Semin Arthritis Rheum. 2002;32(1):10-37. [62] LISIGNOLI G, GRASSI F, ZINI N, et al. Anti-Fas-induced apoptosis in chondrocytes reduced by hyaluronan: evidence for CD44 and CD54 (intercellular adhesion molecule 1) invovement. Arthritis and rheumatism. 2001;44(8):1800-1807. [63] 杨俊龙,王艳娉,张源,等.透明质酸治疗膝骨关节炎相关机制的研究进展[J].中国疼痛医学杂志,2017,23(6):451-454. [64] 张勤勤,谌亮,岑莲,等.透明质酸凝胶的制备及其在关节软骨再生中的应用[J].现代化工,2019,39(10):128-131. [65] HE T, LI B, COLOMBANI T, et al. Hyaluronic acid-based shape-memory cryogel scaffolds for focal cartilage defect repair. Tissue Eng Part A. 2020 Oct 27. [66] 赵峰,何薇,刘少俊,等.负载软骨细胞的透明质酸可注射材料修复软骨缺损[J].中国组织工程研究,2017,21(30):4787-4792. [67] LIU MH, SUN JS, TSAI SW, et al. Icariin protects murine chondrocytes from lipopolysaccharide-induced inflammatory responses and extracellular matrix degradation. Nutr Res. 2010;30(1):57-65. [68] 郝德峰,张鲁青,刘玉栋.低强度脉冲超声联合关节腔内注射玻璃酸钠修复关节软骨缺损[J].中国组织工程研究,2017,21(30):4775-4780. [69] PARK YB, HA CW, KIM JA,et al. Single-stage cell-based cartilage repair in a rabbit model: cell tracking and in vivo chondrogenesis of human umbilical cord blood-derived mesenchymal stem cells and hyaluronic acid hydrogel composite. Osteoarthritis Cartilage. 2017;25(4):570-580. [70] SUDHA PN, ROSE MH. Beneficial effects of hyaluronic acid. Adv Food Nutr Res. 2014;72:137-176. [71] OHYA Y, TAKEDA S, SHIBATA Y, et al. Evaluation of polyanion-coated biodegradable polymeric micelles as drug delivery vehicles. J Control Release. 2011;155(1):104-110. [72] ROSEN J, NIAZI F, DYSART S. Cost-Effectiveness of Treating Early to Moderate Stage Knee Osteoarthritis with Intra-articular Hyaluronic Acid Compared to Conservative Interventions. Adv Ther. 2020;37(1):344-352. [73] TAMURA T, HIGUCHI Y, KITAMURA H, et al. Novel hyaluronic acid-methotrexate conjugate suppresses joint inflammation in the rat knee: efficacy and safety evaluation in two rat arthritis models. Arthritis Res Ther. 2016;18:79. [74] ISHIKAWA M, YOSHIOKA K, URANO K, et al. Biocompatibility of cross-linked hyaluronate (Gel-200) for the treatment of knee osteoarthritis. Osteoarthritis Cartilage. 2014;22(11):1902-1909. [75] LO GH, LAVALLEY M, MCALINDON T, et al. Intra-articular hyaluronic acid in treatment of knee osteoarthritis: a meta-analysis. JAMA. 2003;290(23):3115-3121. |
| [1] | Tan Xinfang, Guo Yanxing, Qin Xiaofei, Zhang Binqing, Zhao Dongliang, Pan Kunkun, Li Yuzhuo, Chen Haoyu. Effect of uniaxial fatigue exercise on patellofemoral cartilage injury in a rabbit [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-6. |
| [2] | Zhang Jichao, Dong Yuefu, Mou Zhifang, Zhang Zhen, Li Bingyan, Xu Xiangjun, Li Jiayi, Ren Meng, Dong Wanpeng. Finite element analysis of biomechanical changes in the osteoarthritis knee joint in different gait flexion angles [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1357-1361. |
| [3] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhou Qian, Zhang Qiang, Chen Qiu. Human salivary components and osteoporosis/osteopenia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1439-1444. |
| [4] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| [5] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| [6] | Wu Cong, Jia Quanzhong, Liu Lun. Relationship between transforming growth factor beta1 expression and chondrocyte migration in adult articular cartilage after fragmentation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1167-1172. |
| [7] | Wang Baojuan, Zheng Shuguang, Zhang Qi, Li Tianyang. Miao medicine fumigation can delay extracellular matrix destruction in a rabbit model of knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1180-1186. |
| [8] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [9] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [10] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [11] | Fan Yiming, Liu Fangyu, Zhang Hongyu, Li Shuai, Wang Yansong. Serial questions about endogenous neural stem cell response in the ependymal zone after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1137-1142. |
| [12] | Guo Jia, Ding Qionghua, Liu Ze, Lü Siyi, Zhou Quancheng, Gao Yuhua, Bai Chunyu. Biological characteristics and immunoregulation of exosomes derived from mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1093-1101. |
| [13] | Wu Weiyue, Guo Xiaodong, Bao Chongyun. Application of engineered exosomes in bone repair and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1102-1106. |
| [14] | Zhou Hongqin, Wu Dandan, Yang Kun, Liu Qi. Exosomes that deliver specific miRNAs can regulate osteogenesis and promote angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1107-1112. |
| [15] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||