Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (10): 1609-1615.doi: 10.3969/j.issn.2095-4344.3062
Previous Articles Next Articles
Calcium citrate: an interesting organic calcium biomedical material
Yang Yanan1, Li Junfeng1, Wang Li1, Liu Hengquan1, Lai Xuefei2
- 1College of Materials, Chemistry & Chemical Engineering, Chengdu University of Technology, Chengdu 610059, Sichuan Province, China; 2College of Chemical Engineering, Sichuan University, Chengdu 610064, Sichuan Province, China
-
Received:2020-05-08Revised:2020-05-13Accepted:2020-06-19Online:2021-04-08Published:2020-12-18 -
Contact:Li Junfeng, Professor, College of Materials, Chemistry & Chemical Engineering, Chengdu University of Technology, Chengdu 610059, Sichuan Province, China -
About author:Yang Yanan, Master candidate, College of Materials, Chemistry & Chemical Engineering, Chengdu University of Technology, Chengdu 610059, Sichuan Province, China
CLC Number:
Cite this article
Yang Yanan, Li Junfeng, Wang Li, Liu Hengquan, Lai Xuefei . Calcium citrate: an interesting organic calcium biomedical material[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(10): 1609-1615.
share this article
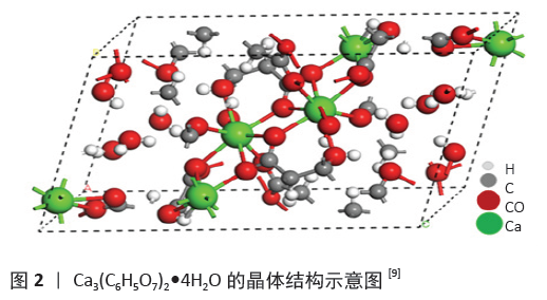
2.1 柠檬酸钙的基本性质 柠檬酸钙通常为白色结晶状粉末固体,微溶于水,能溶于酸,几乎不溶于乙醇(25 ℃,密度0.089 g/L)。通常的柠檬酸钙含有4个结晶水,其化学名为 2-羟基丙烷-1,2,3-三羧酸钙四水合物,分子式为 Ca3(C6H5O7)2?4H2O,此外还有多种水合结晶形态,如不含结晶水的Ca3(C6H5O7)2、3/2 个结晶水的Ca3(C6H5O7)2?3/2H2O、2个结晶水的 Ca3(C6H5O7)2?2H2O 及16个结晶水的Ca3(C6H5O7)2?16H2O。 Ca3(C6H5O7)2?4H2O的热分解过程可分为5个过程:第1阶段为60-140 ℃,该阶段中四水柠檬酸钙脱去2个结晶水成为二水柠檬酸钙;第2阶段为140-190 ℃,该阶段中二水柠檬酸钙再次脱去2个结晶水成为无水柠檬酸钙,此时结晶水完全脱去;第3阶段为230 ℃左右,为无水柠檬酸钙熔融过程;第4阶段为340-480 ℃,该阶段为无水柠檬酸钙分解成为CaCO3;最后一个阶段为640-780 ℃,该过程为CaCO3分解成为CaO[8]。 晶体结构研究显示Ca3(C6H5O7)2?4H2O属三斜晶系,空间群为mC204,晶格参数为:a=5.946 6(4) ?,b=10.224 7(8) ?,c=16.6496(13) ?,α=72.213(7)°,β=79.718(7)°,γ= 89.791(6)°,V=947.06(13) ?3,Z=2,R1=0.042 6,wR2=0.103 7,其结构见图2所示[9]。 "
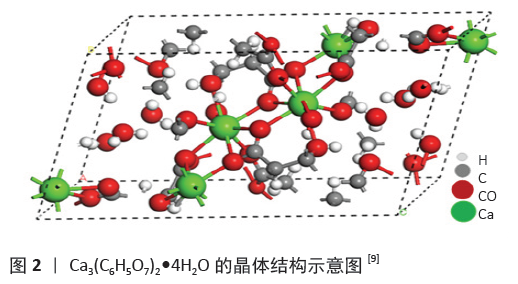
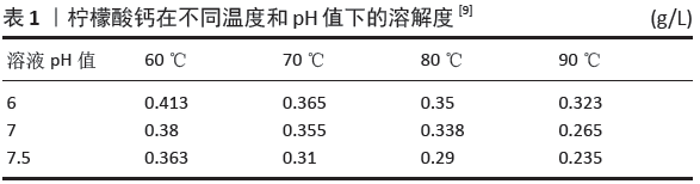
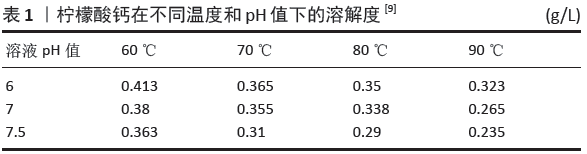
KADUK[10]进一步利用实验室同步X射线粉末衍射数据对六水柠檬酸钙、四水柠檬酸钙和无水柠檬酸钙的晶体结构进行了求解,并利用密度泛函技术进行了优化。研究结果显示六水合物和四水合物结构的特征都是边缘共享的Ca2+配位多面体层,包括三重螯合的Ca2+,另外一个孤立的Ca2+是由水分子配位的,在六水合物结构中存在2个不协调的水分子。先前报道的四水合物的多形态包含相同的层,但只有2个水分子与孤立的Ca2+和2个不协调的水分子配位。无水柠檬酸钙具有Ca2+配位多面体的三维网络结构,结果证明柠檬酸钙四水合物的多晶型是几种商业钙补充剂中的主要结晶相。 从柠檬酸钙水中的沉淀及水合结晶特性来看,如果在较低温(≤50 ℃)环境下中和通常会生成Ca3(C6H5O7)2?6H2O,它在水中溶解度较大;如在柠檬酸钠溶液中加入CaCl2则能生成凝胶状带正电荷且能溶于水的Ca3(C6H5O7)2?16H2O+,继而会失去电荷成为Ca3(C6H5O7)2?16H2O,它在冷水中会形成白色沉淀,如果升温至70 ℃则失去部分结晶水成为Ca3(C6H5O7)2?6H2O[9]。柠檬酸钙在不同温度和不同酸碱度下的溶解度见表1[9],从表中能够清楚地看出柠檬酸钙的溶解度随着温度和pH值的升高而降低。 "

在柠檬酸钙的基本性质和结构研究基础上,关于它的制备问题也逐渐被研究和发展,而且制备方法往往对它的应用性能具有重要影响[11]。 2.2 柠檬酸钙的主要制备方法 最初柠檬酸钙的制备方法多数基于柠檬酸发酵为基础,以各类薯渣、玉米小麦等作为发酵原料,由于操作过程涉及菌种的培养和发酵,整个过程需要无菌操作,对操作环境和工作人员的要求较高,工艺复杂。发酵法主要强调柠檬酸钙的收率,并不着重于柠檬酸钙的制备工艺、形貌及其他特性。近年以自然界中天然钙源制备柠檬酸钙的发展十分迅速,在此基础上开始以化工原料采用沉淀法对柠檬酸钙制备工艺进行探讨,同时关注柠檬酸钙的形貌及结构控制。 2.2.1 以鸡蛋壳作为钙源的制备工艺 鸡蛋壳具有多微孔结构,干蛋壳含碳酸钙约93%,重金属含量极低,是一种优质安全的可食用钙源。 以鸡蛋壳作为钙源制备柠檬酸钙的基本工艺为:首先以适宜浓度酸(如HCl)反应溶解蛋壳,再加入碱(如NaOH)调节pH值,最终加入柠檬酸得到柠檬酸钙[12-13]。该方法通常强调原料及工艺条件对得到柠檬酸钙产品纯度和转化率的影响,通常最终的收率都高于80%,也有较好的纯度。该方法的主要反应是: CaCO3+2HCl=CaCl2+H2O+CO2 (1) CaCl2+2NaOH=Ca(OH)2+2NaCl (2) 3Ca(OH)2+2C6H8O7=Ca3(C6H5O7)2?2H2O+4H2O (3) 采用置换法制备柠檬酸钙[14],该方法是利用介于碳酸和柠檬酸之间的有机酸(醋酸或者草酸等)与蛋壳反应先制得有机钙,有机钙再与柠檬酸反应置换出柠檬酸钙。该方法得到柠檬酸钙的产率为85.4%,纯度达 99%以上。其反应过程如下: CaCO3(蛋壳粉)+有机酸 有机酸钙+H2O+CO2 (4) 有机酸钙+2C6H8O7?4H2O Ca3(C6H5O7)2?4H2O + 有机酸 (5) 在制备过程中,先高温煅烧蛋壳,使蛋壳中的CaCO3经高温煅烧后分解为CaO,再加入柠檬酸进行反应制备柠檬酸钙,生成物中柠檬酸钙的含量为(87.84±0.51)%,该工艺较简易,但是产率一般[15]。 也有利用超声波强空化作用和机械振动破坏细胞结构,促进了蛋壳中钙的溶出[16],提高了蛋壳柠檬酸钙产率,而且超声波的空穴作用对于晶核的形成有利,提高反应速度,制备柠檬酸钙的产率均高于90%。 总的来看,以鸡蛋壳作为钙源的制备工艺,大部分是从鸡蛋壳分离纯化钙出发,然后利用柠檬酸与钙组分反应得到柠檬酸钙,不同的工艺路线和条件或许得到不同形貌、性能有差异的柠檬酸钙,但因为大多数以鸡蛋壳作为钙源的制备方法并未对此进行进一步的表征探讨,因此也无法进一步分析这些信息。 2.2.2 以贝壳作为钙源的制备工艺 贝壳中含90%以上的碳酸钙,也是一种良好的生物钙源。以贝壳作为钙源制备柠檬酸钙[17],由于贝壳杂质较多且反应活性偏弱,通常对预处理后的贝壳先采取高温煅烧得到氧化钙灰,再加入柠檬酸反应,最后中和沉淀制得产品,该方法的报道同样对于得到柠檬酸钙的形貌及性能缺少关注。其主要反应如下: CaCO3(贝壳) CaO+CO2(g) (6) CaO+H2O Ca(OH)2 (7) 3Ca(OH)2+2C6H8O7?H2O Ca3(C6H5O7)2?4H2O + 4H2O (8) 2.2.3 可溶性钙源的制备工艺 沉淀法:为提高柠檬酸钙品质和加强形貌、结构控制,可使用可溶性钙源(如氯化钙、硝酸钙、氢氧化钙)和可溶性柠檬酸盐(柠檬酸钠)或柠檬酸反应,通过液相沉淀法制得柠檬酸钙。该方法通常用2种方式改变产物的溶解度析出沉淀,一种是通过加热降低柠檬酸钙的溶解度形成沉淀;另一种是利用柠檬酸钙难溶于乙醇的特点,加入乙醇之后使柠檬酸钙的沉淀析出。用醇-水混合溶剂加热时,其原因是醇的介电常数低,加热也引起溶液介电常数下降,导致溶液的溶剂化能和混合溶液的溶解能力下降,溶液变的过饱和而析出沉淀。反应方程如下: 3CaCl2 + 2Na3C6H5O7 +4H2O = Ca3(C6H5O7)2 + 6H2O + 6NaCl (9) 使用该方法对柠檬酸钙的形貌控制效果突出,有研究使用可溶性钙盐制备得到的纤维状柠檬酸钙[18]、片状柠檬酸钙及自组织球形柠檬酸钙扫描电镜图如图3所示[19-20]。 "


HUANG等[21]通过物理制备方法采用脉冲射流磨机对柠檬酸钙进行纳米晶化,但缺点是能耗大,很难获得均匀纳米颗粒,需要进行筛选才能获得纳米级的柠檬酸钙,其形貌如图4。 水热法:HERDTWECK等[9]采用水热法制备针状柠檬酸钙,优点是该方法可以控制晶体的生长条件,如溶液的温度、溶解度等,使晶体沿某个方向定向生长,形状、生长速度等可控,缺点是由于水热法工艺复杂,设备要求高,时间长,难以工业化。 多种柠檬酸钙的制备方法逐渐被研究者重视起来,不仅是工艺的简化需要,更是对于柠檬酸钙的形貌、结构及性能的更多要求,以希望柠檬酸钙能具有更好的应用性能。 2.3 柠檬酸钙制备方法对其形貌及应用的影响 在以上制备方法中,体现出从传统的天然钙源制备到注重柠檬酸钙微观形貌控制的软化学合成变化,也体现出制备方法不断随着应用性能的需求发展进步。 作为优良的补钙剂,早期柠檬酸钙的制备方法追求产物的成本、纯度和产量,所以在制备工艺上选择简单易行的钙源置换或者钙源煅烧后反应得到柠檬酸钙,但是忽视了对所制备柠檬酸钙形貌及结构的控制。随着柠檬酸钙在抗炎剂、抗凝效果、药物缓释、生物荧光标记、骨修复材料等的研究开发,对所制备柠檬酸钙的形貌及结构提出更高要求,因此出现了通过水热法、沉淀法等制备新型的柠檬酸钙,注重了对其形貌及结构控制,钟良兆[22]也探讨过这一制备方法的变化。 当柠檬酸钙新的应用需求出现,就会有相应的制备工艺被开发,说明制备方法影响了材料的结构与形貌,进而影响了应用性能。今后随着柠檬酸钙在生物医用或其他领域新的应用进展,相适应的新制备方法一定会得到发展及完善。 2.4 柠檬酸钙的生物医用进展 2.4.1 抗炎剂 发炎是生理性宿主防御的重要组分,过量的活性氧也会导致炎症反应和氧化应激,最终产生多种生化和生理病变的形成[23]。有研究结果显示柠檬酸钙是一种有效的抗炎剂[24],它能抑制细胞内活性氧的产生,同时促进超氧化物歧化酶、过氧化氢酶、谷胱甘肽过氧化物酶等抗氧化酶的活动增加。在一些抗炎剂药物中柠檬酸钙也被作为成分加入,其中包括氢氧化铝/氢氧化镁共沉淀、氢氧化铝/碳酸氢钠共沉淀、甘氨酸铝、醋酸钙、碳酸氢钙、硼酸钙、碳酸钙等,用于治疗胃酸相关疾病和炎症性疾病的方法,使用的药物包括质子泵抑制剂、缓冲剂和非类固醇抗炎药[25]。 2.4.2 抗凝作用 安全、有效的体外抗凝对血液净化是必要的,特别是对长期持续肾脏替代治疗。与全身抗凝相比,局部柠檬酸盐抗凝具有降低出血发生率、更好的膜生物相容性、延长过滤器寿命等优点[26-28]。常用抗凝剂阻止血液凝固的原理是应用化学和物理学的方法,抑制或者除去血液中某些凝血因子,以阻止血液凝固。而能阻止血液凝固的化学试剂柠檬酸钠(枸橼酸钠),它能与血液中的钙离子形成可溶性的螯合物,使钙离子失去凝血作用,从而阻止血液凝固。 彭磊等[29]专门研究了柠檬酸钙对新鲜血液的影响,在兔血中分别加入0.0,1.0,5.0,9.0 mg的柠檬酸钙于相同体积血液中,测得凝固时间分别是(189±17),(255±21),(291±15),(300±9)s,从数据上可以明显看出柠檬酸钙的抗凝血功效,且柠檬酸钙载体在体内经过肝脏、肌肉、肾脏皮质,转化为三羧酸循环,最后以碳酸氢根结束,对临床医用来说好处明显。 2.4.3 药物载体及荧光标记 Wang等[30]在使用柠檬酸钙复合骨形态发生蛋白2的成骨实验中发现,将10 mg柠檬酸钙与2 mg骨形态发生蛋白2复合植入小鼠肌肉中较单独使用骨形态发生蛋白2对照组的成骨面积明显增多,且骨密度更高,说明柠檬酸钙与骨形态发生蛋白2复合后能诱导破骨细胞在早期出现,参与成熟骨质的重建,是一种比较理想的骨形态发生蛋白2载体材料。Wang等[5]也发现柠檬酸钙联合重组人骨形态发生2对骨缺损骨再生的促进作用,特别是植入2周的早期阶段,在柠檬酸钙和人类重组骨形态蛋白的共同作用下骨缺损部位已有成熟的松质骨形成。 还有以柠檬酸钙为基体掺杂6%的Eu3+制备具有荧光效果的柠檬酸钙粉体。柠檬酸钙作为一种新型的发光基质值得进一步开发其应用,如C12H18Ca3O18:xEu3+发光粒子可尝试用于生物荧光标记[31]。 2.4.4 补钙剂 柠檬酸钙是一种理想的钙剂,用作钙供给物时它比碳酸钙具有更高的生物利用率[32-34]。从多个不同临床数据来看,柠檬酸钙在吸收、生物利用度、耐受性或致结石性方面的性质表现不同。例如HELLER等[35]对25例绝经后妇女服用500 mg柠檬酸钙或碳酸钙+125 IU维生素D的生物利用度进行了测量,并分为3个阶段进行评估,在此期间每位妇女在早餐时服用柠檬酸钙、碳酸钙。观察发现与碳酸钙相比,柠檬酸钙在血钙浓度-时间曲线下面积增加了94%,在尿钙中增加了>41%,在血清甲状旁腺激素水平上减少了56%。对15项钙吸收和生物利用度研究的荟萃分析报告称,柠檬酸钙的吸收率比碳酸钙高22%-27%[33],从这些数据中得到柠檬酸钙中钙的生物利用度比碳酸钙高2.5倍。 ADLURI等[36]研究证明钙可以促进成骨细胞的矿化,显著提高碱性磷酸酶活性,这是成骨细胞分化的经典生物标志物。WALSDORF等[37]发明了涉及有效膳食补钙的方法和组合物,所述组合物包括在柠檬酸和乳酸或其盐存在下的钙,一方面提供了一种用于钙相关病理治疗的方法,另一个方面提供了一种用于生产复方柠檬酸-乳酸二钙的方法。有研究应用柠檬酸钙苹果酸盐治疗骨质疏松症及相关疾病,受试者接受安全有效的柠檬酸钙苹果酸盐90 d,而且柠檬酸钙苹果酸盐是口服剂型,含有药物可接受的载体和赋形剂,使药物的效果更好[38]。最常见的钙补充剂中有碳酸钙和柠檬酸钙,柠檬酸钙对比于碳酸钙可以不需食物服用,是无色素血症患者或正在服用组胺-2阻滞剂或蛋白泵抑制剂患者的首选补充剂[39]。 KOZIK-JAROMIN等[40]将微米级的柠檬酸钙使用气流粉碎得到纳米级的柠檬酸钙,然后分别将微米级和纳米级的柠檬酸钙喂养ICR小鼠,血清浓度和骨密度测试结果表明,纳米级柠檬酸钙的效果要明显优于微米级柠檬酸钙,这不仅说明了柠檬酸钙的良好补钙效果,也显示尺寸形貌会影响柠檬酸钙的性能。 2.5 骨修复的应用及机制 2.5.1 柠檬酸钙用于骨修复研究进展 MAENO等[41]发现,当局部钙浓度为2-4 mmol/L时有利于成骨细胞的增殖;6- 8 mmol/L可以促进成骨细胞在二维、三维支架上的增殖和分化;10 mmol/L以上则具有一定的细胞毒性。丁秀明等[42]用模拟体液浸泡法测定柠檬酸钙降解过程中的钙离子浓度及pH值变化,发现随着柠檬酸钙材料的逐渐降解,材料能平稳高效地释放钙离子,使溶液中的Ca2+浓度增大,慢慢稳定在7 mmol/L左右,有利于成骨细胞的增殖、分化,且柠檬酸钙在降解过程中并未明显改变体液的pH值,整个pH值在7.20-7.46之间波动,对人体刺激性少,表明柠檬酸钙具有优良的生物特性,是可选的人工骨修复材料。 ZHANG等[43]对柠檬酸钙用于日本大白兔肱骨缺损的骨整合效果进行了研究,发现当骨缺损较小时,柠檬酸钙对兔骨组织的早期愈合有积极作用,能在体内快速释放钙离子并促成新骨形成,但是柠檬酸钙难以提供长期的三维结构,这也是后期研究中会和其他骨修复材料复合的原因之一。 2016年,LI等[19]提出了一种方便有效的方法合成纳米级柠檬酸钙片状,随后的细胞和动物实验表明,所得到的柠檬酸钙可以促进MG63细胞的增殖及新骨形成。 基于以上,柠檬酸钙用于骨缺损修复表现出积极效果,但是存在无力学强度且降解快等不足,进一步的研究多聚焦于以柠檬酸钙和其他骨修复材料复合。 2.5.2 柠檬酸钙复合材料的骨修复效果 2014年,SUN等[44]研究了柠檬酸基羟基磷灰石促进颅骨修复的效果,将材料制备成盘状支架(65%羟基磷灰石,70%孔隙率)作为裸体植入物修复大鼠4 mm直径的颅骨缺损,放射学和组织学数据显示与空白组对比,使用复合材料支架处理的缺损成骨能力显著增强。这些结果表明,该复合材料裸种植体在修复骨科缺陷方面具有生物相容性、成骨性和支架可用性的潜力。 2015年,有研究将海藻酸钠与明胶液混合再加入柠檬酸钙粉末,得到凝固性能良好、可注射型的海藻酸钠-明胶-柠檬酸钙复合材料,并在合适动物实验模型中将复合材料注入骨键间隙中,结果表明该注射型海藻酸钠-明胶-柠檬酸钙对骨腱愈合具有明显的早期促进作用[45]。 Xie等[46]研制了一种可注射型柠檬酸盐复合羟基磷灰石的生物骨种植体,用于兔桡骨粉碎性骨折的治疗,结果显示与阴性对照组相比骨形成明显增加,三点弯曲强度显著增强,观察到新生血管和骨长入及高度有序的骨形成,显示出柠檬酸钙基复合材料治疗粉碎性骨折的潜力。 XIAO等[47]利用柠檬酸钙与聚乳酸的共混制备多孔复合材料,该复合材料表现出良好的力学性能,且柠檬酸钙和聚乳酸的协同降解有效中和了酸性环境,缓解了酸性产物引起的局部炎症,而且在体外28 d降解曲线可以看出该复合多孔材料的降解性良好,柠檬酸钙含量越高复合材料早期失重较明显,但在后期由于柠檬酸钙降解引起的微碱性环境中和了部分聚乳酸降解的酸性产物,抑制了复合材料的过快降解。这些研究说明柠檬酸钙的骨修复医用性较好,这对于高生物活性医用柠檬酸钙复合材料的发展是一个良好的趋势。 2.5.3 柠檬酸盐对骨磷灰石晶体生长的影响及生物矿化机制 柠檬酸钙的结构里有柠檬酸根和钙离子,很久之前就有人研究它的一些机制问题,而更多的研究是关于骨修复的矿化沉积[48],依赖于血清中存在的物理化学平衡。钙离子在这些平衡中起重要作用,了解血清总钙离子中钙离子的比例是很重要的。血清中有一部分钙与蛋白质结合在不易扩散的化合物中,CLAWSON等[49]和KLINKE[50]也支持这一结论,即血清中还有一部分钙以类似柠檬酸钙的微电离、可扩散的有机钙化合物形式存在。 RODRIGO等[51]最近也研究了柠檬酸钙在液相的耦合作用,泰勒色散测量表明三元柠檬酸+柠檬酸钙溶液中的相互扩散与二元柠檬酸和柠檬酸钙溶液中的相互扩散存在显著差异。柠檬酸-柠檬酸钙相互作用增加了柠檬酸和柠檬酸钙在三元溶液中的扩散速率,而柠檬酸钙浓度梯度驱动柠檬酸的大逆流耦合流动。这样的耦合作用或许对于骨修复过程中钙离子的稳定释放和柠檬酸根的循环有一定意义,对柠檬酸钙在骨修复过程中可控性释放的研究有所帮助,包括在骨矿化沉积过程中的钙离子滞留和流失都是一种可能因素。 认识磷灰石晶体生长的机制对骨科临床应用来说有莫大的益处,柠檬酸盐长期都被认为可以调节磷灰石晶体的生长[52-56],但是与羟基磷灰石结合的柠檬酸盐构象、相互作用官能团在羟基磷灰石表面的识别方面存在明显不足。 2008年,JIANG等[57]通过原子力显微镜方法可以在原子水平上精确直接地理解生物表面,运用模拟系统的羟基磷灰石表面与柠檬酸盐(100),它显示了只有一侧表面羧酸盐和钙离子参与绑定在柠檬酸盐上。原子力显微镜检测还发现在羟基磷灰石晶体表面存在柠檬酸盐分子,可以增强羟基磷灰石表面的结合力。 2010年,研究发现结合柠檬酸占骨有机质的5.5%[53],以约1分子/ (2 nm)2的密度覆盖磷灰石,其3个羧酸基团距离磷灰石表面0.3-0.45 nm,而且枸橼酸盐在鱼类、鸟类和哺乳动物的骨骼中含量较高,这表明它在干扰骨中磷灰石纳米晶体增厚和稳定方面具有重要作用。 2014年,有研究显示柠檬酸盐在诱导无定型前驱体的板状形貌及控制磷灰石纳米晶厚度方面具有独特的作用。该实验在柠檬酸离子存在下进行生物激发,随时间沉淀得到磷灰石纳米颗粒,且通过X射线总散射技术在结构、尺寸、形貌和组成方面对纳米磷灰石颗粒进行了表征,探讨了板状晶体形态的起源,打破了六方结构对称及柠檬酸离子的作用,而且尝试用得到的数据重构了非晶转变的可能机制[58]。 2016年,WANG等[59]使用力场基准测试和密度泛函理论计算得出,随着柠檬酸盐浓度的增加,晶体形态由针状转化为片状;存在2个不同的结合构象,1个或2个柠檬酸末端羧基与3个或5个表面钙离子相互作用,另一个是柠檬酸羟基氢键与羟基磷灰石表面之间的相互作用。 这为大家认识生物矿化沉积的自发过程提供了有力的证据,了解他们的界面反应是一个关键环节[60-61],可以解开有机分子在生物矿物形成中的作用。生物矿化过程中基质的修饰非常重要,这会使诱导矿化的物理化学及生物功能都可以受到明显调控[62-63]。柠檬酸根和钙离子在生物生长过程中扮演着不可或缺的角色,从内部结构到表面键合及官能团的构象,对于生物矿化机制来说都是最本质的认识,以后的研究可能会更加深入地认识这一问题,对于人们了解人体骨骼生长机制来说是一个非常值得期待的发现。 "

| [1] CHENG SW, WANG W, YU ZM, et al. Effects of extracellular calcium on viability and osteogenic differentiation of bone marrow stromal cells in vitro. Hum Cell. 2013;26(3):114-120. [2] SHAO CY, ZHAO RB, JIANG SQ, et al. Citrate Improves Collagen Mineralization via Interface Wetting: A Physicochemical Understanding of Biomineralization Control. Adv Mater. 2018;30(8):1704876. [3] GADOLA L, NOBOA O, MIARQUEZ MN, et al. Calcium citrate ameliorates the progression of chronic renal injury. Kidney International. 2004;65(4): 1224-1230. [4] 杨旭.柠檬酸钙骨水泥的力学性能及诱导成骨的研究[D].苏州:苏州大学,2016. [5] WANG LM, WANG W, LI XC, et al. Calcium citrate a new biomaterial that can enhance bone formation in situ. Chin J Traumatol. 2012;15(5):291-296. [6] GAO Y, LI JF, LIU YQ, et al. Shape-controlled porous carbon from calcium citrate precursor and their intriguing application in lithium-ion batteries. Ionics. 2017;23(9):2301-2310. [7] XU J, ZHANG YX, QU YN, et al. Direct Coagulation Casting of Alumina Suspension from Calcium Citrate Assisted by pH Shift. J Am Ceram Soc. 2014; 97(4):1048-1053. [8] MANSOUR SAA. Thermal decomposition of calcium citrrate tetrahydrate. Thermochimica acta. 1994; 233(2):243-256. [9] HERDTWECK E, KORNPROBST T, SIEBER R, et al. Crystal Structure, Synthesis, and Properties of tri-Calcium di-Citrate tetra-Hydrate [Ca3(C6H5O7)2(H2O)2]·2H2O. Z Anorg Allg Chem. 2011;637(6):655-659. [10] KADUK JA. Crystal structures of tricalcium citrates. Powder Diffraction. 2018;33(2):98-107. [11] HE W, LIU PJ, HE GQ, et al. Highly Reactive Metastable Intermixed Composites (MICs): Preparation and Characterization. Adv Mater. 2018; 30(41):e1706293. [12] 王卫兵,赵跃强,孙鸿.以鸡蛋壳为原料制备柠檬酸钙工艺研究[J].应用化工,2012,41(3):557-558. [13] 熊星星,司伟达,王培.蛋壳中碳酸钙转化成柠檬酸钙的研究[J].食品科技,2012,37(11):254-258. [14] 曾习,马美湖.蛋壳中碳酸钙转化为柠檬酸钙的研究[J].中国农业科技, 2010,43(5):1031-1040. [15] 李逢振,马美湖,张雯婷.鸡蛋壳中碳酸钙转化制备柠檬酸钙的研究[J].食品工业科技,2013,34(5):192-199. [16] 林松毅,魏薇,赵颂宁.超声波法制备蛋壳柠檬酸钙的工艺研究[J].食品科学,2009,33(22):126-131. [17] 罗威,许为.以贝壳为钙源一次煅烧法制取柠檬酸钙[J].中国食品添加剂,2007,2007(4):119-203. [18] ZHONG LZ, LI JF, GAO Y, et al. Preparation and characterisation of calcium citratewires. Micro Nano Lett. 2015;10(8):419-421. [19] LI J F, LIU YQ, GAO Y, et al. Preparation and properties of calcium citrate nanosheets for bone graft substitute. Bioengineered. 2016;7(5):376-381. [20] LI J F, GAO Y, ZHONG LZ, et al. Facile Self-Assembly Synthesis of Hierarchical 3D Flowerlike Calcium Citrate Microspheres. J Nano Res. 2017;45:185-192. [21] HUANG S, CHEN J C, HSU C W, et al. Effects of nano calcium carbonate and nano calcium citrate on toxicity in ICR mice and on bone mineral density in an ovariectomized mice model. Nanotechnology. 2009;20(37):375102. [22] 钟良兆.生物医用形貌可控柠檬酸钙的制备及表征[D].成都:成都理工大学,2015. [23] CONFORTI F, SOSA S, MARRELLI M, et al. The protective ability of Mediterranean dietary plants against the oxidative damage: The role of radical oxygen species in inflammation and the polyphenol, flavonoid and sterol contents. Food Chem. 2009; 112(3):587-594. [24] YOUNG CE, JU KH, SOOK HJ. Anti-inflammatory effects of calcium citrate in RAW 264.7cells via suppression of NF-kappaB activation. Environ Toxicol Pharmacol. 2015; 39(1):27-34. [25] PROEHL G T, OLMSTEAD K, HALL W.COMBINATION OF PROTON PUMP INHIBITOR, BUFFERING AGENT, AND NONSTEROIDAL ANTI NFLAMMATORY DRUG[P]. US2005O249806A1,2005. [26] BUTUROVIC-PONIKVAR J. Is Regional Citrate Anticoagulation the Future of Hemodialysis? . Ther Apher Dial. 2016;20(3):234-239. [27] TIRANATHANAGUL K, JEARNSUJITWIMOL O, SUSANTITAPHONG P, et al. Regional Citrate Anticoagulation Reduces Polymorphonuclear Cell Degranulation in Critically Ill Patients Treated With Continuous Venovenous Hemofiltration. Ther Apher Dial. 2011;15(6):556-564. [28] GRITTERS M, GROOTEMAN MPC, SCHOORL M, et al. Citrate anticoagulation abolishes degranulation of polymorphonuclear cells and platelets and reduces oxidative stress during haemodialysis. Nephrol Dial Transplant. 2006; 21(1):153-159. [29] 彭磊,杨枚,周英勇.柠檬酸钙在体外条件下对新鲜血液影响的实验研究[J].生物骨科材料与临床研究,2017,14(4):11-14. [30] WANG W, LI X C, ZHANG W, et al. Osteogenetic efect of the compound of calcium citrate and recombinant hum an bone morphogenefic. Chin J Orthop Trauma. 2011;13(10):951-954. [31] HE H, LI JF, LIU L, et al. Synthesis and characterization of Eu3+-doped C12H18Ca3O18 phosphor. Ceram Int. 2018;44(5):5070-5075. [32] TONDAPU P, PROVOST D, ADAMS-HUET B, et al. Comparison of the absorption of calcium carbonate and calcium citrate after Roux-en-Y gastric bypass. Obes Surg. 2009;19(9):1256-1261. [33] SAKHAEE K, BHUKET T, ADAMS-HUET B. Meta-analysis of calcium bioavailability: a comparison of calcium citrate with calcium carbonate. AmJ Ther. 1999;6(6):313-321. [34] NICAR MJ, PAK CY. Calcium bioavailability from calcium carbonate and calcium citrate. J Clin Endocrinol Meta. 1985;61(2):391-393. [35] HELLER HJ, GREER LG, HAYNES SD, et al. Pharmacokinetic and Pharmacodynamic Comparison ofTwo Calcium Supplements in Postmenopausal Women. J Clin Pharmacol. 2000; 40(11):1237-1244. [36] ADLURI RS, ZHAN LJ, BAGCHI M, et al. Comparative effects of a novel plant-based calcium supplement with two common calcium salts on proliferation and mineralization in human osteoblast cells. Mol Cell Biochem. 2010; 340(1-2):73-80. [37] WALSDORF NB, ALEXANDRIDES G, ANTONIO S, et al. Calcium supplementation by dicalcium citrate-lactate [P]. USA507599,1991. [38] A B, KOCHANOWSKI. Use of calcium citrate malate for the treatment of osteoporosis and related disorders [P]. US5128374A. 1992. [39] STRAUB DA. Calcium supplementation in clinical practice: a review of forms, doses, and indications. Nutr Clin Pract. 2007;22(3):286-296. [40] KOZIK-JAROMIN J, NIER V, HEEMANN U, et al. Citrate pharmacokinetics and calcium levels during high-flux dialysis with regional citrate anticoagulation. Nephrol Dial Transplant. 2009;24(7):2244-2251. [41] MAENO S, NIKI Y, MATSUMOTO H, et al. The effect of calcium ion concentration on osteoblast viability, proliferation and differentiation in monolayer and 3D culture. Biomaterials. 2005; 26(23):4847-4855. [42] 丁秀明,彭磊,文峰.模拟体液浸泡法评价柠檬酸钙的生物学特性[J].中国组织工程研究,2013,17(38):6811-6816. [43] ZHANG W, WANG W, CHEN QY, et al. Effect of calcium citrate on bone integration in a rabbit femur defect model. Asian Pac J Trop Med. 2012; 5(4):310-314. [44] SUN DW, CHEN YH, WANG YC, et al. Citric acid-based hydroxyapatite composite scaffolds enhance calvarial regeneration. SCIENTIFIC REPORTS. 2014; 4(6912):1-9. [45] AN T, CHEN Q Y, LI S, et al. Bonetendon healing enhancement using injectable gelatinsodium alginate-calcium citrate in rabbits. J Trauma Surg. 2015;17(3):247-251. [46] XIE DH, GUO JS, MEHDIZADEH MR, et al. Development of Injectable Citrate-Based Bioadhesive Bone Implants. J Mater Chem B. 2015; 21(3):387-398. [47] XIAO YF, YANG YN, LI JF, et al. Porous composite calcium citrate/polylactic acid materials with high mineralization activity and biodegradability for bone repair tissue engineering. Int J Polym Mater Polym Biomate.2020.doi.org/10.1080/00914037.2020.1740984 [48] SHEAR BMJ, KRAMER B. Composition of bone. V. Some characteristics of calcium citrate. J Biol Chem. 1928; 79(125):161-175. [49] CLAWSON AJ, GARLICH JD, COFFEY MT, et al. The effect of lactose on calcium-phosphorus balance in dogs. J Bioll Chem. 1926; 80(3):661-672. [50] KLINKE K. Neuere Ergebnisse der Calcium forschung. Ergebnisse Der Physiologie. 1927; 26(2):235-238. [51] RODRIGO MM, RIBEIRO ACF, VERISSIMO LMP, et al. Coupled diffusion in aqueous citric acid + calcium citrate solutions.J Chem Thermodyn. 2019; 131(2019):314-321. [52] RHEE SH, TANAKA J. Effect of citric acid on the nucleation of hydroxyapatite in a simulated body fluid. Biomaterials. 1999;20(22):2155-2160. [53] HU YY, RAWAL A, SCHMIDT ROHR K. Strongly bound citrate stabilizes the apatite nanocrystals in bone. Proc Natl Acad Sci USA. 2010; 107(52): 22425-22429. [54] BREDEVIC L, FFIREDI-MILHOFER H. Precipitation of Calcium Phosphates from Electrolyte Solutions. Calcif Tissue Int. 1979; 28(2):131-136. [55] MARTINS MA, SANTOS C, ALMEIDA MM, et al. Hydroxyapatite micro- and nanoparticles: nucleation and growth mechanisms in the presence of citrate species. J Colloid Interface Sci. 2008; 318(2):210-216. [56] LI CC, ZHAO LP, HAN JJ, et al. Synthesis of citrate-stabilized hydrocolloids of hydroxyapatite through a novel two-stage method: a possible aggregates-breakdown mechanism of colloid formation. J Colloid Interface Sci. 2011; 360(2):341-349. [57] JIANG W, PAN H, CAI Y, et al. Atomic Force Microscopy Reveals Hydroxyapatite-Citrate Interfacial Structure at the Atomic Level. Langmuir. 2008; 24(21):12446-12451. [58] DELGADO-LóPEZ JM, FRISON R, CERVELLINO A, et al. Crystal Size, Morphology, and Growth Mechanism in Bio-Inspired Apatite Nanocrystals. Adv Funct Mater. 2014; 24(8):1090-1099. [59] WANG Z, XU Z, ZHAO W, et al. Isoexergonic Conformations of Surface-Bound Citrate Regulated Bioinspired Apatite Nanocrystal Growth. ACS Appl Mater Interfaces. 2016; 8(41):28116-28123. [60] PAN HH, TAO JH, XU XR, et al. Adsorption processes of Gly and Glu amino acids on hydroxyapatite surfaces at the atomic level. Langmuir. 2007; 23(17):8972-8981. [61] STAYTON PS, DROBNY GP, SHAW WJ, et al. Molecular recognition at the protein-hydroxyapatite interface. Crit Rev Oral Biol Med. 2003;14(5): 370-376. [62] BELCHER AM, WU XH, CHRISTENSEN RJ, et al. Control of crystal phase switching and orientation by soluble mollusc-shell proteins. Nature. 1996; 381(6577):56-58. [63] ORME CA, NOY A, WIERZBICKI A, et al. Formation of chiral morphologies through selective binding of amino acids to calcite surface steps. Nature. 2001; 411(6839):775-779. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [3] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [4] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [5] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [6] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [7] | Jiang Hongying, Zhu Liang, Yu Xi, Huang Jing, Xiang Xiaona, Lan Zhengyan, He Hongchen. Effect of platelet-rich plasma on pressure ulcers after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1149-1153. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||