Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (21): 3409-3415.doi: 10.3969/j.issn.2095-4344.2663
Previous Articles Next Articles
Mechanism of autophagy in osteosarcoma
Li Shibin1, Zhang Xiaoyun2, Zhang Xuan3
- 1Guangxi University of Chinese Medicine; 2Department of Traumatic Orthopedics and Hand Surgery, Ruikang Hospital, Guangxi University of Chinese Medicine; 3School of Osteopathy, Guangxi University of Chinese Medicine
-
Received:2019-10-31Revised:2019-11-08Accepted:2019-12-21Online:2020-07-28Published:2020-04-19 -
Contact:Zhang Xuan, MD, Attending physician, School of Osteopathy, Guangxi University of Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China Zhang Xiaoyun, Master, Attending physician, Department of Traumatic Orthopedics and Hand Surgery, Ruikang Hospital, Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China -
About author:Li Shibin, Master candidate, Guangxi University of Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China -
Supported by:the National Natural Science Foundation of China, No. 81760796 and 81960803; the Basic Research Ability of Young and Middle-aged Teachers in Colleges and Universities of Guangxi Zhuang Autonomous Region of China, No. 2019KY0352; the Science and Research Project of Guangxi University of Chinese Medicine in 2019, No. 2019QN027; the First-Level Subject Project of Guangxi University of Chinese Medicine, No. 2019XK029; the PhD Research Startup Foundation of Guangxi University of Chinese Medicine in 2017, No. B170045
CLC Number:
Cite this article
Li Shibin, Zhang Xiaoyun, Zhang Xuan. Mechanism of autophagy in osteosarcoma[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(21): 3409-3415.
share this article
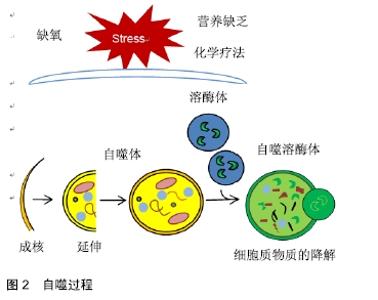
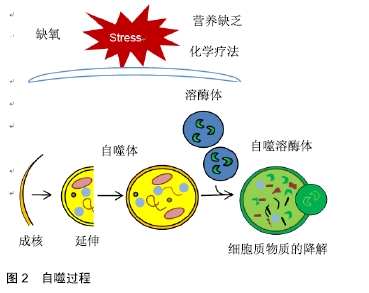
2.1 自噬 自噬是一种动态过程,它促进细胞器和蛋白质的周转,并通过溶酶体依赖性降解大分子、细胞器和其他细胞成分产生代谢前体分子[6]。其过程分为几个步骤,包括起始、成核、延伸、闭合、成熟和降解或挤出(见图2),所有步骤都由30多个自噬相关(Atg)基因调节。在营养缺乏、缺氧条件或化疗治疗的情况下,ATG1复合物的活化诱使扁平膜池、吞噬细胞或隔离膜形成,并通过激活由VPS34、磷脂酰肌醇3激酶(phospho Inositide3-Kinase,PI3K)和Beclin1(第一特征性自噬蛋白之一)形成的复合物而成核。这些复合物和其他因素的相互作用有助于重新聚集自噬体形成所必需的蛋白质和脂质[7]。 "
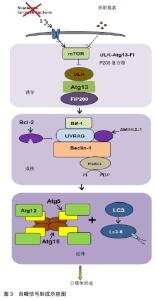
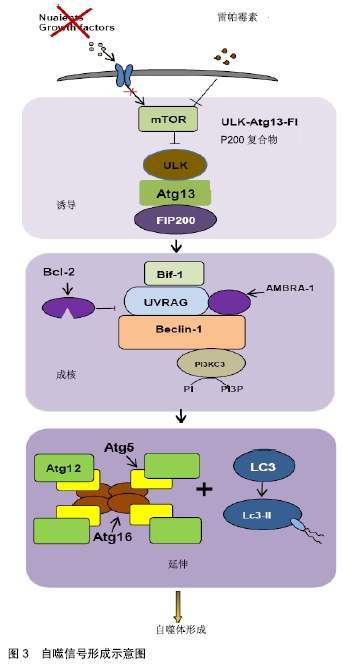
下一步是延伸,这一步由2个泛素样系统介导。第1个系统参与Atg12、Atg5和Atg16复合物的构成,该复合物由E1样酶Atg7介导。第2个系统介导主要表现为LC3首先合成为未加工形式的Prolc3,再转化为蛋白水解形式的LC3-Ⅰ,LC3-Ⅰ由蛋白酶Atg4切割经修饰形成PE结合型LC3-Ⅱ,并由细胞质转移到自噬体膜[8-9]。在这个过程中,溶酶体与自噬体相融合并形成自溶体。 最后,蛋白质在自溶体中分解,氨基酸开释到细胞质中。这些产物可参与蛋白质的合成,以产生ATP用于细胞存活。目前发现除了细胞成分的周转,自噬还参与各种组织的发育、分化和组织重塑。此外,自噬被认为是一种独特的信号途径,它影响许多病理状况,如肿瘤的发生和癌症治疗耐药性。目前自噬的失调已经与许多人类疾病联系在一起,并在肿瘤研究中越来越受到关注。 2.2 骨肉瘤自噬的调节机制 2.2.1 miRNAs调节的自噬与骨肿瘤 微小核糖核酸(miRNAs)是内源性非编码核糖核酸,在哺乳动物的一系列细胞过程中调节基因表达。目前miRNAs与自噬相关性成为研究热点,许多研究表明,多种miRNAs被认为是肿瘤发生发展中的关键表观遗传调节因子,包括骨肉瘤[10]。 miRNAs控制几个基本的生物进程,自噬也不例外,目前已发现miRNAs通过对各种自噬调节蛋白的作用来调节自噬。例如,在化疗过程中,骨肉瘤细胞的自噬会被miR-22抑制[11]。另外miR-141在许多人类疾病中调节自噬[12-13],其在骨肉瘤中呈下调的表现,并促进骨肿瘤的发生[14-15]。实验中表明SNHG15的上调与组织中miR-141的表达呈负相关,SNHG15敲除和miR-141过表达显著抑制细胞自噬、增殖、侵袭、迁移。而SNHG15过表达和miR-141抑制对骨肉瘤细胞的作用相反。此外,SNHG15能直接与miR-141相互作用,调节其表达[16]。因此miR-141的过分表达除了减低骨癌细胞增殖,也引诱细胞凋亡。且根据MEI等[17]报道,miR-200家族微小核糖核酸可以调节骨肉瘤的体内外自噬,激活miR-200家族可能具有抗骨肉瘤作用。 目前发现miRNAs不编码蛋白质,但它们控制蛋白质编码基因信使核糖核酸的稳定性和翻译,并改变由其编码的蛋白质的丰度,通过这种方式,miRNAs调节和协调细胞途径,包括细胞生长、分化、凋亡和迁移途径[18]。 2.2.2 Beclin1调节的自噬与骨肿瘤 Beclin1是死亡相关蛋白激酶(death associated protein kinase,DAPK)的一种新磷酸化底物。其结构具有3个可识别的结构域,包括短的Bcl-2-同源性-3(BH3)基序、中心螺旋环域(CCD)和包含进化保守域(ECD)的C端半结构。是第一个被鉴定的哺乳动物自噬基因,它通过与PI3KCIII/ Vps34和其他正负共因子如Bcl-2/Bcl-XL、Vps15、ATG14L/ Barkor、Rubicon、Ambra1、高迁移率族蛋白B1和Survivin结合形成Beclin-1胞间体来积极调节自噬[19]。 Beclin1由直接相互作用调节,既通过蛋白如ATG14L1和AMBRA1(Beclin1调节的自噬中的激活分子)正向调节[20-21],也通过直接相互作用负向调节,包括含BH3的癌基因和抗凋亡蛋白BCL-2和Bim[22-23]。有趣的是,c-Jun末端激酶也可能参与另一个BH3家族成员Bim的磷酸化。Bim桥接Beclin1-dynein轻链1相互作用,从而通过将Beclin1错定位于dynein运动复合体来抑制自噬。饥饿对Bim磷酸化实行催化,并致使其从Beclin1中解离,从而引诱自噬。据报道,包括雷帕霉素、死亡相关蛋白激酶Beclin1和胱天蛋白酶的机械靶标在内的几个重要信号通路参与了自噬过程[19,24]。此前在许多肿瘤类型里,包括人类乳腺癌、脑瘤和前列腺癌中都有下调Beclin1的表现[25-26]。而在最近的研究中将Beclin 1基因质粒转染到MG63人骨肉瘤细胞系中,并监测自噬进程,不出所料,随着Beclin1的过度表达,LC3B的表达和自噬活性增强,表明Beclin1的功能促进了MG63肿瘤细胞系的自噬过程[27]。因此,beclin1诱导的自噬可能影响化疗诱导的癌细胞凋亡。目前已经有许多研究证明Beclin1与许多疾病有关,然而,Beclin1介导的自噬在骨肉瘤中的确切作用和分子机制至今仍不清楚。 2.2.3 PI3K/AKT/哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)通路调节的自噬与骨肿瘤 自噬信号的经典途径通过mTOR起作用,mTOR在PI3K/AKT下游被激活,对于控制翻译和细胞周期进程以及自噬的负调节非常重要。其成核2种复合物:mTOR1和mTOR2。自噬的一个主要调节因子是mTORC1,mTORC2也有助于通过AKT途径调节来控制自噬。在正常条件下,mTORC1通过直接灭活ULK1/2蛋白复合物来控制自噬[28]。这些复合物是细胞途径的关键和必需的调节剂,控制着基因翻译和核糖体生物发生的启动,并对细胞代谢、脂解和自噬表现出重要的监测作用[29-31]。 自噬信号形成的示意图见图3。当营养或生长因子缺乏,或用雷帕霉素处理导致mTOR的抑制和ULKeAtg13eFIP200复合物的激活,这诱导自噬体的构成[32]。首先,自噬液泡的合成需要囊泡成核,这需要组装的PI3KC3复合体。在这个复合体中,Beclin-1(Atg6)作为结合PI3K 3(Vps34)、UVRAG、Bif-1和AMBRA-1的平台,它们都积极调节PI3K 3活性[33]。饥饿过程中,Bcl-2磷酸化,分泌Beclin1并刺激自噬[34]。PI3K 3(Vps34)合成物的活化最终致使PI3P的生成。最后,细胞质内容物递送至溶酶体,在溶酶体成分中融合,然后降解并再循环。 "

目前PI3K/AKT/mTOR通路已经受到研究者的关注,作为自噬途径的主要上游调节剂,含有mTOR蛋白质复合物和该途径中的其他蛋白质被证明是许多miRNAs的直接或间接靶标,更深层次的了解其作用机制对于骨肉瘤的治疗有更好的效果。 2.2.4 高迁移率族蛋白B1调节的自噬与骨肿瘤 高迁移率族蛋白B1是一种具有氧化还原敏感性的应激传感器,由炎症细胞主动性分泌,也可以被动的由损伤/坏死细胞释放。1973年首次将其确定为一组酸性和碱性氨基酸量较高的染色质结合蛋白。自从它被发现以来,高迁移率族蛋白B1已经卷入了许多疾病状态,包括炎症、免疫紊乱和癌症。 在癌症中,高迁移率族蛋白B1的功能障碍已经被证实与癌症的所有核心特征相关联[35],导致骨肉瘤细胞产生耐药性的一个重要因素是由其参与的自噬,因此抑制高迁移率族蛋白B1和自噬能够增加骨肉瘤细胞体内和体外的药物敏感性。研究表明,高迁移率族蛋白B1在不同的肿瘤模型(如白血病、结肠癌和胰腺癌)中调节其他抗癌药物(如阿糖胞苷、三氧化二砷、长春新碱、美罗华、紫杉醇和吉西他滨)的疗效,目前主要关注甲氨蝶呤、阿霉素和顺铂等,因为这些药物通常用于骨肉瘤。shRNA对高迁移率族蛋白B1的抑制作用降低了骨肉瘤细胞的自噬,减弱了对这些抗癌药物的耐受性,而cDNA转染的HMBG1的表达增强了体外细胞的自噬能力和抗化疗能力。然而,雷帕霉素对其基因敲除细胞的保护作用较小,因为其自噬能力减弱。这些结论证实了高迁移率族蛋白B1是一种主要的调控自噬介导的细胞存活[6]。此外有实验数据表明:高迁移率族蛋白B1通过控制Beclin 1/PI3KC3复合物的形成,在自噬的调节中起到主要作用,这些发现揭示了骨肉瘤治疗的新的方向[36]。通过发展一种新的靶向高迁移率族蛋白B1介导的骨肉瘤患者耐药性的治疗策略来提高癌症化疗的疗效,未来的方向可能包括将高迁移率族蛋白B1的表达水平与化疗耐药和人类骨肉瘤患者的治疗结果联系起来。 2.2.5 STAT3调节的自噬与骨肿瘤 信号转导子和转录激活子(signal transducers and activators of transcription,STAT)蛋白是一个由6个转录因子组成的家族,首先以其在细胞因子信号传导中的作用为特征。这些多功能蛋白可在特定的酪氨酸残基上磷酸化,引起构象变化,随后发生sh2结构域依赖性二聚化[37]。STAT3最初被鉴定为一种转录因子,由白细胞介素6激活,参与炎症、肿瘤发生和代谢紊乱[38]。最近研究发现STAT3在调节自噬中发挥不可忽视的作用[39]。其在细胞中以基础水平表达,通过自激活快速增加,在大多数恶性肿瘤中是组成型激活的或维持转化表型所需的。作为许多致癌信号通路的汇聚点,转录因子STAT3通过下游信号分子如BCL-2和细胞周期蛋白D1参与细胞生长。在骨肉瘤细胞中阿帕替尼的作用以及siRNA抑制STAT3的研究中,进一步证实了阿帕替尼治疗的骨肉瘤细胞中STAT3信号的负调节,与Apatinib治疗相一致,STAT3的下调会导致细胞凋亡,且与切割的PARP的增加相一致,并导致自噬、LC3-II表达的增加、Beclin-1表达的增强。这些结果表明,STAT3失活与阿帕替尼诱导的细胞增殖抑制、诱导凋亡和自噬相关[40]。值得注意的是,许多研究有助于揭示STAT3在自噬中的作用。然而,最近的一些研究并没有区分STAT3信号在自噬中的转录和非转录功能。因此,如果未来的研究能解决这些差异,就能更好地了解STAT3的作用。 2.3 自噬与骨肉瘤的化学耐药性 骨肉瘤是骨中最常见的间充质肉瘤,尽管在操作系统诊断和治疗方面已经做出了巨大的努力,但是化疗耐药性仍然是导致5年生存率低的主要问题[41]。近年来,越来越多的证据表明GFRA1介导的自噬对骨肉瘤中顺铂耐药性的发展至关重要,其促进了体内对顺铂的自噬反应,并且这种自噬反应促进了骨肉瘤肿瘤的存活。GFRA1是顺铂诱导骨肉瘤化疗耐药性的关键调节剂,顺铂通过NFKB1信号转导增加GFRA1的表达,诱导其下游激酶SRC磷酸化,随后增强AMPK-MTOR介导的自噬,这有助于化疗耐药性,GFRA1可能是预防骨肉瘤和其他类型癌症化疗耐药性的潜在治疗靶点[42]。此外,有研究表明紫杉醇治疗可增强ST2M1在U2OS细胞中的表达,随着自噬的激活,STMN1表达下调抑制紫杉醇诱导的自噬,增强紫杉醇对U2OS细胞的细胞毒作用。另外在其他肿瘤中所示,自噬通过促进细胞存活和肿瘤细胞对化疗的抗性或者通过作为化疗诱导细胞死亡的机制之一而发挥双重作用。然而目前的研究关于自噬在肿瘤细胞对化疗的敏感性或耐药性中的作用了解是有限的,接下来更好地理解控制自噬过程的分子途径将有助于识别调节这些途径的模式,从而增强化疗的活性。 2.4 自噬与骨肉瘤的转移性 肺转移仍然是骨肉瘤患者目前需要面临的重要问题,目前一直在寻找新的治疗策略。研究发现自噬能够促进也能抑制肿瘤转移。 自噬促进肿瘤转移。自噬可通过抵抗失巢凋亡来发挥促进肿瘤转移的作用,“失巢凋亡”是细胞-基质相互作用不足导致的。研究中发现癌细胞能够主要通过整合素的调节和上皮间充质转化的启动来促进失巢凋亡抗性[43]。在正常上皮细胞中,自噬和失巢凋亡可作为适应外界刺激的重要方式,例如通过维持细胞内环境稳定来分离细胞外基质;但在原发性肿瘤中,自噬大概起到促进转移的作用,通过使肿瘤细胞抵抗失巢凋亡从而增进转移[44]。另外还发现自噬可以通过维持抗氧化、抗DNA损伤、产生三磷酸腺苷等一系列正常的线粒体功能来降低细胞凋亡的可能性,以达到促进肿瘤转移的效果[45]。 自噬抑制肿瘤转移。自噬可能通过减轻代谢应激和与细胞凋亡同时防止坏死导致的死亡进而抑制巨噬细胞浸润的炎症来抑制肿瘤。肿瘤细胞侵袭和转移的可能性取决于肿瘤微环境,由于肿瘤相关巨噬细胞(TAMs)主要构成了肿瘤微环境,它们在增进这些过程中起着主导地位。经典激活的(M1)巨噬细胞受到微生物底物如脂多糖、toll样受体配体和细胞因子如干扰素g的刺激,并参与Th1型反应被激活,M1巨噬细胞释放促炎细胞因子,如白细胞介素6、白细胞介素12、白细胞介素23和肿瘤坏死因子α,具有很强的杀微生物和抗肿瘤功能。替代激活的(M2)巨噬细胞受白细胞介素4和白细胞介素13刺激,分泌白细胞介素10、转化生长因子B和趋化因子,参与组织重塑并发挥抗肿瘤作用[46]。此外,自噬通过调节高迁移率族蛋白B1等免疫调节因子抑制肿瘤转移。死亡肿瘤细胞选择性释放高迁移率族蛋白B1,激活树突状细胞触发抗肿瘤免疫应答,阻止肿瘤细胞转移[47]。 综上所述自噬在肿瘤转移过程中有双重作用,如果能够了解自噬在肿瘤转移中角色转变的机制有可能开发出利于抗肿瘤转移的有效药物。 2.5 骨肉瘤细胞自噬与凋亡 细胞凋亡,是一种基因调控的现象,其特征是细胞膜起泡、细胞收缩、核分裂、染色质凝聚、脱氧核糖核酸分裂和凋亡小体的形成[48]。在各种肿瘤的化疗中细胞凋亡是不可缺少的[49]。凋亡由2个中心途径介导,当线粒体外膜通透化后,包括细胞因子c和AIF在内的分子释放到胞质溶胶中时,线粒体凋亡途径继续进行[50]。骨肉瘤细胞的实验中表明,KNK437诱导热休克蛋白70进一步加剧黄芩素诱使的细胞凋亡,相反,热休克蛋白70的过度表达拯救了黄芩素诱导的细胞凋亡,热休克蛋白70的过表达激活ERK和AKT,然后启动下游信号事件,包括部分抑制黄芩素诱导的凋亡。这说明热休克蛋白70通过MAPK/ERK和PI3K/AKT信号途径发挥保护作用[51]。热休克蛋白70的表达对肿瘤细胞的存活和细胞凋亡的抑制具有重要意义。且在实验中还发现凋亡抑制通过JNK信号通路加强姜黄素诱导的自噬,姜黄素诱导细胞凋亡的机制大概与MG63细胞caspase3通路的激活有关;值得注意的是,JNK抑制剂SP600125有效逆转联合治疗诱导的MG63细胞自噬,提示JNK途径信号在姜黄素诱导的自噬中可能具有重要作用。且当MG63细胞的自噬被3-MA完全抑制时,姜黄素诱导的凋亡增加[52]。这些结果为了解骨肉瘤细胞凋亡和自噬之间的相互作用提供了重要的线索。 "

| [1] OTTAVIANI G, JAFFE N .The epidemiology of osteosarcoma. Cancer Treat. Res.2009;152:3-13. [2] HATTINGER CM, FANELLI M, TAVANTI E, et al. Advances in emerging drugs for osteosarcoma.Expert Opin Emerg Drugs. 2015;20: 495-514. [3] RAYMOND AK, JAFFE N. Osteosarcoma multidisciplinary approach to the management from the pathologist's perspective. Cancer Treat. Res.2009;152: 63-84. [4] GOBIN B, MORICEAU G, ORY B, et al. Imatinib mesylate exerts anti-proliferative effects on osteosarcoma cells and inhibits the tumour growth in immunocompetent murine models. PLoS ONE. 2014;9: e90795. [5] DE SC, PIETRABISSA A, MOSCA F, et al. Methylation of quercetin and fisetin, flavonoids widely distributed in edible vegetables, fruits and wine, by human liver.Int J Clin Pharmacol Ther. 2002;40: 207-212. [6] HUANG J, LIU K, YU Y, et al. Targeting HMGB1-mediated autophagy as a novel therapeutic strategy for osteosarcoma. Autophagy.2012;8: 275-277. [7] DUPREZ L, WIRAWAN E, VANDEN BT, et al. Major cell death pathways at a glance.Microbes Infect. 2009;11: 1050-1062. [8] GOZUACIK D, KIMCHI A. Autophagy as a cell death and tumor suppressor mechanism.Oncogene.2004;23: 2891-2906. [9] LIU EY, RYAN KM. Autophagy and cancer - issues we need to digest.J Cell Sci. 2012;125(Pt 10):2349-2358. [10] BERLANGA P, MUÑOZ L, PIQUERAS M, et al. miR-200c and phospho-AKT as prognostic factors and mediators of osteosarcoma progression and lung metastasis.Mol Oncol. 2016;10: 1043-1053. [11] LI X, WANG S, CHEN Y, et al. miR-22 targets the 3′ UTR of HMGB1 and inhibits the HMGB1-associated autophagy in osteosarcoma cells during chemotherapy.Tumor Biology.2014; 35(6):6021-6028. [12] ZHU H, HUANG LI, ZHU S, et al. Regulation of autophagy by systemic admission of microRNA-141 to target HMGB1 in l-arginine-induced acute pancreatitis in vivo.Pancreatology. 2016;16:337-346. [13] YANG Y, LIU Y, XUE J, et al. MicroRNA-141 Targets Sirt1 and Inhibits Autophagy to Reduce HBV Replication.Cell Physiol Biochem.2017;41: 310-322. [14] XU H, MEI Q, XIONG C, et al. Tumor-suppressing effects of miR-141 in human osteosarcoma.Cell Biochem Biophys. 2014;69:319-325. [15] CUI SQ, WANG H. MicroRNA-144 inhibits the proliferation, apoptosis, invasion, and migration of osteosarcoma cell line F5M2.Tumour Biol.2015;36: 6949-6958. [16] LIU K, HOU Y, LIU Y, et al. LncRNA SNHG15 contributes to proliferation, invasion and autophagy in osteosarcoma cells by sponging miR-141. J Biomed Sci.2017; 24: 46. [17] MEI Q, LI F, QUAN H, et al. Busulfan inhibits growth of human osteosarcoma through miR-200 family microRNAs in vitro and in vivo.Cancer Sci.2014;105: 755-762. [18] WHITE E, KARP C, STROHECKER AM, et al. Role of autophagy in suppression of inflammation and cancer. Curr Opin Cell Biol. 2010;22(2):212-217. [19] KANG R, ZEH HJ, LOTZE MT, et al. The Beclin 1 network regulates autophagy and apoptosis. Cell Death Differ. 2011; 18(4):571-580. [20] ZHONG Y, WANG QJ, LI X, et al. Distinct regulation of autophagic activity by Atg14L and Rubicon associated with Beclin 1–phosphatidylinositol-3-kinase complex.Nature Cell Biology.2009; 11(6):468-476. [21] FIMIA GM, STOYKOVA A, ROMAGNOLI A, et al. Ambra1 regulates autophagy and development of the nervous system. Nature.2007;447: 1121-1125. [22] MAIURI MC, LE TG, CRIOLLO A, et al. Functional and physical interaction between Bcl-XL and a BH3-like domain in Beclin-1. EMBO J.2007; 26(10):2527-2539. [23] LUO S, GARCIA AM, ZHAO R, et al. Bim Inhibits Autophagy by Recruiting Beclin 1 to Microtubules. Molecular Cell. 2012; 47(3):359-370. [24] KIM J,KUNDU M, VIOLLET B , et al. AMPK and mTOR regulate autophagy through direct phosphorylation of Ulk1. Nat Cell Biol. 2011;13(2):132-141. [25] YORIMITSU T, KLIONSKY DJ. Eating the endoplasmic reticulum: quality control by autophagy. Trends Cell Biol. 2007; 17(6):279-285. [26] AITA VM, LIANG XH, MURTY VV, et al. Cloning and Genomic Organization of Beclin 1, a Candidate Tumor Suppressor Gene on Chromosome 17q21. Genomics.1999;59(1):60-65. [27] TAO H, CHEN F, LIU H, et al.Wnt/β-catenin signaling pathway activation reverses gemcitabine resistance by attenuating Beclin1-mediated autophagy in the MG63 human osteosarcoma cell line.Mol Med Rep.2017;16: 1701-1706. [28] MIZUSHIMA N, YOSHIMORI T, OHSUMI Y. The role of Atg proteins in autophagosome formation.Annu Rev Cell Dev Biol.2011;27: 107-132. [29] LAPLANTE M, SABATINI D. mTOR Signaling in Growth Control and Disease.Cell. 2012;149(2):274-293. [30] ZONCU R, EFEYAN A, SABATINI DM. mTOR: from growth signal integration to cancer, diabetes and ageing. Nat Rev Mol Cell Biol. 2011;12(1):21-35. [31] BEAUCHAMP EM, PLATANIAS LC .The evolution of the TOR pathway and its role in cancer.Oncogene. 2013;32(34): 3923-3932. [32] JUNG CH, JUN CB, RO SH, et al. ULK-Atg13-FIP200 Complexes Mediate mTOR Signaling to the Autophagy Machinery.Mol Biol Cell. 2009;20(7):1992-2003. [33] PATTINGRE S, ESPERT L, BIARD PM, et al. Regulation of macroautophagy by mTOR and Beclin 1 complexes. Biochimie.2008;90(2):313-323. [34] WEI Y, PATTINGRE S, SINHA S, et al. JNK1-mediated phosphorylation of Bcl-2 regulates starvation-induced autophagy. Molecular Cell.2008;30(6):678-688. [35] GUO ZS ,LIU Z, BARTLETT DL, et al. Life after death: targeting high mobility group box 1 in emergent cancer therapies.Am J Cancer Res. 2013;3(1):1-20. [36] HUANG J, NI J D, LIU K, et al. HMGB1 promotes drug resistance in osteosarcoma.Cancer Res.2012; 72: 230-238. [37] LEVY DE, DARNELL JE. STATS: Transcriptional control and biological impact. Nat Rev Mol Cell Biol.2002;3(9):651-662. [38] YU H, PARDOLL D, JOVE R. STATs in cancer inflammation and immunity: a leading role for STAT3. Nat Rev Cancer. 2009;9(11):798-809. [39] YOU LK, WANG ZG, LI HS, et al. The role of STAT3 in autophagy.Autophagy.2015;11: 729-739. [40] LIU KS, REN TT, HUANG Y, et al. Apatinib promotes autophagy and apoptosis through VEGFR2/STAT3/BCL-2 signaling in osteosarcoma.Cell Death Dis.2017;8:e3015. [41] THOMPSON LD.Osteosarcoma.Ear Nose Throat J.2013; 92(7):288, 290. [42] KIM M, JUNG J, CHOI S, et al.GFRA1 promotes cisplatin-induced chemoresistance in osteosarcoma by inducing autophagy.Autophagy.2017;13: 149-168. [43] CAO Z, LIVAS T, KYPRIANOU N. Anoikis and EMT: Lethal "Liaisons" during Cancer Progression.Crit Rev Oncog. 2016; 21(3-4):155-168. [44] YANG J, ZHENG Z, YAN X, et al. Integration of autophagy and anoikis resistance in solid tumors.Anat Rec (Hoboken). 2013;296:1501-1508. [45] WHITE E, MEHNERT JM, CHAN CS. Autophagy, metabolism, and cancer. Clin Cancer Res. 2015;21(22):5037-5046. [46] FAN X, ZHANG H, CHENG Y, et al. Double Roles of Macrophages in Human Neuroimmune Diseases and Their Animal Models.Mediators Inflamm.2016;2016: 8489251. [47] APETOH L, GHIRINGHELLI F, TESNIERE A, et al. Toll-like receptor 4–dependent contribution of the immune system to anticancer chemotherapy and radiotherapy. Nat Med.2007; 13(9):1050-1059. [48] URGESS DJ. Apoptosis: Refined and lethal.Nat Rev Cancer. 2013;13: 79. [49] ZIMMERMANN KC, BONZON C, GREEN DR. The machinery of programmed cell death.Pharmacol Ther.2001; 92(1):57-70. [50] VERESOV VG, DAVIDOVSKII AI. Activation of Bax by joint action of tBid and mitochondrial outer membrane: Monte Carlo simulations. Eur Biophys J. 2009;38(7):941960. [51] DING L, HE S, SUN X. HSP70 desensitizes osteosarcoma cells to baicalein and protects cells from undergoing apoptosis. Apoptosis.2014;19(8):1269-1280. [52] ZHANG Y, CHEN P, HONG H, et al.JNK pathway mediates curcumin-induced apoptosis and autophagy in osteosarcoma MG63 cells.Exp Ther Med.2017;14: 593-599. |
| [1] | Geng Qiudong, Ge Haiya, Wang Heming, Li Nan. Role and mechanism of Guilu Erxianjiao in treatment of osteoarthritis based on network pharmacology [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1229-1236. |
| [2] | Pei Lili, Sun Guicai, Wang Di. Salvianolic acid B inhibits oxidative damage of bone marrow mesenchymal stem cells and promotes differentiation into cardiomyocytes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1032-1036. |
| [3] | Li Shibin, Lai Yu, Zhou Yi, Liao Jianzhao, Zhang Xiaoyun, Zhang Xuan. Pathogenesis of hormonal osteonecrosis of the femoral head and the target effect of related signaling pathways [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 935-941. |
| [4] | Ma Zetao, Zeng Hui, Wang Deli, Weng Jian, Feng Song. MicroRNA-138-5p regulates chondrocyte proliferation and autophagy [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 674-678. |
| [5] | Xie Yang, Zhang Shujiang, Liu Menglan, Luo Ying, Yang Yang, Li Zuoxiao. Mechanism by which rapamycin protects spinal cord neurons in experimental autoimmune encephalomyelitis mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 695-700. |
| [6] | Xu Yinqin, Shi Hongmei, Wang Guangyi. Effects of Tongbi prescription hot compress combined with acupuncture on mRNA expressions of apoptosis-related genes,Caspase-3 and Bcl-2, in degenerative intervertebral discs [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 713-718. |
| [7] | Zhang Wenwen, Jin Songfeng, Zhao Guoliang, Gong Lihong. Mechanism by which Wenban Decoction reduces homocysteine-induced apoptosis of myocardial microvascular endothelial cells in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 723-728. |
| [8] | Liu Qing, Wan Bijiang. Effect of acupotomy therapy on the expression of Bcl-2/Bax in synovial tissue of collagen-induced arthritis rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 729-734. |
| [9] | Xie Chongxin, Zhang Lei. Comparison of knee degeneration after anterior cruciate ligament reconstruction with or without remnant preservation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 735-740. |
| [10] | Ma Rui, Wang Jialin, Wu Mengjun, Ge Ying, Wang Wei, Wang Kunzheng. Relationship of pathogenic bacteria distribution with drug resistance and treatment cycle for periprosthetic joint infection after total joint arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 380-385. |
| [11] | Su Liping, Lu Ziyang, Liu Li, Zhang Wei, Su Tianyuan, Hu Xiayun, Pu Hongwei, Han Dengfeng. C-jun, Cytc and Caspase-9 in the apoptosis of cerebellar granule neurons induced by diacetylmorphine in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 3943-3948. |
| [12] | Zuo Zhenkui, Han Jiarui, Ji Shuling, He Lulu. Pretreatment with ginkgo biloba extract 50 alleviates radiation-induced acute intestinal injury in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3666-3671. |
| [13] | Zhang Liang, Ma Xiaoyan, Wang Jiahong. Regulatory mechanism of Shenshuai Yin on cell apoptosis in the kidney of chronic renal failure rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3672-3677. |
| [14] | Xie Yang, Lü Zhiyu, Zhang Shujiang, Long Ting, Li Zuoxiao. Effects of recombinant adeno-associated virus mediated nerve growth factor gene transfection on oligodendrocyte apoptosis and myelination in experimental autoimmune encephalomyelitis mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3678-3683. |
| [15] | Xu Bin, Yang Xiushu, Liu Xuan, Wang Zhenxing. Changes of intestinal epithelial cells and their apoptotic factors Caspase-3, Bax and Bcl-2 under urinary environment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3173-3177. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||