Chinese Journal of Tissue Engineering Research ›› 2014, Vol. 18 ›› Issue (8): 1263-1269.doi: 10.3969/j.issn.2095-4344.2014.08.019
Previous Articles Next Articles
Tissue-engineered soft tissue oriented manufacturing technologies and additive manufacturing
Lian Qin, Li Di-chen, Chen Cheng, Zhang Wei-jie, Liu Ya-xiong, He Jian-kang, Jin Zhong-min
- State Key Laboratory for Manufacturing Systems Engineering, Xi’an Jiaotong University, Xi’an 710049, Shaanxi Province, China
-
Received:2013-12-17Online:2014-02-19Published:2014-02-19 -
About author:Lian Qin, M.D., Associate professor, State Key Laboratory for Manufacturing Systems Engineering, Xi’an Jiaotong University, Xi’an 710049, Shaanxi Province, China -
Supported by:the National Natural Science Foundation of China, No. 51375371, 51075320; the Fundamental Research Funds for the Central Universities
CLC Number:
Cite this article
Lian Qin, Li Di-chen, Chen Cheng, Zhang Wei-jie, Liu Ya-xiong, He Jian-kang, Jin Zhong-min. Tissue-engineered soft tissue oriented manufacturing technologies and additive manufacturing[J]. Chinese Journal of Tissue Engineering Research, 2014, 18(8): 1263-1269.
share this article
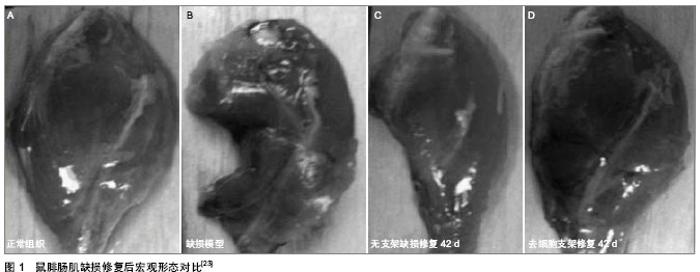
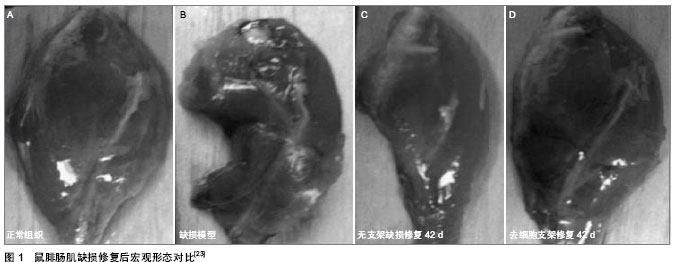
2.1 软组织的需求 2.1.1 软组织的生物学要求 人体软组织主要有血管、肌肉、软骨、内脏(肝胆等)组织,不同的组织具有不同的生物学要求。软组织不仅单位体积内细胞含量高,新陈代谢中营养供给和氧气、废物运输要求高,而且针对软组织本身在体内所完成的功能,需要满足一定的生物活性功能,不同的组织也具有不同的生物学要求。例如骨骼肌具有收缩性和兴奋性,接收到刺激后通过收缩牵动骨骼来实现运动功能,所以骨骼肌实现其功能就需要满足一定的力学强度要求,同时还要求在受到刺激或信号作用下会实现收缩功能;血管是血液流通的通道,在血液运输过程中,血管除满足强度外,还必须有一定的扩张性和弹性,能够承担血液流通压力[13]。在研究不同软组织中还需要基于自身细胞的生长、增殖、分化观察其生物学特征,利用种子细胞来满足生物学要求。 组织工程软组织支架不仅要模拟实现自然软组织的功能,还需要支架本身能够达到软组织本身的生物学要求。通过移植组织工程化支架本身与周围软组织的结合,带血管的软组织要求支架还需要与周围血管结合,能够实现血管化对周围结构输送氧气和营养物质及排出代谢废物。此外,支架还需要满足细胞亲和性要求,避免免疫排斥反应,能够促进细胞在支架上的生长、增殖、分化;支架还需要具有一定的含水量及渗透率,给细胞生长提供三维空间等[14]。 2.1.2 生物力学模型 软组织根据其功能特性,需要一定的结构及其材料属性实现软组织在体内的功能。通过借助Micro-CT、核磁共振(MRI)医学影像技术扫描获得软组织的形状,经过切片、组织学染色等获得组织内部结构,获得整体的解剖学结构,再利用力学测试系统,获得软组织的力学参数,从而建立软组织的生物力学模型,根据软组织特征优化模型数据来实现支架的参数化制造。生物力学模型建立,可以从力学角度分析模型本身结构与力学的关系,可以解决其结构在加工过程中的力学问题。人体组织器官的快速建模技术,例如建立在分形理论基础上的肝脏血管树模型[15],结构复杂,不仅成形难度高,而且难以用于多材料结构成型的有限元功能化分析和工艺优化;肌肉组织生物力学研究尽管已经从Hill三元模型发展到磁力控制下形成细胞膜片的三维本构模型[16],受薄层人工组织及其组装方式的限制,还未用于软组织及其血管化的人工干预下的重建组织性能的评估与预测。 2.1.3 组织工程材料 理想的组织工程支架材料具有良好的生物相容性、一定的机械性能、降解速度可调性、无毒性、孔隙率、细胞亲和性、可加工性及重复性等特征[17]。高分子水凝胶是一种含水的具有一定机械强度的材料,具有一定的孔隙率,其多孔的内部结构能够模拟细胞生长的微环境,为细胞在支架中提供三维空间,促进细胞在类自然环境下生长、爬行、分化等[18]。高分子水凝胶的三维网络结构和黏弹性特征与生物体内由生物大分子构成的细胞外基质环境特征具有相似的特点,使得水凝胶可以作为生物医用材料,基于水凝胶和细胞制备的组织工程血管化支架在软组织支架广泛应 用[7, 10, 19]。在组织工程材料的发展过程中,高分子水凝胶的出现,使得软组织器官修复在材料方面得到支持,通过有效利用水凝胶制备软组织支架来达到组织修复的目的。 2.2 制造技术 2.2.1 去细胞支架 国内外在大块人工组织制造方法上,目前已形成为整体、片层、片层组装等3个层次上制造血管化支架的研究趋势。去除自然组织中的细胞,保留细胞外基质的去细胞支架[20-22],是典型的整体式人工组织。美国匹兹堡大学和德克萨斯大学等对受损肌肉组织的研究证明,大块肌肉组织缺损造成肌肉体积明显减小,移植的去细胞支架能够诱导宿主的肌细胞迁移和血管网形成,再生出肌肉组织,肌肉缺损修复效果见图1所示[3, 23];但在修复过程中发现,只有去细胞支架与骨髓间充质干细胞复合后移植的条件下,才能重建骨骼肌收缩功能[23]。这也说明了在制造支架的同时,细胞因素的影响也不能忽略。 在整体人工支架与细胞复合构建人工软组织的研究中,多孔细胞质基质与转化生长因子β2,成纤维细胞生长因子2等生长因子复合,能够促进骨髓间充质干细胞的生长、黏附与分化,可促进软骨的修复[24]。法国拉瓦尔大学Bourget等[25]从人体中提取成纤维细胞培养,细胞培养产生细胞基质并形成组织片,组织片有表面渗透压形成自组装细胞质基质支架,再将平滑肌细胞种植在支架上来获得组织工程血管网,并通过卷曲的方式获"

得三维立体带血管的三维支架。解放军北京军事医学科学院将基因改造细胞及其他细胞与胶原复合,制造出血管化人工心脏组织[26];哈尔滨医科大学附属第二医院使用胶原制造出心肌补片,并将人骨髓间充质干细胞与管内皮细胞生长因子种植于补片上,该支架可以改善内皮细胞的存活并促进血管网络的新生[27]。尽管多因子封装和多细胞共培养技术可有效促进人工支架血管化的形成,但是新生血管网的随意结构很难与宿主组织的血管网对接长合,进而造成大块软组织植入血管化困难,直接影响了支架与宿主组织后期的长合及组织功能重建。 2.2.2 微制造技术 组织工程支架制造方法中,静电纺丝技术提供了导向极性纤维微薄层支架[28-31],例如使用纺丝方法制备具有极性方向的导电纳米纤维,使用聚乳酸-羟基乙酸共聚物与导电的PANi混合,纺丝获得不同浓度的纳米纤维并将成纤维细胞种植在支架上,获得组织工程肌肉支架。微制造技术提供了构建具有三维预定仿生血管网的方法。西安交通大学使用冷冻干燥法制造了琼脂糖/胶原多孔支架,通过改变温度和pH值控制支架的孔隙结构及性能,获得具有三维微孔道结构支架,其微孔道结构可以使细胞铺展[32]。解放军医学院在体外构建预血管化的片状工程化肝组织,将生长因子、细胞与基质材料混合培养制造出片状,并植入大鼠肝脏表面,使构建物与肝脏尽快建立血液联通[33]。哈佛医学院和剑桥大学等利用光固化掩膜法制造出具有凹槽结构的明胶凝胶/细胞,该方法目前仅制造出了一层流道结构,还难以用之制造出具有复杂血管网络的类组织器 官[34]。台湾大学Wang等[35]使用立体光刻技术,首先在硅板上或PDMS表面光刻出设计机构做为实验模具,在硅橡胶板上涂覆一层修饰RGDS/YIGSR肽链的聚乳酸-羟基乙酸共聚物薄膜,形成了带有微管道的支架,在支架上种植小鼠C2C12细胞获得具有定向生长的肌肉支架;美国西维吉尼亚大学使用微制造方式制造圆柱微流道仿生血管管道结构,模拟流体动态仿生获得微血管流动参数模型,利用双层PDMS基板和AZ P4620光刻胶模具制造出圆柱型仿生管道,虽然在制造过程中由于升温融化光刻胶模具会导致管道表面出现孔隙,但该技术可制造出不同厚度的微流道,用以形成连续的微细血管腔和脉管网络[36];美国伊利诺伊大学使用微制造技术制造藻酸盐类水凝胶支架,并且在表面种植成纤维细胞,支架上的成纤维细胞能够增殖,并且出现血管内皮生长因子的表达[37];通过微制造技术制造微管道来形成组织工程的血管化,东京大学使用微制造技术对心肌细胞和神经元细胞共培养,在培养系统上增加电刺激实验,实现在微结构中的多细胞共培养[38]。微制造技术通常制造单层薄片结构,多层制造工艺困难,复杂的叠加黏合工艺的层间结合能力有限,层面功能涂层对细胞生长亦有抑制作用,而且由于组织薄片机械性能差,造成微结构保型困难,组装后立体网络的结构和连续性难以保证,营养扩散受限而出现坏死。 去细胞支架能够采用自然组织的细胞基质,该支架具有良好的生物相容性,但是去细胞支架细胞质基质的机械强度不足,且去细胞的过程中一旦发生蛋白质残余,会导致免疫排斥反应,因而其应用有限;微制造技术通过制造纤维微薄层,通过卷裹、叠加等方法只能维持其三维结构,不能模拟自然组织的形状,在制造三维支架方法上仍存在技术上的不足,同时微流道制造实现血管化的工艺研究也因其结构及制造方法的限制,支架血管化的效果差。然而,近年来在生物医学应用方面发展迅速的增材制造技术,利用水凝胶可为高效制造复杂形状的仿生结构三维支架提供有效的途径。 2.3 增材制造技术 增材制造技术是将预设计的复杂结构件,经过计算机技术离散化为面、线、点数据作为结构单元,在控制材料实现结构单元有序堆积、累加过程,直接加工成型为立体结构。增材制造的方法有多种,较为成熟的成型方法主要有光固化成型、熔融沉积法、选择性激光烧结法、三维打印技术、分层实体制造法等,这些方法在金属、陶瓷、复合物等材料机械加工及生物组织工程的应用中具有无可替代的优势。其中,主要应用于生物医学方面的增材制造技术包括主要有光固化成型技术、三维打印技术、熔融沉积技术等。 光固化成型、三维打印技术等增材制造技术,是应用于生物医学领域中的人工组织制造技术的重要手 段[39-42]。光固化成型、三维打印技术等增材制造技术利用CAD先对组织具体结构进行造型,然后根据其内部微小的结构造模,在常温下将种子细胞及生物活性因子加入到生物可降解材料中并进行分层制造,制造出一种类细胞质基质的微环境,这种微环境是通过增材制造出的细胞载体框架来实现的,对细胞的黏附增殖及功能化具有一定的促进作用,最终实现组织工程化支架制造及组织修复的目的。目前已发展形成了左旋聚乳酸,聚乳 酸-羟基乙酸共聚物,PPF/DEF等以高分子聚合物为主、多材料递变结构的制造工艺。同时,随着水凝胶、细胞和生长因子的复合技术在临床上的不断取得成功[43-44],基于水凝胶材料的人工组织支架增材制造正在成为新的研究热点。 西安交通大学利用自行开发的光固化成型机制造出复杂外形结构的大块聚乙二醇水凝胶支架,形成了光固化水凝胶支架的结构精度控制方法与理论[10]。西安交通大学边卫国等[45]使用快速成型技术制造出宏微观一体化成型的多孔生物陶瓷支架,该多孔支架便于周围组织的长入,并促进骨组织的血管化,细胞实验中兔骨髓干细胞在骨支架与软骨支架内可良好的黏附、增殖,细胞形态逐步成熟,证明以快速成型技术为基础的骨支架及软骨支架制造工艺具有良好的生物安全性。清华大学颜永年等[46-47]提出基于离散堆积快速成形原理和溶胶/凝胶转变机制的细胞直接三维受控组装等技术,在计算机控制下,将基质材料与细胞准确的定位和运输,直接装配成型,形成具有特定空间排列的带细胞的复杂三维结构。所开发的低温沉积技术将溶液挤压到低温环境中,冷冻凝固,同时出现相分离形成微孔,随着冷冻干燥使得溶剂挥发,留下梯度孔隙结构的支架,该多孔的梯度结构有利于新生组织长入。英国谢菲尔德大学Gill和Claeyssens[48]采用微光固化原型技术利用可降解高分子材料造出可调节物理性质的支架,并研究不同成分材料的光固化成型工艺。美因茨大学和荷兰特文特大学Seck等[49]采用高分辨率的光固化快速成型方法,利用可降解的聚乙二醇和聚D,L-乳酸制造出三维水凝胶支架,多孔支架和非多孔支架具有较高的机械性能。二十四面体的多孔支架具有良好的孔隙连接性和机械性,该结构表现出良好的细胞亲和性,细胞在材料上能够很好黏附和分化。 在快速成型组织工程支架制造过程中,细胞与支架一体化制造成为制造的难点,要考虑到细胞与支架材料的组装、材料成胶方式及影响细胞在体外成活率的因素等问题。因此,在体外实现活细胞支架的制造,能够实现血管化的功能。目前,已有研究细胞与支架一体化制造的方法,例如伊利诺伊大学使用光固化成型方式[7, 9-10],使用的不同分子质量的聚乙二醇双丙烯酸酯水凝胶与细胞及生长因子混合,研究其加工工艺过程,制造出单细胞单材料三维活细胞支架和多细胞多材料的三维活细胞支架,并通过细胞的成活率等来评价支架材料及制造方法。匹兹堡大学医学院使用投影光固化成型技术采用水凝胶制造活细胞支架[19],将聚乙二醇双丙烯酸酯与人体脂肪干细胞及不同浓度的光引发剂混合,观察细胞生长的影响因素,该方法有效制造了大块多孔的软组织三维活细胞支架。但是三维支架对细胞的生长有一定的限制,同时针对大块软组织支架的血管化问题,也没有提出可靠的解决方法。 三维打印技术已被应用到生物制造和医学领域,2009年美国ganovo公司首次使用三维打印技术制造出人造血管[50],2010年澳大利亚Invetech公司和美国Organovo公司合作尝试以活体细胞为打印人体的组织和器官[51]。美国南加利福尼亚医科大学和密歇根大学以琼脂糖为支撑,利用三维打印装置将细胞混合液滴(300-500 μm) 与其混合打印,制造出管径<3 mm的血管分支网[52]。哈佛大学医学院制造了可用于复合细胞的胶原水凝胶逐层打印设备,其制造支架见图2所示[53]。该设备制造主要问题是受限于胶原水凝胶成胶速度缓慢,导致水凝胶制造时间过长,从而影响水凝胶内部细胞的活性,因而难以满足人工软组织需求。宾夕法尼亚大学和麻省理工大学等利用牺牲材料的方法制造血管支架[54]。首先利用三维打印机打印出多糖的管状网络结构作为消失模,在消失模外层涂覆一层聚乳酸-羟基乙酸共聚物,防止多糖管状网络溶解时液体渗透到外部影响外部基质环境。将制造好的多糖管状网络放入模具,把包埋细胞的水凝胶或高分子材料倒入模具中,材料固化,从而完成细胞和多糖管状网络在生物材料中的包埋,然后溶解排出多糖网络,最终实现带有血管结构的活细胞三维支架。增材制造能够实现宏微观结构成形,与其他制造方法结合能够更大程度上满足软组织支架的制造要求。 然而目前水凝胶与细胞复合增材制造的成形机制论仍存在不足,例如对三维打印技术,成型精度的首要影响因素是细胞液滴的黏弹性和表面张力[40]。其次是支架材料的应用研究亟待进行。目前使用的琼脂糖、胶原等水凝胶强度不高,在短期内新生细胞外基质难以维持人工组织结构。而近年来用于开发抗撕裂、高细胞量人工软组织的高强度水凝胶的发展[55-59],如双网络水凝 胶[60],如果能利用其光固化成型特性,使其制造方式与高精度成型的光固化原型技术结合,将解决微制造技术"

| [1] 90%患者在等待中绝望,器官捐献亟待更多人参与.中国器官捐献网,2012.http://www.organdonation.org.cn/wap.aspx?nid=6059&cp=2&cid=423[2] Salmi M,Paloheimo KS,Tuomi J,et al.Accuracy of medical models made by additive manufacturing (rapid manufacturing).J Craniomaxillofac Surg.2013;41(7):603-609.[3] Wolf MT,Daly KA,Reing JE,Badylak SF. Biologic scaffold composed of skeletal muscle extracellular matrix. Biomaterials. 2012;33:2916-2925.[4] Cleary MA,Geiger E, Grady C,et al. Vascular tissue engineering: the next generation. Trends Mol Med.2012;18: 394-404.[5] Park SH,Kim MS,Lee D,et al.Hybrid microfabrication of nanofiber-based sheets and rods for tissue engineering applications.J Lab Autom.2013;18(6):494-503.[6] Daggumati P,Kurtulus O,Chapman CA,et al.Microfabrication of Nanoporous Gold Patterns for Cell-material Interaction Studies.J Vis Exp.2013;(77):e50678.[7] Chan V, Zorlutuna P, Jeong JH,et al.Three-dimensional photopatterning of hydrogels using stereolithography for long-term cell encapsulation. Lab hip.2010;10:2062-2070.[8] Melchels FP,Feijen J,Grijpma DW.A review on stereolithography and its applications in biomedical engineering.Biomaterials.2010;31:6121-6130.[9] Arcaute K,Mann B,Wicker R.Stereolithography of spatially controlled multi-material bioactive poly(ethylene glycol) scaffolds.Acta Biomater.2010;6:1047-1054.[10] 朱林重,连芩,靳忠民,等.PEGDA水凝胶的光固化成形工艺研究及其性能评价[J].西安交通大学学,2012,46(12):121-126.[11] Castilho M,Dias M,Gbureck U,et al.Fabrication of computationally designed scaffolds by low temperature 3D printing.Biofabrication.2013;5(3):035012.[12] Chan V,Jeong JH,Bajaj P,et al.Multi-material bio-fabrication of hydrogel cantilevers and actuators with stereolithography.Lab Chip 2012;12:88-98.[13] 《中国组织工程研究与临床康复》杂志社学术部.中国血管组织工程研究[J].中国组织工程研究与临床康复,2011,15(28):5307- 5308.[14] Bolgen N,Yang Y,Korkusuz P,et al.3D ingrowth of bovine articular chondrocytes in biodegradable cryogel scaffolds for cartilage tissue engineering. J Tissue Eng Regen Med.2011;5: 770-779.[15] Khait L,Birla RK.Bypassing the patient: comparison of biocompatible models for the future of vascular tissue engineering. Cell Transplant.2012;21:269-283.[16] Yamamoto Y,Ito A,Fujita H,et al.Functional evaluation of artificial skeletal muscle tissue constructs fabricated by a magnetic force-based tissue engineering technique.Tissue Eng Part A.2011;17:107-114.[17] Chien HW,Tsai WB,Jiang S.Direct cell encapsulation in biodegradable and functionalizable carboxybetaine hydrogels. Biomaterials.2012;33:5706-5712.[18] Kloxin AM,Tibbitt MW,Kasko AM,et al.Tunable hydrogels for external manipulation of cellular microenvironments through controlled photodegradation.Adv Mater.2010;22:61-66.[19] Lin H,Zhang D,Alexander PG,et al.Application of visible light-based projection stereolithography for live cell-scaffold fabrication with designed architecture. Biomaterials.2013; 34(2): 331-339.[20] Campbell EM,Cahill PA, Lally C. Investigation of a small-diameter decellularised artery as a potential scaffold for vascular tissue engineering; biomechanical evaluation and preliminary cell seeding.J Mech Behav Biomed Mater.2012; 14: 130-142.[21] Corona BT,Ward CL,Baker HB,et al.Implantation of in vitro tissue engineered muscle repair (TEMR) constructs and bladder acellular matrices (BAM) partially restore in vivo skeletal muscle function in a rat model of volumetric muscle loss (VML) injury. Tissue Eng Part A.2014:20(3-4):705-715.[22] Mangold S,Schrammel S,Huber G, et al. Evaluation of decellularized human umbilical vein (HUV) for vascular tissue engineering - comparison with endothelium-denuded HUV. J Tissue Eng Regen Med.2012.doi:10.1002/term.1603.[23] Merritt EK,Cannon MV,Hammers DW, et al. Repair of traumatic skeletal muscle injury with bone-marrow-derived mesenchymal stem cells seeded on extracellular matrix. Tissue Eng Part A.2010;16:2871-2881. [24] Bosetti M,Boccafoschi F,Leigheb M,et al.Chondrogenic induction of human mesenchymal stem cells using combined growth factors for cartilage tissue engineering. J Tissue Eng Regen Med.2012;6:205-213.[25] Bourget JM,Gauvin R,Larouche D,et al.Human fibroblast-derived ECM as a scaffold for vascular tissue engineering.Biomaterials.2012;33:9205-9213.[26] 刘志强.基于壳聚糖水凝胶的可注射性心肌组织工程研究[D].中国人民解放军军事医学科学院,2012.[27] 康凯,曲辉,汤继权,等.共价结合生长因子的胶原补片改善大鼠室壁瘤修补术后移植细胞生存率的实验研究[J].中国胸心血管外科临床杂志,2013,20(4):451-456.[28] Chung S,Ingle NP,Montero GA,et al.Bioresorbable elastomeric vascular tissue engineering scaffolds via melt spinning and electrospinning.Acta Biomater. 2010;6(6): 1958-1967.[29] Han J,Lazarovici P,Pomerantz C,et al.Co-electrospun blends of PLGA, gelatin, and elastin as potential nonthrombogenic scaffolds for vascular tissue engineering. Biomacromolecules. 2011;12:399-408.[30] McKeon-Fischer KD,Flagg DH,Freeman JW.Coaxial electrospun poly(ε-caprolactone), multiwalled carbon nanotubes, and polyacrylic acid/polyvinyl alcohol scaffold for skeletal muscle tissue engineering.J Biomed Mater Res Part A.2011;99:493-499.[31] Zhou J,Cao C,Ma X,et al.Electrospinning of silk fibroin and collagen for vascular tissue engineering.Int J Biol Macromol. 2010;47:514-519.[32] 朱琳,贺健康,刘亚雄,等.琼脂糖/胶原复合水凝胶的制备及性能研究[J].西安交通大学学报,2013,47(10):121-126.[33] 刘巨超.片状工程化肝组织体外构建及大鼠原位移植的实验研究[D].中国人民解放军医学院,2012.[34] Nikkhah M,Eshak N,Zorlutuna P,et al.Directed endothelial cell morphogenesis in micropatterned gelatin methacrylate hydrogels.Biomaterials.2012;33:9009-99018.[35] Wang PY,Wu TH,Tsai WB,et al.Grooved PLGA films incorporated with RGD/YIGSR peptides for potential application on skeletal muscle tissue engineering. Colloids Surfaces BBiointerfaces.2013;110:88-95.[36] Huang Z,Li X,Martins-Green M,et al.Microfabrication of cylindrical microfluidic channel networks for microvascular research.Biomed Microdevices.2012;14:873-883.[37] DeVolder RJ,Zill AT,Jeong JH,et al.Microfabrication of proangiogenic cell-laden alginate-g-pyrrole hydrogels. Biomaterials.2012;33:7718-7726.[38] Takeuchi A,Nakafutami S,Tani H,et al. Device for co-culture of sympathetic neurons and cardiomyocytes using microfabrication. Lab Chip.2011;11:2268-2275.[39] Chopra K,Mummery PM,Derby B,et al.Gel-cast glass-ceramic tissue scaffolds of controlled architecture produced via stereolithography of moulds.Biofabrication. 2012;4:045002.[40] Lee H,Fang NX. Micro 3D printing using a digital projector and its application in the study of soft materials mechanics. J Vis Exp.2012:e4457.[41] Melchels FP,Bertoldi K,Gabbrielli R,et al.Mathematically defined tissue engineering scaffold architectures prepared by stereolithography.Biomaterials. 2010;31:6909-6916.[42] Romano PE.3D Printing Live Stem Cells; Hobbit in 3D; Super "Retina Displya"; Your Microbiome; Hospitals Takeover; Income Taxes; Bicyclists; Deer Dangers. Binocular vision & strabology quarterly, Simms-Romano's.2013;28:52-64.[43] Chaim IA,Sabino MA,Mendt M,et al.Evaluation of the potential of novel PCL-PPDX biodegradable scaffolds as support materials for cartilage tissue engineering. J Tissue Eng Regen Med.2012;6:272-279.[44] Chang NJ,Jhung YR,Yao CK,et al. Hydrophilic gelatin and hyaluronic acid-treated PLGA scaffolds for cartilage tissue engineering.J Appl Biomater Funct Mater.2013;11:e45-52.[45] Bian W,Li D,Lian Q,et al.Design and fabrication of a novel porous implant with pre-set channels based on ceramic stereolithography for vascular implantation. Biofabrication. 2011;3:034103.[46] 胡金夫,徐铭恩,徐莹,等.基于细胞三维受控组装技术的细胞芯片构建[J].中国生物医学工程学报,2012,31(3):374-81.[47] 颜永年,李生杰,熊卓,等.基于快速原型的组织工程支架成形技术[J].机械工程学报,2010,46(5):93-98.[48] Gill AA, Claeyssens F.3D structuring of biocompatible and biodegradable polymers via stereolithography.Methods Mol Biol.2011;695:309-321.[49] Seck TM,Melchels FP,Feijen J,et al.Designed biodegradable hydrogel structures prepared by stereolithography using poly(ethylene glycol)/poly(D,L-lactide)-based resins. J Control Release.2010;148(1):34-41.[50] 黄健,姜山.3D 打印技术将掀起"第三次工业革命"?[J].新材料产业,2013,15(1):62-67.[51] 王雪莹.3D 打印技术及其产业发展的前景预见[J].创新技术, 2012,11(12):3-5.[52] Mironov V,Kasyanov V,Markwald RR.Organ printing: from bioprinter to organ biofabrication line. Curr Opin Biotechnol. 2011;22:667-673.[53] Lee W,Lee V,Polio S,et al.On-demand three-dimensional freeform fabrication of multi-layered hydrogel scaffold with fluidic channels.Biotechnol Bioeng. 2010;105(6):1178-1186.[54] Miller JS,Stevens KR,Yang MT,et al.Rapid casting of patterned vascular networks for perfusable engineered three-dimensional tissues.Nature Mat.2012;11:768-774.[55] Arakaki K,Kitamura N,Fujiki H,et al.Artificial cartilage made from a novel double-network hydrogel: In vivo effects on the normal cartilage and ex vivo evaluation of the friction property.J Biomed Mater Res Part A.2010;93:1160-1118.[56] Kirschner CM,Anseth KS.Hydrogels in Healthcare: From Static to Dynamic Material Microenvironments.Acta Mater. 2013;61:931-944.[57] Ronken S,Wirz D,Daniels AU,et al.Double-network acrylamide hydrogel compositions adapted to achieve cartilage-like dynamic stiffness.Biomech Model Mechanobiol. 2013;12(2):243-248.[58] Sharma B,Fermanian S,Gibson M,et al.Human cartilage repair with a photoreactive adhesive-hydrogel composite.Sci Transl Med.2013;5(167):167ra6.[59] Sun JY,Zhao X,Illeperuma WR,et al.Highly stretchable and tough hydrogels. Nature. 2012;489:133-136.[60] Chen YM,Dong K,Li ZQ,et al.Double network hydrogel with high mechanical strength:Performance, progress and future perspective.Sci China Tech Sci.2012;55(8):2241-2254. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [3] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [4] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [5] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [6] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [7] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||