Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (2): 303-311.doi: 10.3969/j.issn.2095-4344.1957
Previous Articles Next Articles
Hypoxia-mediated miRNAs affect glucose metabolism: new recognition of preventing and controlling glucose metabolism
Jiang Han1, 2, Ding Jie2, Chen Gen2, Xie Qiang2, Li Wei2, Wang Zhibin2, Zhu Lei
- 1School of Physical Education, Qufu Normal University, Qufu 273100, Shandong Province, China; 2National Institute of Sports Medicine, Beijing 100061, China
-
Received:2019-03-16Revised:2019-03-23Accepted:2019-05-05Online:2020-01-18Published:2019-12-25 -
Contact:Zhu Lei, Associate professor, School of Physical Education, Qufu Normal University, Qufu 273100, Shandong Province, China -
About author:Jiang Han, Master candidate, School of Physical Education, Qufu Normal University, Qufu 273100, Shandong Province, China; National Institute of Sports Medicine, Beijing 100061, China -
Supported by:the General Project of National Science Foundation for Postdoctorate of China, No. 2017M622161; the Graduate Education Innovation Program of Shandong Province, No. SDYY16089
CLC Number:
Cite this article
Jiang Han, Ding Jie, Chen Gen, Xie Qiang, Li Wei, Wang Zhibin, Zhu Lei. Hypoxia-mediated miRNAs affect glucose metabolism: new recognition of preventing and controlling glucose metabolism[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(2): 303-311.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
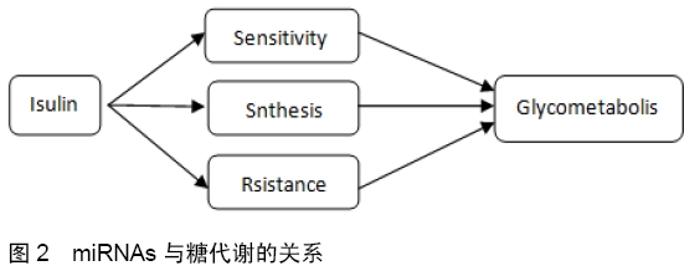
2.1 miRNAs miRNA是调节基因表达的微小非编码RNA,通过降低其目标mRNA来抑制基因表达,在调节蛋白质编码基因中起着十分重要的作用。它们是长度约为22个核苷酸的单链RNA分子,通过miRNA的3'UTR区域结合并使它们不稳定或抑制其翻译而起基因表达调节剂的作用[13]。研究发现,miRNAs参与了糖代谢过程,并作为调控糖类代谢内稳态的重要调节因子,作为糖代谢疾病潜在生物标志物的作用,在糖类代谢过程中发挥了重要作用[14-15]。 2.2 miRNAs与糖代谢疾病 糖代谢在人体中起到非常重要的作用,一旦代谢出现紊乱,会引起糖尿病、高脂血症、低血糖症、果糖代谢障碍等多种疾病,虽然导致肥胖和2型糖尿病的个体变化的分子机制仍然不清楚,但许多研究结果表明miRNAs可能成为糖尿病诊断和防治的潜在生物标志物。近年研究显示,miRNAs还参与调控糖脂代谢、胰岛素的产生和分泌、脂肪细胞的分化等,提示miRNAs可能与肥胖、糖尿病等代谢性疾病的发病有关。大量的研究表明miRNAs在肥胖、糖尿病及其并发症的发病机制中起着重要的作用[16-21]。 2.2.1 miRNAs对肥胖的调控 肥胖是体内脂肪积聚过多而呈现的一种状态,是一种代谢性疾病,众所周知一些miRNAs在血清中稳定存在,与多种疾病密切相关,众多研究表明如miR-138,miR-26b,miR-27a,miR-122,miR-802和miR-143等miRNAs对肥胖具有调控作用。 2014年XU等[22]研究显示miR-26b是一种与肥胖有关的内含子miRNA。miR-26b与肥胖的发展有关,尤其是在腹部皮下脂肪组织中,miR-26b与浸润巨噬细胞的数量密切相关[8],同时在小鼠脂肪生成过程中被上调[23]。miR-26b在小鼠和成熟的人类脂肪细胞中大量表达,与脂肪因子的表达有关。2015年XU等[24]又通过荧光PCR检测肥胖大鼠模型中miR-26b的表达,分析了miR-26b在脂肪细胞中过度表达和抑制葡萄糖摄取的作用,探讨miR-26b在脂肪细胞中与肥胖相关的胰岛素抵抗中的表达和作用机制,结果显示在肥胖的啮齿动物模型、人类肥胖和胰岛素抵抗性脂肪细胞中,内脏脂肪组织miR-26b水平降低。miR-26b通过抑制靶基因PTEN调节胰岛素,并通过PTEN/PI3K/AKT通路显著提高胰岛素敏感性。miR-26b的表达水平与人肥胖受试者的体质量指数和体内稳态模型评估呈负相关。孟娅妮等[25]通过对妊娠期肠系膜脂肪细胞摄取葡萄糖的研究,结果显示miR-26b及其下游靶基因的表达进一步调控PI3K/AKT-Mglut4信号通路来发挥脂肪细胞摄取葡萄糖的作用,提示miR-26b具有调节肠系膜脂肪细胞代谢的功能,但目前研究仅仅局限于体外实验,相关机制和体内实验还需进一步研究。研究结果表明,miR-26b的表达受多种因素的影响,这些因素与肥胖和胰岛素敏感性相关。因此,miR-26b可能是肥胖相关胰岛素抵抗发展的重要介质。WU等[11]通过对25例肥胖患者和25例健康者对照,通过miRNA聚合酶链反应研究了两组血清样品,通过肥胖组与对照组数据相比,肥胖组的miR-152和miR-17显著升高,而miR-138显著降低,研究结果表明miRNAs在肥胖预测中的潜在效用。另外研究显示,miR-27a通过抑制PPARγ在肥胖的脂肪形成和病理生理学中发挥重要作用[26],miR-130通过抑制PPARγ生物合成减少脂肪生成[27],miRNA簇miR-200c/141和miR-200b/a/429在ST2细胞中促进脂肪形成[28],同时在脂肪生成过程中,miR-34a与体质量指数呈正相关[8]。 根据目前的证据表明,miRNAs在胰岛素生产、分泌和作用以及葡萄糖稳态和脂肪细胞分化的不同方面中发挥重要作用,与肥胖相关的组织特异性miRNAs的鉴定可能对未来有关肥胖相关医学并发症的早期诊断和治疗干预策略的发展有重要作用。 2.2.2 miRNAs对糖尿病的调控 近期研究表明,miRNAs在糖尿病中扮演着不同的角色[16,29-33]。1型糖尿病和2型糖尿病是糖尿病的2种主要类型。1型糖尿病的特点是胰腺细胞的胰岛素释放减少,而2型糖尿病是由胰岛细胞功能障碍引起的胰岛素抵抗引起的。目前2型糖尿病是最常见的发病率高的一种代谢性紊乱疾病。研究显示2型糖尿病并不一定是终身性疾病,一项新的临床试验提供了明确的证据,证明2型糖尿病是可以被逆转的,即便对于患病多年的人群也是如此[34]。将miRNAs的表达恢复至正常水平对于维持胰岛素分泌和胰岛素敏感性可能具有治疗潜力,抗miRNA寡核苷酸(Anti miRNA oligodeoxynucleotides,AMOs)是miRNA基因治疗中最常见的策略之一。基于病毒的转染对miRNAs的调控已经成功地用于动物实验,显示出糖尿病的治疗潜力。证据表明,胰岛素敏感性和胰岛素分泌的下降都有遗传因素[5]。miRNAs作为基因表达的关键调控因子在胰岛素的分泌和调节胰岛素功能的功能中发挥着重要作用[20],部分miRNAs参与调节糖脂代谢以及一些重要的生理过程,在调控糖尿病和肥胖中发挥重要作用。并且通过与靶基因的相互作用,如miR-128,miR-7,miR-25,miR-92a,miR-375以及miR-15家族(miR-15a和miR-15b)等miRNAs在调节糖脂代谢中起重要作用,从而维持糖脂代谢的稳定状态[35]。 此外MOTOHASHI等[36]证明miR-128下调肌细胞中参与胰岛素信号转导的基因(例如胰岛素受体,胰岛素受体底物-1和磷脂酰肌醇3-激酶调控1)。综上认为miR-128水平的升高可能与2型糖尿病相关的血脂异常的发生有关。与此同时,大量研究显示miR-7是最丰富的内分泌miRNA[2, 37- 38]。miR-7通过靶向胰腺发育的关键转录因子来控制胰腺的分化和成熟[39]。此外,miR-7的内分泌特异性受胰腺转录因子网络支配,包括Neurogenin-3(Ngn3)和NeuroD/Beta2,暗示miR-7是微调β细胞的关键靶点发展并可用于β细胞再生。事实上,miR-7在人胚胎干细胞向胰岛素分泌细胞分化过程中都表现出动态表达模式[40]。MAO等[4]研究表明miR-7可能成为糖尿病的治疗靶点,miR-7强调的重要性表明调控miR-7表达可用于控制糖尿病的发展。 通过深入研究miRNAs对糖代谢的研究将有助于找到主要的调控指标,miRNAs模拟物或抑制剂作为用于治疗糖代谢疾病提供新的潜在治疗选择,为今后生物医学研究的发展提供参考。 2.3 miRNAs调节糖代谢的作用机制 糖代谢失调会引起肥胖、糖尿病等多种疾病,miRNAs在肥胖中过度表达抑制胰岛素刺激的AKT活化并损害葡萄糖代谢。miRNAs在糖尿病中表达的改变直接导致胰岛素释放和胰岛素抵抗的功能障碍[16]。胰岛素是机体内唯一降低血糖的激素,也是唯一同时促进糖原、脂肪、蛋白质合成的激素。胰岛素能促进全身组织对葡萄糖的摄取和利用,并抑制糖原的分解和糖原异生,胰岛素通过合成或抵抗对糖代谢产生影响(见图2)。 "
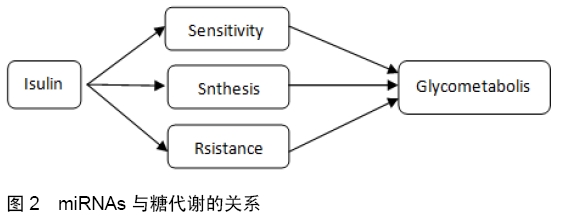
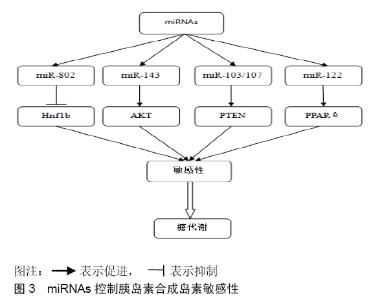
2.3.1 miRNAs促进胰岛素敏感性 有研究显示miRNAs过度表达会损害糖代谢,比如miR-802和miR-143的表达在肥胖患者的肝脏中上调,导致糖的耐受量受损。KORNFELD等[41]通过对肥胖小鼠模型和肥胖人类受试者肝脏的研究,显示miR-802的表达在肝脏中增加。在小鼠中诱导的miR-802的诱导基因过表达导致糖耐量受损,胰岛素敏感性减弱,而miR-802表达的降低则提高了葡萄糖耐受性和胰岛素的作用。将Hnf1b(也称为Tcf2)作为miR-802依赖的消音靶点,并显示短发夹RNA (shRNA)介导的肝内Hnf1b的减少引起葡萄糖耐受不良,损害胰岛素信号,促进肝糖异生。反过来,Hnf1b的肝脏过表达改善了Leprdb/db小鼠的胰岛素敏感性。由此确定了miR-802在糖代谢障碍过程中起着调控表达的关键作用,并在肝胰岛素敏感性的控制中分配Hnf1b。 JORDAN等[42]通过对8周大的doxycycline- inducible转基因小鼠和C57BL/6 littermates(野生型)小鼠的研究,显示miR-143的表达在肥胖小鼠肝脏中被上调,miR-143在小鼠体内的条件过表达损害葡萄糖的代谢,诱导的miR-143转基因过表达损害胰岛素刺激的蛋白激酶(protein kinase B,AKT/PKB)活化和葡萄糖稳态。通过研究确定了一种miR-143控制的AKT信号在肥胖中的调控途径,为发展miR-143靶基因奠定了基础,作为未来肥胖相关疾病的治疗靶点。 TRAJKOVSKI等[43]在肥胖的小鼠模型中,研究结果显示miR-103/107被上调。miR-103/107的阻断通过提高小窝蛋白1介导的IR激活来促进胰岛素敏感性,磷酸化酶和张力蛋白同源基因在10号染色体上缺失(如PTEN基因),是Akt关键的磷酸化酶,能够负向调控Akt信号通路。根据VIVACQUA等[44]已发表的研究,miR-103/107被发现在胰岛素抵抗和某些类型的癌症中被上调,已经显示在诸如PTEN、Dicer等基因上,这些基因在很大程度上参与了胰岛素抵抗和癌症相关的重要过程。miR-103/107的沉默导致葡萄糖稳态和胰岛素敏感性的改善,相反,在肝脏或脂肪组织中激活miR-103/107功能足以维持葡萄糖体内平衡。Caveolin-1已被确定为INSR的关键调控因子,并作为miR-103/107的直接靶标。证实在脂肪细胞中miR-103/107失活后,蛋白-1上调,伴随着胰岛素受体的稳定化,胰岛素信号传导增强,脂肪细胞减小,同时增强了在胰岛素刺激下的葡萄糖摄取能力。这些发现证明了miR-103/107在胰岛素敏感性中的核心重要性,并为治疗2型糖尿病和肥胖设定了新的目标。TRAJKOVSKI等[43,45]研究的另一个重要发现在小鼠系统中对miR- 107/103的抑制会导致与脂肪酸氧化有关基因的表达水平增加。miR-107/103是作为脂肪酸氧化抑制剂的地方,肥胖者的脂肪酸氧化水平较低,已经证明提高脂肪酸氧化的速度可以改善小鼠的胰岛素敏感性。 WANG等[46]通过对112名肥胖者和对照组(男女比例各半)采集的血清样本随机分为4个组(每个肥胖或对照组有28个样本)。通过微阵列检测到全基因组循环miRNA的分布。从123例肥胖患者(46.7%男性)和107例对照组(50.0%男性)的个体血清样本中选择并验证了miR-122的升高。ORTEGA等[47]发现在中度肥胖患者中血浆miR-122浓度增加,但病态肥胖患者的浓度降低,但在手术引起的体质量减轻后,miR-122的浓度显著降低。与此相反,Rui Wang的数据显示,在肥胖患者中,miR-122的水平明显升高,并呈现出随肥胖程度增加的趋势。进一步评估了miR-122水平与脂肪、胰岛素抵抗、脂质谱和肝酶相关参数之间的关系,结论显示miR-122升高与青少年肥胖和胰岛素抵抗呈正相关,这些发现有助于更好地理解miRNAs在脂肪和胰岛素敏感性中的作用,miR-122可能是肥胖的有希望的生物标志物。 miRNAs的表达受多种因素的影响,这些因素与胰岛素敏感性相关(见图3)。因此,miRNAs可能是参与胰岛素抵抗的重要介质,未来对有关肥胖相关医学并发症的早期诊断和治疗干预策略的发展有重要作用。 "
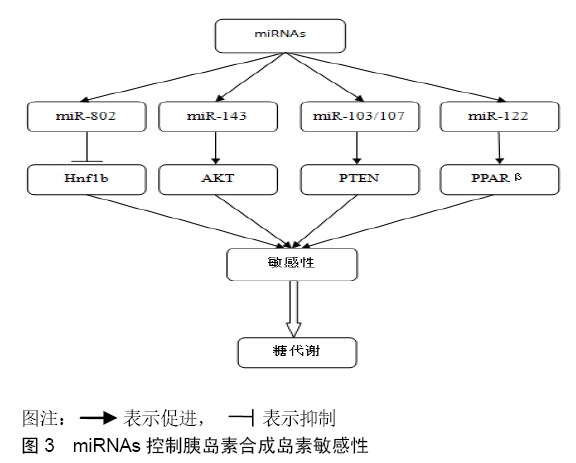
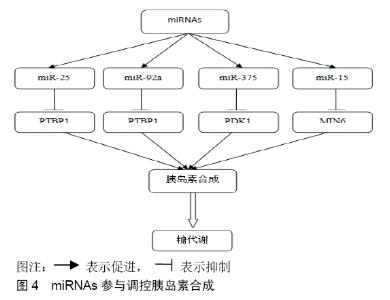
2.3.2 miRNAs控制胰岛素合成 众所周知miRNA通过控制mRNA的稳定性和翻译来参与调控基因表达,但当前研究显示的是miRNAs调节胰岛素表达的间接含义。迄今为止,还没有关于miRNAs对胰岛素合成的直接调控作用的报道。近年来关于miRNAs控制胰岛素的报道有很多,比如miR-25,miR-92a,miR-375以及miR-15家族(miR-15a和miR-15b)的表达都能够降低胰岛素的产生,控制胰岛素的合成。 miR-25和miR-92a可以通过控制胰岛素Ⅰ表达直接调节胰岛素生物合成和胰岛素反应。胰岛素的3'UTR对于促进葡萄糖激发的转录是十分重要的,是赋予miRNAs稳定性的关键区域。miRNAs作为基因表达的调节剂,这种调节功能通常是通过互补结合其mRNA靶标的3'UTR来影响随后的翻译过程。参与葡萄糖稳态调节的基因,特别是胰岛素生产中的基因已经被发现为几种miRNAs的靶标。但是并没有发现基于miRNAs胰岛素生物合成的直接调节剂。SETYOWATI KAROLINA等[48]将12只体质量约150 g,6周雄性Wistar大鼠,随机分为2组(n=6),其中一组正常饮食,另一组采用高脂饮食。2周后,高脂饮食的动物在一夜禁食后,在腹膜内注射低剂量链脲佐菌素STZ(40 mg/kg)。研究表明,miR-25和miR-92a为胰岛素表达的直接调节剂,联合控制胰岛素miRNAs的合成。另外Ortega等[49]通过对具有正常葡萄糖耐量的6名和6例2型糖尿病男性患者进行初步研究评估了miRNA谱,在一个随机、双盲和安慰剂控制下进行3个月的二甲双胍治疗,结果表明miR-25或miR-92a的表达能够降低胰岛素Ⅰ的产生。目前已经有研究证实miR-25,miR-92a通过3'UTR结合负调节胰岛素Ⅰ表达的潜力,表明葡萄糖刺激而增加的胰岛素Ⅰ表达与miR-25和miR-92a的下调一起发生,miR-25和miR-92a被鉴定为胰岛素Ⅰ表达的负调节物。 另外miR-375与葡萄糖诱导的胰岛素分泌有关,miR-375通过靶向3'-磷酸肌醇依赖性蛋白激酶1(Phosphoric acid muscle dependent protein kinase1,PDK1)并降低葡萄糖诱导的胰岛素基因表达和蛋白质合成[50],通过靶向胰岛素转录因子负调节因子MAFA(MAP4K4)诱导胰岛素在β细胞中的表达[6]。CHAKRABORTY等[51]研究证明在成年β细胞胰岛中存在高水平葡萄糖时miR-375的水平显著降低,miR-375的表达倾向于通过下调肌营养素的表达来诱导胰岛素分泌,在高水平成人中葡萄糖细胞胰岛中miR-375水平下降。miR-375的表达往往通过下调肌蛋白的表达而引起胰岛素分泌,这最终控制了胰岛素的胞外分泌。与此相反,通过抑制其目标磷酸肌依赖性蛋白激酶1,抑制miR-375的表达增强了胰岛素分泌。也就是说,miR-375胰岛素基因转录的减少会导致葡萄糖诱导的胰岛素分泌降低。 关于miR-15家族(miR-15a和miR-15b)调节有助于胰腺发育进程的胰腺转录因子的表达,miR-15a在胰岛素合成中起重要作用[51]。SUN等[52]先前在胰腺细胞中进行的研究显示,在1 h的高血糖暴露后,miR-15a水平升高,而在暴露3 d后下调。2003年,MICHAEL等[53]在人类身上展示了miR-15b的表达。JOGLEKAR等[54]研究显示miR-15a和miR-15b调控胰腺转录因子的表达,有助于胰腺发育的进展,miR-15a在胰岛素合成中起着重要作用。ZAMPETAKI等[55]指出,在2型糖尿病期间,miR-15a在血浆中被广泛下调。BORK-JENSEN等[56]的结果表明miR-15b可以调节关键的胰岛素信号蛋白水平。目前还需要进一步的研究来了解miR-15家族在胰岛素抵抗和2型糖尿病发展中的作用,以望早期防治2型糖尿病。 到目前为止,2型糖尿病是科学界在处理现代医学和新药发现方面面临的最大挑战之一。可以得出结论, miRNAs控制胰岛素的合成(见图4),具有调节胰岛素信号传导途径主要蛋白质级联表达的潜力。miRNAs也可以用作单个分子或联合治疗,迫切需要整合有关miRNAs对胰岛素信号传导途径,开发新的miRNAs相关诊断和治疗方法,以望在不久的将来解决2型糖尿病。 "
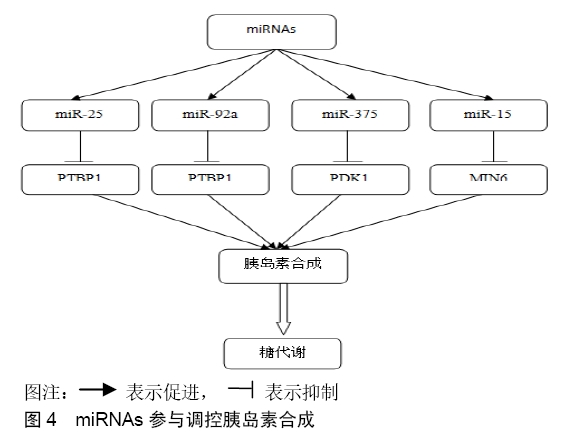
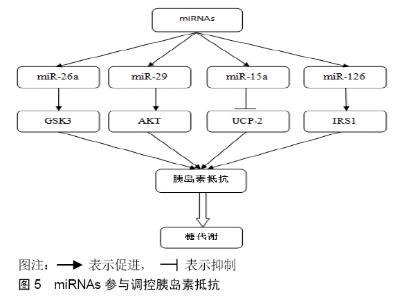
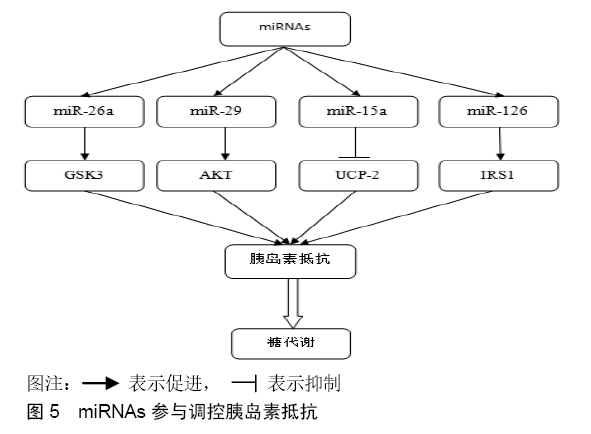
2.3.3 miRNAs参与调控胰岛素抵抗 miRNA作为一种小的非编码RNA,在转录后调控中起关键作用,胰岛素抵抗在2型糖尿病的发展过程中是一个标志,发生在与糖尿病相关的糖代谢紊乱的发病机制中。miRNAs可以结合并促进目标mRNA的去腺苷酸化和降解。翻译抑制是miRNAs的另一个重要功能,它可以直接与靶mRNA的3'-UTR结合并抑制翻译起始。研究表明,miRNAs参与调节由胰岛素抵抗引起的多种疾病。在2型糖尿病中,已经显示miR-144通过直接靶向IRS1 mRNA来促进胰岛素抵抗[56],已经显示miR-126介导的IRS1的抑制导致线粒体功能障碍和胰岛素抵抗[51]。胰岛素对Akt活化的调节作用对于糖代谢是至关重要的,肥胖诱导的miR-143过表达已经显示通过失活Akt信号传导途径导致高血糖症。蛋白酪氨酸磷酸酶1B(Protein tyrosine phosphatase 1B,PTP1B)通过酪氨酸残基的IR去磷酸化来损害胰岛素信号传导途径。PTP1B mRNA的3'-UTR是miR-122的靶标,而miR-122的表达降低导致肝脏胰岛素抵抗。 在胰岛素抵抗的脂肪细胞中,已经观察到抑制的miR-21的表达和受损的Akt信号传导。葡萄糖的转运也受miRNA的调控,跨膜蛋白GLUTs在葡萄糖转运中起重要作用。已经显示通过下调GLUT4的表达来降低胰岛素刺激的葡萄糖摄取,使miR-133水平升高。在心肌细胞中,已经显示miR-223促进GLUT4表达并增加葡萄糖摄取,研究表明miRNAs,如miR-144,通过抑制IR/IRS信号通路的激活,在促进胰岛素抵抗中发挥重要作用[57]。 以前的研究表明,miRNAs通过抑制胰岛素受体底物1(insulin receptor substrate 1,IRS1)蛋白翻译来调节线粒体功能障碍或糖尿病诱导的胰岛素抵抗[58]。研究显示miR-26a可以防止肥胖诱导的胰岛素抵抗,脂质过度合成和HGP升高。miR-26a靶向编码参与胰岛素信号传导(GSK3β,PKCδ和PKCθ),脂肪酸代谢(ACSL3和ACSL4)和糖异生(PCK1和TCF7L2)的因子的基因。揭示了miR-26a在肝脏代谢中的关键作用,并提示其作为改善胰岛素敏感性和抑制脂肪生成和糖异生的治疗靶标,从而阻止饮食诱导的肥胖(DIO)患者发生2型糖尿病[59]。 HONARDOOST等[1]研究发现miR-29家族成员(miR-29a,miR-29b和miR-29c)在大鼠的脂肪组织和骨骼肌中上调。通过在高葡萄糖和胰岛素的存在下孵育3个T3-L1脂肪细胞,体外可以复制升高的miR-29a和miR-29b。已知这些条件诱导胰岛素抵抗,表明在此过程中miR-29可能在脂肪细胞中发挥作用。事实上,3个T3-L1脂肪细胞中miR-29的过表达降低了胰岛素刺激的葡萄糖摄取,推测可能是通过抑制胰岛素信号通过AKT磷酸化和部分介导了2型糖尿病中的胰岛素抵抗[60-61]。在另一项研究中,伴有高血糖的高胰岛素血症导致miR-29a和miR-29b的表达增加,而miR-29c表达增加(原因不明)。因此,miR-29可能是糖尿病的另一个值得注意的目标。 miRNAs参与胰岛素的基因表达、生物合成和分泌。miR-15a通过抑制大鼠胰岛β细胞内源性耦合蛋白2 (uncoupling protein 2,UCP-2) 促进胰岛素生物合成。UCP-2是线粒体内膜载体蛋白家族的成员,并且miR-15a通过靶向UCP-2来调节氧消耗和ATP产生。任彦红等[62]研究表明,miR-126通过靶向胰岛素受体底物1参与了胰岛素抵抗的发展。因此,miRNAs可能成为开发有效的糖尿病药物的靶点。 近年来,一些研究集中在对胰岛素信号通路和胰岛素抵抗调控miRNAs的鉴定,从而与2型糖尿病的发病机制有关。不同组织中不同蛋白质级联的胰岛素抵抗的miRNAs谱可用于诊断2型糖尿病,而且miRNAs可以作为治疗剂来上调或下调与胰岛素抵抗相关的蛋白质表达(见图5)。广泛研究miRNAs在胰岛素抵抗的发展,以及在2型糖尿病发展期间的表达调控机制,为治疗和干预糖尿病等代谢疾病的新治疗靶标提供帮助。 "

2.4 在低氧运动中miRNAs对糖代谢的影响 研究显示miR-27a和miR-130等通过抑制PPARγ在肥胖的脂肪形成和病理生理学中发挥重要作用,miR-802的诱导基因Tcf2过表达导致胰岛素敏感性减弱。miR-103/107通过激活关键的磷酸化酶PTEN基因,负向调控Akt信号通路来促进胰岛素敏感性。miR-375通过靶向作用于PDK1降低葡萄糖诱导的胰岛素基因表达和蛋白质合成,同时通过靶向胰岛素转录因子负调节因子MAFA诱导胰岛素在β细胞中的表达,这些miRNAs在一定程度上对糖代谢产生影响进而影响胰岛素的稳态,在低氧运动中miRNAs也通过作用于靶基因间接影响胰岛素的表达。在低氧运动中miRNA-33的表达显著降低,miRNA-122显著升高。miR-34a的直接靶标LDHA,与mRNA的3-UTR区域结合,通过糖酵解的恢复抑制了miR-34a来减弱低氧诱导的功能障碍,结果显示miR-34a等在低氧诱导的功能障碍中起着重要的作用。 国内外的研究发现,低氧环境下的体质量显著降低。王宁琦等[63]、黄徐根等[64]发现,在低氧环境下4周或6周后,体质量明显下降。在海拔4 500 m的高空观察了7 d,平均体质量下降1.9 kg;停留32 d,减4 kg;缺氧刺激加速身体的能量代谢,并结合适当的运动强度和严格的饮食,身体吸收大于能力摄入,能源消耗的能量负平衡,导致低氧组明显高于减肥常氧组、低氧训练减肥效果优于常氧训练。Homa-ir是评价胰岛素的常用指标,Homa-ir计算的胰岛素抵抗指数与血糖夹持试验的胰岛素抵抗指数有明显的关系[65]。王宁琦等[63]通过对18名肥胖成年人(低氧组11人,常氧组7人)进行每周6 d,为期4周的训练,结果表明,低氧运动和常氧运动都能降低人的体质量,都能有效改善胰岛素抵抗,并在降低2型糖尿病风险方面发挥作用。 MACKENZIE等[36]通过对8例2型糖尿病患者进行 60 min以下的正常运动和低氧运动。研究证明,在2型糖尿病中,一次中等强度的运动可以增加葡萄糖的代谢,此外,当运动与低氧暴露相结合时,葡萄糖稳态的改善也增加了。MACKENZIE等[66]研究发现60 min的中等强度低氧运动,与常氧或低氧的间歇性运动相比,葡萄糖耐量提高最大。常氧的间歇性运动也刺激了2型糖尿病急性血糖的清除。也就是说,在低氧条件下持续锻炼60 min是血糖控制的最大改善,并可能使用低氧运动来治疗2型糖尿病。 国内外研究显示,miRNA-33和miRNA-122在肥胖患者的肝组织中都有表达且发挥着重要作用,同时参与了肝内糖脂肪代谢过程。李明锐等[67]通过运动干预对高脂饮食诱导的肥胖小鼠肝组织miRNA的探讨得出,与对照组相比,肥胖组miRNA-33的表达显著降低,miRNA-122的表达显著升高,与其他文献得出的结论一致[68-69]。经过运动干预之后,运动组的miRNA-33的表达显著升高。结果显示在运动调节高脂饮食诱导的肥胖中,miRNA-33可能在其中扮演着重要角色。 众所周知,在低氧诱导下miR-34a与心肌细胞凋亡有关,但其分子机制尚不清楚。在ZHANG等[70]目前的研究中证明了在低糖供应下大鼠的心肌细胞容易受到缺氧的影响,研究结果显示miR-34a在短时间缺氧的情况下诱导摄取葡萄糖和产生乳酸,但是在长期缺氧的情况下,细胞葡萄糖代谢受到抑制。另外还发现在体内和体外均观察到由于长期缺氧导致的miR-34a适应性上调,从而抑制心肌细胞的糖酵解。乳酸脱氢酶-A(LDHA)为miR-34a的直接靶标,与心肌细胞中LDHA mRNA的3-UTR区域结合,通过糖酵解的恢复抑制了miR-34a来减弱低氧诱导心肌细胞的功能障碍。miR-34a在低氧诱导心肌细胞功能障碍中起着重要的作用,抑制miR-34a来功能障碍性心肌细胞的糖酵解可能是治疗I/R损伤的有效治疗方法。具有诱导型细胞miR-222表达的小鼠在低氧运动中抑制了葡萄糖酵解[71]。推测miR-222可能通过血液循环进入组织器官诱发胰岛素抵抗,在生长发育调控中可能起重要作用,同时能改善糖代谢,降低胰岛素抵抗,降低2型糖尿病的风险[72-73]。 大量研究表明,间歇性低氧运动可以改善胰岛素抵抗大鼠的血脂代谢[65,74-75],增加肌肉含量,降低脂肪含量,增加胰岛素敏感性,改善胰岛素抵抗。国外学者MACKENZIE等[66,76-77]通过低氧和运动干预8例糖尿病患者发现,低氧能改善糖耐量,增加胰岛素敏感性,并提出运动与低氧对改善2型糖尿病患者胰岛素敏感性存在交互作用。在此基础上,Mackenzie研究了低氧条件下的运动方式和运动强度,发现中等强度的运动刺激了急性和中期胰岛素敏感性的改善。间歇运动不仅可以改善葡萄糖利用率,同时还改善运动后的胰岛素抵抗,当与运动和低氧结合时,效果更显著。低氧对胰岛素抵抗也有负面影响。长期暴露于低氧状态下,机体可能产生胰岛素抵抗,这与氧化应激程度与炎症有很大关系[78]。在肝脏中的间歇性缺氧会诱导胰岛素抵抗,损害β细胞功能,增加肝糖原输出并增加氧化应激水平,停止缺氧并不能完全改善上述观察到的葡萄糖代谢的变化。张荷 等[65]建立高脂饮食4周的低氧运动模型,观察大鼠血脂相关指标的变化,为相关实验研究提供参考,为胰岛素抵抗的治疗提供理论依据。 根据目前的研究显示,低氧运动和无氧运动都能有效改善糖代谢,降低胰岛素抵抗,增加胰岛素敏感性。但是,低氧运动对于miRNAs调控糖代谢的分子机制尚不明确,有待进一步研究,其研究成果可以为糖代谢紊乱引起的疾病提供理论依据。"

| [1] HONARDOOST M, SAROOKHANI MR, AREFIAN E, et al.Insulin resistance associated genes and mirnas. Appl Biochem Biotechnol. 2014;174(1):63-80. [2] BRAVO-EGANA V, ROSERO S, MOLANO RD, et al. Quantitative differential expression analysis reveals mir-7 as major islet microrna. Biochem Biophys Res Commun.2008;366(4):922-926. [3] KADAMKODE V, BANERJEE G. Micro rna: An epigenetic regulator of type 2 diabetes. Microrna. 2014;3(2):86-97. [4] MAO Y, MOHAN R, ZHANG S, et al. Micrornas as pharmacological targets in diabetes. Pharmacol Res. 2013;75:37-47. [5] 胡蕴,毛晓明.Mirna在2型糖尿病中的研究进展[J].医学研究生学报, 2011,24(9):1003-1006. [6] CHEN L, CAO ZL, HAN F, et al. Chronic intermittent hypoxia from pedo-stage decreases glucose transporter 4 expression in adipose tissue and causes insulin resistance. Chin Med J (Engl). 2010;123(4):463-470. [7] FU C, JIANG L, ZHU F, et al. Chronic intermittent hypoxia leads to insulin resistance and impaired glucose tolerance through dysregulation of adipokines in non-obese rats. Sleep Breath. 2015;19(4):1467-1473. [8] KLÖTING N, BERTHOLD S, KOVACS P, et al. Microrna expression in human omental and subcutaneous adipose tissue. Plos One. 2009;4(3):e4699. [9] CHAKRABORTY C1, GEORGE PRIYA DOSS C, BANDYOPADHYAY S. Mirnas in insulin resistance and diabetes-associated pancreatic cancer: The 'minute and miracle' molecule moving as a monitor in the 'genomic galaxy'. Curr Drug Targets. 2013;14(10):1110-1107. [10] FENG J, XING W, XIE L. Regulatory roles of micrornas in diabetes. Int J Mol Sci. 2016;17(10). pii: E1729. [11] WU L, DAI X, ZHAN J, et al.Profiling peripheral micrornas in obesity and type 2 diabetes mellitus. Apmis.2015;123(7): 580-585. [12] HINAULT C, DUMORTIER O, VAN OBBERGHEN E. microrna and diabetes: Tiny things causing huge effects. Med Sci (Paris). 2013;29(8-9):785-790. [13] VICKERS KASEY C, SHOUCRI BASSEM M, LEVIN MICHAEL G,et al Microrna‐27b is a regulatory hub in lipid metabolism and is altered in dyslipidemia. Hepatology.2013; 57(2): 533-542. [14] NING H, TAO H, WENG Z,et al.Plasma fatty acid-binding protein 4 (fabp4) as a novel biomarker to predict gestational diabetes mellitus. Acta Diabetologica.2016; 53(6):1-8. [15] VENIGALLA RK, TURNER M.Rna-binding proteins as a point of convergence of the pi3k and p38 mapk pathways. Front Immunol. 2012;3:398. [16] GUAY C,REGAZZI R.Circulating micrornas as novel biomarkers for diabetes mellitus. Nat Rev Endocrinol. 2013;9(9):513-521. [17] PRABU P, ROME S, SATHISHKUMAR C, et al. Circulating mirnas of 'asian indian phenotype' identified in subjects with impaired glucose tolerance and patients with type 2 diabetes. Plos One. 2015;10(5): e0128372. [18] 汪娅. Hmga2及let--7d mirna对糖尿病肾脏病肾小管上皮细胞转分化及肾脏纤维化的调控[D]. 广州:南方医科大学,2017. [19] 张冬雪,陈璐璐,廖云飞.微小rna在2型糖尿病相关机制中的研究进展[J]. 中华内分泌代谢杂志, 2012,28(11):944-947. [20] 尤卫绝.Mir-24在糖尿病胰岛β细胞损伤中的作用和机制研究[D]. 南京:南京医科大学,2016. [21] 郑宗基.Mir-26a和mir-30c协同调控tgfβ1诱导肾小管上皮细胞转分化在糖尿病肾脏病中的作用机制研究[D]. 广州:南方医科大学, 2016. [22] XU G, SHI C, JI C, et al. Expression of microrna-26b, an obesity-related microrna, is regulated by free fatty acids, glucose, dexamethasone and growth hormone in human adipocytes. Mol Med Rep. 2014;10(1):223-228. [23] KAJIMOTO K, NARABA H, IWAI N. Microrna and 3t3-l1 pre-adipocyte differentiation. Rna-a Publication of the Rna Society. 2006;12(9):1626-1632. [24] XU G, JI C, SONG G,et al. Mir-26b modulates insulin sensitivity in adipocytes by interrupting the pten/pi3k/akt pathway. Int J Obes (Lond). 2015;39(10):1523-1530. [25] 孟娅妮,于海伦. 7-二氟甲氧基-5,4'-二甲氧基金雀异黄素上调mir-26b对妊娠期糖尿病脂肪细胞葡萄糖摄取的影响[J].中国现代应用药学,2017,34(8):1104-1108. [26] KARBIENER M, FISCHER C, NOWITSCH S, et al.Microrna mir-27b impairs human adipocyte differentiation and targets ppargamma. Biochem Biophys Res Commun. 2009;390(2):247-251. [27] LEE EK, LEE MJ, ABDELMOHSEN K, et al.Mir-130 suppresses adipogenesis by inhibiting peroxisome proliferator-activated receptor gamma expression. Mol Cell Biol. 2011;31(4):626-638. [28] KENNELL JA, GERIN I, MACDOUGALD OA, et al. The microrna mir-8 is a conserved negative regulator of wnt signaling. Proc Natl Acad Sci U S A. 2008;105(40):15417-15422. [29] BHATIA P, RAINA S, CHUGH J, et al. Mirnas: Early prognostic biomarkers for type 2 diabetes mellitus?. Biomark Med. 2015; 9(10):1025-1040. [30] CHEN H, LAN HY, ROUKOS DH, et al. Application of micrornas in diabetes mellitus. J Endocrinol. 2014;222(1):R1-R10. [31] GONG W, XIAO D, MING G, et al. Type 2 diabetes mellitus- related genetic polymorphisms in micrornas and microrna target sites. J Diabetes. 2014;6(4):279-289. [32] MIRRA P, RACITI GA, NIGRO C, et al. Circulating mirnas as intercellular messengers, potential biomarkers and therapeutic targets for type 2 diabetes. Epigenomics. 2015; 7(4):653-667. [33] PARK SY, JEONG HJ, YANG WM, et al. Implications of micrornas in the pathogenesis of diabetes. Arch Pharm Res. 2013;36(2): 154-166. [34] LESLIE WS, FORD I, SATTAR N, et al. The diabetes remission clinical trial (direct): Protocol for a cluster randomised trial. Bmc Family Practice. 2016;17(1):20. [35] 陆康,李晔. Mirna与糖脂代谢[J].生命的化学, 2016, 36(3): 347-353. [36] MOTOHASHI N, ALEXANDER MS, SHIMIZU-MOTOHASHI Y,et al. Regulation of irs1/akt insulin signaling by microrna-128a during myogenesis. J Cell Sci. 2013;126(Pt 12):2678-2691. [37] CORREA-MEDINA M, BRAVO-EGANA V, ROSERO S, et al. Microrna mir-7 is preferentially expressed in endocrine cells of the developing and adult human pancreas. Gene Expr Patterns. 2009; 9(4):193-199. [38] KREDO-RUSSO S, NESS A, MANDELBAUM AD, et al. Regulation of pancreatic microrna-7 expression. 2014; 2012(10): 695214. [39] KREDO-RUSSO S, MANDELBAUM AD, NESS A, et al. Pancreas-enriched mirna refines endocrine cell differentiation. Development. 2012;139(16):3021-3031. [40] WEI R, YANG J, LIU GQ, et al. Dynamic expression of micrornas during the differentiation of human embryonic stem cells into insulin-producing cells. Gene.2013;518(2): 246-255. [41] KORNFELD JW, BAITZEL C, KÖNNER AC, et al. Obesity-induced overexpression of mir-802 impairs glucose metabolism through silencing of hnf1b. Nature.2013; 494(7435): 111-115. [42] JORDAN SD, KRÜGER M, WILLMES DM,ET AL. OBESITY-INDUCED OVEREXPRESSION OF MIRNA-143 INHIBITs insulin-stimulated akt activation and impairs glucose metabolism. Nature Cell Biology.2011; 13(4): 434-446. [43] TRAJKOVSKI M, HAUSSER J, SOUTSCHEK J, et al. Micrornas 103 and 107 regulate insulin sensitivity. Nature.2011;474(7353): 649. [44] VIVACQUA A, DE MARCO P, BELFIORE A,et al. Recent advances on the role of micrornas in both insulin resistance and cancer. Curr Pharm Des. 2017;23(25):3658-3666. [45] OLIVIERI F, RIPPO MR, PRATTICHIZZO F, et al.Toll like receptor signaling in “inflammaging”: Microrna as new players. Immun Ageing. 2013;10(1):11. [46] WANG R, HONG J, CAO Y, et al. Elevated circulating microrna-122 is associated with obesity and insulin resistance in young adults. Eur J Endocrinol. 2015;172(3):291-300. [47] ORTEGA FJ, MERCADER JM, CATALÁN V,et al. Targeting the circulating microrna signature of obesity. Clin Chem. 2013; 59(5): 781-792. [48] SETYOWATI KAROLINA D, SEPRAMANIAM S, TAN HZ,et al. Mir-25 and mir-92a regulate insulin i biosynthesis in rats. Rna Biology. 2013;10(8):1365-1378. [49] ORTEGA FJ, MERCADER JM, MORENO-NAVARRETE JM, et al. Profiling of circulating micrornas reveals common micrornas linked to type 2 diabetes that change with insulin sensitization. Diabetes Care. 2014; 37(5): 1375-1383. [50] LI X. Mir-375, a microrna related to diabetes. Gene. 2014; 533(1): 1-4. [51] CHAKRABORTY C, DOSS CG, BANDYOPADHYAY S, et al. Influence of mirna in insulin signaling pathway and insulin resistance: Micro-molecules with a major role in type-2 diabetes. Wiley Interdiscip Rev RNA. 2014;5(5):697-712. [52] SUN LL, JIANG BG, LI WT, et al. Microrna-15a positively regulates insulin synthesis by inhibiting uncoupling protein-2 expression. Diabetes Res Clin Pract.2011; 91(1): 94-100. [53] MICHAEL MZ, O' CONNOR SM, van Holst Pellekaan NG, et al. Reduced accumulation of specific micrornas in colorectal neoplasia. Mol Cancer Res. 2003;1(12):882-891. [54] JOGLEKAR MV, PAREKH VS, MEHTA S,et al.Microrna profiling of developing and regenerating pancreas reveal post-transcriptional regulation of neurogenin3. Dev Biol. 2007; 311(2):603-612. [55] ZAMPETAKI A, KIECHL S, DROZDOV I,et al.Plasma microrna profiling reveals loss of endothelial mir-126 and other micrornas in type 2 diabetes. Circ Res. 2010;107(6):810-817. [56] BORK-JENSEN J, SCHEELE C, CHRISTOPHERSEN DV, et al. Glucose tolerance is associated with differential expression of micrornas in skeletal muscle: Results from studies of twins with and without type 2 diabetes. Diabetologia.2015; 58(2):363-373. [57] YU Y, CHAI J. The function of mirnas and their potential as therapeutic targets in burn-induced insulin resistance (review). Int J Mol Med. 2015;35(2):305-310. [58] MA H, ZHANG S, SHI D, et al. Microrna-26a promotes regulatory t cells and suppresses autoimmune diabetes in mice. Inflammation. 2015;39(1):1-9. [59] FU X, DONG B, TIAN Y, et al. Microrna-26a regulates insulin sensitivity and metabolism of glucose and lipids. J Clin Invest. 2015;125(6):2497-2509. [60] FERLAND-MCCOLLOUGH D, OZANNE SE, SIDDLE K, et al. The involvement of micrornas in type?2 diabetes. Biochem Soc Trans. 2010;38(6):1565-1570. [61] FATJON L, MATTHEW T, JOHANNA DK. The role of ncrna in diabetes.Springer. 2015. [62] 任彦红,黄婷,时学秀,等. 循环mirna-126在2型糖尿病患者中的表达变化及其相关性研究[J].中国糖尿病杂志,2014, 22(7): 633-636. [63] 王宁琦,胡扬,官余凌,等. 4周低氧运动结合饮食控制对肥胖青年体重、血脂及胰岛素抵抗的影响[J].中国运动医学杂志,2012, 31(4): 289-294. [64] 黄徐根,冯连世,徐建方,等. 低氧训练过程中大鼠体重及能量代谢的变化[J].体育科学,2007,27(10):61-68. [65] 张荷,周越,张一民,等. 低氧运动对肥胖大鼠胰岛素抵抗及血脂代谢的影响[J].北京体育大学学报,2016,39(9):44-49,56. [66] MACKENZIE R,MAXWELL N,CASTLE P, et al. Intermittent exercise with and without hypoxia improves insulin sensitivity in individuals with type 2 diabetes. J Clin Endocrinol Metab.2012; 97(4): E546. [67] 李明锐,何劲松,吴让兵,等. Mirna?33在运动调节c57/bl6小鼠肥胖中的作用及机制探讨 [J]. 热带医学杂志,2017,17(8):1035-1038. [68] 邵芳,朱斌,顾志良. Microrna在脂类代谢中的功能研究进展[J].生命科学, 2013, 25(7): 676-684. [69] 杨卫利,王君佩,崔庆华,等.非编码rna与肝脏糖脂代谢调控[J].生理科学进展, 2016,47(3):194-202. [70] ZHANG Y, LIU G, GAO X. Attenuation of mir-34a protects cardiomyocytes against hypoxic stress through maintenance of glycolysis . Biosci Rep. 2017;37(6). pii: BSR20170925. [71] 林延艳,赵林双.运动诱导 mir-222在糖尿病小鼠心肌损害中的保护作用及机制[J].中华内分泌代谢杂志, 2017, 33(1):56-61. [72] 林延艳,赵林双,刘意,等.有氧运动对糖尿病小鼠心肌保护的作用机制及其与微小核糖核酸222的相关性研究[J].中国糖尿病杂志, 2017, 25(2):163-167. [73] HEMMATI AA, ALBOGHOBEISH S, AHANGARPOUR A.Chronic exposure to high fat diet exacerbates arsenic-induced lung damages in male mice: Possible role for oxidative stress. Monaldi Arch Chest Dis. 2018;88(1):903. [74] 林文弢,李颖,翁锡全.间歇性低氧和运动对高脂饮食诱导胰岛素抵抗大鼠血清内脂素的影响[J].中国运动医学杂志,2008,27(2):161-164. [75] 潘哲浩,翁锡全,朱宪锋,等.间歇低氧暴露对高脂膳食大鼠胰岛素敏感性的影响[J].中国运动医学杂志, 2012, 31(3): 244-247. [76] MACKENZIE R, ELLIOTT B, MAXWELL N,et al. The effect of hypoxia and work intensity on insulin resistance in type 2 diabetes. J Clin Endocrinol Metab.2012;97(1):155-162. [77] MACKENZIE R, MAXWELL N, CASTLE P,et al. Acute hypoxia and exercise improve insulin sensitivity (s(i) (2*)) in individuals with type 2 diabetes. Diabetes Metab Res Rev. 2011;27(1): 94-101. [78] 谭健,莫海兰,李洁,等.慢性间歇性缺氧对大鼠骨骼肌葡萄糖转运蛋白4表达的影响 [J]. 南方医科大学学报, 2014,34 (7): 1061-1064. |
| [1] | Kong Yamin, Yan Juntao, Ma Bingxiang, Li Huawei. Massage vibration intervenes with MyoD expression and proliferation and differentiation of muscle satellite cells in rats with sciatic nerve injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1160-1166. |
| [2] | Chen Xianghe, Liu Bo, Yang Kang, Lu Pengcheng, Yu Huilin. Treadmill exercise improves the myocardial fibrosis of spontaneous type 2 diabetic mice: an exploration on the functional pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1210-1215. |
| [3] | Zeng Xinyu, Chen Xianghe, Liu Bo, Lu Pengcheng, Jin Shengjie, Li Wenxiu, Tian Zhikai, Sun Changliang. Mechanism of exercise improving bone metabolism in type 2 diabetics mellitus based on "Muscle-Bone" Crosstalk [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 289-295. |
| [4] | Zhang Shuping, Dai Lingli, Wang Yajun, Liu Wenjuan, Huang Zuoyi. Effects of angiotensin converting enzyme inhibitors on oxidative stress related factors in a rat model of beta-amyloid 1-42 dementia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(35): 5650-5655. |
| [5] | Wen Miaomiao, Fan Junbai. Relationship between biological activities of Apelin and Elabela and diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(35): 5735-5740. |
| [6] | Zhang Chuanhui, Li Jianjun, Yang Jun. Effect of dynamic compression combined with insulin-like growth factor-1 gene transfection on chondrogenic differentiation of rabbit adipose-derived mesenchymal stem cells in chitosan/gelatin scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(28): 4485-4491. |
| [7] | Chen Ziyang, Pu Rui, Deng Shuang, Yuan Lingyan. Regulatory effect of exosomes on exercise-mediated insulin resistance diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 4089-4094. |
| [8] | Liu Yulin, Li Guotai. Combined effects of hyperbaric oxygen, vibration training and astaxanthin on bone mineral density, glucose metabolism and oxidative stress in diabetic osteoporosis rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3117-3124. |
| [9] | Zhang Chuanhui, Li Jianjun, Yang Jun. Effects of dynamic pressure on the proliferation and mechanical properties of rabbit adipose mesenchymal stem cells transfected with insulin-like growth factor-1 [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(13): 1982-1987. |
| [10] | Cao Guolong, Tian Faming, Liu Jiayin. Lovastatin combined with insulin effects on fracture healing in rat models of bilateral ovariectomized type 2 diabetic mellitus [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(5): 673-681. |
| [11] |
Li Ying, Lin Wentao, Weng Xiquan.
Effects of different exercise intensities on visfatin level and glucose metabolism in type 2 diabetic rats [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(26): 4196-4200. |
| [12] |
Zeng Zhaomu, Wen Xichao, Zhang Yuhao, Geng Lianting, Shen Yang, Zheng Kebin.
Role and application of exosomes-mediated miRNAs in the treatment of glioma [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(25): 4073-4080. |
| [13] | Li Hong, Wu Shaohua, Qiu Mingxing, Deng Qingfu, Lei Guolin, Li Qinglong. Mechanism underlying basic fibroblast growth factor and insulin-like growth factor-1 effects on proliferation and apoptosis of spermatogonial stem cells [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(19): 3017-3022. |
| [14] | Liu Xing, Wei Xiaohan, Deng Jie, Li Zhongming. Resveratrol repairs skeletal muscle injury by up-regulating basic fibroblast growth factor and insulin-like growth factor 1 [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(14): 2184-2191. |
| [15] | Zhao Jianfeng, Geng Yu, Chen Qianbo, Yang Jinghui, Li Yan. Changes in insulin resistance and inflammatory factors in cataract patients with glaucoma after phacoemulsification and trabeculectomy: a self-controlled trial [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(11): 1750-1755. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||