Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (2): 289-295.doi: 10.12307/2022.047
Previous Articles Next Articles
Mechanism of exercise improving bone metabolism in type 2 diabetics mellitus based on "Muscle-Bone" Crosstalk
Zeng Xinyu1, Chen Xianghe1, Liu Bo1, Lu Pengcheng1, Jin Shengjie1, Li Wenxiu1, Tian Zhikai1, Sun Changliang2
- 1School of Physical Education, Yangzhou University, Yangzhou 225127, Jiangsu Province, China; 2School of Physical Education and Health, Hebei Normal University of Science and Technology, Qinhuangdao 066004, Hebei Province, China
-
Received:2020-12-31Revised:2021-01-06Accepted:2021-02-10Online:2022-01-18Published:2021-10-28 -
Contact:Chen Xiaohe, MD, Associate professor, School of Physical Education, Yangzhou University, Yangzhou 225127, Jiangsu Province, China -
About author:Zeng Xinyu, School of Physical Education, Yangzhou University, Yangzhou 225127, Jiangsu Province, China -
Supported by:China Postdoctoral Science Foundation, No. 2019M661957 (to CXH)
CLC Number:
Cite this article
Zeng Xinyu, Chen Xianghe, Liu Bo, Lu Pengcheng, Jin Shengjie, Li Wenxiu, Tian Zhikai, Sun Changliang. Mechanism of exercise improving bone metabolism in type 2 diabetics mellitus based on "Muscle-Bone" Crosstalk[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 289-295.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
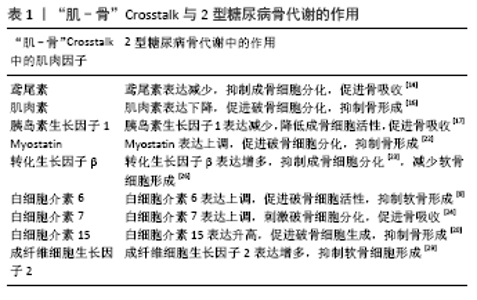
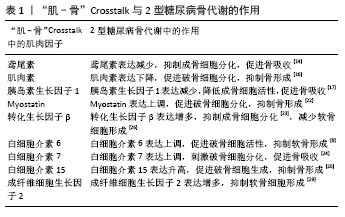
2.1 “肌-骨”Crosstalk 肌肉中的成肌细胞和骨骼中的成骨细胞共同来源于多功能间充质干细胞,两者在分化过程中通过“肌-骨”轴调控肌、骨代谢[6]。骨骼和肌肉是两个紧密相互作用的组织,最直观的是它们在运动功能上的互补性,肌肉收缩所产生的力需要施加在如骨骼之类的固体支撑物上,同时它本身也会刺激骨骼生长和重塑。但是,骨骼和肌肉之间的双向关系还发生在其他的串扰中,尤其是通过内分泌系统的体液途径,发生于细胞和分子中。所以,“肌-骨”Crosstalk不仅通过物理和机械方式相互作用,为机体提供基本运动能力,还通过串扰信号传导机制介导肌肉骨骼细胞代谢。 基于内分泌腺的定义,骨骼被认为是内分泌器官,可分泌成纤维细胞因子23和骨钙素等调节能量代谢。其中,成纤维细胞生长因子23是主要由成骨细胞产生的骨源性细胞因子,可作为循环激素来调节肾脏中磷酸盐运输和维生素D代谢,降低血磷水平,间接调节肌肉,引起肌肉无力[7]。骨钙素是由成骨细胞分泌并部分储存于骨基质中的骨形成标志物,可维持葡萄糖稳态,增强胰岛素耐受性。除了骨骼外,肌肉也可充当内分泌器官,产生并释放肌动蛋白,发挥特定作用影响其他器官。胰岛素生长因子1受肌肉分泌的胰岛素生长因子结合蛋白(IGFBPs)调节,可作用于骨骼。胰岛素生长因子1既可通过刺猬蛋白(hedgehog,HH)信号通路提高成骨细胞活性,也可经磷脂酰肌醇3-激酶(phosphatidylinositide 3-kinases,PI3K)/丝氨酸/苏氨酸特异性蛋白激酶(protein kinase B,Akt)信号通路增加破骨细胞表达。在骨骼肌中,肌纤维分泌的白细胞介素6可与白细胞介素6受体和糖蛋白130(gp130)受体反应,激活Janus激酶(the Janus kinase,JAK)/信号转导与转录激活因子(signal transducer and activator of transcriptions,STAT)通路,提高破骨细胞相关因子核因子κB活性[8]。白细胞介素6还激活膜受体酪氨酸蛋白激酶信号途径,导致转录因子CCAAT增强子结合蛋白β(CCAAT enhancer binding proteins,C/EBPβ)激活后与诱导型一氧化氮合酶和环氧化酶2等基因的启动子序列结合,刺激胰岛素生长因子1表达,其中C/EBPβ能够产生亮氨酸氨基肽酶(LAP)和血清脂肪酶,亮氨酸氨基肽酶介导成骨细胞成熟和破骨细胞形成,而脂肪酶抑制破骨细胞形成。在破骨细胞中,亮氨酸氨基肽酶和脂肪酶表达之间的平衡取决于mTOR活性,降低mTOR活性有利于亮氨酸氨基肽酶表达,而提高mTOR活性有利于脂肪酶表达,但白细胞介素6是否影响成骨细胞和破骨细胞中的mTOR活性尚不清楚[9]。白血病抑制因子是白细胞介素6家族细胞因子,被证明是从人类培养的肌管中分泌,具有多种生物学功能。其通过细胞因子共同受体糖蛋白130与白血病抑制因子受体结合进行信号传导,影响骨骼系统[9]。另一肌肉因子神经胶质细胞分化调节因子样因子(METRNL)对成骨细胞也有显著抑制作用,其在2型糖尿病机体血清内的含量较高,会抑制骨保护素(Osteoprotegerin,OPG)和骨桥蛋白的mRNA表达,降低成骨细胞活性,对骨形成有消极影响[10]。 2.2 “肌-骨”Crosstalk对2型糖尿病骨代谢的作用机制 2.2.1 “肌-骨”Crosstalk对2型糖尿病成骨细胞分化的作用机制 2型糖尿病会导致骨髓间充质干细胞分化产生的成骨细胞数量减少,抑制骨形成,对成骨细胞进行碱性磷酸酶染色后发现,2型糖尿病确实使成骨细胞介导的骨形成能力显著下降[11]。研究发现,骨骼中的Wnt信号传导在骨代谢中起核心作用,经典Wnt/β-catenin信号通路对成骨细胞分化的调节与骨硬素和Dickkopf相关蛋白1(DKK1)等受体抑制剂有关,2型糖尿病患者骨骼中DKK1表达水平高于正常人群,骨硬素表达减少,β-catenin水平降低,使成骨细胞分化减少,对骨代谢有消极影响。此外,β-catenin、骨髓细胞瘤癌基因(c-myc)、细胞周期蛋白D1(cyclin D1)、Runt相关转录因子2(Runx2)等Wnt信号通路相关基因表达下调,也会抑制成骨细胞活性,降低骨转换率[12]。 骨源性细胞因子通过内/旁分泌方式作用于骨骼,影响骨细胞分化。肌肉中分泌的肌动蛋白对肌肉的生长、萎缩起调控作用的同时还对骨组织各类细胞产生不同的作用。近年发现的鸢尾素是运动后由骨骼肌产生的新型肌动蛋白,能使白色脂肪组织引起褐变反应。运动通过过氧化物酶体增殖物激活受体γ辅激活因子1α(peroxisome proliferator-activated receptor-γ coactivator-1α,PGC-1α)依赖性机制增强肌组织中鸢尾素表达。产生的鸢尾素通过激活P38丝裂原活化蛋白激酶(P38 mitogen-activated protein kinase,p38MAPK)/细胞外信号调节激酶(extracellular signal-regulated kinase,ERK)途径,增强成骨细胞增殖分化及碱性磷酸酶活性和矿化作用。另一方面,鸢尾素通过抑制骨细胞中的核因子κB受体活化因子配体(receptor activator of NF-kB ligand,RANKL)和活化T细胞的核因子(nuclear factor of activated T-cells,NFATC1)来抑制破骨细胞形成[13]。由于鸢尾素在高血糖的环境下会出现有偿代谢现象,所以2型糖尿病机体内鸢尾素水平较健康机体明显偏低,易造成骨质疏松症状[14]。骨形态发生蛋白是在肌肉组织中释放,具有自、旁及内分泌功能的因子,能够使肌组织分化成表达骨性标志物的细胞,同样卫星细胞衍生的成肌细胞也可分化为成骨细胞。细胞外的骨形态发生蛋白与细胞膜上骨成型蛋白受体(BMPR)结合,刺激膜内Smads蛋白活性,使其进入细胞核内与DNA序列结合,激活BMP/Smads途径,促进骨髓间充质干细胞向成骨细胞分化,提高骨形成能力[15]。 在肌肉中高度表达的胰岛素生长因子1是肌肉生长、骨骼发育和骨量维持的关键生长因子,并具有胰岛素样代谢效应,胰岛素生长因子1可通过减少蛋白质降解,增加收缩性蛋白质mRNA含量和翻译率来加快蛋白质的合成速率。在骨形成过程中,从肌组织中分泌胰岛素生长因子1通过突触小泡作用于PI3K/Akt/mTOR途径诱导成骨细胞分化。多项研究发现,血清胰岛素生长因子1水平与骨密度正相关,是骨质疏松性骨折的预测因素,对维持骨代谢至关重要[16]。可促进1,25二羟基维生素D生成,增加钙的吸收,促进骨基质的合成,维持骨量和骨密度,改善2型糖尿病骨代谢[17]。而2型糖尿病的机体长期处于高血糖状态,致使肌组织中胰岛素生长因子1表达较少,骨形成能力下降。另一骨骼肌源性分泌因子肌肉素,也可作为诱导胰岛素抵抗的刺激物,其在2型糖尿病骨骼肌和血浆内水平较高,抑制成肌细胞中胰岛素刺激的2-去氧-D-葡萄糖(2-DG)摄取和糖原合成,降低胰岛素信号级联反应中PI3K/Akt活化,抑制破骨细胞分化,导致骨代谢紊乱[18]。 综上所述,2型糖尿病的发生使机体内形成高血糖的环境,胰岛素分泌减少,骨骼中骨硬素和DKK1分泌减少,抑制经典Wnt信号通路,下调β-catenin、cyclin D1、Runx2等,降低骨形成。肌动蛋白鸢尾素受2型糖尿病影响分泌减少,抑制P38MAPK/ERK途径,使RANKL和NFATC1活性增强,碱性磷酸酶活性减弱;还有肌肉因子肌肉素和胰岛素生长因子1表达也下调,抑制PI3K/Akt通路,造成糖原合成减少,蛋白质降解增多,对成骨细胞分化产生消极影响,破骨细胞介导的骨吸收能力强于成骨细胞介导的骨形成能力,致使骨密度下降。 2.2.2 “肌-骨”Crosstalk对2型糖尿病破骨细胞分化的作用机制 破骨细胞生成涉及的蛋白因子包括巨噬细胞集落刺激因子、NFATC1、RANKL等[19]。核因子κB受体活化因子(receptor activator of NF-kB,RANK)和RANKL结合可促进破骨细胞分化,而骨保护素会阻断两者结合,延缓破骨细胞分化并抑制骨吸收。2型糖尿病机体内血糖较高使组织蛋白酶K(CTSK)及RANKL/OPG的比例升高,促进RANKL诱导的破骨细胞分化,降低骨转换[20]。在核因子κB通路中,RANKL信号经RANK传递给肿瘤坏死因子受体相关蛋白6(TRAF6),肿瘤坏死因子受体相关蛋白6通过核因子κB诱导激酶(NF-κB inducible kinase,NIK)和IκB激酶(the IκB kinase,IKK)活化核因子κB。2型糖尿病机体骨骼中核因子κB抑制蛋白α(Inhibitor of nuclear factor kappa-B α,IκBα)磷酸化水平升高,促使破骨细胞分泌增加,延缓骨形成[21]。 在肌肉组织中,Myostatin是最早被发现的肌肉因子,属于转化生长因子β家族的细胞外信使,对肌肉生长有负调控作用,是骨骼肌细胞增殖分化最有效的抑制剂。它与ⅡB型激活素受体(ACVR2B)结合,激活素受体样激酶4(Activin receptor-like kinase 4,ALK4)、ALK5活化,Smad2和Smad3(转化生长因子β特异性Smads)磷酸化,进而调节NFATC1,增强骨细胞中RANKL诱导的促破骨细胞形成受体活化剂,提高骨吸收能力[22]。2型糖尿病机体血清中的Myostatin含量升高,促进Smad2和Smad3分泌激活RANKL,提高破骨细胞活性,导致骨代谢紊乱。肌组织中的转化生长因子β对骨吸收有重要影响,当其浓度偏高时可诱导破骨细胞分泌,降低骨形成能力。研究发现2型糖尿病机体内转化生长因子β表达高于健康人群,且转化生长因子β与2型糖尿病引发的骨病有关,所以其对2型糖尿病骨代谢有消极作用[23]。白细胞介素6是由肌管分泌的一种多效性细胞因子,可通过诱导成骨细胞和基质细胞分泌的RANKL表达,积极参与破骨细胞形成。也可通过与白细胞介素6受体、糖蛋白130结合而激活JAK/STAT通路,诱导RANKL分泌刺激破骨细胞生成[8]。白细胞介素6通过诱导细胞因子信号传导抑制蛋白3(SOCS-3)的表达来破坏胰岛素受体底物(IRS)和胰岛素受体底物1的磷酸化,从而引起胰岛素抵抗。肌组织中的白细胞介素7间接地通过T细胞诱导破骨细胞相关因子RANKL和肿瘤坏死因子α生成,提高破骨细胞形成。此外,白细胞介素7还可以通过诱导信号传导及转录激活蛋白5(STAT5)激活,直接独立于RANKL而直接诱导破骨细胞形成[24]。白细胞介素15是一种在肌肉组织中高度表达的细胞因子,在人体骨骼肌细胞培养物中,白细胞介素15诱导分化的肌管中肌球蛋白重链(MHC)蛋白的积累,表明白细胞介素15对肌肉细胞培养具有合成代谢作用,降低肌肉降解速率,影响肌肉生长。以前研究发现,白细胞介素15是骨骼中肿瘤坏死因子α的强刺激剂,可诱导成骨细胞和骨基质细胞中RANKL表达,从而导致破骨细胞生成增强。最近发现,白细胞介素15通过诱导ERK活化,在破骨细胞形成中与RANKL发挥协同作用[20]。 综上所述,2型糖尿病会造成胰岛细胞功能紊乱,破骨细胞凋亡能力高于成骨细胞分化能力,骨吸收和骨形成之间代谢失衡。骨骼中核因子κB途径激活,RANKL诱导的促进破骨细胞形成的受体活化剂含量增多,同时在骨骼肌中Myostatin表达上调,Smad2和Smad3分泌激活RANKL,促进破骨细胞分化。白细胞介素6、白细胞介素7、白细胞介素15等肌肉因子也可诱导RANKL表达,参与破骨细胞形成,进而导致成骨细胞分化能力下降,骨组织细胞降解过多,易发生骨质疏松。 2.3 “肌-骨”Crosstalk对2型糖尿病软骨细胞分化的作用机制 关节软骨是关节的承重表面,具有单一细胞类型的软骨细胞。软骨基质产生受多种因素控制,包括生长激素、甲状旁腺激素相关肽(PTHrP)、成纤维细胞生长因子和转化生长因子β家族成员等,这些信号被系统地提供给软骨及发育中的软骨周围组织或软骨细胞本身,以维持软骨内平衡。骨骼中的核因子κB信号通路在软骨细胞中被激活,对软骨细胞具有调控作用,其通过诱导白细胞介素1β、肿瘤坏死因子α、基质金属蛋白酶13及核因子κB蛋白抑制剂的分泌,使软骨细胞凋亡,进而造成骨关节炎等发生[24]。2型糖尿病患者骨骼中核因子κB通路受高糖环境影响被激活,肿瘤坏死因子α、白细胞介素1β等因子表达上调,导致软骨细胞凋亡坏死;也可诱导转录因子核因子κB活性的p38MAPK信号通路,增加环氧化酶2和前列腺素E2的表达,促进组蛋白去乙酰化酶4(HDAC4)降解,释放Runx2,加速肿瘤坏死因子α活化,促进软骨细胞凋亡[25]。此外,核因子κB途径中的白细胞介素1β可诱导白细胞介素6、前列腺素E2和环氧合酶2等过度表达,进而激活一系列肌组织中的基质金属蛋白酶,如基质金属蛋白酶1和13。在2型糖尿病机体内,晚期糖基化终末产物含量增多,其与细胞表面的晚期糖基化终产物受体和Toll样受体(TLRs)结合诱导关节软骨细胞促炎和分解,激活MAPK和核因子κB途径,同时下调过氧化物酶体增殖物激活受体γ(Peroxisome proliferator-activated receptor gamma,PPARγ)活性,导致Ⅱ型胶原蛋白生成减少,软骨细胞凋亡[26]。 肌肉因子转化生长因子β可调节细胞生长分化及免疫抑制,对骨形成及修复有重要作用。在2型糖尿病患者体内的转化生长因子β含量较正常人群明显增高,其能诱导辅助性T细胞17(Th17)细胞分泌白细胞介素17及多种炎症因子生成,损害免疫系统,加剧炎症反应,导致软骨细胞凋亡[27]。而骨形态发生蛋白信号通路通过维持转录因子性别决定区Y-box蛋白9(sex determining region Y-box protein 9,SOX9)的表达来促进软骨细胞增殖分化,骨形态发生蛋白2和骨形态发生蛋白4协同促进软骨细胞分化增殖,骨形态发生蛋白7和骨形态发生蛋白受体1A(BMPR1A)能调节软骨新陈代谢,维持软骨稳态[28]。而肌组织中成纤维细胞生长因子家族的成纤维细胞生长因子2可通过激活p44/p42 MAPK增加血管内皮生长因子的水平,两者协同作用对软骨细胞有消极作用[29]。 综上所述,2型糖尿病使机体内胰岛素分泌减少时导致机体代谢紊乱,对葡萄糖利用能力下降,蛋白质和脂肪消耗增多,骨胶原分解大于合成。骨骼中的核因子κB通路激活,诱导肿瘤坏死因子α、白细胞介素1β等促软骨细胞凋亡因子上调,PPARγ活性下调,减少Ⅱ型胶原蛋白生成。且核因子κB因子可激活p38MAPK通路,促使环氧化酶和前列腺素E2分泌增多,肿瘤坏死因子α表达上调,抑制软骨细胞分化。肌肉因子转化生长因子β在2型糖尿病机体内含量较高,可诱导炎症因子,对软骨细胞造成损害;白细胞介素6可通过肌肉分泌也能由骨骼中的白细胞介素1β诱导产生,激活肌肉中的基质金属蛋白酶,促使软骨细胞分化能力下降;成纤维细胞生长因子2与自身激活p44/p42 MAPK诱导的血管内皮生长因子协同反应,促进炎症因子生成,破坏软骨结构。 “肌-骨”Crosstalk中的肌肉因子与2型糖尿病骨代谢的作用见表1。"
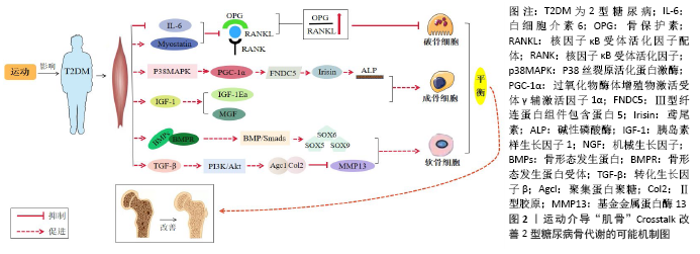
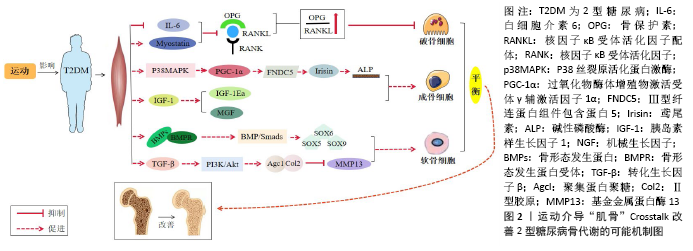
2.4 运动介导“肌-骨”Crosstalk对2型糖尿病骨代谢的作用 2.4.1 运动介导“肌-骨”Crosstalk对2型糖尿病成骨细胞分化的作用 运动可刺激肌骨系统相关因子表达和通路转导作用于骨组织,起到增加骨量、减少骨丢失的作用,对骨代谢产生积极影响。骨组织中Wnt/β-catenin途径是骨量的重要调节剂,可将机械负荷信号传递到骨表面细胞上,该途径与前列腺素途径串扰激活,使骨骼形成的负调节剂(如骨硬素和Dkk1)减少。在2型糖尿病大鼠骨髓间充质干细胞中,细胞代谢活性、碱性磷酸酶活性及成骨基因表达降低,这可能是由于Wnt途径传导受到抑制及β-catenin、cyclin D1、c-myc和Runx2的mRNA和蛋白表达水平下降导致。研究发现,老年骨质疏松大鼠进行9周中、低强度运动后Wnt信号和β-catenin mRNA表达显著提高,促进成骨细胞分化[30];在另一研究中,青春期男女进行短时间大强度递增负荷运动后,Wnt信号通路被激活并促进了骨保护素分泌,提高了成骨细胞活性[31]。从医学角度发现,跑步运动可上调骨组织中的Wnt1、Wnt3a、β-catenin蛋白,进而激活Runx2,增加骨保护素和骨钙素的表达,促进成骨细胞分化,且负重运动的效果也十分显著[32]。其他研究发现,运动可增强Wnt信号通路的成骨因子卷曲蛋白6(FZD6)、受体酪氨酸激酶样孤立受体2(Ror2)和β-catenin蛋白的表达及抑制分泌性卷曲相关蛋白4(sFRP4)、DDK1的表达,促进成骨细胞生成,且还可降低Wnt通路抑制剂骨硬素的表达激活通路,促进骨的形成[33]。 肌肉因子鸢尾素是位于骨骼肌中的跨膜蛋白。在运动过程中,活性氧水平提高激活p38MAPK途径,诱导PGC-1α 产生,使PGC-1α上调肌肉中Ⅲ型纤连蛋白组件包含蛋白5(fibronectin typeⅢ domain-containing protein 5,FNDC5)的表达,经蛋白水解酶水解后形成鸢尾素。鸢尾素由PGC-1α介导产生,PGC-1α在2型糖尿病肌肉中表达减少,导致鸢尾素分泌含量降低。研究发现,每次6 min的全身性震动运动、3组为30 min直立式原地踏车运动、为期8周或24周的阻力运动,这类长时间运动会使血液中鸢尾素水平升高,而自由泳运动、原地脚踏车或持续定速跑步30 min等单次运动也可能会使鸢尾素水平升高,增强碱性磷酸酶活性,促进成骨细胞分化[34]。2型糖尿病患者肌组织中骨形态发生蛋白系列蛋白受抑制,使成骨细胞分化不足,进而导致2型糖尿病骨质疏松,对2型糖尿病骨代谢有消极影响。运动可上调骨形态发生蛋白中的骨形态发生蛋白2表达,使β-catenin含量积累增多和减少糖原合成酶激酶3β(GSK-3β)分泌,以激活骨组织中Wnt/β-catenin信号通路,提高骨形成能力。骨形态发生蛋白形成的BMP/Smads信号通路对成骨细胞的生成也具有调控作用,运动加强细胞外的骨形态发生蛋白与骨形态发生蛋白受体结合,激活BMP/Smads途径,促进骨髓间充质干细胞向成骨细胞分化[35]。胰岛素生长因子1是一种在分子结构上与胰岛素相当的因子,来自胰岛素生长因子1基因剪接变体的IGF-1Ea和IGF-1Eb/c[也称为机械生长因子(mechano growth factor,MGF)]对肌肉和骨骼之间的平衡起作用。在骨骼肌中,通过拉伸被动施加负荷或通过神经元启动的收缩活性主动施加机械负荷,都会刺激IGF-1Ea和机械生长因子的表达。胰岛素生长因子1通过PI3K/Akt/mTOR途径加快肌纤维蛋白翻译的速率,抑制分解代谢型泛素连接酶E3(ubiquitin-protein ligase E3)的表达,增加肌肉质量。同时,通过PI3K/Akt/mTOR途径增强成骨细胞前体细胞分化,刺激成骨细胞中RANKL的表达[36]。研究发现,进行8周,每周6次,每次持续50 min的游泳和下坡跑的运动训练后,游泳组和下坡跑组小鼠肌肉中的胰岛素生长因子1蛋白表达量显著增加,跳跃组小鼠肌肉中的胰岛素生长因子1蛋白表达量比安静组有增高的趋势,但无统计学差异[37]。这说明长时间动力性收缩可有效增加肌肉分泌胰岛素生长因子1,平衡2型糖尿病骨代谢,而静力性收缩效果不显著。 2.4.2 运动介导“肌-骨”Crosstalk对2型糖尿病破骨细胞分化的作用 2型糖尿病骨质疏松的发生与破骨细胞分化增多和成骨细胞分化减少,骨基质、骨密度下降有关。运动作为一种非药物性干预方式,可直接刺激肌骨系统,调节各细胞基因的分泌表达,有效改善2型糖尿病骨代谢。破骨细胞相关因子RANKL由骨组织中骨髓间充质干细胞和成骨细胞产生,是骨量丢失的主要介质,与其受体RANK和诱饵受体骨保护素形成的RANKL/RANK/OPG轴对破骨细胞形成、功能和存活起着至关重要的作用[38]。研究发现,2型糖尿病小鼠体内破骨细胞分化异常升高,RANKL/OPG比值高于正常小鼠,骨密度下降。通过下坡跑运动能抑制2型糖尿病小鼠骨中OPG/RANKL/RANK信号通路,使肿瘤坏死因子受体相关因子与RANK胞质区结合抑制骨组织中CN/NFAT途径,或与肌肉因子肌球蛋白重链、骨形态发生蛋白2、白细胞介素3等共同抑制NFATC1表达,促使OPG/RANKL比值升高,抑制破骨细胞生成,提高骨形成,改善骨代谢[39]。在其他动物实验中,跑步或振动刺激运动可抑制2型糖尿病机体骨骼中晚期糖基化终末产物诱导的RANKL活性,促进骨保护素表达升高,提高成骨细胞分化水平;受运动人群、年龄、运动强度、运动时间、运动频率等因素影响,急性运动、长期运动或负荷运动对2型糖尿病机体骨骼中的OPG/RANKL/RANK轴的影响有待进一步探究[40]。 研究发现,在大鼠进行为期5 d的游泳训练后24 h,腓肠肌和外侧股肌的Myostatin mRNA水平下降了一半以上;在人体试验中,进行9周的自行车耐力运动训练也使Myostatin mRNA水平降低了一半以上[41]。10名职业拳击手和10名久坐男性进行4×30 s Wingate测试后发现两组Myostatin水平升高[42],这说明急性高强度间歇运动可增加Myostatin水平,而耐力运动会降低Myostatin表达。已发现Myostatin可增强RANKL的表达,刺激破骨细胞的分化和活性;相反,Myostatin缺失小鼠的骨骼中间充质干细胞向成骨细胞分化增加[43]。在对2型糖尿病男性患者进行每周3次为期12周的有氧耐力和抗氧训练,训练结束后发现运动组血清鸢尾素浓度均增加,对照组血清Myostatin浓度均下降,抑制RANKL分泌,减少破骨细胞分化,改善2型糖尿病骨代谢[44]。白细胞介素6是肌肉中的骨钙素靶基因,是一种在运动过程中循环水平升高并能提高运动能力的肌肉因子。其通过使前列腺素E2进入骨组织并增加成骨细胞表面RANKL的分泌来促进破骨细胞的分化;或白细胞介素6与可溶性白细胞介素6受体一起在成骨细胞表面上诱导核因子κB配体RANKL的受体活化剂表达,RANKL与破骨细胞祖细胞表面表达的RANK相互作用[8]。在2型糖尿病导致RANKL和骨保护素水平升高并降低骨密度的过程中,白细胞介素6通过诱导细胞因子信号转导抑制因子3的表达来破坏胰岛素受体和胰岛素受体底物1的磷酸化,从而引起胰岛素抵抗[17]。研究发现,进行长期运动(包括有氧运动或抗阻运动)会使2型糖尿病血浆中的白细胞介素6水平降低,减少RANKL表达,抑制破骨细胞活性[45]。而进行单次运动、急性耐力运动或高强度间歇训练后,发现血浆中白细胞介素6水平随运动而增加,对骨代谢有消极影响[46]。 2.4.3 运动介导“肌-骨”Crosstalk对2型糖尿病软骨细胞分化的作用 间充质干细胞来自人的骨髓,可被诱导形成成骨细胞或软骨细胞,2型糖尿病的特征包括全身性慢性低度炎症,骨关节炎是2型糖尿病引起的并发症之一,因为活性氧的过度产生,改变细胞内信号传导、软骨细胞生命周期及软骨基质的代谢。运动使机体骨骼负重或各关节肌肉活动,这些应力刺激使2型糖尿病机体内的肌骨因子分化并通过 旁/内分泌方式分泌作用于软骨组织,影响软骨细胞的增殖、分化和凋亡。骨骼中的Wnt信号通路,其作用广泛、影响之深,对软骨、骨以及关节的形成有重要调节作用,且在调节软骨生成、维持软骨细胞表型及基质完整性等方面也有影响。Wnt途径中的β-catenin 蛋白是软骨细胞增殖分化以及软骨细胞直接转分化为骨细胞的关键调节剂,但2型糖尿病发生会抑制经典Wnt途径中β-catenin信号,使Wnt/β-catenin信号通路失活,对软骨细胞生成有消极影响。而运动产生的刺激可抑制肌肉中糖原合成酶激酶3β而上调β-catenin的表达,激活Wnt/β-catenin信号通路,促进软骨内成骨的生长,增加软骨细胞分泌[47]。 在肌肉组织中释放的骨形态发生蛋白在基于间充质干细胞的软骨再生中表现出重要作用。骨形态发生蛋白不仅可以增强间充质干细胞的软骨分化能力,而且可以将内源性间充质干细胞募集到受伤部位,以刺激软骨的修复过程。其可以调控SOX5、SOX6和SOX9等软骨形成因子的表达,进而影响小鼠胚胎中骨髓间充质干细胞向软骨细胞分化,促进软骨细胞的增殖和成熟。研究发现,适度的运动能提高骨形态发生蛋白2、骨形态发生蛋白4、骨形态发生蛋白6、骨形态发生蛋白受体2、磷酸化Smad-5(p Smad-5)和DNA结合蛋白1(DBP-1)抑制剂的表达,增强软骨分化能力,抑制软骨退 变[16]。转化生长因子β在调节间充质干细胞分化和软骨形成中至关重要。转化生长因子β亚型及其受体包括转化生长因子β RI或间变性淋巴瘤激酶5(ALK5)和转化生长因子β RII或重组人转化生长因子B受体2(TGFbR2)等在软骨内和膜内骨化中都起重要作用。肌肉中分泌的转化生长因子β通过突触小泡释放激活骨骼中的PI3K/Akt/mTOR通路,降低软骨细胞和软骨外植体中基质金属蛋白酶13的表达,维持软骨胶原之间的肽链,防治软骨破坏,其中PI3K/AKT/mTOR通路是软骨动态平衡所必需的[48]。2型糖尿病的发生导致机体出现炎症反应,作用于PI3K/Akt/mTOR途径的转化生长因子β表达减少,基质金属蛋白酶13大量分泌,破坏软骨间肽链,抑制软骨细胞生成,造成软骨退化。运动可以促进肌肉组织中转化生长因子β分化,激活PI3K/Akt/mTOR信号通路,促进软骨细胞表达软骨特异的细胞外基质分子Ⅱ型胶原蛋白和天冬氨酸谷氨酸载体蛋白亚型1(Agc1)表达,降低基质金属蛋白酶13分泌,促进软骨细胞分化,维持正常软骨细胞功能[49]。 综上所述,运动对2型糖尿病中的成骨细胞和软骨细胞分化有促进作用,对破骨细胞活性有抑制作用。骨骼中的Wnt信号通路受运动影响被激活,上调途径中β-catenin、DKK1和Runx2等蛋白表达,促进成骨细胞分化和软骨细胞生。肌肉中P38MAPK通路激活,产生的PGC-1α使FNDC5分泌增多,蛋白水解后形成鸢尾素,提高碱性磷酸酶活性,同时胰岛素生长因子1表达上调,促进IGF-1Ea和机械生长因子生成,促进成骨细胞分化。骨形态发生蛋白可增强间充质干细胞向软骨细胞分化的能力,其系列蛋白如骨形态发生蛋白2、骨形态发生蛋白6等对软骨细胞分化有积极意义,还有肌肉中分泌的转化生长因子β释放作用于骨骼中的PI3K/Akt通路也可维持软骨中的动态平衡。相反地,运动后可减少破骨细胞分化,通过增多肌肉因子Myostatin和降低白细胞介素6表达,使RANKL/OPG比值下降,抑制RANKL和NFATC1表达。详细机制见图2。"
| [1] MATHIEU C. Developments in the management of type 1 and type 2 diabetes. Eur Endocrinol. 2018;14(2):13-14. [2] HERMANS MP, AMOUSSOU GKD, BOUENIZABILA E, et al. Size, density and cholesterol load of HDL predict microangiopathy,coronary artery disease and β-cell function in men with T2DM. Diabetes Metab Syndr. 2017;11: 125-131. [3] 江洪. 不同运动强度干预2型糖尿病模型大鼠的骨密度变化[J].中国组织工程研究,2016,20(27):3963-3969. [4] 陈祥和. 不同方式运动对II糖尿病小鼠骨代谢的影响及分子机制研究[D]. 上海:华东师范大学,2016. [5] 方幸, 李世昌, 徐帅. 肌肉因子与运动对骨骼的作用[J]. 中国体育科技, 2017,53(6):71-78. [6] LI G, ZHANG L, ZHANG L, et al. Muscle-bone crosstalk and potential therapies for sarco-osteoporosis. J Cell Biochem. 2019;120(9):14262-14273. [7] 黄宏兴, 吴青, 李跃华, 等. 肌肉、骨骼与骨质疏松专家共识[J]. 中国骨质疏松杂志,2016,22(10):1221-1229+1236. [8] MIHARA M, HASHIZUME M, YOSHIDA H, et al. IL-6/IL-6 receptor system and its role in physiological and pathological conditions. Clin Sci (Lond). 2012; 122(4):143-159. [9] BAKKER AD, JASPERS RT. IL-6 and IGF-1 signaling within and between muscle and bone: how important is the mTOR pathway for bone metabolism?. Curr Osteoporos Rep. 2015;13(3):131-139. [10] GONG W, LIU Y, WU Z, et al. Meteorin-like shows unique expression pattern in bone and its overexpression inhibits osteoblast differentiation. PLoS One. 2016;11(10):e0164446. [11] ERJAVEC I, BORDUKALO NT, BRKLJACIC J, et al. Constitutively elevated blood serotonin is as sociated with bone loss and type 2diabetes in rats. PLoS One. 2016;11(2):e0150102. [12] HUYBRECHTS Y, MORTIER G, BOUDIN E, et al. WNT Signaling and Bone: Lessons From Skeletal Dysplasias and Disorders. Front Endocrinol (Lausanne). 2020;11:165. [13] KWON JH, MOON KM, MIN KW. Exercise-Induced Myokines can Explain the Importance of Physical Activity in the Elderly: An Overview. Healthcare (Basel). 2020;8(4):378. [14] 王贺, 王莲地, 阳琰, 等. 2型糖尿病合并骨质疏松患者血清25羟维生素D、鸢尾素水平观察及其与骨密度的关系[J]. 中国糖尿病杂志,2018, 26(7):569-572. [15] WEI XF, CHEN QL, FU Y, et al. Wnt and BMP signaling pathways co-operatively induce the differentiation of multiple myeloma mesenchymal stem cells into osteoblasts by upregulating EMX2. J Cell Biochem. 2019; 120(4):6515-6527. [16] BIKLE DD, TAHIMIC C, CHANG W, et al. Role of IGF-I signaling in muscle bone interactions. Bone. 2015;80:79-88. [17] 陆鹏程, 陈祥和, 杨康, 等. 自噬介导运动改善2型糖尿病骨代谢紊乱的作用机制[J].中国组织工程研究,2020,24(20):3256-3262. [18] CHEN WJ, LIU Y, SUI YB, et al. Increased circulating levels of musclin in newly diagnosed type 2 diabetic patients. Diab Vasc Dis Res. 2017;14(2):116-121. [19] Willems WF, Larsen M, Friedrich PF, et al. Induction of angiogenesis and osteogenesis in surgically revascularized frozen bone allografts by sustained delivery of FGF-2 and VEGF. J Orthop Res. 2012;30(10):1556-1562. [20] RATHINAVELU S, RATHINAVELU S, BANU J. Molecular modulation of osteoblasts and osteoclasts in type 2 diabetes. J Diabetes Res. 2018:6354787. [21] 马涛, 李世昌. 上、下坡跑台运动对去卵巢小鼠破骨细胞分化NF-κB信号通路的影响[J]. 中国运动医学杂志,2015,34(5):468-474. [22] DANKBAR B, FENNEN M, BRUNERT D, et al. Myostatin is a direct regulator of osteoclast differentiation and its inhibition reduces inflammatory joint destruction in mice. Nat Med. 2015; 21(9):1085-1090. [23] 鲍晓雪, 王娜, 李玉坤, 等. 血清OPG、TGF-β和IL-6水平对绝经后骨量减少合并2型糖尿病患者骨折风险的预测[J]. 中华老年骨科与康复电子杂志,2018,4(1):9-13. [24] AMARASEKARA DS, YUN H, KIM S, et al. Regulation of Osteoclast Differentiation by Cytokine Networks. Immune Netw. 2018;18(1):e8. [24] CHOI MC, JO J, PARK J, et al. NF-κB signaling pathways in osteoarthritic cartilage destruction. Cells. 2019;8(7):734. [25] 刘波, 陈祥和, 杨康, 等. DNA甲基化在运动干预骨质疏松中的作用机制[J].中国组织工程研究,2021,25(5):791-797. [26] CANNATA F, VADALÀ G, Ambrosio L, et al. Osteoarthritis and type 2 diabetes: From pathogenetic factors to therapeutic intervention. Diabetes Metab Res Rev. 2020;36(3):e3254. [27] BLANEY DEN, SCHARSTUHL A, VINERS EL, et al. Reduce IX1 transforming growth factor-bets signaling in cartilge of old mice:role in impaired repair capadty. Arthritis Res Ther. 2005;7(6):R1338-1347. [28] WANG Z, SUN J, LI Y, et al. Experimental study of the synergistic effect and network regulation mechanisms of an applied combination of BMP-2, VEGF, and TGF-β1 on osteogenic differentiation.J Cell Biochem. 2020;121(3): 2394-2405. [29] HUANG H, LUO L, LIU Z, et al. Role of TNF-α and FGF-2 in the fracture healing disorder of type 2 diabetes model induced by high fat diet followed by streptozotocin. Diabetes Metab Syndr Obes. 2020;13:2279-2288. [30] CHEN X, LI L, GUO J, et al. Treadmill running exercise prevents senile osteoporosis and upregulates the Wnt signaling pathway in SAMP6 mice. Oncotarget. 2016;7(44):71072-71086. [31] KLENTROU P, ANGRISH K, AWADIA N, et al. Wnt signalingrelated osteokines at rest and following plyometric exercise in prepubertal and early pubertal boys and girls. Pediatr Exerc Sci. 2018;30(4):457-465. [32] CHENG L, KHALAF A T, LIN T, et al.Exercise promotes the osteoinduction of HA/β-TCP biomaterials via the Wnt signaling pathway. Metabolites. 2020;10(3):E90. [33] Bullock WA, Pavalko FM, Robling AG. Osteocytes and mechanical loading:The Wnt connection. Orthod Craniofac Res. 2019;22(1):175-179. [34] ZHANG J, VALVERDE P, ZHU X, et al. Exercise-induced irisin in bone and systemic irisin administration reveal new regulatory mechanisms of bone metabolism. Bone Res. 2017;5:16056. [35] 李广周, 吴伟. 运动对MSCs向成骨细胞分化相关信号通路的影响[J]. 中国细胞生物学学报,2016,38(8):1031-1035. [36] KANAZAWA I, NOTSU M, MIYAKE H, et al. Assessment using serum insulin-like growth factor-I and bone mineral density is useful for detecting prevalent vertebral fractures in patients with type 2 diabetes mellitus. Osteoporos Int. 2018;29(11):2527-2535. [37] 方幸. 运动介导肌肉因子IGF-1、FGF-2对小鼠骨的影响[D].上海:华东师范大学,2018. [38] MARAHLEH A, KITAURA H, OHORI F, et al. TNF-α Directly Enhances Osteocyte RANKL Expression and Promotes Osteoclast Formation. Front Immunol. 2019;10:2925. [39] 陈祥和, 李世昌, 孙朋, 等. 游泳和下坡跑通过CN/NFAT信号途径对2型糖尿病小鼠吸收代谢的影响[J]. 中国体育科技,2018,54(4):113-119+145. [40] TOBEIHA M, MOGHADASIAN MH, AMIN N, et al. RANKL/RANK/OPG Pathway: A Mechanism Involved in Exercise-Induced Bone Remodeling. Biomed Res Int. 2020:6910312. [41] MESINOVIC J, ZENGIN A, DE CB, et al. Sarcopenia and type 2 diabetes mellitus: a bidirectional relationship. Diabetes Metab Syndr Obes. 2019;12: 1057-1072. [42] KABAK B, BELVIRANLI M, OKUDAN N. Irisin and myostatin responses to acute high-intensity interval exercise in humans. Horm Mol Biol Clin Investig. 2018;35(3):/j/hmbci. [43] KONOPKA AR, WOLFF CA, SUER MK, et al. Relationship between intermuscular adipose tissue infiltration and myostatin before and after aerobic exercise training. Am J Physiol Regul Integr Comp Physiol. 2018; 315(3):R461-R468. [44] MOTAHARI RAD M, BIJEH N, ATTARZADEH HOSSEINI SR, et al. The effect of two concurrent exercise modalities on serum concentrations of FGF21, irisin, follistatin, and myostatin in men with type 2 diabetes mellitus. Arch Physiol Biochem. 2020;1-10. [45] CHEN X, SUN X, WANG C, et al. Effects of Exercise on Inflammatory Cytokines in Patients with Type 2 Diabetes: A Meta-analysis of Randomized Controlled Trials. Oxid Med Cell Longev. 2020;2020:6660557. [46] KWON JH, MOON KM, MIN KW. Exercise-Induced Myokines can Explain the Importance of Physical Activity in the Elderly: An Overview. Healthcare (Basel). 2020;8(4):378. [47] BULLOCK WA, PAVALKO FM, ROBLING AG. Osteocytes and mechanical loading:The Wnt connection. Orthod Craniofac Res. 2019;22(Suppl 1):175-179. [48] LE H, XU W, ZHUANG X, et al. Mesenchymal stem cells for cartilage regeneration. J Tissue Eng. 2020;11:2041731420943839. [49] SUN K, LUO J, GUO J, et al. The PI3K/AKT/mTOR signaling pathway in osteoarthritis: a narrative review. Osteoarthritis Cartilage. 2020;28(4):400-409. [50] ZAMFIROV K, PHILIPPE J. Manifestations musculosquelettiques du diabète sucré : une complication fréquente Musculoskeletal complications in diabetes mellitus. Rev Med Suisse. 2017;13(560):917-921. |
| [1] | Tan Xinfang, Guo Yanxing, Qin Xiaofei, Zhang Binqing, Zhao Dongliang, Pan Kunkun, Li Yuzhuo, Chen Haoyu. Effect of uniaxial fatigue exercise on patellofemoral cartilage injury in a rabbit [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-6. |
| [2] | Wu Min, Zhang Yeting, Wang Lu, Wang Junwei, Jin Yu, Shan Jixin, Bai Bingyi, Yuan Qiongjia. Effect of concurrent training sequences on body composition and hormone response: a Meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1305-1312. |
| [3] | Gu Zhengqiu, Xu Fei, Wei Jia, Zou Yongdi, Wang Xiaolu, Li Yongming. Exploratory study on talk test as a measure of intensity in blood flow restriction training [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1154-1159. |
| [4] | Chen Xianghe, Liu Bo, Yang Kang, Lu Pengcheng, Yu Huilin. Treadmill exercise improves the myocardial fibrosis of spontaneous type 2 diabetic mice: an exploration on the functional pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1210-1215. |
| [5] | Shui Xiaoping, Li Chunying, Li Shunchang, Sun Junzhi, Su Quansheng . Effects of aerobic and resistance exercises on brain-derived neurotrophic factor, nuclear factor-kappa B and inflammatory cytokines in skeletal muscle of type II diabetic rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 669-675. |
| [6] | Deng Shuang, Pu Rui, Chen Ziyang, Zhang Jianchao, Yuan Lingyan . Effects of exercise preconditioning on myocardial protection and apoptosis in a mouse model of myocardial remodeling due to early stress overload [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 717-723. |
| [7] | Mo Weibin, Huang Tianchang, Zeng Zhiwei, Yan Linbo. Effects of Pueraria lobata flavonoids on expressions of beta-catenin and glycogen synthase kinase 3beta in the brain of rats undergoing exhaustive exercise after long endurance exercise [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 736-741. |
| [8] | Wei Xing, Liu Shufang, Mao Ning. Roles and values of blood flow restriction training in the rehabilitation of knee joint diseases [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 774-779. |
| [9] | Tang Jiping, Zhang Yeting. Exercise regulates adult hippocampal neurogenesis in Alzheimer’s disease: mechanism and role [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 798-803. |
| [10] | Liu Yiyi, Qiu Junqiang, Yi Longyan, Zhou Cailiang. Effect of resistance training on interleukin-6 and C-reactive protein in middle-age and elderly people: a Meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 804-812. |
| [11] | Geng Yuanwen, Lin Qinqin, Li Ruoming, Tang Shaokai, Wang Baihui, Tian Zhenjun. A single bout of exhaustive exercise induces renal NOD-like receptor protein 3 inflammasome expression in rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 190-196. |
| [12] | Jia Ruizhen, Jiang Chao, Jin Qiguan, Lou Xujia, Hu Yulong. Effects and mechanism of the combined use of L-carnitine, pantothenic acid and coenzyme Q10 on aerobic exercise-induced fatigue in mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 165-170. |
| [13] | Kan Jie. Guidelines for exercise during pregnancy in developed countries and revelation for the Healthy China Action [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 308-314. |
| [14] | Sun Xinzheng, Chen Xiaoke, Wang Chenghao, He Hui. Exercise improves pain induced by sciatic nerve injury in animal models: a Meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 321-328. |
| [15] | Shen Jinbo, Zhang Lin. Micro-injury of the Achilles tendon caused by acute exhaustive exercise in rats: ultrastructural changes and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1190-1195. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||