Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (21): 3438-3444.doi: 10.12307/2023.510
Application of Chinese medicines of tonifying kidney and strengthening bones in the repair of segmental bone defects using bone tissue engineering scaffolds
Xiong Wei1, Yuan Lingmei2, Qian Guowen3, Huang Jinyang1, Pan Bin1, Guo Ling1, Zeng Zhikui1, 2
- 1Jiangxi University of Chinese Medicine, Nanchang 330004, Jiangxi Province, China; 2Affiliated Hospital of Jiangxi University of Chinese Medicine, Nanchang 330006, Jiangxi Province, China; 3Jiangxi University of Science and Technology, Nanchang 330013, Jiangxi Province, China
-
Received:2022-08-12Accepted:2022-09-21Online:2023-07-28Published:2022-11-26 -
Contact:Zeng Zhikui, MD, Doctoral supervisor, Jiangxi University of Chinese Medicine, Nanchang 330004, Jiangxi Province, China; Affiliated Hospital of Jiangxi University of Chinese Medicine, Nanchang 330006, Jiangxi Province, China -
About author:Xiong Wei, Master candidate, Jiangxi University of Chinese Medicine, Nanchang 330004, Jiangxi Province, China -
Supported by:the National Natural Science Foundation of China, No. 81960880 (to ZZK)
CLC Number:
Cite this article
Xiong Wei, Yuan Lingmei, Qian Guowen, Huang Jinyang, Pan Bin, Guo Ling, Zeng Zhikui. Application of Chinese medicines of tonifying kidney and strengthening bones in the repair of segmental bone defects using bone tissue engineering scaffolds[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(21): 3438-3444.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
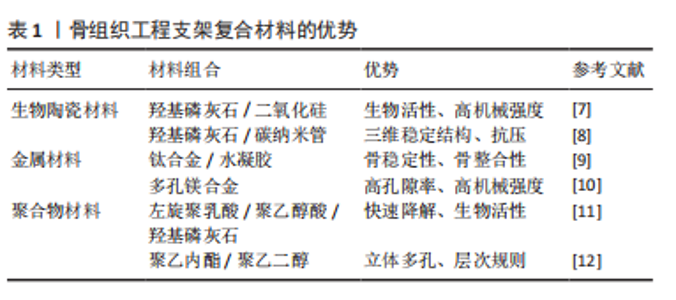
2.1 骨组织工程支架材料 20世纪80年代建立的组织工程学是将细胞生物学、工程学和生物材料学融合的新兴交叉学科,作为一个独立的研究领域,旨在开发人体组织、器官的替代物,用以修复和改善病损的人体组织,或通过外科移植取代功能衰竭的器官。骨组织工程学作为组织工程学的重要分支,致力于设计出与人体骨组织成分类似、结构相像、生物功能相同的人工材料。近年来,由各种生物材料制成的支架作为骨组织再生的框架已备受关注,试图实现体内不同骨缺损及软骨组织损伤的修复与再生。现阶段骨组织工程中单一支架材料性能往往存在不足,包括生物陶瓷、医用金属、聚合物(天然高分子/合成高分子)等在内的众多单一材料均无法满足临床需求。综合各材料的物理、化学及生物性能优点,将多种材料与生长因子或药物联合使用,制备性能优异的复合人工支架被视为骨组织工程材料学的重要发展方向之一,见表1。"
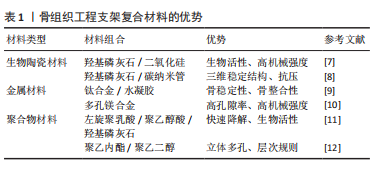
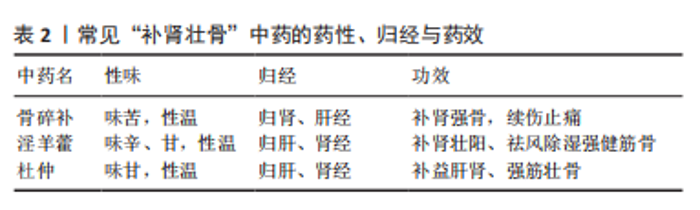
2.1.1 生物陶瓷材料 生物陶瓷是骨组织工程中的一类重要无机生物材料,以良好的生物相容性、生物可降解性、多孔孔隙结构及易加工等优点被认为是最理想的骨替代材料之一。现越来越多的学者聚焦于生物陶瓷与宿主系统之间的信号分子互通和其在体内释放的活性离子与细胞外基质的相关作用[13]。羟基磷灰石(hydroxyapatite,Hap)与磷酸钙(CaP)材料作为最常见的生物陶瓷,因其化学性质与天然骨组织细胞外基质相似而被广泛应用于骨缺损的修复[14]。β-磷酸三钙作为应用最广泛的磷酸钙陶瓷,其最大优势是极好的生物相容性,植入后与天然骨可直接融合,对人体无免疫排斥反应、炎症反应及全身毒副作用[15-16]。 为弥补生物陶瓷材料性能单一的缺点,将其与特性互补的材料相结合,通过二者的协同效应可制备出性能优异的复合材料。ZHANG等[7]将二氧化硅掺杂在羟基磷灰石中,采用3D打印技术制备了具有模拟骨小梁结构的支架,在保留了羟基磷灰石体外生物活性的同时赋予了高强度优势。RAVOOR等[8]以羧甲基纤维素(CMC)为黏合剂,将羟基磷灰石与碳纳米管混合,采用机械铸造技术研制出三维结构陶瓷支架,再通过真空烧结处理使支架获得致密稳定的结构,提高支架抗压强度同时保留了羟基磷灰石的生物活性。 2.1.2 医用金属材料 医用金属材料是人类开发最早、骨科临床应用最多的生物材料之一,金属材料因机械性能优异、抗疲劳和易加工等特点,在骨、牙齿的修复再生等领域中拥有得天独厚的优势。钛、镁及其合金是骨组织工程中最常用的金属,被广泛应用于人工关节、人工假肢、医疗器械和骨缺损修复等领域[17]。金属支架材料展示出优异的骨传导性及机械特性,可以替代自体骨承受压力,预防新生骨的崩解,但其机械特性往往不能与天然骨相匹配,因大部分载荷由金属承受,容易产生应力屏蔽,骨截面的骨细胞受到的机械刺激降低,从而导致新生骨量减少、骨密度下降、减弱了成骨效能[18]。 金属钛性能优异已经在临床广泛应用,极佳的稳定性也导致其缺乏生物活性,通过化学修饰后,可赋予其生物活性[19]。相比传统植入材料有不同程度的物理、化学性能缺陷,金属材料具有较好的弹性模量、较高的摩擦系数以及优良的生物相容性、骨再生能力。钛及钛合金植入物作为骨科植入材料之一,不仅可为BMSCs提供稳定的成骨微环境,还可增加周围骨组织的骨整合性,起到促进骨整合的效果[9]。然而,由于钛本身不能被降解,纯钛材料通常需要在达到骨整合目的后二次手术去除,因此它并非骨组织工程的最理想生物材料。 镁作为构成人体的元素之一,植入体内可通过腐蚀降解为镁离子,除了部分被周围机体组织吸收的镁离子外,剩余的可经过体液循环排出体外。由于镁的密度接近于人体骨组织,且弹性模量亦与人骨相近,减少了应力遮挡发生率,因此较金属钛更适合应用于骨组织工程。JIA等[10]发现镁支架的孔径对BMSCs的细胞迁移意义重大,同时阐述了孔径分布对镁支架机械强度、降解行为和细胞迁移能力的影响,提出了一种可量化的方法来评价不同孔径分布的可降解镁支架的细胞迁移潜力。 2.1.3 聚合物材料 目前,聚合物材料分为天然高分子材料和人工合成高分子聚合物材料。备受学者青睐的天然高分子聚合物材料有胶原、明胶、丝素蛋白和海藻酸盐等。由于天然生物材料结构类似于细胞质基质,有利于骨组织的修复与重建。此类材料通常具有良好的亲水性,能形成高含水量的水凝胶,有利于提高组织自愈能力。且天然高分子聚合物植入后连续矿化,随着矿化循环次数的增加,可使支架具有骨诱导和骨传导双重作用[20]。 在骨组织工程中以左旋聚乳酸(poly-L-lactic acid,PLLA)、聚己内酯(polycaprolactone,PCL)等可降解合成聚合物材料为关注热点[21]。左旋聚乳酸因具有良好的生物相容性和骨传导性[22-23],已被广泛应用于骨组织工程支架的研发中。SHUAI等[11]利用聚乙醇酸(polyglutamic acid,PGA)的快速降解特性,通过与左旋聚乳酸、羟基磷灰石粉末等比混合,利用激光3D打印技术制备高孔隙率的左旋聚乳酸/聚乙醇酸/羟基磷灰石复合支架,不仅可提高成骨细胞碱性磷酸酶(ALP)活性和促BMSCs成骨分化,还可加快支架降解速度。 聚己内酯是一种可降解聚合物材料,经美国食品和药物管理局(FDA)批准,已经作为手术缝线和伤口敷料应用于临床,因其优异的加工性能在骨组织工程领域受到广泛关注。然而,聚己内酯材料缺乏细胞黏附性,且体内降解速率缓慢[24]。需对聚己内酯材料表面进行涂层处理以改变其疏水性和表面性质,从而提高细胞的黏附性[25]。GUASTAFERRO等[12]利用聚乙二醇(PEG)的发泡功能作为增塑剂与聚己内酯混合,采用超临界CO2干燥法制备了具有层次化、规则多孔的聚己内酯/聚乙二醇支架,其相比其他常规方式制备的立体多孔结构支架更适合用作再生医学材料。 2.2 “补肾壮骨”中药 《素问?痿论篇》曰:“肾主身之骨髓。” “《素问?五藏生成篇》曰:“肾之合骨也。”《素问?逆调论篇》曰:“肾不生,则髓不能满。”中医经典理论指出骨的作用,不但为立身之主干,还内藏精髓,与肾气有密切关系,肾藏精,精生髓,髓养骨,合骨者肾也,故骨的成长、壮健和再生与肾气的充盈有紧密联系,肾气充盈,则充骨生髓,筋骨强劲有力,肾衰则骨失所养,骨疏不健,易导致不荣而痛、腰膝酸软,肢体乏力,甚至发生脆性骨折。调控肾气的盛衰可以调节患者机体的免疫功能和体质,进而作用于骨折局部的代谢。中医骨伤科学从“肾主骨”的指导思想出发,将补肾法融入中医骨伤三期辨证的骨折后期治疗中,发现其促进骨形成与骨修复疗效确切。常见的“补肾壮骨”中药见表2。"
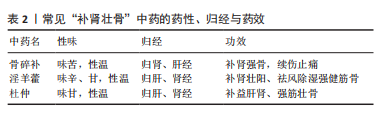
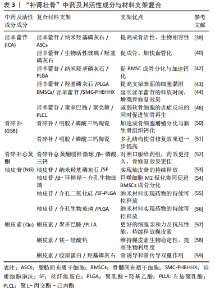
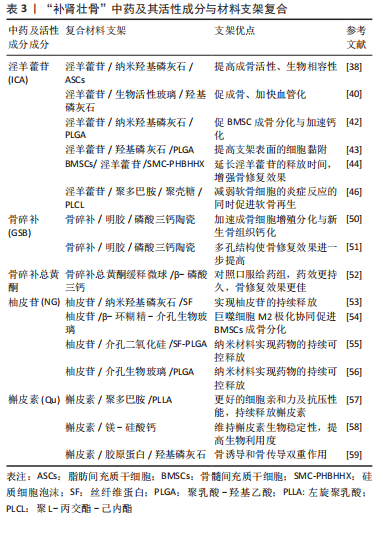
“补肾壮骨”代表中药(如淫羊藿、骨碎补、杜仲等)均能对BMSCs的成骨分化发挥积极作用[26],它们往往可促进成骨细胞增殖、抑制破骨细胞活性,或具有双向调节的作用。骨碎补具有活血续筋、补肾强骨功效,是“补肾壮骨”的代表性药物。既往研究发现其有效成分骨碎补总黄酮对骨形成及修复具有显著促进作用[6]。招文华等[27]研究表明骨碎补能显著促进BMSCs增殖和成骨分化,在成骨分化过程中上调了转化生长因子β1(TGF-β1)、骨形态发生蛋白2的表达,这可能是骨碎补参与诱导BMSCs向成骨分化的分子机制之一。最新研究发现骨碎补的活性单体柚皮苷不仅可促进BMSCs成骨分化,还具有调控巨噬细胞的抗炎作用,可通过上调巨噬细胞M2向极化,抑制M1向极化,从而进一步对骨髓间充质干细胞的成骨分化产生协同作用[53]。 淫羊藿亦是“补肾壮骨”常用中药。李智奎等[28]采用不同剂量的淫羊藿苷对大鼠BMSCs进行干预,发现其可激活Wnt/β-catenin信号通路,上调β-连环蛋白(β-catenin)和Wnt7蛋白的表达,以10 ng/mL的淫羊藿苷效果最明显。陈花英等[29]在高糖环境下评估淫羊藿甘对BMSCs的促成骨分化性能,发现淫羊藿苷可上调骨钙素、骨桥蛋白和Ⅰ型胶原等成骨分化相关基因表达,提示在糖尿病患者的骨重建中,淫羊藿可作为治疗用药。 杜仲以补肝肾、强筋骨、安胎见长,其有效成分包括黄酮类(槲皮素、紫云英苷、陆地锦苷等)与环烯醚萜类成分(杜仲醇、杜仲醇苷、筋骨草苷等)。杜仲水提取物可通过促进小鼠肠道乳酸菌生长,增加短链脂肪酸的产生,从而抑制破骨细胞生成[30]。针对RAW264.7巨噬细胞分化研究发现,杜仲可下调TRAP、组织蛋白酶K、H+atp酶、基质金属蛋白酶9 (MMP-9)和多通道跨膜蛋白(DC-STAMP)的表达,抑制核因子κB受体活化因子配体(RANKL)诱导的破骨细胞生成,减少骨吸收[31]。汤军[32]研究表明,使用杜仲乙醇提取物诱导BMSCs,能激活Wnt/β-catenin信号通路,显著提高β-catenin表达,促进骨髓间充质干细胞向成骨分化。段雨劼等[33]将葛根、杜仲和淫羊藿配伍使用,观察其对去势SD大鼠骨密度影响,研究表明杜仲显著提高了大鼠骨形态发生蛋白2表达水平,改善了新生骨组织的骨小梁微结构。 2.3 “补肾壮骨”中药复合支架 随着国内外学者对支架功能多样性的研究深入,发现将活性因子与人工支架材料结合,用以修复节段性骨缺损可获得良好效果[34]。然而,外源性生长因子存在单价昂贵、体内半衰期短、复杂的加载及消毒过程易致生长因子降解和失活等问题,为了保证性能往往需要超生理剂量使用,既增加了成本,亦带来了风险(如肿瘤等病理改变)[35]。近些年大量研究表明在治疗慢性骨科疾病和创伤后骨缺损的修复重建过程中BMSCs发挥着不可替代重要的作用。采用“补肾壮骨”中药及其有效成分作为BMSCs的诱导剂,较以往使用化学物质和生长因子干预,具有多靶点作用和经济实用等优点。故将“补肾壮骨”中药有效成分作为生长因子替代品负载于生物支架上,是修复骨缺损的有效方法,临床应用前景广阔。 2.3.1 淫羊藿复合支架 淫羊藿具有补肾阳、强筋骨的功效,其有效成分淫羊藿苷(Icariin,ICA)对BMSCs的成骨分化有着积极作用。研究表明淫羊藿苷可显著提高碱性磷酸酶、骨钙素、骨桥蛋白和骨形态发生蛋白等成骨相关蛋白的表达,同时降低破骨细胞活性与抑制骨吸收[36-37]。纳米羟基磷灰石与人体骨组织的无机物构成相仿,作为骨修复材料已在临床应用多年,表现出良好的生物活性与生物相容性。研究发现将淫羊藿苷负载于纳米羟基磷灰石上较单纯使用纳米羟基磷灰石可以获得更好的骨修复效果,而将脂肪间充质干细胞与淫羊藿苷一同负载于纳米羟基磷灰石的孔隙上,骨修复效果又进一步提高[38]。 生物活性玻璃作为另一种生物陶瓷材料,将其加入传统陶瓷材料中可提高其降解性能[39]。JING等[40]将淫羊藿苷和脂肪间充质干细胞加载于生物活性玻璃植入大鼠颅骨缺损模型后,发现可显著增强成骨和成血管作用。王德欣等[41]观察不同浓度淫羊藿苷对BMSCs的成骨分化影响,发现BMSCs的成骨活性与淫羊藿苷的浓度存在正相关联系。另有学者研究表明淫羊藿苷/纳米羟基磷灰石/聚乳酸-羟基乙酸复合支架对成骨细胞的增殖无明显促进作用,其主要是通过诱导BMSCs的成骨分化及矿化而表现出促成骨作用[42]。亦有研究报道淫羊藿苷/羟基磷灰石/聚乳酸-羟基乙酸支架表面亲水性差,但是其表面的纳米结构可为BMSCs的黏附提供一定支持[43]。 LIU等[44]利用硅质细胞泡沫的三维结构结合淫羊藿苷与BMSCs制备复合支架修复大鼠节段性骨缺损,发现复合支架可延长淫羊藿苷的释放,相比未加载药物的对照组,骨修复的效果更加显著。XIE等[45]观察到负载淫羊藿苷的多孔支架,其宏观/微观结构以及力学性能均未发生改变,可应用于非承载区骨缺损的治疗,缘于其可诱导成骨、抑制破骨细胞活性及激活成骨分化基因进行耦合成骨。李慧娟等[46]使用壳聚糖(chitosan,CC)、聚多巴胺 (polydopamine,PDA)和聚L-丙交酯-己内酯(PLCL)混合制备壳聚糖基支架(PDA/PLCL/CC),采用物理吸附的方式对支架加载淫羊藿苷,制成ICA/PDA/PLCL/CC支架,该研究证实淫羊藿苷复合支架可在减弱软骨细胞的炎症反应的同时促进软骨再生。 2.3.2 骨碎补复合支架 骨碎补作为“补肾壮骨”类中药的代表药物,具有活血续筋、补肾强骨的功效,其活性成分黄酮类物质(包括骨碎补总黄酮等)及单体(如柚皮苷等)均具有一定的成骨活性。大量基础研究已证实,骨碎补总黄酮在动物骨缺损、骨质疏松等模型中,表现出加快血管再生、促进成骨细胞增殖、抑制破骨细胞活性及改善成骨质量等作用[47-49]。 DONG等[50]通过将天然交联剂吉尼平/交联明胶/磷酸三钙混合物与骨碎补共同制备复合支架应用于兔颅骨骨缺损模型,研究表明骨碎补在显著加快成骨细胞增殖分化的同时,还可促进钙、磷酸盐沉积,加速新生骨组织钙化。同时发现100 μg/mL的骨碎补能显著促进成骨细胞线粒体和碱性磷酸酶活性,加速其增殖。CHEN等[51]采用浸盐法成功制备了孔径为280-430 μm的明胶/β-磷酸三钙/骨碎补多孔可降解生物支架,将BMSCs接种在多孔支架应用于兔颅骨临界骨缺损模型,发现中药复合支架具有良好的骨修复潜力。因此,将骨碎补和BMSCs复合到多孔人工支架中,是骨缺损修复的理想选择。 申震等[52]通过对比负载骨碎补总黄酮骨缓释微球材料支架与传统药物灌胃联合骨材料支架在大鼠胫骨节段性骨缺损的修复效果发现,材料支架的缓释微球局部给药可以保障药物随时间缓慢释放,同时药物可直接作用于骨缺损区域,骨修复效果更佳。YU等[53]在大鼠椎体骨缺损模型中采用明胶微球包裹柚皮苷加载于纳米羟基磷灰石/丝素蛋白复合支架进行修复效果评估,发现借助明胶微球和丝素蛋白组成的药物传递系统可实现柚皮苷的持续缓释有效促进椎体骨缺损修复。 MO等[54]采用β-环糊精修饰后的生物活性玻璃装载柚皮苷,发现载药的生物活性玻璃具有免疫调节功能与抑制巨噬细胞炎症反应作用,其可促进巨噬细胞向M2极化和诱导BMSCs成骨分化。现越来越多的学者在对复合支架进行药物装载时选用纳米微球作为载体,不仅克服了传统口服给药方式的首过效应,提高了药物生物利用度,实现了对缺损部位的可控缓释靶向给药,还能减少药物对胃肠道等组织伤害,降低毒副作用[55-56]。 2.3.3 杜仲复合支架 杜仲功效为补肝肾、强筋骨、安胎。《神农本草经》记载其可治疗腰脊痛,善补中益精气,强健筋骨。杜仲树的皮与花均可入药,树皮作为常用药用部位。现代药理学常将其有效成分包括黄酮类(槲皮素、山奈酚等))与环烯醚萜类成分(杜仲醇、杜仲醇苷、筋骨草苷等)及醇提取物用于对骨代谢的作用机制研究。 槲皮素作为杜仲活性成分中的热门角色倍受关注,CHEN等[57]利用3D打印制备PLLA支架,使用聚多巴胺(PDA)与槲皮素(Qu)对支架进行表面修饰,发现修饰后的PLLA支架具有更粗糙的表面、更佳的细胞亲和力及抗压性能;通过聚多巴胺涂层可实现持续释放槲皮素,利于小鼠胚胎成骨细胞的增殖和附着,增加碱性磷酸酶活性和钙结节数,上调相关成骨基因和蛋白的表达。 PREETHI等[58]通过共沉淀技术将槲皮素加载到掺镁的硅酸钙(CMS)陶瓷,并利用静电纺丝合成纳米纤维支架,在不影响槲皮素生物稳定性的同时,提高其生物利用度,在硅酸盐产生抗菌和促成骨作用基础上发挥了槲皮素的协同抗菌活性。SONG等[59]利用冻干处理的胶原蛋白3D孔隙结构吸附槲皮素,表面再涂覆一层羟基磷灰石材料,获得多孔槲皮素/胶原蛋白/羟基磷灰石(Qu/DC/Hap)海绵,证实其可有效诱导BMSCs成骨分化,并具有骨传导的特征。 “补肾壮骨”中药及其活性成分与材料支架复合资料汇总,见表3。"
| [1] 买吾拉尼江·加马力,艾合买提江·玉素甫. Masquelet技术治疗大段骨缺损的最新进展[J].实用骨科杂志,2020,26(2):136-139. [2] MAUFFREY C, BARLOW BT, SMITH W. Management of segmental bone defects. J Am Acad Orthop Surg. 2015;23(3):143-153. [3] TAYTON E, PURCELL M, SMITH J O, et al. The scale-up of a tissue engineered porous hydroxyapatite polymer composite scaffold for use in bone repair: an ovine femoral condyle defect study. J Biomed Mater Res A. 2015;103(4):1346-1356. [4] ALMUBARAK S, NETHERCOTT H, FREEBERG M, et al. Tissue engineering strategies for promoting vascularized bone regeneration. Bone. 2016; 83:197-209. [5] 孙丙银.骨碎补总黄酮促进股骨缺损牵张成骨新骨形成的实验研究[D].广州:广州中医药大学,2013. [6] PANG WY, WANG XL, MOK SK, et al.Naringin improves bone properties in ovariectomized mice and exerts oestrogen-like activities in rat osteoblast-like (UMR-106) cells. Br J Pharmacol. 2010;159(8): 1693-1703. [7] ZHANG C, YUAN Y, ZENG Y, et al. DLP 3D printed silica-doped HAp ceramic scaffolds inspired by the trabecular bone structure. Ceramics International. 2022;48(19):27765-27773. [8] RAVOOR J, RENOLD ES. A study on retention of MWCNT in robocasted MWCNT-HAP scaffold structures using vacuum sintering technique and their characteristics. Ceramics International. 2022;48(21): 31289-31298. [9] YIN C, ZHANG T, WEI Q, et al. Surface treatment of 3D printed porous Ti6Al4V implants by ultraviolet photofunctionalization for improved osseointegration. Bioactive Materials. 2022;7:26-38. [10] JIA G, HUANG H, NIU J, et al. Exploring the interconnectivity of biomimetic hierarchical porous Mg scaffolds for bone tissue engineering: Effects of pore size distribution on mechanical properties, degradation behavior and cell migration ability. J Magnesium Alloys. 2021;9(6):1954-1966. [11] SHUAI C, YANG W, FENG P, et al. Accelerated degradation of HAP/PLLA bone scaffold by PGA blending facilitates bioactivity and osteoconductivity. Bioactive Materials. 2021;6(2):490-502. [12] GUASTAFERRO M, BALDINO L, CARDEA S, et al. Supercritical processing of PCL and PCL-PEG blends to produce improved PCL-based porous scaffolds. J Supercritical Fluids. 2022;186:105611. [13] ZHOU Y, WU C, CHANG J. Bioceramics to regulate stem cells and their microenvironment for tissue regeneration. Materials Today. 2019;24:41-56. [14] FÉLIX LANAO R P, LEEUWENBURGH S C G, WOLKE J G C, et al. Bone response to fast-degrading, injectable calcium phosphate cements containing PLGA microparticles. Biomaterials. 2011;32(34):8839-8847. [15] 刘锌,杜斌,孙光权,等.多孔β磷酸三钙-聚吡咯-生物素-淫羊藿素微球复合支架促进骨髓间充质干细胞的募集[J].中国组织工程研究,2020,24(34):5532-5537. [16] 乔永杰,张吕丹,李旭升,等.β-磷酸三钙填充载药微球治疗兔感染性骨缺损[J].中国矫形外科杂志,2021,29(11):1013-1018. [17] YU M, YOU D, ZHUANG J, et al. Controlled Release of Naringin in Metal-Organic Framework-Loaded Mineralized Collagen Coating to Simultaneously Enhance Osseointegration and Antibacterial Activity. ACS Appl Mater Interfaces. 2017;9(23):19698-19705. [18] KOONS GL, DIBA M, MIKOS AG. Materials design for bone-tissue engineering. Nature reviews. Materials. 2020;5(8):584-603. [19] MA L, WANG X, ZHOU Y, et al. Biomimetic Ti–6Al–4V alloy/gelatin methacrylate hybrid scaffold with enhanced osteogenic and angiogenic capabilities for large bone defect restoration. Bioact Mate. 2021;6(10):3437-3448. [20] REN X, ZHOU Q, FOULAD D, et al. Osteoprotegerin reduces osteoclast resorption activity without affecting osteogenesis on nanoparticulate mineralized collagen scaffolds. Sci Adv. 2019;5(6):w4991. [21] YEDEKÇI B, TEZCANER A, YıLMAZ B, et al. 3D porous PCL-PEG-PCL / strontium, magnesium and boron multi-doped hydroxyapatite composite scaffolds for bone tissue engineering. J Mech Behav Biomed Mater. 2022;125:104941. [22] BERTOLDI C, ZAFFE D, CONSOLO U. Polylactide/polyglycolide copolymer in bone defect healing in humans. Biomaterials. 2008; 29(12):1817-1823. [23] 吴东进,郝爱华,张程,等.内皮祖细胞与纳米羟基磷灰石/胶原/聚乳酸复合物在修复兔骨缺损中的作用[J].中华医学杂志,2012, 92(23):1630-1634. [24] LI L, LI J, GUO J, et al. 3D Molecularly Functionalized Cell‐Free Biomimetic Scaffolds for Osteochondral Regeneration. Adv Funct Mater. 2019;29(6):1807356. [25] HASANI-SADRABADI MM, SARRION P, NAKATSUKA N, et al. Hierarchically Patterned Polydopamine-Containing Membranes for Periodontal Tissue Engineering. ACS Nano. 2019;13(4):3830-3838. [26] 李姣,黄委委,陶林,等.中药促骨髓间充质干细胞成骨分化的研究进展[J].吉林中医药,2021,41(4):544-548. [27] 招文华,沈耿杨,任辉,等.骨碎补活性单体成分调控骨质疏松症相关信号通路的研究进展[J].中国骨质疏松杂志,2017,23(1): 122-129. [28] 李智奎,孔俊博,赵王林.淫羊藿苷调控Wnt/β-catenin信号通路干预大鼠MSCs成脂成骨双向分化实验研究[J].中国免疫学杂志, 2019,35(24):2985-2990. [29] 陈花英,周娟,吴焕成,等.淫羊藿苷对高糖环境下骨髓间充质干细胞凋亡及成骨分化的影响[J].兰州大学学报(医学版),2019, 45(4):37-42. [30] ZHAO X, WANG Y, NIE Z, et al. Eucommia ulmoides leaf extract alters gut microbiota composition, enhances short‐chain fatty acids production, and ameliorates osteoporosis in the senescence‐accelerated mouse P6 (SAMP6) model. Food Sci Nutr. 2020;8(9):4897-4906. [31] CHENG C, CHIEN-FU LIN J, TSAI F, et al. Protective effects and network analysis of natural compounds obtained from Radix dipsaci, Eucommiae cortex, and Rhizoma drynariae against RANKL-induced osteoclastogenesis in vitro. J Ethnopharmacol. 2019;244:112074. [32] 汤军.杜仲醇提取物诱导大鼠骨髓间充质干细胞成骨分化中Wnt信号通路研究[D].南京:南京中医药大学,2013. [33] 段雨劼,聂焱,吴媛妮,等.葛根、杜仲和淫羊藿对去势大鼠增加骨密度实验研究[J].预防医学情报杂志,2019,35(9):1068-1071. [34] SENATOV F, ZIMINA A, CHUBRIK A, et al. Effect of recombinant BMP-2 and erythropoietin on osteogenic properties of biomimetic PLA/PCL/HA and PHB/HA scaffolds in critical-size cranial defects model. Mater Sci Eng C Mater Biol Appl. 2022;135:112680. [35] CUI J, YU X, YU B, et al. Coaxially Fabricated Dual‐Drug Loading Electrospinning Fibrous Mat with Programmed Releasing Behavior to Boost Vascularized Bone Regeneration. Adv Healthc Mater. 2022; 11(16):e2200571. [36] 周先进,张延芳.淫羊藿苷对成骨细胞中β-catenin、ALP和RUNX2表达的影响[J].中国医药导报,2017,14(36):57-59. [37] QIAN W, LINGYAN C, YANG L, et al.Evaluation of synergistic osteogenesis between icariin and BMP2 through a micro /meso hierarchical porous delivery system. Int J Nanomedicine. 2017;12: 7721-7735. [38] 宁兆荣,郭延伟,李松,等.脂肪干细胞复合载淫羊藿苷支架材料对兔下颌骨缺损的修复[J].实用口腔医学杂志,2013,29(5):611-615. [39] QI X, PEI P, ZHU M, et al. Three dimensional printing of calcium sulfate and mesoporous bioactive glass scaffolds for improving bone regeneration in vitro and in vivo. Sci Rep. 2017;7:42556. [40] JING X, YIN W, TIAN H, et al. Icariin doped bioactive glasses seeded with rat adipose-derived stem cells to promote bone repair via enhanced osteogenic and angiogenic activities. Life Sci. 2018;202:52-60. [41] 王德欣,许战武,裴国献.不同浓度ICA-nHA/PLGA复合支架对兔骨髓间充质干细胞增殖、分化的影响[J].中国骨与关节损伤杂志, 2020,35(5):470-472. [42] 管明强,朱志霞,周观明.淫羊藿苷对聚乳酸/纳米羟基磷灰石支架上成骨细胞增殖与分化的影响[J].包头医学院学报,2018,34(1): 92-94. [43] 王德欣,许战武,裴国献.骨髓间充质干细胞在淫羊藿苷/羟基磷灰石/聚乳酸-羟基乙酸共聚物支架上的成骨[J].中国组织工程研究,2020,24(25):3974-3980. [44] LIU T, ZHANG X, LUO Y, et al. Slowly Delivered Icariin/Allogeneic Bone Marrow-Derived Mesenchymal Stem Cells to Promote the Healing of Calvarial Critical-Size Bone Defects. Stem Cells Int. 2016;2016:1416047. [45] XIE Y, SUN W, YAN F, et al. Icariin-loaded porous scaffolds for bone regeneration through the regulation of the coupling process of osteogenesis and osteoclastic activity. Int J Nanomedicine. 2019;14: 6019-6033. [46] 李慧娟,王先流,沈炎冰,等.负载淫羊藿苷的壳聚糖基仿生支架的促软骨形成和炎症缓解作用[J].生物工程学报,2022,38(6): 2308-2321. [47] 曾志奎,黄枫,李悦,等.骨碎补总黄酮对大鼠Masquelet诱导膜血管新生因子表达的影响[J].中华中医药学刊,2019,37(10): 2345-2348. [48] 蔡群斌,李定,李悦,等.骨碎补总黄酮对Masquelet技术诱导膜内血管形成的影响[J].广州中医药大学学报,2017,34(6):867-871. [49] 李定,李悦,黄枫,等.骨碎补总黄酮在诱导膜技术中对骨缺损区域血管形成和成骨质量的影响[J].中华中医药杂志,2019,34(11): 5086-5089. [50] DONG GC, CHEN HM, YAO CH. A novel bone substitute composite composed of tricalcium phosphate, gelatin and drynaria fortunei herbal extract. J Biomed Mater Res A. 2008;84(1):167-177. [51] CHEN KY, DONG GC, HSU CY, et al. Autologous bone marrow stromal cells loaded onto porous gelatin scaffolds containing Drynaria fortunei extract for bone repair. J Biomed Mater Res A. 2013;101(4):954-962. [52] 申震,郭英,姜自伟,等.基于骨组织工程技术比较骨碎补总黄酮两种给药方式修复大鼠大段骨缺损模型的效果[J].中国组织工程研究,2022,26(27):4346-4352. [53] YU X, SHEN G, SHANG Q, et al. A Naringin-loaded gelatin-microsphere/nano-hydroxyapatite/silk fibroin composite scaffold promoted healing of critical-size vertebral defects in ovariectomised rat. Int J Biol Macromol. 2021;193(Pt A):510-518. [54] MO Y, ZHAO F, LIN Z, et al. Local delivery of naringin in beta-cyclodextrin modified mesoporous bioactive glass promotes bone regeneration: from anti-inflammatory to synergistic osteogenesis and osteoclastogenesis. Biomater Sci. 2022;10(7):1697-1712. [55] ZHAO Z, MA X, MA J, et al. Sustained release of naringin from silk-fibroin-nanohydroxyapatite scaffold for the enhancement of bone regeneration. Materials Today Bio. 2022;13:100206. [56] 陈筱宇.新型介孔生物活性玻璃复合PLGA微球用于药物缓释及骨修复的研究[D].广州:华南理工大学,2021. [57] CHEN S, ZHU L, WEN W, et al. Fabrication and Evaluation of 3D Printed Poly(L-lactide) Scaffold Functionalized with Quercetin-Polydopamine for Bone Tissue Engineering. ACS Biomater Sci Eng. 2019;5(5): 2506-2518. [58] PREETHI AM, BELLARE JR. Concomitant Effect of Quercetin- and Magnesium-Doped Calcium Silicate on the Osteogenic and Antibacterial Activity of Scaffolds for Bone Regeneration. Antibiotics. 2021;10(10):1170. [59] SONG JE, TIAN J, KOOK YJ, et al. A BMSCs‐laden quercetin/duck’s feet collagen/hydroxyapatite sponge for enhanced bone regeneration. J Biomed Mater Res A. 2020;108(3):784-794. |
| [1] | Wen Xinghua, Ding Huanwen, Cheng Kai, Yan Xiaonan, Peng Yuanhao, Wang Yuning, Liu Kang, Zhang Huiwu. Three-dimensional finite element model analysis of intramedullary nailing fixation design for large femoral defects in Beagle dogs [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1371-1376. |
| [2] | Yang Yitian, Wang Lu, Yao Wei, Zhao Bin. Application of the interaction between biological scaffolds and macrophages in bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1071-1079. |
| [3] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [4] | Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109. |
| [5] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [6] | Xu Yan, Li Ping, Lai Chunhua, Zhu Peijun, Yang Shuo, Xu Shulan. Piezoelectric materials for vascularized bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1126-1132. |
| [7] | Qin Yuxing, Ren Qiangui, Li Zilong, Quan Jiaxing, Shen Peifeng, Sun Tao, Wang Haoyu. Action mechanism and prospect of bone microvascular endothelial cells for treating femoral head necrosis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 955-961. |
| [8] | Zhang Min, Zhang Xiaoming, Liu Tongbin. Application potential of naringin in bone tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 787-792. |
| [9] | Cheng Kang, Wang Bin, Tu Zhenxing, Wang Zixin, Zheng Yongxin, Tian Yuqing, Yang Xiao. Relationship of the morphology of three types of callus in the extension area after tibial bone transfer with bone healing [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(27): 4373-4378. |
| [10] | Zhou Hongxing, Zhang Baojian, Yuan Xiangsheng. Recent evaluation of individual biological acetabular cup application in hip revision [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(22): 3521-3525. |
| [11] | Qi Junqiang, Guo Chao, Niu Dongyang, Wang Haotian, Xiao Bing, Xu Guohua. Characteristics and application of bone repair materials of metal ion doped hydroxyapatite [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(21): 3415-3422. |
| [12] | Hou Jianming, Li Qi. Bioactive scaffolds in repairing osteoporotic bone defects [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(21): 3423-3429. |
| [13] | Cui Hongwang, Wang Liangsheng, Wen Peng, Meng Zhibin. Effect of osteoclast TRPV5 channel on in vitro degradation of biological coral artificial bone [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(21): 3337-3342. |
| [14] | Sun Lianlian, Liu Yongchao, Wang Zhixing. Repair effects of two kinds of bone repair materials on rabbit femoral defects compared using synchrotron-radiation-based micro-computed tomography [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(21): 3343-3348. |
| [15] | Sun Kexin, Zeng Jinshi, Li Jia, Jiang Haiyue, Liu Xia. Mechanical stimulation enhances matrix formation of three-dimensional bioprinted cartilage constructs [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(21): 3293-3299. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||