Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (6): 955-961.doi: 10.12307/2023.279
Previous Articles Next Articles
Action mechanism and prospect of bone microvascular endothelial cells for treating femoral head necrosis
Qin Yuxing1, Ren Qiangui2, Li Zilong1, Quan Jiaxing3, Shen Peifeng2, Sun Tao2, Wang Haoyu3
- 1Department of Hand and Foot Microsurgery, 2Department of Emergency, Second Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010030, Inner Mongolia Autonomous Region, China; 3Inner Mongolia Medical University, Hohhot 010110, Inner Mongolia Autonomous Region, China
-
Received:2022-02-25Accepted:2022-05-06Online:2023-02-28Published:2022-08-12 -
Contact:Ren Qiangui, Master, Chief physician, Master’s supervisor, Department of Emergency, Second Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010030, Inner Mongolia Autonomous Region, China -
About author:Qin Yuxing, Master, Physician, Department of Hand and Foot Microsurgery, Second Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010030, Inner Mongolia Autonomous Region, China
CLC Number:
Cite this article
Qin Yuxing, Ren Qiangui, Li Zilong, Quan Jiaxing, Shen Peifeng, Sun Tao, Wang Haoyu. Action mechanism and prospect of bone microvascular endothelial cells for treating femoral head necrosis[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 955-961.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
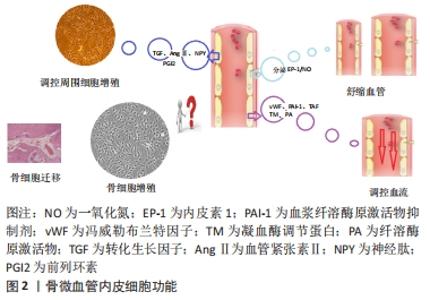
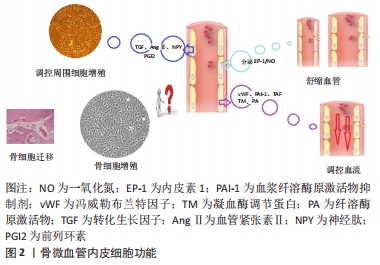
2.1 股骨头血供 想要认识骨微血管内皮细胞的重要意义,必须先熟悉股骨头的血液供应。股骨的特殊结构导致其供血相应较少,主要的供血来源是股深动脉的分支旋股内、外侧动脉[12],其中旋股内侧动脉通过股骨颈周围的滑膜在股骨颈后内侧发出下支持动脉,下支持动脉于股骨颈和关节软骨相交的部位发出下干骺动脉进入股骨头内部,供应股骨头2/3区域[13],旋股内侧动脉在股骨颈上外侧发出上支持动脉到股骨头关节囊内发出外骺动脉,供应股骨头80%区域。旋股外侧动脉的分支(横支)在股骨颈与旋股内侧动脉形成动脉环。其次是髓内的血液供应,来自于股骨干和转子向上的分支。最后是来自圆韧带的血供,但该部位血供来源较少[14]。 2.1.1 股骨头微循环 微循环是末梢循环即微动脉经毛细血管向微静脉回流形成的循环网络,其中微动脉的主要结构内皮细胞可接受血管内壁信号向上向下传递,进而调节血管平滑肌实现对微动脉血流量的调控。毛细血管是血液和组织液营养物质交换的场所,毛细血管壁虽无平滑肌,但其内皮细胞同样有着舒缩功能可以调控血流量。交换后的血液被微静脉收集[15]。通常来说,微动脉与微静脉是成对的,微动脉发出多条毛细血管束汇流成微静脉。股骨头微循环有着其独有的特点,其微动脉与微静脉沿着股骨头表面大体是平行存在的,这使得毛细血管越往头深部走,折返角度越大,且越往深部数量也越少,好在深部毛细血管管腔不规则,存在间隙且基底膜不完整,再加上内皮细胞舒张作用,才能维持股骨头深部血供[16]。 2.1.2 骨微血管内皮细胞结构 骨微血管内皮细胞是微血管壁的主要结构,是微循环物质交换的基础,在形态和功能上不同部位的微血管内皮细胞有着不同特点。微循环内皮细胞在股骨头的特异细胞是H型内皮细胞,股骨干则为L型内皮细胞[17],以高/低表达CD31和内粘蛋白(EMCN)而区别[18]。H型内皮细胞以分泌成骨细胞增殖生长的相关因子而被学者广泛研究,是成血管-成骨偶联机制的研究基础,其可将成骨相关的蛋白及早期成骨相关细胞募集至周围,这些细胞又可分泌成血管相关因子,从而促进血管生成[19]。一项研究表明,当基因修饰后的H型血管内皮细胞减少时,其周围骨组织形成同样减少,骨量降低[20]。GAO等[21]成功从股骨头坏死患者组织内提取出H型内皮细胞,体外培养证实H型血管存在于人股骨头内。 2.1.3 骨微血管内皮细胞功能 骨微血管内皮细胞不仅形成一个惰性的血液容器,还有明显的屏障和运输功能,也是一个巨大的内分泌腺,在局部微环境发生改变时,其可分泌数十种活性物质作用于周围细胞来调节微环境稳态。作为微循环网络中血管内壁的主要物理屏障,其可根据局部组织微环境变化,绕过中枢调节,直接调控局部血管来控制血流,进而调节微循环功能,其对微血管的局部调控甚至超过了自主影响[22]。功能方面多功能性和灵活性是骨微血管内皮细胞的基本特性[17]。值得注意的是,骨微血管内皮细胞在功能上是依据这些活性物质进行双向调节的,以时刻的动态平衡来维持内微环境稳态。首先是舒张与收缩血管功能,骨微血管内皮细胞可分泌内皮素1,通过抑制Rab1A和Rab1A依赖的β1表面亚基转移,迅速产生强烈的缩血管作用[23],同样是其分泌的与其作用相反的活性因子是一氧化氮(NO),通过升高细胞内环磷酸鸟苷(cGMP)水平而舒张血管[24],而内皮素1的产生可以诱导NO的分泌,但NO增加抑制内皮素1分泌,所以在生理情况下,相较于NO和内皮素1来说,舒张血管作用占主导优势。其次是促进凝血与抗凝血功能,骨微血管内皮细胞可分泌冯威勒布兰特因子(vWF)、血浆纤溶酶原激活物抑制剂(plasminogen activator inhibitor,PAI)、血小板激活因子(PAF)等促进凝血因子,凝血酶调节蛋白(TM)和纤溶酶原激活物(PA)等抗凝因子[25],生理状况下,这些抗凝与促凝因子共同维持微循环血流状态。最后就是促进细胞增殖和抑制细胞增殖的功能,其可分泌转化生长因子(TGF)、血管紧张素Ⅱ(AngⅡ)、神经肽(NPY)等促进周围细胞,主要是平滑肌细胞增殖,分泌前列环素等抑制细胞增殖[17]。见图2。"

2.2 股骨头坏死发病机制 创伤性和非创伤性股骨头坏死是股骨头坏死的两大类型,由于需要长期应用激素治疗相关疾病的患者人群增加以及未能正确合理地应用激素,使得激素性股骨头坏死在中国每年新发的15万-20万股骨头坏死患者中占30%-50%[26],且病例数量和所占比例呈逐年上升趋势,导致糖皮质激素应用所导致的股骨头坏死流行病学调查发病率居于首位[3],但具体发病机制尚未达成一致,所以在治疗方面一直止步不前。骨微血管内皮细胞分泌的活性物质时刻处于动态平衡中来保持微血管内环境的稳态。当受到外界干预刺激时,生理平衡状态被打破,则可能出现血栓形成、血管舒缩紊乱、出血倾向等问题,进而导致负责区域血供不足,无能力维持原有组织营养而坏死。一项研究通过对股骨头坏死患者血管造影及显微镜下检查发现,大部分微血管内存在血栓形成的问题[27]。基于此,作者认为股骨头缺血性坏死可能是各种原因导致骨微血管内皮细胞受损,进而微循环血栓形成,阻塞血液流动引起股骨头缺血;其次,血栓形成后血液外渗至股室内压力增高会进一步加剧股骨头坏死。 2.2.1 骨微血管内皮细胞损伤 骨与血管的关系密不可分,骨细胞不能在距离血管超过 100 mm的地方存活[6],骨微血管内皮细胞的损伤直接影响骨细胞的增殖及存活能力。YANG 等[28]在研究激素对股骨头微血管内皮细胞影响的体外实验中证实,激素组比对照组微血管内皮细胞内活性氧浓度高,差异有显著性意义,指出活性氧浓度增高是激素所致微血管内皮细胞不可逆损伤的关键因素。血液中的活性氧增加能促进炎细胞浸润,抑制微血管内皮细胞活性,且高浓度的活性氧导致的氧化应激反应也可直接造成微血管内皮细胞损伤,微血管内皮细胞损伤造成血管壁破坏、血液外渗,增加骨室内压力,导致股骨头水肿、坏死[29]。在一项股骨头骨微血管内皮细胞的体外实验中发现,激素对于骨微血管内皮细胞有着直接损伤作用,指出骨微血管内皮细胞上或许存在激素作用靶点,且在这项实验中发现激素剂量与骨微血管内皮细胞损伤呈线性关系[30]。VOGT等[31]以0.5 mg/kg地塞米松大鼠肌肉注射5 d后发现,地塞米松能以细胞核碎片和体积减少的凋亡途径使肠系膜内皮细胞长度、密度降低及死亡。基于此,作者认为,氧化应激反应造成的微血管内皮细胞损伤和可能存在激素靶点的微血管内皮细胞凋亡均参与了股骨头坏死发病过程。 2.2.2 基于微血管内皮细胞的血栓形成 在非创伤性股骨头坏死发病机制中,血栓形成倾向是被大部分学者认可的,认为激素应用会使血液处于高凝状态[32],过度饮酒会使脂肪细胞分化增多[33],镰状红细胞贫血直接引起血管闭塞等等[34],这些都会促进股骨头血栓形成倾向,但股骨头骨微血管内皮细胞可根据局部组织微环境变化,绕过中枢调节,直接调控局部血管来控制血流,进而调节微循环功能,其对微血管的局部调控甚至超过了自主影响[16]。在对血栓形成研究中,血浆组织型纤溶酶原激活物(t-PA)缺乏是血栓形成的关键[35],而骨微血管内皮细胞能够分泌PAI-1,它是组织型纤溶酶原激活物的抑制物,且激素便可促进内皮细胞PAI表达[36]。孙伟等[37]在重症急性呼吸综合征(SARS)激素治疗后股骨头坏死患者的血液学指标中发现,PAI表达量明显升高。因此,作者坚持血栓形成的关键在于微血管内皮细胞的损伤,产生功能失调,导致抗凝系统紊乱。 因为凝血系统体外的不可复制性,人们对于股骨头坏死血栓形成原因是全身因素导致还是局部特异性存在一定分歧,随着microRNAs(简称miRNA)的出现,或许能够解决此问题。miRNA是一组18-25 nt长的小型非编码RNA[38],它们通过调节转录或转录后翻译以沉默其靶基因的表达,参与大量生理和病理过程[39]。YUE等[40]通过实时定量聚合酶链反应(qPCR)和基因微阵列鉴定了4种在激素性股骨头坏死大鼠骨微血管内皮细胞中差异表达的miRNA,包括2种上调(miR-335,miR-132-3p)和2种下调(miR-466b-2-3p,let-7c-1-3p),其中miR-335表达差异变化最大。据报道,miR-335参与内皮细胞多种活性物质的调控,如超氧化物歧化酶2(SOD2)、内皮型一氧化氮合酶(eNOS)和Rasp21蛋白激活物1(RASA1)等[41],其中,内皮型一氧化氮合酶是骨微血管内皮细胞中的一种特异性蛋白酶,具有多种生理作用,如血管舒张、抗血小板聚集和促进受损骨微血管内皮细胞的功能修复[40]。超氧化物歧化酶是一种抗氧化酶,可将活性氧催化为过氧化氢和氧分子,从而抑制衰老和细胞凋亡[41]。Rasp21蛋白激活物1是RasGDP和GTP的调节剂,在血管生成、细胞增殖和凋亡等多种生理过程中发挥重要作用[41]。此外,LEI等[42]观察到股动脉闭塞后miR-132-3p表达明显上调,与野生型小鼠相比,miR-132-3p敲除小鼠缺血后后肢灌注恢复较慢。因此,miR-335和miR-132-3p可能参与调节受损骨微血管内皮细胞的功能修复和激素性股骨头坏死中的血管生成。然而,miR-466b-2-3p,let-7c-1-3p对骨微血管内皮细胞增殖和凋亡的影响尚未见报道[40]。同时,没有研究评估糖皮质激素受体(GR)对骨微血管内皮细胞在激素性股骨头坏死发病机制中的作用。最近的一项研究调查了糖皮质激素受体对小鼠内皮细胞的影响,确定了Wnt信号通路在通过糖皮质激素受体抑制血管炎症中的关键作用[43],这一结果可能会指导进一步研究糖皮质激素受体介导的骨微血管内皮细胞信号通路,这些信号通路是激素性股骨头坏死发病机制的关键因素。 2.3 成血管-成骨偶联 股骨头坏死的原因是股骨头微循环障碍所致的股骨头缺血、骨量不足而塌陷,即使组织工程植入或松质骨植入,如果未能恢复良好的血液供应,仍不能逆转坏死结局。成血管和成骨在时间和空间上是存在协同作用的,如,H型内皮细胞能够分泌维持骨细胞存活的血小板衍生生长因子(PDGF)、血小板生长因子(PGF)等活性因子;成骨细胞同样可以表达促血管内皮细胞和平滑肌增殖的Slit同源蛋白3[44]。Notch是经典的成血管通路,在一项抑制FBXW7表达激活Notch通路的研究中再一次证实,激活内皮细胞成血管的Notch通路不仅能够增加成血管相关蛋白的表达,促进新血管形成,同时对于显著缩短了骨组织形成过程[44]。 骨微血管内皮细胞偶联成血管-成骨理论:骨微血管内皮细胞作为微血管内壁的主要结构,除维持微环境的稳态,还能够通过增殖、出芽、募集成血管相关活性物质、迁移形成功能性新血管。骨微血管内皮细胞对于成骨细胞也有着重要的协同作用,主要是促进增殖与迁移,通过缺氧诱导因子1α(HIF-1α)的表达来募集成骨相关转录因子表达和刺激成骨细胞增殖,并能促进成骨细胞由血运丰富的骨膜区向血运较差的中心区域迁移[44]。在一项拮抗血管内皮生长因子受体(VEGFR)而抑制骨微血管内皮细胞增殖的实验研究中再次证实,骨微血管内皮细胞能正向促进成骨细胞增殖、迁移;随着对骨微血管内皮细胞调控成血管-成骨过程的不断深入研究,多种基因表达调控物和内源蛋白被广泛应用[44]。 2.4 基于骨微血管内皮细胞的股骨头坏死治疗 微循环障碍是股骨头坏死发病机制的关键因素一致被大家接受,而骨微血管内皮细胞在维持血管的正常结构和功能方面发挥着关键作用,骨微血管内皮细胞功能障碍导致的血管生成受损、细胞凋亡异常、血栓形成和脂肪栓塞均参与了股骨头缺血性坏死的发生和发展。股骨头坏死的治疗主要是两个方面,抑制股骨头坏死的进一步恶化和促进骨组织新生重建,而这两方面皆离不开血运,且血管的生成与骨组织重建是一个高度偶联的过程,如前文叙述的H型内皮细胞可以将骨祖细胞及成骨相关蛋白募集到周围,而骨祖细胞又可分泌促进血管生成的活性物质。基于此,从骨微血管内皮细胞入手,改善股骨头微循环来治疗股骨头坏死是一个新的切入点。 2.4.1 中药改善微循环 从中医学理论来说,同样认为各种原因所致的“血淤”是股骨头坏死的主要原因,所以中医药治疗股骨头坏死的重要途径之一便是以活血化瘀来改善股骨头微循环,像黄芪、当归、三七、淫羊藿苷、川芎、红花、牛膝、丹参等活血化瘀药物被广泛引用(表1),其中大部分药物都得到了现代药理学理论的证实,如三七被证实能够抗氧化、调控炎症反应、促进成血管相关因子血管内皮生长因子的表达。章友才等[45]同样在探讨三七的主要成分三七总皂苷对股骨头坏死的作用中发现,三七总皂苷能够有效增加股骨头微血管数量来治疗股骨头坏死。 "


目前中医则以整体观念与辨证论治的思想将股骨头坏死的治疗从活血化瘀进展到目前更深层次的机制探讨中。赵丁岩等[46]在股骨头微血管内皮细胞在激素刺激损伤后,淫羊藿苷含药血清对其进行体外实验,推测淫羊藿苷通过促进血管生成因子(主要是G-CSF)表达,抑制炎性因子(主要是白细胞介素4)释放,来恢复微血管内皮细胞功能,调节微循环,从而实现股骨头坏死的治疗,为淫羊藿苷治疗股骨头坏死指出现代药理学理论研究方向。李新建等[47]在研究红花的主要成分羟基红花黄色素A溶液对股骨头坏死的作用机制中证实,羟基红花黄色素A通过两个方面改善微循环功能、治疗股骨头坏死,其一,上调促血管生成因子(主要是血管内皮生长因子)的表达来增加微血管数量;其二,下调血液黏稠度,改善血流状态。尽管中药干预微循环来治疗股骨头坏死疗效确切,但单纯的中药治疗起效慢、服药周期长、容易引起肝肾功能损害,在治疗期间还需要患者有着较好的依从性来定期随访检测血液生化指标,所以采用中药辅助手术治疗股骨头坏死是治疗股骨头坏死的一大热点,几年来广大学者证实中药联合髓芯减压术、钽棒植入术、骨组织工程技术、游离腓骨移植术等均在股骨头坏死治疗方面有一定的临床效果[48-49]。 2.4.2 组织工程血管化 骨组织工程技术是目前比较热门的新技术,在修复组织损伤及缺损方面疗效显著,其机制是在缺损或者损伤部位彻底清除坏死、无活性组织,植入生物替代品,该替代品包括维持原组织形态及功能的支架、形成代替组织的原始种子细胞和促进新组织快速稳定生长的活性因子,完成组织修复[50]。修复不同组织有着不同的要求,如股骨头坏死修复,则需要具有稳定成骨效应的细胞、提供稳定力学支撑、生物相容性好、可控降解的支架材料等等要求。目前基于股骨头坏死中微循环功能障碍的特点及成骨-成血管偶联理论提出,需要在恢复及重建受损的微循环障碍的前提下来完成坏死股骨头修复。因此,骨组织工程技术治疗股骨头坏死的研究热点主要有两个方面:①在成骨的细胞培养中加入成血管细胞(内皮细胞、内皮祖细胞、基因转染的内皮细胞)共培养,促进血管形成,改善微循环,从而促进以细胞为基础构建体的骨形成;②控释细胞因子的添加或体外直接预构建血管形成可以明显缩短植入物血管化的时间。 (1)种子细胞共培养改善微循环:微血管内皮细胞是血管形成的关键环节,起始于微血管内皮细胞增殖,而后募集和分泌成血管相关活性物质,降解细胞外基质,在现存血管网络形成基础血管管状结构,招集平滑肌细胞、周细胞等其他血管管壁结构物质,最后稳定地促进新血管成熟。尽管内皮细胞在新血管形成中有着举足轻重的地位,但在体外研究发现,内皮细胞在体外生存能力较差,不能够稳定增殖,很容易老化、凋亡[51]。内皮祖细胞作为内皮细胞的前体细胞,由于其体外增殖能力强且可定向分化为微血管内皮,对新血管形成及维持血管修复有重要意义,而广受骨组织工程研究者喜爱。近期研究发现,在股骨头坏死发生后,随着内皮祖细胞数量显著降低,微血管内皮细胞迅速衰老,血管损伤加快[52]。基于此,学者们对于骨组织工程修复股骨头坏死的体外实验中,在原有成骨种子细胞的基础上增加了内皮祖细胞共培养,发现细胞共培养后,不仅内皮祖细胞自身有着成血管能力,加入的成骨种子细胞也可分泌促进血管生成的活性物质,能够加快血管结构的形成[51]。由于内环境本身就是复杂环境,是多种细胞及活性物质共同调控的,所以细胞共培养是有据可依的,共培养后细胞之间可以互相调控,促进细胞增殖分化,尤其对于微循环来说,能够更迅速地实现早期血管化问题,从而保证成骨的种子细胞能够更好地成活。 ZIGDON-GILADI等[53]在骨组织工程共培养种子细胞治疗骨缺损的研究中同样证实,共培养细胞的协同作用对成血管、成骨皆有利。虽然微血管内皮细胞体外成管能力差,但其可分泌各种活性物质来维持微循环内环境稳态,还是特别有吸引力的。近期研究发现,微血管内皮细胞体外成血管能力弱的主要原因是缺少促进血管合成的活性因子,在添加活性因子,如血管内皮生长因子、碱性成纤维细胞生长因子后,可明显观察到血管生成[54]。基于此,学者们采用目前新技术基因治疗来解决这一问题,在一项微血管内皮细胞导入血管内皮生长因子165基因的研究中发现,这一技术是有效的,不仅能使微血管内皮细胞稳定增殖,还能维持其原有的功能特性[55]。但也有学者指出,基因修饰后的微血管内皮细胞所形成的新血管无功能性[56]。基因修饰内皮细胞或许在种子细胞共培养实现早期血管化、改善微循环的问题上有着不错的前景,但对于基因修饰后的细胞后期是否存在更多问题就不得而知了,因为对其调控转录机制尚未明确,这需要广大学者继续努力。 (2)细胞因子添加改善微循环:细胞因子的添加可以促进内皮细胞增殖迁移、内皮祖细胞定向分化、增殖,是骨组织工程实现早期血管化、改善微循环的另一种策略。常用的细胞因子有血管内皮生长因子(VEGF)、骨形态发生蛋白(BMP)、胰岛素样生长因子(IGF)、富血小板血浆(PRP)等。对细胞因子作用的大量研究表明,单一细胞因子的使用不足以创造稳定的血管结构,因为许多生长因子是协同作用的。STONE等[57]的一项研究发现,仅靠内源性血管内皮生长因子A不能正确地诱导血管生成和动脉生成,因此多因子联合促血管化作用是骨组织工程研究热点。在一项双因子促进细胞血管化的研究中证实,联合血管内皮生长因子165(VEGF-165)与血小板衍生生长因子BB(PDGF-BB)相较于单独使用其中任何一种细胞因子在血管数量上有着显著差异,且双因子作用有利于维持完整的血管结构[58]。但此实验也存在一定的问题,由于细胞因子的生物半衰期一般都较短,释放后很快便失活,该实验远期效果未必有显著意义,且对于细胞因子添加浓度问题,一直没有确切的标准,因此,关于细胞因子添加实现早期血管化改善微循环还有一研究热点便是如何保证细胞因子可控地释放,从而解决半衰期短、过量产生的不良反应,而让其稳定地发挥作用,目前的大多数报道都是与球囊包裹技术的联合使用。作者所在课题组前期同样采用仿生控释血管内皮生长因子、骨形态发生蛋白2的聚乳酸-聚乙二醇-聚乳酸三嵌段共聚物(PELA)球囊支架,治疗早期股骨头坏死,结果认为相较于对照组,持续稳定地输出细胞因子更有利于成骨及成血管且安全[59]。 2.4.3 以miRNAs为靶点的药物设计 RNA是存在于细胞及病毒中遗传信息的载体,可以编码蛋白质,实现遗传信息在蛋白质上的表达,但98%RNA是不能编码蛋白质的,这种RNA被称为非编码RNA,miRNAs便是其中的一种。近期研究发现miRNA与许多疾病有一定的关联性,所以miRNAs受到越来越多的学者关注。miRNAs在股骨头坏死的研究中同样被发现多个异常表达,尤其是在激素对骨微血管内皮细胞作用机制的研究中得到了证实,有上调(miR-339,miR-132-3p)的,也有下调(miR-466b-2-3p,miR-222,miR-23b)的,基于此,广大学者思考是否影响miRNA的因素是发病机制的关键因素,所以可以从此入手,恢复下调miRNA的表达,抑制上调miRNA的表达,来设计相应药物使表达量失衡的miRNA恢复到正常水平[21]。目前,该想法的实践方面主要是通过观察miRNA的作用,正向模拟促进、反向拮抗抑制,而偶氮苯-2能特异性抑制miR-21的表达使得其在治疗心脏疾病中首先取得了显著成果[60]。因此,miRNA抑制剂也成为miRNA靶向药物研究的方向。由于miRNA应用的安全性问题、有效性问题、远期不良反应等仍有待考究,目前仍处于动物实验阶段。 "

| [1] AMANATULLAH DF, STRAUSS EJ, DI CESARE PE, et al. Current management options for osteonecrosis of the femoral head: part II, operative management. Am J Orthop (Belle Mead NJ). 2011;40(10): E216-225. [2] KUBO T, UESHOMA K, SAITO M, et al. Clinical and basic research on steroid-induced osteonecrosis of the femoral head in Japan. J Orthop Sci. 2016;21(4):407-413. [3] LARSON E, JONES LC, GOODMAN SB, et al. Early-stage osteonecrosis of the femoral head:where are we and where are we going in year 2018. Int Orthop. 2018;42(7):1723-1728. [4] IKEUCHI K, HASEGAWA Y, SEKI T, et al. Epidemiology of nontraumatic osteonecrosis of the femoral head in Japan. Mod Rheumatol. 2015; 25(2):278-281. [5] TAN B, LI W, ZENG P, et al. Epidemiological study based on Chinaosteonecrosis of the femoral head database. Orthop Surg. 2021; 13(1):153-160. [6] ZHAO D, ZHANG F, WANG B. Guidelines for Clinical Diagnosis and Treatment of Osteonecrosis of the Femoral Head in Adults (2019 Version). J Orthop Translat. 2020;21:100-110. [7] JOHNSON AJ,MONT ML A, TSAO AK, et al. Treatment of femoral head osteonecrosis in the United States: 16-year analysis of the Nationwide Inpatient Sample. Clin Orthop Relat Res. 2014;472:617-623. [8] XU H, WANG C, LIU C, et al. Cotransplantation of mesenchymal stem cells and endothelial progenitor cells for treating steroid-induced osteonecrosis of the femoral head. Stem Cells Transl Med. 2021;10: 781-796. [9] YU H, VANDEVORD PJ, MAO L, et al. Improved tissue-engineered bone regeneration by endothelial cell mediated vascularization. Biomaterials. 2009;30(4):508-517. [10] RABQUER BJ, TAN GJ, SHAHEEN PJ, et al. Synovial inflammation in patients with osteonecrosis of the femoral head. Clin Transl Sci. 2009; 2(4):273-280. [11] COHEN-ROSENBLUM A, CUI Q. Osteonecrosis of the femoral head. Orthop Clin North Am. 2019;50(3):139-149. [12] KALHOR M, HOROWITZ K, GHAREHDAO HI, et al. Anatomic variations in femor al head circulation. Hip int. 2012;22(3):307-312. [13] 赵德伟,邱兴.股骨头血液供应及其临床意义[J].临床外科杂志, 2017,25(8):568-570. [14] 张向南,耿凯龙,巨积辉,等.股骨头血供评估在股骨颈骨折诊断与治疗中的应用[J].国际骨科学杂志,2021,42(6):333-337. [15] PRIES AR, SECOMB TW, GAEHTGENA P, et al. Blood Flow in microvascular Networks-Experiments and Simulation. Circulation Res. 1990;67(4):826-834. [16] 张建色,张崇智,姜文学,等.大剂量激素对兔股骨头内血管影响的研究[J].实用骨科杂志,2009,15(5):351-353. [17] KUSUMBE AP, RAMASAMY SK, ADAMS RH. Coupling of Angiogenesis and Osteogenesis by a Specific Vessel Subtype in Bone. Nature. 2007; 507(7492):323-328. [18] ZHANG JK, PAN J, JING W. Motivating role of type H vessels in bone regeneration. Cell Prolif. 2020;53:e12874. [19] ZHOU CH, MENG JH, ZHAO CC, et al. PTH[1-34] improves the effects of core decompression in early-stage steroid-associated osteonecrosis model by enhancing bone repair and revascularization. PLoS One. 2017; 12:e0178781. [20] LANE NE, MOHAN G, YAO W, et al. Prevalence of glucocorticoid induced osteonecrosis in the mouse is not affected by treatments that maintain bone vascularity. Bone Rep. 2018;9:181-187. [21] GAO F, MAO T, ZHANG Q, et al. H subtype vascular endothelial cells in human femoral head: an experimental verification. Ann Palliat Med. 2020;9(4):1497-1505. [22] lE NOBLE F, LE NOBLE J. Bone biology: Vessels of rejuvenation. Nature. 2014;507:313-314. [23] 黄钰婷,张恺,苏菁,等.射血分数保留型心力衰竭与微血管内皮炎症[J].临床心血管病杂,2021,37(6):512-515. [24] LI H, HORKE S, FRSTERMANN U. Vascular oxidative stress,nitric oxide and atherosclerosis. Atherosclerosis. 2014;237:208-219. [25] 潘丽娜,汪泽扬,陈丽媛,等.血小板微囊泡对人微血管内皮细胞功能的影响[J].第三军医大学学报,2020,42(8):758-764. [26] 周占国,郭浩山,关涛,等.股骨头坏死病因的相关因素分析[J].中医正骨,2020,32(1):7-10. [27] 沈俊杰,李华灿,乐宇民.股骨头缺血性坏死数字减影血管造影及介入治疗效果观察[J].蚌埠医学院学报,2009,34(1):53-55. [28] YANG Y, LOU J, LI Z, et al. Effect of glucocorticoid on production of reactive oxygen species in bone microvascular endothelial cells. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2011;25:533-537. [29] XUE Y, XING Z, HELLEM S, et al. Endothelial cells influence the osteogenic potential of bone marrow stromal cells. Biomed Eng Online. 2009;8(17):34. [30] 王佰亮,李子荣,娄晋宁,等.淫羊藿苷对糖皮质激素诱导的骨微血管内皮细胞损伤的保护作用[J].中国微循环,2009,13(6):461-464. [31] VOGT CJ, SCHMID-SCHNBEIN GW. Microvascular endothelial cell death and rarefaction in the glucocorticoid - induced hypertensive rat. Microcirculation. 2001;8:129-139. [32] XU JZ. Animal models of steroid-induced osteonecrosis of the femoral head-a comprehensive research review up to 2018. Int Orthop. 2018; 42(7):1729-1737. [33] YOON BH. Alcohol intake and the risk of osteonecrosis of the femoral head in Japanese populations: a dose-response meta-analysis of case-control studies. Clin Rheumatology. 2017;36(11): 2517-2524. [34] NASEER ZA, BACHABI M, JONES LC, et al. Osteonecrosis in Sickle Cell Disease. South Med J. 2016;109(9):525-530. [35] 彭雯雯,刘国英,潘燕霞,等.ACE2基因过表达减轻血管紧张素Ⅱ诱导的神经细胞氧化应激[J].中国病理生理杂志,2019,35(6):1081-1088. [36] YAMAMOTO Y, ISHIZU A, IKEDA H, et al. Dexamethasone increased plasminogen activator inhibitor-1 expression on human umbilical vein endothelial cells: an additive effect to tumor necrosis factor-alpha. Pathobiology. 2004;71(6):295-301. [37] 孙伟,李子荣,史振才,等.严重急性呼吸综合征后激素性骨坏死患者的凝血和纤溶指标观察[J].中华全科医师杂志,2006,5(2):89-94. [38] KROL J, LOEDIGE I, FILIPOWICZ W. The widespread regulation of microRNA biogenesis, function and decay. Nat Rev Genet. 2010;11: 597-610. [39] AMBROS V. The functions of animal microRNAs. Nature. 2004;431:350-355. [40] YUE J, WAN F, ZHANG QD, et al. Effect of glucocorticoids on miRNA expression spectrum of rat femoral head microcirculation endothelial cells. Gene. 2018;651:126-133. [41] NGUYEN NH, TRAN GB, NGUYEN CT. Anti-oxidative effects of superoxide dismutase 3 on inflammatory diseases. J Mol Med (Berl). 2020;98:59-69. [42] LEI Z, VAN MIL A, BRANDT MM, et al. MicroRNA-132/212 family enhances arteriogenesis after hindlimb ischaemia through modulation of the Ras-MAPK pathway. J Cell Mol Med. 2015;19(8):1994-2005. [43] ZHOU H, MEHTA S, SRIVASTAVA SP, et al. Endothelial cell-glucocorticoid receptor interactions and regulation of Wnt signaling. JCI Insight. 2020; 5:314-319. [44] 陈培生,林小凤,林凤飞,等.H型血管耦联成血管-成骨机制在骨微环境重构机制的研究进展[J].中华创伤杂志,2021,37(11):1048-1054. [45] 章友财,刘金浪,蔡声麟,等.三七总皂苷对兔酒精性股骨头坏死微血管血供及超微结构的影响[J].江西医药,2016,51(1):23-25. [46] 赵丁岩,俞庆声,郭万首,等.淫羊藿甘对激素诱导损伤人股骨头微血管内皮细胞蛋白质表达谱的影响[J]. 中华医学杂志,2016, 96(13):1026-1030. [47] 李新建,齐振熙,余航,等.髓芯减压术联合羟基红花黄色素A对激素性股骨头坏死模免股骨头微循环的影响[J].中华中医药杂志, 2015,30(5):1538-1541. [48] 张蕾蕾,梁大伟,刘又文,等.微创粗通道减压病灶清除植骨术 联合中药治疗非创伤性股骨头坏死32例[J].中国中医骨伤科杂志, 2019,27(6):63-65. [49] 任博文.温肾活血汤合钽棒植入治疗早期非创伤性股骨头 缺血性坏死的临床观察[D].郑州:河南中医药大学,2016. [50] 秦宇星,任前贵,沈佩锋,等.组织工程技术治疗骨缺损:应用于临床还有多远?[J].中国组织工程研究,2021,25(29):4703-4708. [51] 冯勇.内皮祖细胞在股骨头坏死发病机制及治疗中的作用研究[D].武汉:华中科技大学,2010. [52] 王新刚,封占增,郭明峰,等.组织工程促血管化策略的研究进展[J].中华烧伤杂志,2012,28(5):374-377. [53] ZIGDON-GILADI H, BICK T, LEWINSON D, et al. Co-transplantation of endothelial progenitor cells and mesenchymal stem cells promote neovascularization and bone regeneration. Clin Implant Dent Relat Res. 2015;17(2):353-359. [54] KRUGER-GENGE A, BLOCKI A, FRANKE RP. et al. Vascular Endothelial Cell Biology:An Update. Int J Mol Sci. 2019;20(18):4411 [55] 明华伟,何芸,夏德林,等.VEGF 165基因转染HUVEC促进大鼠血管生成的实验研究[J].口腔颌面外科杂志,2017,27(3):161-165. [56] JIN HT, XU TT, CHEN QQ, et al. The Fate and Distribution of Autologous Bone Marrow Mesenchymal Stem Cells with Intra-Arterial Infusion in Osteonecrosis of the Femoral Head in Dogs. Stem Cells Int. 2016;86: 116-143. [57] STONE OA, CARTER JG, LIN PC, et al. Differential regulation of blood flow-induced neovascularization and mural cell recruitment by vascular endothelial growth factor and angiopoietin signalling. J Physiol. 2017; 595:1575-1591. [58] 毕翔宇,孙安,何惠宇.联合VEGF-165和PDGF-BB促进骨髓间充质干细胞血管化的体内研究[J].口腔医学,2020,40(1):7-12. [59] 任前贵,王瞾,张坤.仿生控释BMP-2和VEGF的PELA微球支架对骨髓间充质干细胞向成骨细胞分化的Wnt/β-catenin通路的影响[J].中国生物制品学杂志,2018,31(10):1118-1121+1125. [60] SIVARAJ KK, ADAMS RH. Blood vessel formation and function in bone. Development. 2016;143(15):2706-2715. [61] 徐海侠.联合移植骨髓间充质干细胞和内皮祖细胞治疗兔激素性股骨头坏死的实验研究[D].广州:南方医科大学,2021. [62] ZHOU P, LI Y, DI R, et al. H19 and Foxc2 synergistically promotes osteogenic differentiation of BMSCs via Wnt-beta-catenin pathway. J Cell Physiol. 2019;234(8):13799-13806. [63] LIAO H, ZHONG Z, LIU Z, et al. Bone mesenchymal stem cells coexpressing VEGF and BMP-6 genes to combat avascular necrosis of the femoral head. Exp Ther Med. 2018;15(1):954-962. |
| [1] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [2] | Chen Guanting, Zhang Linqi, Li Qingru. Meta-analysis of the value of exosomal miRNA for the diagnosis of chronic kidney disease [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 970-976. |
| [3] | Liu Gang, Deng Bowen, Jiang Shengyuan, Xu Lin, Fan Xiao, Tao Jingwei, Zhang Houjun, He Feng, Zhao Yi, Mu Xiaohong. Tetramethylpyrazine improves hemorheological indexes in rats with complete spinal cord transection: a dynamic observation [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(2): 282-286. |
| [4] | Wang Xinmin, Liu Fei, Xu Jie, Bai Yuxi, Lü Jian. Core decompression combined with dental pulp stem cells in the treatment of steroid-associated femoral head necrosis in rabbits [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1074-1079. |
| [5] | Zhou Hongqin, Wu Dandan, Yang Kun, Liu Qi. Exosomes that deliver specific miRNAs can regulate osteogenesis and promote angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1107-1112. |
| [6] | Xu Jing, Yan Yongmin, Cai Mengjie . miR-373 inhibits hepatic stellate cell activation by downregulating transforming growth factor beta type II receptor [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 756-761. |
| [7] | Fan Jilin, Zhu Tingting, Tian Xiaoling, Liu Sijia, Su Jing, Zhang Shiliang. Effect and mechanism of non-coding RNA regulating autophagy in myocardial ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(35): 5716-5723. |
| [8] | Deng Xiaohui, Zhang Zengzeng, Zhang Zhihua, Zhu Lingyan. Mechanism and application prospects of mesenchymal stem cell exosomes gene-modified microRNA in the treatment of diabetic foot [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(31): 5076-5084. |
| [9] | Liang Haoran, Zhou Xin, Yang Yanfei, Niu Wenjie, Song Wenjie, Ren Zhiyuan, Wang Xueding, Liu Yang, Duan Wangping. Pathogenesis of femoral head necrosis after internal fixation of femoral neck fractures in young adults [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 456-460. |
| [10] | Yang Qiongqiong, Li Ping, Wang Qian. Role and regulatory mechanism of microRNA in bone tissue repair around dental implants [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(28): 4539-4545. |
| [11] | Chen Xia, Shang Yuwei, Wang Linxiao, Shi Yichao, Liu Huijun, Sun Huiting. Transcriptome sequencing of the uterine in a mouse model of vitamin D deficiency [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(26): 4101-4106. |
| [12] | Wei Yufan, Fan Feiyan, Li Shuangli, Zhang Yunke. Future of exosomes and mesenchymal stem cell-derived exosomes in the diagnosis and treatment of Parkinson’s disease [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(25): 4076-4083. |
| [13] | Wu Zhongshu, Wei Yurou, Chen Xiaojun, Wuri Shana, He Wei, Wei Qiushi. Huo Xue Tong Luo capsule improves osteoblastogenesis of bone marrow mesenchymal stem cells through the ERα-Wnt/β-catenin signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(25): 3937-3943. |
| [14] | Yu Chunbo, Li Dayu, Fan Fang, Li Changfu. Transcription factor-miRNA-mRNA network analysis of osteogenic differentiation of adipose-derived stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(24): 3908-3913. |
| [15] | Qian Xiaofen, Zeng Ping, Liu Jinfu, Chen Cai, Fan Siqi, Nong Jiao, Deng Wei. Comprehensive analysis of competing endogenous RNA network and potential biomarkers in alcohol-induced osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(23): 3670-3675. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||