Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (5): 779-786.doi: 10.12307/2023.130
Previous Articles Next Articles
Research progress in promoting tendon to bone healing during anterior cruciate ligament reconstruction
Xiong Bohan1, Yu Yang1, Lu Xiaojun1, Wang Xu2, Yang Tengyun1, Zhang Yaozhang1, Liao Xinyu1, Zhou Xiaoxiang1, He Lu1, Li Yanlin1
- 1Department of Sports Medicine, the First Affiliated Hospital of Kunming Medical University, Kunming 650032, Yunnan Province, China; 2Department of Orthopedics, the Second Affiliated Hospital of Kunming Medical University, Kunming 650032, Yunnan Province, China
-
Received:2022-03-28Accepted:2022-05-11Online:2023-02-18Published:2022-07-25 -
Contact:Li Yanlin, Chief physician, Professor, Department of Sports Medicine, the First Affiliated Hospital of Kunming Medical University, Kunming 650032, Yunnan Province, China -
About author:Xiong Bohan, Master candidate, Department of Sports Medicine, the First Affiliated Hospital of Kunming Medical University, Kunming 650032, Yunnan Province, China -
Supported by:Yunnan Provincial Major Science and Technology Project, No. 202102AA100015 (to LYL); Yunnan Provincial Osteoarthritis Clinical Medical Center Project, No. ZX2019-03-04 (to LYL)
CLC Number:
Cite this article
Xiong Bohan, Yu Yang, Lu Xiaojun, Wang Xu, Yang Tengyun, Zhang Yaozhang, Liao Xinyu, Zhou Xiaoxiang, He Lu, Li Yanlin. Research progress in promoting tendon to bone healing during anterior cruciate ligament reconstruction[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 779-786.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
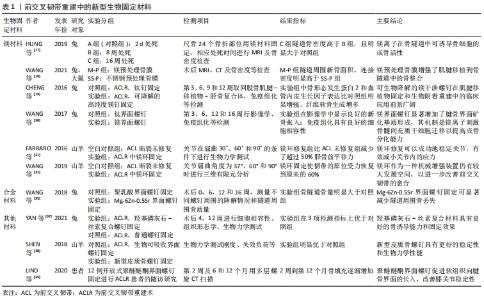
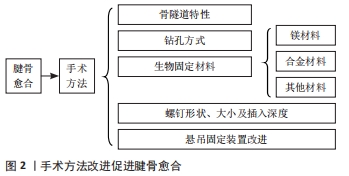
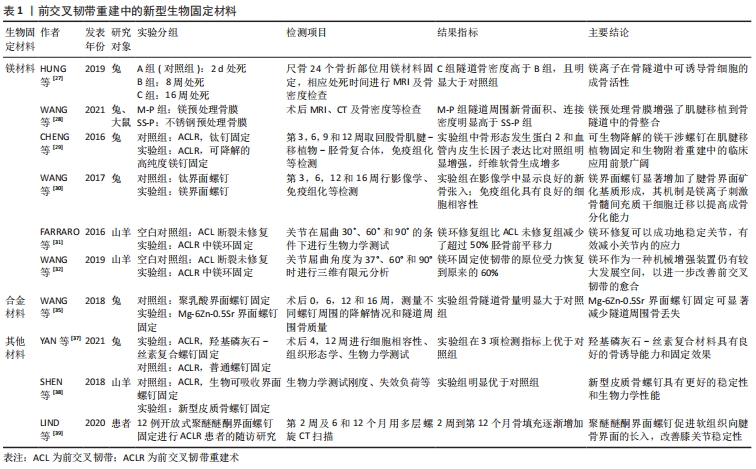
2.1.1 骨隧道特性 ZHAO等[11]为评估扁平骨隧道是否对前交叉韧带(ACL)重建后早期的肌腱-骨愈合(TBH)过程有积极的影响,将72只新西兰大白兔随机分为2组:扁平隧道组和常规圆形隧道组,分别对其进行前交叉韧带重建;术后4,8,12周采用组织学分析、显微CT扫描及生物力学检查评价两组的肌腱-骨愈合结果。结果在扁平隧道组发现了更快胶原蛋白重塑过程,腱骨界面区形成了更多纤维软骨;染色显示,扁平隧道组的界面区组织染色更深;Micro-CT扫描显示,扁平隧道组界面区新骨形成较多;生物力学测试还表明,扁平隧道组前交叉韧带重建将形成更牢固的腱骨界面。以上实验结果均证明在兔前交叉韧带重建模型中,平坦的骨隧道在术后早期加速了肌腱-骨愈合,为该前交叉韧带重建方法的进一步临床应用奠定了基础。FINK等[12]根据前交叉韧带似乎是一个扁平的“带状”结构这一最新解剖学研究结果,描述了一种新型前交叉韧带重建技术,旨在接近这一自然解剖结构,他们没有采用传统的圆形隧道,而是使用矩形股四头肌腱移植物或“扁平”腘绳肌移植物以创建一种薄的椭圆形插入物和一个C形胫骨插入物,结果发现这种结构不仅可以提供生物力学优势,增加旋转稳定性,还可以通过增加骨腱接触来改善腱骨愈合。 2.1.2 钻孔方式改进 前交叉韧带重建术主流的钻孔方式主要有2种,即机械钻孔和人工钻孔。人工钻孔保留了隧道内的骨量,减少了热坏死,并提供了一个更好的微环境以加快界面愈合[13],所以目前主要集中在人工钻孔对前交叉韧带重建预后效果的研究上。PLACELLA等[14]对24例前交叉韧带重建术后的运动员进行了为期8年的随访研究,结果发现原始的全内技术(即人工钻取隧道和植入短移植物)对于儿童/青少年运动员前交叉韧带损伤的外科治疗是一种非常有效的技术,对于腱骨愈合可能有积极的作用。TEI等[15]对28只成年雌性新西兰大白兔进行自体半腱肌腱移植重建前交叉韧带,并随机分为3组,在A组(n?12),使用机动设备钻取隧道;在B组(n?12),使用手动钻头钻取隧道;C组(n?4)为假手术对照组。结果表明,手动钻孔(B组)具有更高的肌腱-骨隧道愈合评分和更好的力学行为,反映出骨-纤维组织界面处良好的胶原纤维连续性,使得移植物和骨之间更好地结合。以上研究结果说明在前交叉韧带重建过程中使用手动钻孔可在关键的早期几周内实现更好的肌腱-骨愈合。 2.1.3 生物固定材料的选择 在前交叉韧带重建中,选择最佳的固定材料是非常重要的。在前交叉韧带重建术开展早期,人们发现用于固定的永久性金属界面螺钉具有较强的初始固定能力[16]。然而随着研究的深入,人们发现了刚性金属界面螺钉的一些缺点,如在重建时存在移植物损伤和断裂的风险,术后影像学检查干扰成像模式(如磁共振成像)等[17]。在之后,为了克服传统金属螺钉的这些局限性,具有生物相容性的聚合物干扰螺钉被开发用于前交叉韧带重建,以提供牢固的初始固定,减小移植损伤[18]。但近年来的研究发现这种螺钉的局限性同样明显,如据报道在前交叉韧带重建中使用聚乳酸干扰螺钉固定移植物时,该装置的机械性能比金属装置弱,并且在植入时经常断裂[19]。一项长期随访临床研究表明,随着聚合物质量的减少,界面螺钉被含有巨噬细胞的纤维组织所取代,并且聚合物降解产生的物质聚集形成了酸性环境,不利于骨隧道的愈合[20]。以上研究结果说明,一些传统固定材料的临床效果不甚理想,故近年来,新型生物固定材料的开发逐渐成为了研究的热点。 (1)镁材料:近几十年来,基于生物可降解镁(Mg)的骨科材料研发引起了材料工程师、基础研究人员和临床医生的极大关注[21-25]。镁基材料还具有骨诱导作用,尤其是在组织工程中具有很大优势,可促进骨愈合,并可作为药物、细胞和细胞因子传递的支架[26]。 有研究表明,镁材料通过有关通路调节干细胞的多能性而对腱骨愈合有积极作用。如HUNG等[27]证实用镁离子处理骨髓间充质干细胞,使得典型的Wnt/β-catenin通路被激活,镁离子在骨再生中的独特贡献突出了镁材料干扰螺钉在肌腱-骨界面愈合中的潜在应用价值。因此,WANG等[28]比较了镁预处理骨膜(M-P)和不锈钢预处理骨膜(SS-P)在前交叉韧带重建中的作用,并将其应用到鼠及兔模型中,结果证明镁预处理骨膜显著地增加了骨膜和肌腱交界面纤维软骨的形成,显著防止了隧道周围骨丢失,使更多的骨组织向肌腱移植物生长。 镁材料对腱骨愈合的促进作用还体现在促进特定生物活性因子的分泌和聚集上。如CHENG等[29]发现镁干扰螺钉通过加强骨形态发生蛋白2和血管内皮生长因子的分泌,以促进兔前交叉韧带重建模型中纤维软骨内皮细胞的再生,这说明镁界面螺钉在前交叉韧带重建中具有促进纤维软骨再生的潜力。WANG等[30]则发现,从高纯度镁界面螺钉中释放的镁离子有利于转化生长因子β1和血小板衍生生长因子BB的分泌,从而招募更多的骨髓间充质干细胞用于腱骨愈合,以促进肌腱-骨界面的血管生成和骨长入。 近年来,镁环固定装置也逐渐应用于临床研究。FARRARO等[31]设计了一种生物可吸收的单晶镁环装置,将其应用于山羊尸体模型,结果发现镁环修复组比前交叉韧带未修复组减少了超过50%胫骨前平移力,且前交叉韧带和内侧半月板原位受力恢复到接近正常水平。以上生物力学结果说明镁环修复可以成功地在术后立即稳定关节并保护前交叉韧带,为未来的体内研究奠定了框架。WANG等[32]则建立了山羊膝关节三维有限元模型,以量化镁环修复后的前交叉韧带及股骨隧道口的负荷和应力水平,结果发现镁环修复后,前交叉韧带原位受力恢复至完整时的近60%,隧道口的最大应力为完整前交叉韧带的71%,说明镁环机械固定装置对前交叉韧带的修复有明显的增强作用。上述定量数据可以作为开发新型设备的基础,以机械地增强人类前交叉韧带的腱骨愈合。 (2)合金材料:合金化是改善金属力学性能最有效的方法之一[33]。越来越多研究人员将营养元素(如钙、锌、锶、锰等)和稀土元素作为合金元素来制造新型镁基合金作为潜在的骨科植入物,以解决生物安全问题和寻求促进腱骨愈合的新型材料[34]。 WANG等[35]为了解决生物可降解镁基固定器械强度较差这一问题,运用镁(Mg)、锌(Zn)、锶(Sr)等金属元素开发出了最佳Zn含量(质量分数6%)和Sr含量(质量分数0.5%)的Mg-6Zn-0.5Sr界面螺钉,与传统可降解聚乳酸组相比,Mg-6Zn-0.5Sr界面螺钉在16周内显著增加了兔前交叉韧带重建后隧道周围骨量,显著减少隧道周围骨丢失。此外,另一种使用等离子注入的合金化技术也显示了镁或其合金作为新型固定材料的潜力。例如,将纯Mg注入锌(Zn)和铝(Al)离子,以及将稀土WE43镁合金注入钕(Nd)离子,由于在其表面形成致密的氧化膜,其耐蚀性得到了提高[36]。但这类材料对腱骨愈合的作用仍需进一步研究。 (3)其他材料:近年来由于组织工程、3D打印、生物工程等新兴技术的兴起,运用这类技术制造的固定材料在临床上得到了一定的研究。YAN等[37]制备了一种新型高含量羟基磷灰石-丝素(HA-SF)杂化颗粒的复合材料螺钉,其中含有羟基磷灰石-丝素蛋白杂化纳米颗粒,并重点优化了丝素蛋白与无机物质之间的界面黏附,以产生均匀的内部结构。后将其应用于兔前交叉韧带重建模型,发现这种复合材料制成的界面螺钉显示出优异的生物力学性能,并且在宿主骨隧道中发现显著的新骨长入,具有很好的临床应用潜力。SHEN等[38]通过比较新型皮质骨螺钉(BCIS)与生物可吸收界面螺钉(BIS)在山羊前交叉韧带重建术后的效果,发现新型皮质骨螺钉具有较好的初始固定强度,生物力学性能优于生物可吸收界面螺钉,适合于积极的康复计划。LIND等[39]对12例前交叉韧带重建患者术中采用开放式聚醚醚酮界面螺钉固定胫骨,术后通过CT骨扫描发现聚醚醚酮界面螺钉可促进软组织向螺钉及腱骨界面的长入,12个月时螺钉平均骨填充量达到理想效果,并有助于膝关节功能及稳定性的提升。 前交叉韧带重建中的新型生物固定材料总结见表1。 "
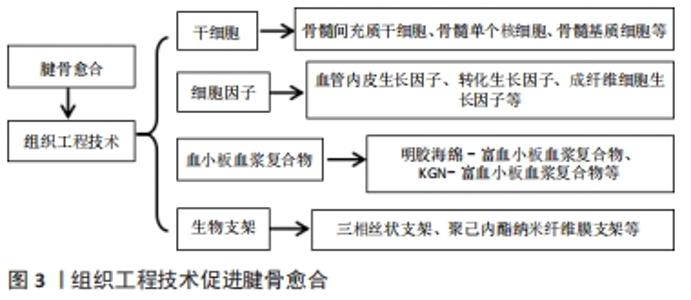
2.1.4 螺钉形状、大小及插入深度 在前交叉韧带重建中,移植的肌腱通过界面螺钉(IFSs)锚定,经常被用来替代损坏的韧带[40]。螺钉的形状、大小及插入深度决定其是否与移植物或骨隧道匹配,直接影响前交叉韧带重建术后腱骨愈合的程度。为研究这一问题,MAU等[41]采用有限元分析方法,对六边形、四边形、环形、三角形、三叶形和涡轮式6种驱动设计进行对比研究,结果发现螺钉插入经典转距(2 Nm)时,最大von Mises应力和剪切应力集中在驱动器的转角或转弯处,当剪切应力大于镁的屈服应力(193 MPa)时,会导致剥离;随着驱动深度增加4倍,驱动宽度增加30%,使得最大应力值显著降低了75%以上;以上结果说明螺钉合适的形状、大小及插入深度可以通过减少植入装置的失败来改善腱骨愈合,提高手术成功率。BAYDOUN等[42]对猪模型的研究表明,一种用于单级修正前交叉韧带重建的堆叠螺钉结构与模型中的单一螺钉结构相比,显示出足够的生物力学强度和线性刚度。 2.1.5 悬吊固定装置改进 在前交叉韧带重建术中,股骨与胫骨的固定装置有很多种,每种装置对移植物的愈合情况还不甚了解。为解决这一问题,HEXTER等[43]使用2个不同的股骨固定装置评估脱细胞猪超屈肌腱(pSFT)异种移植物的愈合情况,方法是将12只绵羊采用脱细胞猪超屈肌腱进行单侧单束前交叉韧带重建,第1组(n=6)采用股骨皮质悬吊固定,第2组(n=6)采用交叉钉固定,结果发现与交叉钉固定相比,股骨皮质悬吊固定移植物重塑更强、功能恢复更早,以上结果说明股骨皮质悬吊固定可能在促进腱骨愈合方面有积极作用。PUTNIS等[44]对38例采用可悬吊固定装置(ASF)重建前交叉韧带患者术后进行MRI检查,分析骨隧道中的骨丢失程度和移植物信号强度,并与普通螺钉固定比较,最后发现胫骨可悬吊固定装置有效减少了胫骨隧道的扩大,降低例隧道炎症的发生率。以上研究说明无论是股骨还是胫骨的皮质悬吊固定,都可能促进前交叉韧带重建术后的腱骨愈合。 2.2 组织工程技术促进腱骨愈合 目前肌腱和韧带移植的高失败率和复发率促使研究人员探索通过组织工程技术激发肌腱和韧带的新潜力。这可以启发研究者运用组织工程三联体(细胞、支架、生物因子)配合有关细胞衍生物(如富血小板血浆等),以制备类似于天然组织的组织工程肌腱和韧带[45]。见图3。"
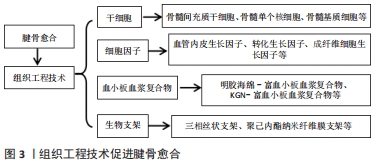

2.2.1 干细胞 干细胞是具有多向分化潜能和自我复制能力的原始的未分化细胞,由于其自我更新能力、长期生存能力和多系分化潜能,因此在组织工程中应用广泛[46]。干细胞在组织工程中又包括到骨髓间充质干细胞、骨髓单个核细胞及骨髓基质细胞等。 骨髓间充质干细胞是存在于骨髓基质中非造血系的具有多向分化潜能的成体干细胞,具有自我更新能力强、多向分化、可塑性高等特点,在分泌细胞因子、免疫调节等方面具有独特作用。骨髓间充质干细胞具有显著的自我更新能力、长期生存能力和多线性培养能力,是组织工程技术的重要细胞[46]。干细胞条件培养基(conditioned culture medium,CM)在再生医学中的应用也日益广泛。SUN等[47]为研究前交叉韧带重建后移植物-宿主整合的情况,将人骨髓干细胞条件培养基(hBMSC-CM)应用于大鼠前交叉韧带损伤模型,结果发现hBMSC-CM可促进移植物与骨结合并促进肌腱韧带化,增强成纤维细胞的增殖、分化和胶原合成。BI等[48]将骨髓间充质干细胞联合丝胶原支架对新西兰大白兔模型进行前交叉韧带重建,结果发现骨髓间充质干细胞明显促进膝关节内韧带再生和移植物界面骨整合,这提示丝胶原蛋白支架与骨髓间充质干细胞的组合在未来临床应用上具有很大的前景。 骨髓单个核细胞和骨髓间充质干细胞在韧带重建过程中都具有较强的增殖能力。LU等[49]为探究不同来源的骨髓细胞在同种异体前交叉韧带重建中的作用,将新鲜分离的骨髓单个核细胞和骨髓间充质干细胞进行对比研究,并构建了兔同种异体腘绳肌前交叉韧带重建模型,随机分为骨髓单个核细胞组、骨髓间充质干细胞组和对照组,结果发现新鲜分离的骨髓单个核细胞在兔同种异体前交叉韧带重建模型中的再生能力与体外培养的骨髓间充质干细胞相当,都在一定程度上促进了腱骨界面的愈合。 2.2.2 细胞因子 细胞因子是免疫原、丝裂原或其他刺激剂诱导多种细胞产生的低分子质量可溶性蛋白质,具有调节固有免疫和适应性免疫、促进血细胞生成、加快细胞生长以及促进损伤组织修复等多种功能。目前细胞因子在前交叉韧带重建中的应用越来越广泛。骨形态发生蛋白、转化生长因子β、血管内皮生长因子、成纤维细胞生长因子以及粒细胞集落刺激因子等在多种动物模型中均表现出对腱骨愈合有促进意义的研究结果[50]。SETIAWATI等[51]将骨髓间充质干细胞联合血管内皮生长因子注射入兔前交叉韧带重建的骨隧道中,结果发现接受处理的股骨隧道具有更好的晚期愈合,增加了Ⅲ型胶原纤维的合成,MRI和生物力学分析结果更加优越。WANG等[52]发现转化生长因子β在骨髓间充质干细胞中过表达导致转化生长因子β/MAPK信号通路上调,最终促进前交叉韧带重建后骨隧道骨形成和腱骨愈合。KIM等[53]在残余保存前交叉韧带重建(RP-ACLR)的患者中检测其关节液中相关因子的浓度,结果发现在术后3个月内,白细胞介素8浓度非常高且其浓度随时间的增加与血管内皮生长因子浓度的增加是一致的,因此说明在残余保存前交叉韧带重建早期,白细胞介素8可能有助于血管生成,有助于移植物肌腱的血管重建和韧带化。CHEN等[54]发现在兔前交叉韧带重建模型中,共注射人脂肪基质细胞和人重组骨形态发生蛋白2/纤维蛋白凝胶可以明显增强肌腱与移植物的骨整合。LU等[55]则发现酸性胶原成纤维细胞生长因子(aFGF/collagen)复合材料可以促进前交叉韧带重建后肌腱-骨界面的早期愈合,尤其是在酸性胶原成纤维细胞生长因子处于高浓度的情况下,这一促进作用尤为明显。BEZ等[56]将超声介导的骨形态发生蛋白6基因传递到内源性间充质祖细胞可以有效改善大型动物的前交叉韧带重建效果,为此项技术应用于临床提供了可能性。 2.2.3 血小板血浆复合物 富血小板血浆(platelet-rich plasma,PRP)是通过离心方法从自体血中提取的血小板浓缩物,其中含有各种生长因子,可为局部组织再生提供有利环境,同时亦可促进组织的血管化和神经再生[57],对腱骨愈合可能有潜在的促进作用。ZHANG等[58]探讨了富血小板血浆联合明胶海绵促进肌腱-骨界面愈合的作用,结果发现明胶海绵负载富血小板血浆可延长富血小板血浆的生物活性时间,促进骨髓间充质干细胞增殖和成骨基因表达;在该研究的兔前交叉韧带重建模型中,它也促进了肌腱-骨交界处的早期愈合过程。近年来,富血小板血浆联合胶原基质或相关化学物质对前交叉韧带重建的影响也得到了一定的研究。MILLAN等[59]回顾性分析了14例采用Ⅰ型可吸收胶原基质浸染富血小板血浆的增强四股同种异体腘绳肌移植前交叉韧带重建的患者,结果发现用该方法可以提高生物移植物进入宿主骨隧道的能力,取得了良好的临床效果。ZHENG等[60]将地榆(蔷薇科,一种名贵的中药)中提取的多糖成分SOWPa加入富血小板血浆中用于前交叉韧带重建,研究发现SOWPa能够通过阻断TLR-4/NF-κB通路,协助富血小板血浆降低前交叉韧带中成纤维细胞凋亡,提高细胞活力、迁移和分化,说明SOWPa作为佐剂可能提高了富血小板血浆在前交叉韧带重建手术中的成纤维细胞的再生潜力,可能间接促进了腱骨愈合。ZHOU等[61]使用一种名为kartogenin (KGN)的化合物与富血小板血浆构建了KGN-富血小板血浆复合物,他将实验大鼠分为3组:分别在肌腱-骨隧道界面注射KGN-富血小板血浆复合物、富血小板血浆或生理盐水(对照组);结果免疫组化和免疫荧光染色显示KGN-富血小板血浆组形成了大量蛋白多糖,表明了该组产生了更优越的软骨样过渡区,且过渡区中存在大量Ⅰ型胶原和Ⅱ型胶原;相比之下,富血小板血浆组和对照组没有软骨样组织,只有少量的Ⅰ型胶原和Ⅱ型胶原染色;最后,在8周时,KGN-富血小板血浆组的移植物均高于其余两组。这些结果表明,以富血小板血浆为载体的KGN促进了肌腱移植物与骨界面间纤维软骨带的形成,提高了肌腱-骨界面的机械强度,促进了腱骨愈合。 2.2.4 生物支架 制备组织工程生物支架的材料应当具有良好的力学性能、生物相容性及与骨相似的特性,这样才能研制出适合临床骨组织工程的支架[62-63],制备支架的方法必须考虑包括骨传导性、生物相容性、孔隙率、力学性能、生物可降解性等几个基本因素,还应考虑生物材料的组成、结构和分子质量等有关特性[64-65]。 运用组织工程技术制造的人工韧带重建前交叉韧带是一种快速恢复的良好治疗方法。然而,由于人工韧带的常用材料聚对苯二甲酸乙二醇酯(PET)具有疏水性和较低的生物诱导活性,导致治疗效果的不确定性。所以近年来,人们在改善人工韧带的生物相容性方面做了很多努力,之前的研究则表明,运用有关化学物质或生物活性物质进行表面改性是一种有效的策略[66]。ZHANG等[67]开发了一种新型的混合仿生人工韧带支架,由搭载骨形态发生蛋白7的聚己内酯(PCL)纳米纤维膜和聚对苯二甲酸乙二醇酯(PET)纤维网织物组成,该支架具有良好的生物相容性和骨诱导性,不仅增强了肌腱-骨界面的成骨作用,而且缩短了腱骨愈合时间,具有较好的力学性能,这种支架为今后前交叉韧带重建移植物的制备和研究提供了新的思路。JIANG等[68]用等离子法制备壳聚糖丝素蛋白/聚对苯二甲酸乙二醇酯(CTS-SF/PET)、聚糖丝素蛋白/聚对苯二甲酸乙二醇酯/羟基磷灰石(CTS-SF/PET/HAP)和壳聚糖丝素蛋白/聚对苯二甲酸乙二醇酯/银@羟基磷灰石(CTSSF/PET/Ag@HAP)等支架。体内和体外结果表明,以上支架材料通过扩大细胞增殖和上调肌腱发育相关特性,使肌腱再生得到了根本性改善;组织相容性试验表明,羟基磷灰石和银@羟基磷灰石支架减少了骨隧道的骨丢失,提高了骨连接复合体的生物力学质量。 近年来,利用逐层自装技术(Lbl)、3D打印技术和基因固定增强技术所制造的生物支架也得到了一定研究。HAN等[69]以聚己内酯(PCL)静电纺丝膜和壳聚糖/透明质酸(CS/HA)多层膜为材料,利用逐层自装技术,制备了肌腱-骨结合仿生纳米纤维膜,结果发现壳聚糖/透明质酸多层膜沉积在聚己内酯纳米纤维表面,使基质细胞衍生因子1α和骨形态发生蛋白2在腱骨界面局部传递以促进细胞增殖和募集,并诱导骨髓间充质干细胞的成骨分化,有效促进了前交叉韧带重建术后的腱骨愈合。PARK等[70]在兔前交叉韧带重建模型中植入间充质干细胞(MSCs)的三维生物打印支架套筒,结果在组织学评估中,治疗组通过宽纤维软骨形成平滑的骨-肌腱转换,免疫组化染色显示界面区有丰富的Ⅱ型胶原生成,骨隧道面积明显高于对照组,且在治疗的所有时间点中,治疗组的骨肌腱愈合组织学评分均显著高于对照组。LIU等[71]研制了一种用于软组织-骨连接重建的仿生随机-对齐-随机肌腱复合支架,并将其用于兔前交叉韧带重建模型中,结果证明这种支架促进了兔间充质干细胞在体外的成骨和成骨基因表达,同时也促进了腱骨界面骨和纤维软骨的形成。FAN等[72]则开发了一种基因固定的分层三相丝状支架用于前交叉韧带重建,结果在兔模型体外检测表明,该基因固定的三相丝状支架能显著促进骨髓间充质干细胞的增殖和分化;在术后12周时,骨结合恢复基本完整,形成明显的三层组织,力学能力强;这些结果表明,采用分层方法和基因固定技术有效地加强了丝状支架对前交叉韧带重建后腱骨界面的形成,扩大了基于丝状支架的韧带移植重建前交叉韧带的治疗潜力。 2.3 术后康复优化促进腱骨愈合 2.3.1 术后固定时间 以前的研究证明,术后过度的基质金属蛋白酶活动可能会损害肌腱到骨的愈合[73]。NAKAGAWA等[74]对60只C57BL雄性小鼠进行前交叉韧带重建,并使用荧光探针检测基质金属蛋白酶浓度,结果发现与长期固定相比,短期固定导致骨隧道周围基质金属蛋白酶活动减少,说明前交叉韧带重建后短时间内固定可能通过减少过度的基质金属蛋白酶表达来增强移植物-骨界面愈合。MA等[75]也发现移植物-骨隧道愈合对前交叉韧带动态移植物力的变化是敏感的,一段时间的固定有利于软组织前交叉韧带移植物和移植物隧道之间的早期愈合过程。但短期固定在人身上是否适用及短期固定的量化标准目前仍需进一步研究。 2.3.2 术后早期机械负荷或应力 前交叉韧带重建后,组织的机械负荷对肌腱-骨愈合有显著影响[76]。CAMP等[77]为确定机械负荷起始时间对骨隧道中肌腱移植物愈合的影响,将56只小鼠采用自体屈肌腱重建前交叉韧带并随机分为4组,设定不同的机械负荷时间:立即,5,10,21 d;手术时将一个外固定架放置在膝关节上,并在计划开始机械负荷时将其移除;取出外固定器后,允许动物自由、不受限制地在笼内活动,术后28 d处死所有小鼠,通过生物力学测试、显微CT (micro-CT)和组织学分析评估肌腱-骨愈合情况。结果发现:5 d组重建前交叉韧带的平均失效力最高,且显著高于其他3组;5 d组在股骨隧道、胫骨隧道和双侧骨隧道中骨体积分数最大;组织学分析显示,5 d组瘢痕组织界面较窄,腱-骨界面的直接接触增加,以上结果说明在前交叉韧带重建后,一段固定时间不负重似乎可以提高愈合肌腱-骨界面的生物力学强度。SONG等[78]采用组织学检测、生物力学分析和肌腱-骨界面基因表达监测等方法,观察连续被动运动治疗对兔前交叉韧带重建模型肌腱-骨愈合的影响,结果发现术后连续被动运动治疗显著促进肌腱-骨愈合,表现为纤维软骨数量增加,肌腱-骨连接处Ⅰ型胶原、碱性磷酸酶、骨桥蛋白和钙调蛋白基因表达上调,以上结果说明机械刺激可促进局部前体细胞的增殖和分化,从而增强骨髓间充质干细胞在肌腱-骨愈合中的再生潜能,提示术后早期活动可能促进腱骨愈合。 2.3.3 术后间歇负压 在临床治疗中,已知一定的下肢间歇性负压(INP)可增加间歇性跛行患者的步行能力[79]。基于这一启发,SUN等[80]将间歇性负压应用于兔前交叉韧带重建术后,将24只新西兰大白兔一侧后腿作为负压组,对侧后腿作为对照组,在重建前交叉韧带后6周提取关节液,检测白细胞介素1β和肿瘤坏死因子α的表达水平;同时测定了肌腱移植物张力,观察腱骨界面的组织形态、血管内皮生长因子的表达。结果发现负压组肌腱最大负荷断裂明显大于对照组;肌腱-骨界面的组织学研究发现,负压组比对照组有更多的含软骨样细胞和新骨形成;血管内皮生长因子表达明显高于对照组;滑膜液中白细胞介素1β和肿瘤坏死因子α较对照组明显降低,以上结果说明间歇负压在兔肌腱-骨愈合和前交叉韧带重建中起积极作用。 "

| [1] 孙畅,郭亭,李林涛,等.前交叉韧带重建术后腱骨愈合的生物学干预研究进展[J].中华骨与关节外科杂志,2020,13(10):863-869. [2] 钱利海,梁清宇.前交叉韧带重建术后腱-骨愈合的生物学研究进展[J].中华解剖与临床杂志,2018,23(3):272-276. [3] 粟玉斌,孙岩,胡军祖,等.膝关节前交叉韧带重建术后腱骨愈合最新进展[J].临床医药文献电子杂志,2020,7(A3):191-192. [4] SUN Z, WANG X, LING M, et al. Acceleration of tendon-bone healing of anterior cruciate ligament graft using intermittent negative pressure in rabbits. J Orthop Surg Res. 2017;12(1):60. [5] AGARWALLA A, PUZZITIELLO R, GARCIA GH, et al. Application of a Beta-Tricalcium Phosphate Graft to Minimize Bony Defect in Bone-Patella Tendon-Bone Anterior Cruciate Ligament Reconstruction. Arthrosc Tech. 2018;7(7):e725-e729. [6] THOMOPOULOS S, PARKS WC, RIFKIN DB, et al. Mechanisms of tendon injury and repair. J Orthop Res. 2015;33(6):832-839. [7] ROTHRAUFF BB, TUAN RS. Cellular therapy in bone-tendon interface regeneration. Organogenesis. 2014;10(1):13-28. [8] SAMITIER G, MARCANO AI, ALENTORN-GELI E, et al. Failure of Anterior Cruciate Ligament Reconstruction. Arch Bone Jt Surg. 2015;3(4):220-240. [9] 辜刘伟,周霖,庹伟,等.促进膝关节前交叉韧带重建术后腱骨愈合方法的研究进展[J].中国现代医学杂志,2021,31(23):49-56. [10] XU Y, ZHANG WX, WANG LN, et al. Stem cell therapies in tendon-bone healing. World J Stem Cells. 2021;13(7):753-775. [11] ZHAO F, HU X, ZHANG J, et al. A more flattened bone tunnel has a positive effect on tendon-bone healing in the early period after ACL reconstruction. Knee Surg Sports Traumatol Arthrosc. 2019;27(11):3543-3551. [12] FINK C, SMIGIELSKI R, SIEBOLD R, et al. Anterior Cruciate Ligament Reconstruction Using a Ribbon-Like Graft With a C-Shaped Tibial Bone Tunnel. Arthrosc Tech. 2020;9(2):e247-e262. [13] YUE L, DEFRODA SF, SULLIVAN K, et al. Mechanisms of Bone Tunnel Enlargement Following Anterior Cruciate Ligament Reconstruction. JBJS Rev. 2020;8(4):e0120. [14] PLACELLA G, BARTOLI M, PERUZZI M, et al. Return to sport activity after anterior cruciate ligament reconstruction in skeletally immature athletes with manual drilling original all inside reconstruction at 8 years follow-up. Acta Orthop Traumatol Turc. 2016;50(6):635-638. [15] TEI MM, PLACELLA G, SBARAGLIA M, et al. Does Manual Drilling Improve the Healing of Bone-Hamstring Tendon Grafts in Anterior Cruciate Ligament Reconstruction? A Histological and Biomechanical Study in a Rabbit Model. Orthop J Sports Med. 2020;8(4):2325967120911600. [16] BARBER FA, ELROD BF, MCGUIRE DA, et al. Preliminary results of an absorbable interference screw. Arthroscopy. 1995;11(5):537-548. [17] HALEWOOD C, HIRSCHMANN MT, NEWMAN S, et al. The fixation strength of a novel ACL soft-tissue graft fixation device compared with conventional interference screws: a biomechanical study in vitro. Knee Surg Sports Traumatol Arthrosc. 2011;19(4):559-567. [18] PILTZ S, STRUNK P, MEYER L, et al. Fixation strength of a novel bioabsorbable expansion bolt for patellar tendon bone graft fixation: an experimental study in calf tibial bone. Knee Surg Sports Traumatol Arthrosc. 2004;12(5):376-383. [19] SMITH CA, TENNENT TD, PEARSON SE, et al. Fracture of Bilok interference screws on insertion during anterior cruciate ligament reconstruction. Arthroscopy. 2003; 19(9):E115-117. [20] WALTON M, COTTON NJ. Long-term in vivo degradation of poly-L-lactide (PLLA) in bone. J Biomater Appl. 2007;21(4):395-411. [21] ZHAO D, WITTE F, LU F, et al. Current status on clinical applications of magnesium-based orthopaedic implants: A review from clinical translational perspective. Biomaterials. 2017;112:287-302. [22] ZHANG Y, XU J, RUAN YC, et al. Implant-derived magnesium induces local neuronal production of CGRP to improve bone-fracture healing in rats. Nat Med. 2016;22(10):1160-1169. [23] SONG B, LI W, CHEN Z, et al. Biomechanical comparison of pure magnesium interference screw and polylactic acid polymer interference screw in anterior cruciate ligament reconstruction-A cadaveric experimental study. J Orthop Translat. 2016;8:32-39. [24] MARRELLA A, LEE TY, LEE DH, et al. Engineering vascularized and innervated bone biomaterials for improved skeletal tissue regeneration. Mater Today (Kidlington). 2018;21(4):362-376. [25] HAN HS, LOFFREDO S, JUN I, et al. Current status and outlook on the clinical translation of biodegradable metals. Mater Today. 2019;23:57-71. [26] FARRARO KF, KIM KE, WOO SL, et al. Revolutionizing orthopaedic biomaterials: The potential of biodegradable and bioresorbable magnesium-based materials for functional tissue engineering. J Biomech. 2014;47(9):1979-1986. [27] HUNG CC, CHAYA A, LIU K, et al. The role of magnesium ions in bone regeneration involves the canonical Wnt signaling pathway. Acta Biomater. 2019;98:246-255. [28] WANG J, XU J, WANG X, et al. Magnesium-pretreated periosteum for promoting bone-tendon healing after anterior cruciate ligament reconstruction. Biomaterials. 2021;268:120576. [29] CHENG P, HAN P, ZHAO C, et al. High-purity magnesium interference screws promote fibrocartilaginous entheses regeneration in the anterior cruciate ligament reconstruction rabbit model via accumulation of BMP-2 and VEGF. Biomaterials. 2016;81:14-26. [30] WANG J, XU J, SONG B, et al. Magnesium (Mg) based interference screws developed for promoting tendon graft incorporation in bone tunnel in rabbits. Acta Biomater. 2017;63:393-410. [31] FARRARO KF, SASAKI N, WOO SL, et al. Magnesium ring device to restore function of a transected anterior cruciate ligament in the goat stifle joint. J Orthop Res. 2016;34(11):2001-2008. [32] WANG H, KANG H, YAO J, et al. Evaluation of a magnesium ring device for mechanical augmentation of a ruptured ACL: Finite element analysis. Clin Biomech (Bristol, Avon). 2019;68:122-127. [33] CHEN J, TAN L, YU X, et al. Mechanical properties of magnesium alloys for medical application: a review. J Mech Behav Biomed Mater. 2018;87:68-79. [34] GUO KW. A review of magnesium/magnesium alloys corrosion, Recent Pat Corros Sci. 2011;1(1):72-90. [35] WANG J, WU Y, LI H, et al. Magnesium alloy based interference screw developed for ACL reconstruction attenuates peri-tunnel bone loss in rabbits. Biomaterials. 2018;157:86-97. [36] JIN WH, WU GS, FENG HQ, et al. Improvement of corrosion resistance and biocompatibility of rare-earth WE43 magnesium alloy by neodymium self-ion implantation. Corrosion Sci. 2015;94:142-155. [37] YAN Z, CHEN W, JIN W, et al. An interference screw made using a silk fibroin-based bulk material with high content of hydroxyapatite for anterior cruciate ligament reconstruction in a rabbit model. J Mater Chem B. 2021;9(26):5352-5364. [38] SHEN XZ, QU F, LI CB, et al. Comparison between a novel human cortical bone screw and bioabsorbable interference screw for graft fixation of ACL reconstruction. Eur Rev Med Pharmacol Sci. 2018;22(1 Suppl):111-118. [39] LIND M, NIELSEN T, SØRENSEN OG, et al. Bone ingrowth into open architecture PEEK interference screw after ACL reconstruction. J Exp Orthop. 2020;7(1):68. [40] SHUMBORSKI S, HEATH E, SALMON LJ, et al. A Randomized Controlled Trial of PEEK Versus Titanium Interference Screws for Anterior Cruciate Ligament Reconstruction With 2-Year Follow-up. Am J Sports Med. 2019;47(10):2386-2393. [41] MAU JR, HAWKINS KM, WOO SL, et al. Design of a new magnesium-based anterior cruciate ligament interference screw using finite element analysis. J Orthop Translat. 2019;20:25-30. [42] BAYDOUN H, ENGLER ID, HOSSEINI A, et al. Stacked Biocomposite Screws in a Single-Stage Revision Anterior Cruciate Ligament Reconstruction Has Acceptable Fixation Strength in a Porcine Cadaveric Model. Am J Sports Med. 2021;49(8): 2144-2149. [43] HEXTER AT, HING KA, HADDAD FS, et al. Decellularized porcine xenograft for anterior cruciate ligament reconstruction: A histological study in sheep comparing cross-pin and cortical suspensory femoral fixation. Bone Joint Res. 2020;9(6): 293-301. [44] PUTNIS SE, OSHIMA T, KLASAN A, et al. Adjustable suspension versus hybrid fixation in hamstring autograft anterior cruciate ligament reconstruction. Knee. 2021;28:1-8. [45] HE X, LI Y, GUO J, et al. Biomaterials developed for facilitating healing outcome after anterior cruciate ligament reconstruction: Efficacy, surgical protocols, and assessments using preclinical animal models. Biomaterials. 2021;269:120625. [46] ZUK PA, ZHU M, ASHJIAN P, et al. Human adipose tissue is a source of multipotent stem cells. Mol Biol Cell. 2002;13(12):4279-4295,. [47] SUN Y, CHEN W, HAO Y, et al. Stem Cell-Conditioned Medium Promotes Graft Remodeling of Midsubstance and Intratunnel Incorporation After Anterior Cruciate Ligament Reconstruction in a Rat Model. Am J Sports Med. 2019;47(10): 2327-2337. [48] BI F, CHEN Y, LIU J, et al. Bone Mesenchymal Stem Cells Contribute to Ligament Regeneration and Graft-Bone Healing after Anterior Cruciate Ligament Reconstruction with Silk-Collagen Scaffold. Stem Cells Int. 2021;2021:6697969. [49] LU CC, HO CJ, HUANG HT, et al. Effect of Freshly Isolated Bone Marrow Mononuclear Cells and Cultured Bone Marrow Stromal Cells in Graft Cell Repopulation and Tendon-Bone Healing after Allograft Anterior Cruciate Ligament Reconstruction. Int J Mol Sci. 2021;22(6):2791. [50] 周云烽,宋斌,李卫平.前十字韧带重建术后腱-骨愈合的研究进展[J].中华骨科杂志,2017,37(9):560-568. [51] SETIAWATI R, UTOMO DN, RANTAM FA, et al. Early Graft Tunnel Healing After Anterior Cruciate Ligament Reconstruction With Intratunnel Injection of Bone Marrow Mesenchymal Stem Cells and Vascular Endothelial Growth Factor. Orthop J Sports Med. 2017;5(6):2325967117708548. [52] WANG R, XU B, XU HG. Up-Regulation of TGF-β Promotes Tendon-to-Bone Healing after Anterior Cruciate Ligament Reconstruction using Bone Marrow-Derived Mesenchymal Stem Cells through the TGF-β/MAPK Signaling Pathway in a New Zealand White Rabbit Model. Cell Physiol Biochem. 2017;41(1):213-226. [53] KIM KO, SIM JA, CHOI JU, et al. The effect of interleukin-8 in the early stage after anterior cruciate ligament reconstruction with remnant preservation. Knee Surg Relat Res. 2020;32(1):5. [54] CHEN P, OUYANG J, XIAO J, et al. Co-injection of human adipose stromal cells and rhBMP-2/fibrin gel enhances tendon graft osteointegration in a rabbit anterior cruciate ligament-reconstruction model. Am J Transl Res. 2018;10(2):535-544. [55] LU D, YANG C, ZHANG Z, et al. Enhanced tendon-bone healing with acidic fibroblast growth factor delivered in collagen in a rabbit anterior cruciate ligament reconstruction model. J Orthop Surg Res. 2018;13(1):301. [56] BEZ M, KREMEN TJ, TAWACKOLI W, et al. Ultrasound-Mediated Gene Delivery Enhances Tendon Allograft Integration in Mini-Pig Ligament Reconstruction. Mol Ther. 2018;26(7):1746-1755. [57] XIE X, ZHAO S, WU H, et al. Platelet-rich plasma enhances auto-graft revascularization and reinnervation in a dog model of anteri-or cruciate ligament reconstruction. J Surg Res. 2013;183(1):214-222. [58] ZHANG M, ZHEN J, ZHANG X, et al. Effect of Autologous Platelet-Rich Plasma and Gelatin Sponge for Tendon-to-Bone Healing After Rabbit Anterior Cruciate Ligament Reconstruction. Arthroscopy. 2019;35(5):1486-1497. [59] MILLAN SM, THORN D, FORD E. A Novel Approach to Augmenting Allograft Hamstring Anterior Cruciate Ligament Reconstructions Utilizing a Resorbable Type I Collagen Matrix with Platelet Rich Plasma. Case Rep Orthop. 2021;2021: 5574676. [60] ZHENG H, HUANG W, HE B, et al. Positive effects of platelet-rich plasma (PRP) and a Sanguisorba officinalis polysaccharide on the proliferation and differentiation of anterior cruciate ligament (ACL) fibroblasts in vitro. Pharm Biol. 2020;58(1):297-305. [61] ZHOU Y, ZHANG J, YANG J, et al. Kartogenin with PRP promotes the formation of fibrocartilage zone in the tendon-bone interface. J Tissue Eng Regen Med. 2017;11(12):3445-3456. [62] 廖欣宇,王福科,王国梁.骨组织工程支架的进展与挑战[J].中国组织工程研究,2021,25(28):4553-4560. [63] SALMORIA GV, PEREIRA RV, FREDEL MC, et al. Properties of PLDLA/ bioglass scaffolds produced by selective laser sintering. Polym Bull (Berl). 2017;75(3): 1299-1309. [64] MONDSCHEIN RJ, KANITKAR A, WILLIAMS CB, et al. Polymer structureproperty requirements for stereolithographic 3D printing of soft tissue engineering scaffolds. Biomaterials. 2017;140:170-188. [65] SHEIKH Z, HAMDAN N, IKEDA Y, et al. Natural graft tissues and synthetic biomaterials for periodontal and alveolar bone reconstructive applications: a review. Biomater Res. 2017;21:9. [66] YANG J, DONG Y, WANG J, et al. Hydroxypropylcellulose Coating to Improve Graft-to-Bone Healing for Anterior Cruciate Ligament Reconstruction. ACS Biomater Sci Eng. 2019;5(4):1793-1803. [67] ZHANG P, HAN F, CHEN T, et al. “Swiss roll”-like bioactive hybrid scaffolds for promoting bone tissue ingrowth and tendon-bone healing after anterior cruciate ligament reconstruction. Biomater Sci. 2020;8(3):871-883. [68] JIANG S, LIU X, LIU Y, et al. Synthesis of silver @hydroxyapatite nanoparticles based biocomposite and their assessment for viability of Osseointegration for rabbit knee joint anterior cruciate ligament rehabilitation. J Photochem Photobiol B. 2020;202:111677. [69] HAN F, ZHANG P, CHEN T, et al. A LbL-Assembled Bioactive Coating Modified Nanofibrous Membrane for Rapid Tendon-Bone Healing in ACL Reconstruction. Int J Nanomedicine. 2019;14:9159-9172. [70] PARK SH, CHOI YJ, MOON SW, et al. Three-Dimensional Bio-Printed Scaffold Sleeves With Mesenchymal Stem Cells for Enhancement of Tendon-to-Bone Healing in Anterior Cruciate Ligament Reconstruction Using Soft-Tissue Tendon Graft. Arthroscopy. 2018;34(1):166-179. [71] LIU H, YANG L, ZHANG E, et al. Biomimetic tendon extracellular matrix composite gradient scaffold enhances ligament-to-bone junction reconstruction. Acta Biomater. 2017;56:129-140. [72] FAN J, SUN L, CHEN X, et al. Implementation of a stratified approach and gene immobilization to enhance the osseointegration of a silk-based ligament graft. J Mater Chem B. 2017;5(34):7035-7050. [73] YUNG PS, LEE YW, FU SC, et al. Differential MMP 1 and MMP 13 expression in proliferation and ligamentization phases of graft remodeling in anterior cruciate ligament reconstruction. Connect Tissue Res. 2021:62(6):681-688. [74] NAKAGAWA Y, LEBASCHI AH, WADA S, et al. Duration of postoperative immobilization affects MMP activity at the healing graft-bone interface: Evaluation in a mouse ACL reconstruction model. J Orthop Res. 2019;37(2): 325-334. [75] MA R, SCHÄR M, CHEN T, et al. Effect of Dynamic Changes in Anterior Cruciate Ligament In Situ Graft Force on the Biological Healing Response of the Graft-Tunnel Interface. Am J Sports Med. 2018;46(4):915-923. [76] KIM BK, KIM TW, HWANG CH, Pet al. Analysis of Mechanical Loading after Anatomic Anterior Cruciate Ligament Reconstruction Using Combined Single-Photon Emission Computerized Tomography and Conventional Computerized Tomography. Knee Surg Relat Res. 2019;31(1):37-43. [77] CAMP CL, LEBASCHI A, CONG GT, et al. Timing of Postoperative Mechanical Loading Affects Healing Following Anterior Cruciate Ligament Reconstruction: Analysis in a Murine Model. J Bone Joint Surg Am. 2017;99(16):1382-1391. [78] SONG F, JIANG D, WANG T, et al. Mechanical Loading Improves Tendon-Bone Healing in a Rabbit Anterior Cruciate Ligament Reconstruction Model by Promoting Proliferation and Matrix Formation of Mesenchymal Stem Cells and Tendon Cells. Cell Physiol Biochem. 2017;41(3):875-889. [79] HOEL H, PETTERSEN EM, HØISETH LØ, et al. Lower Extremity Intermittent Negative Pressure for Intermittent Claudication. Follow-Up after 24 Weeks of Treatment. Ann Vasc Surg. 2021;75:253-258. [80] Sun Z, Wang X, Ling M, et al Acceleration of tendon-bone healing of anterior cruciate ligament graft using intermittent negative pressure in rabbits. J Orthop Surg Res. 2017;12(1):60. |
| [1] | Sun Kexin, Zeng Jinshi, Li Jia, Jiang Haiyue, Liu Xia. Mechanical stimulation enhances matrix formation of three-dimensional bioprinted cartilage constructs [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-7. |
| [2] | Zhang Lichuang, Gao Huali, Wang Jingchao, Lin Huijun, Wu Chonggui, Ma Yinghui, Huang Yunfei, Fang Xue, Zhai Weitao. Effect of tendon manipulation with equal emphasis on muscles and bones on accelerating the functional rehabilitation of quadriceps femoris after total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1383-1389. |
| [3] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [4] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [5] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [6] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [7] | Yang Yitian, Wang Lu, Yao Wei, Zhao Bin. Application of the interaction between biological scaffolds and macrophages in bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1071-1079. |
| [8] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [9] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [10] | Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109. |
| [11] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| [12] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [13] | Xu Yan, Li Ping, Lai Chunhua, Zhu Peijun, Yang Shuo, Xu Shulan. Piezoelectric materials for vascularized bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1126-1132. |
| [14] | Liu Guangluan, Guo Zonglei, Ge Jin, Huang Dong, Wang Yehua. Anatomic risk factors for medial meniscus posterior root tears combined with anterior cruciate ligament injuries [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 663-668. |
| [15] | Zhou Yinan, Yang Kun, Jiang Jiayi, Zhang Sizhuo, Zhu Yingwen. The relationship between glucose transporter 1/4 gene polymorphisms and athletic ability [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 745-750. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||