Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (5): 772-778.doi: 10.12307/2023.098
Previous Articles Next Articles
Construction and application of myocardial ischemia model in miniature pigs
Song Jian1, Zhao Lei2, Liu Aishi2
- 1Inner Mongolia Medical University, Hohhot 010000, Inner Mongolia Autonomous Region, China; 2Department of Imaging Diagnostics, Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010000, Inner Mongolia Autonomous Region, China
-
Received:2022-01-07Accepted:2022-04-24Online:2023-02-18Published:2022-07-23 -
Contact:Liu Aishi, MD, Chief physician, Professor, Master’s supervisor, Department of Imaging Diagnostics, Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010000, Inner Mongolia Autonomous Region, China -
About author:Song Jian, Master candidate, Inner Mongolia Medical University, Hohhot 010000, Inner Mongolia Autonomous Region, China -
Supported by:the Key Technology Research Project of Inner Mongolia Autonomous Region, No. 2019GG070 (to LAS)
CLC Number:
Cite this article
Song Jian, Zhao Lei, Liu Aishi. Construction and application of myocardial ischemia model in miniature pigs[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 772-778.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 用于构建心肌缺血模型的小型猪品系 如今国内外拥有丰富的小型猪资源,中国主要用于造模的有巴马小型猪、五指山小型猪、中国农大小型猪以及贵州小型香猪等,这些猪的普遍优势在于遗传稳定、产仔率高、体型小且易于饲养;国外的主要有尤卡坦小型猪、Obbassaw小型猪和哥廷根小型猪等[9-10]。 2.1.1 中国小型猪品种 五指山小型猪:产于海南省中部少数民族山区,由于长期的近亲交配繁殖,使其主要的特征如体毛、外貌稳定地遗传了下来。该猪体型小、能够稳定遗传、抗逆性强且易饲养。并且其心脏的解剖特点与位置以及常规的生理生化指标与人类相似[11],但五指山小型猪对于手术的耐受性较低,易发生室颤导致死亡。 巴马小型猪:是目前最常用于心血管研究的小型猪动物模型,是目前可以获取的最佳品种[9]。经过20多年对于该猪的培育与研究,巴马小型猪已具有其独特的优势:①遗传性稳定,一致性良好;②适于实验的白毛面积大,约占体表面积92%上;③体质量较小;④具有多产性;⑤对饲料营养要求低[12]。 中国农大小型猪:又称为中国实验用小型猪,其中农大Ⅰ系是以贵州从江地区的小型猪为基础培育出的品种,农大Ⅱ系小型猪是在中国农大Ⅰ系的基础上,与北京地区的黑猪进行杂交,增强了其抗寒、抗病能力[13]。使得其对手术耐受度高,死亡率降低。 贵州小型香猪:经过专家的不断研究,积累了大量的数据,充分肯定了贵州小型香猪的动物实验化的价值,认为贵州小型香猪具有体型小、早熟、产仔率高、性情温顺等优点[14]。 除了以上几种小型猪外,还有藏猪、版纳小型猪,具有抗病力强的特点,但由于培育地点特殊,所以较少用于造模研究。 2.1.2 国外小型猪品种 Obbassaw小型猪:由原欧洲品种的猪经过长时间的地理隔离培育出的品种,有强大的储存脂肪的能力,由于该品种对于高脂饮食的心血管代谢以及对于调节血脂药物的反应与人类相似,多可作为动物模型用于动脉粥样硬化所致慢性冠脉阻塞引起的心肌缺血的研究[15]。 哥廷根小型猪:该品种是德国哥廷根大学通过“三品系”杂交,经过十几年培育形成的品种。该品系体型小、易于繁殖、对饲料要求低。12月龄平均体质量30-35 kg,成年猪(24月龄)平均体质量40-60 kg[13]。 尤卡坦(yucatan)小型猪:美国科罗拉多州立大学于墨西哥的尤卡坦半岛通过野猪杂交培育出的品种。该品种主要用于糖尿病研究,体表无毛。 2.2 心肌缺血小型猪模型构建与应用 2.2.1 急性心肌缺血模型构建方法 此类模型主要适用于研究急性冠状动脉闭塞引起的急性心绞痛和急性心肌梗死,可以模拟临床上急性冠脉综合征的病理过程,为研究急性冠脉综合征病理生理机制、治疗方法提供了极大帮助。这类模型的构建方法主要包括开胸手术法、闭胸手术法、药物法和微电流刺激法[16]。 开胸手术法:分为冠状动脉结扎法和冠状动脉夹闭法。就是通过物理阻断的方法让冠状动脉闭塞,导致急性心肌缺血[17]。开胸手术法的优点在于可以精确阻塞靶血管造成局部心肌梗死。由于此方法为创伤性造模方法,因此缺点有:①对术者的手术娴熟度要求高,并且由于容易引起致死性心律失常,死亡率较高;②由于术中的有创操作对于心肌的损伤,因此心肌酶学指标明显升高,并且较长时间处于高水平,与临床上心肌梗死患者心肌酶衍变规律不相符[18]。 (1)冠状动脉结扎法:通过手术结扎靶血管的方式,达到阻断血流致使心肌急性缺血的目的。MORRISON等[19]在术前麻醉后对小型猪进行开胸,切开心包露出心脏,左冠状动脉前降支被隔离到第二对角分支的远端,并在其下通过1 mm的硅血管环;将血管环的末端穿过一小段硬管,拉紧,用镊子握住,以停止冠状动脉血流。造模手术后利用心电图和目测的方法对造模成功与否进行评价,若目测心肌颜色变暗,心电图示Ⅱ导联、ST段下移及T波倒置,则证明模型构建成功。对于小型猪,研究者认为模型构建时左前降支结扎的部位是位于距终末端1/3处或1/3稍高处,可以明显减少致死性室性心律失常的发生[20-21]。 而结扎法由于手术创伤大,动物死亡率高,所以不利于药物治疗方法的研究,因此,有研究通过按Harris两步结扎法用6.0 prolene缝线就近结扎左前降支冠状动脉来降低造模死亡率,第一步预结扎靶血管,不完全阻断血流,达到缺血预适应的目的,此外还可在术中滴注硝酸甘油或在血管分离前推注利多卡因预防,观察有无致死性心律失常,如果有异常,立即进行抢救,成功后进行正式的第二步结扎,这种方法构建的急性心肌缺血模型成功率高[22]。虽然结扎法创伤性大,动物死亡率高,术后动物的各项指标例如心肌酶谱与真实的急性心肌梗死有差异,但是由于临床上手术操作成熟,目前仍然是临床上研究急性心肌梗死的最常见动物造模方法。 (2)冠状动脉夹闭法:夹闭法原理与结扎法相同,步骤类似,主要的区别就在于将无创缝合线替换成无创动脉夹。相较于结扎法,夹闭法的创伤性较小,且此方法较结扎法更易用于心肌缺血再灌注损伤研究,吴隐雄[23]认为结扎法造模时要将结扎线穿过冠状动脉,分离深度比较大,因此易损伤间隔支,并且结扎线结扎动脉时易损伤血管内膜,影响再灌注血流。但是采用夹闭法仅需分离冠状动脉两侧,不需分离冠脉底部,因此不易损伤间隔支,用动脉夹闭塞动脉即可阻断血流造成急性缺血, 松开动脉钳则可使血管再通,不易损伤血管内膜,且并发症少,有利于血管再通,故此方法优于结扎法。 闭胸手术法:随着介入技术的逐渐成熟,闭胸手术法造模越来越常见。目前常规的方法主要有球囊栓塞法及血栓栓塞法,这个方法的优点在于创伤小、动物存活率高、可重复进行冠状动脉造影以及技术要求相对较低[24],而用血栓法造模,由于可以再通,因此还可以用于研究冠状动脉栓塞后的心肌缺血再灌注以及观察溶栓药物的药效及药理特点,并且中国实验小型猪冠脉形态类似于人类,冠状动脉口径较大,可从容地实施介入操作,因此闭胸手术法可认为是小型猪急性心肌缺血模型的最优方法。而闭胸手术法的缺点是对于模型梗死面积的可控性低,容易超出预估梗死面积。 (1)球囊栓塞法:此造模方法在对小型猪进行麻醉后,需要进行分离颈总动脉或股动脉、注入抗凝剂、冠状动脉造影确定栓塞位置、置入球囊阻断冠脉血流、经冠状动脉造影确定血流终止、结扎颈总动脉、拔出导管、缝合创口、消毒等步骤,无需开胸,是一个相对简单的过程,因此动物术后恢复时间显著缩短,成活率明显提高[24]。KONDO等[25]用6F导引管确定栓塞位置,并在给予硝酸甘油(0.2 mg)后评估冠状动脉大小,将球囊管置入第一对角支远端,气球充气,以6-8 atm的速度封闭左前降支45 min,利用冠状动脉造影观察靶血管阻塞情况。该方法术中通过监测血压、动态心电图判断是否发生致死性心律失常,术后再通过注入对比剂和心电图评价造模是否成功。栓塞过程中由于造模方法的不可控性易出现大范围心肌梗死和致死性心率失常,因此可在操作前给予利多卡因预防室颤,若在栓塞过程中出现室颤,可静脉缓慢给予利多卡因[26]。 (2)血栓栓塞法:急性缺血性心脏病的主要原因就是冠状动脉血栓形成,通过股动脉穿刺置入导管后,诱导血栓形成或者注入自体血栓来造模,可以很大程度上模拟这一病理过程。这一方法主要分为异物血栓法和自体血栓法,前者常使用明胶海绵充当异物阻塞血管,REFFELMANN等[27]在为动物麻醉后经颈总动脉注入抗凝剂,将造影导管插入左冠状动脉主干行冠状动脉造影, 造影成功后经微导管注入手术缝线或细颗粒状明胶海绵,经冠状动脉造影确定造模是否成功。而相较于异物血栓,自体血栓更加符合急性缺血性心脏病的病理过程,LIU等[28]在给小型猪注射戊巴比妥麻醉、分离右侧颈总动脉后,向动脉鞘管内注入抗凝剂,将指引导管置于左冠状动脉开口行冠状动脉造影,造影后将导管置入冠状动脉,通过导管注入自体血栓。此方法手术前后进行冠状动脉造影观察栓塞情况,术后通过胸外心电图来评价造模情况,当心电图示ST段升高大于0.8时,则造模成功。有研究认为血栓栓塞法与动物有很好的同源性,不会发生排斥反应,并且可以通过溶栓药达到再通,因此这个方法不仅可以研究抗心肌缺血药物的药效,还可用于观察溶栓药物的作用特点及药效。 药物干预法:药物法造模是通过强缩血管药物诱导冠状动脉血管收缩、痉挛,引起急性心肌缺血,常使用异丙肾上腺素以及垂体后叶素。评价此方法造模是否成功是通过观察模型组心电图ST-T段与对照组差异大小,若差异显著,则造模成功。异丙肾上腺素为β受体激动剂,能持续刺激β-肾上腺素能受体致心肌收缩增强以及冠状动脉痉挛,并产生大量氧自由基,损伤心肌细胞,最终导致急性心肌梗死[29-30]。 垂体后叶素中含有血管加压素的成分,可使冠状动脉收缩痉挛,造成心肌供血不足;其次,还可以使全身小血管收缩,让外周阻力增加,增强心脏后负荷,进一步加重心肌缺血[31]。目前报道显示,药物造模法多用于大鼠的心肌缺血模型构建,较少用于小型猪。药物法造模的优点是造模简便,维持时间长,可以广泛用于抗心肌缺血药物的研究。 微电流刺激法:目前急性缺血性心脏病动脉模型的构建方法中,应用最广泛的就是冠状动脉结扎法,但是这个方法手术操作难度极大,并且结扎耗时长、易出血,容易造成实验动物的死亡。而电刺激法成功弥补了这些缺点,原理就是使用微电流刺激冠状动脉血管外膜处诱使急性血栓形成或急性血管闭塞[18]。PATEL等[32]将左冠状动脉前降支充分暴露后,将小高频刀的电灼电极置于左冠状动脉前降支深部电凝;手术后通过观测心电图的变化,若在2个以上肢体导联出现ST段上抬或者肉眼观手术区域心肌颜色变灰白,证实模型构建成功。此造模方法操作方便,手术时间短,对于靶血管能够做到精确定位,真实模拟了急性冠脉综合征后的瘢痕组织,可以创造出凝固性坏死的组织,并最终以与冠状动脉梗死相同的方式进行重塑。涉及促进坏死周围肌肉的血管生成和新生血管的研究,以及受损心肌中干细胞的接受性,都可以用此可重现的模型来进行。并且术后的并发症少、效果可靠。 国内外的研究显示药物法和微电流刺激法多是使用大鼠、家兔、犬等动物来构建急性心肌缺血模型,但是,由于小型猪体型大小、代谢等因素不同的影响,因此药物法和微电流法造模的可行性尚待进一步研究。 急性心肌缺血模型构建方法优缺点对比,见表1。 "


2.2.2 慢性心肌缺血小型猪模型构建方法 此类模型主要适用于冠状动脉慢性阻塞以及微循环障碍导致血流动力学障碍引起的慢性心肌缺血的研究,这类模型可以更好地模拟如今高脂高盐饮食以及不健康生活习惯导致的冠状动脉病变引起的慢性缺血性心脏病的病理过程,具有极大研究干预措施和改善预后的价值。目前造模方法有冠状动脉内膜增殖法、冠状动脉外慢性收缩法、微循环栓塞法、高脂饮食法、次全结扎法等。 冠状动脉外慢性收缩法:目前外源性压迫是使用Ameroid环,这是一种圆柱形装置,由酪蛋白(一种吸湿性物质,在吸收液体时缓慢膨胀)的内环组成,周围环绕着金属护套。随着酪蛋白层的扩张,它会造成渐进性的外部压迫,直到血管管腔完全消失[33],造成慢性的心肌缺血。VAN HOUTEN等[34]将左回旋支冠状动脉从心肌中剥离,放置Ameroid环。在术后3-5周行冠状动脉造影,观察狭窄情况及侧支形成情况,若证实狭窄或者形成侧支循环,证明成功构建慢性闭塞模型。有研究表明,左前降支虽然在手术中容易找到,但由于左前降支与心肌组织连接紧密,没有放置Ameroid环的间隙,而左回旋支近段血管间隙大、分支少,利于血管分离,因此,适于Ameroid环的放置[35]。FALLAVOLLITA等[36]通过将Ameroid缩窄环套于冠状动脉血管外构建慢性心肌缺血模型研究发现,在猪左冠状动脉前降支慢性闭塞3个月后,支配区域心肌出现节段性收缩功能减低、血流灌注量减少,注入肾上腺素后,缺血心肌收缩功能与血流灌注出现增加,说明此模型构建方法虽然会引起心肌缺血,但仍然具备增加心肌代谢而不诱发急性缺血性心脏病的能力。 这个方法由于在技术上存在较小的挑战性,因此有成功率高、动物致死率低、重复性好的优点,缺点就是容易加重血管狭窄的程度,对于实验结果的控制性较低[37],并且因为破坏了血管壁的自然结构,造模后无法引起临床上慢性血管阻塞导致的局部血管舒缩性改变。 冠状动脉内膜增殖法:其机制是通过球囊机械性损伤冠状动脉血管内皮,使血管内弹力膜破裂,导致平滑肌细胞移行增殖以及脂质沉积,大量泡沫细胞和淋巴细胞聚集,形成粥样硬化斑块,致管腔狭窄[38];于震[39]通过导管行冠状动脉造影后,置入球囊至左前降支中部,给球囊充气3次后损伤血管内皮,在术后几周后通过冠状动脉脉造影看到斑块明显,管腔狭窄,则证实成功构建慢性狭窄的模型。该方法优点是容易操作,可以精确定位,使管腔狭窄;但是对于狭窄程度的控制比较有限,并且形成的斑块易于脱落形成血栓,导致造模失败。由于内皮损伤以及高脂血症相互促进会加快粥样斑块形成的进程,因此,当造模过程中对小型猪加以高脂饲料的喂养,可以明显提高造模成功率。 微循环栓塞法:该方法的原理就是通过物理栓塞、破坏微血管内皮导致微循环障碍,导致远端心肌缺血,达到造模的目的,注射微栓塞物后,将生理盐水缓慢注射到左前降支远段,并观察心尖搏动及静脉回流情况,当心尖搏动减弱及TIMI血流分级≤2级时证实冠状动脉微循环障碍建模成功,目前常用的有机械性栓塞和化学损伤性栓塞两种[40]。 (1)机械性栓塞:主要通过微导管向冠状动脉内注入栓塞物,堵塞微血管,引发微循环障碍。该方法主要是向冠状动脉内注射微栓塞球或自体微血栓[41]。前者是向靶血管内注入微球混合液,KITAGAWA等[42]取直径20 μm的单分散聚苯乙烯微球原液与非离子对比剂碘海醇充分混合,通过微导管在左前降支或回旋支远端释放微球混合液。这个方法微创、操作简便以及动物存活率高,并且微球与心肌流动特性有良好的相关性。但是由于微球属于化学惰性材料,无法引起微血管的收缩和凝血反应,且不易被纤溶物质溶解,不适用于微血管阻塞后溶栓药临床疗效和血管再通研究[43]。 临床上机械性阻塞微血管的栓子主要是由凝固的血液和动脉粥样硬化斑块碎片组成,除了物理阻塞,栓子的生物成分还通过启动和增强血栓形成、炎症和血管收缩反应引起微循环障碍,因此也通过体外制备微血栓作为栓子,通过微导管注入冠状动脉来构建微循环障碍模型[44]。但是,由于将栓子冲洗到靶血管的力过大,导致逆行血流,容易将栓子注入到非目标血管,导致非靶点缺血梗死。导管操作也可能导致血管痉挛,这也会进一步增加了回流的风险[45],因此BIKOU等[44]对实验方案做出改进,先将球囊管送入左前降支,充气后阻塞左前降支然后将血栓通过球囊管腔注入,同时保持冠状动脉球囊的充气。这使得能够在球囊阻塞的左前降支远端进行定向输送,并防止血栓回流到非靶区。 (2)化学损伤性栓塞法:此法是通过药物破坏微血管内皮,诱导血小板聚集形成血栓,堵塞微血管。目前最常使用的药物是月桂酸钠。月桂酸钠作为血管内皮损伤的诱发物,使血管的完整性受损,内皮下基质暴露,诱发凝血,最终导致原位血栓的形成,因此其常用来构建外周动脉血栓栓塞模型,研究抗血栓药物和抗血小板药物的疗效和机制,由于月桂酸钠的强内皮损伤作用,可造成血管内皮的脱落及穿孔[46]。叶明芳等[47]把动物麻醉、气管插管后,于第二肋间做横切口切开心包暴露主动脉根部,将细针刺入主动脉根部,同时用血管钳夹闭升主动脉后,向主动脉根部注入月桂酸钠,数秒后松开升主动脉,关胸复苏。研究发现,使用月桂酸钠构建微循环栓塞模型可以造成心肌局灶性低氧,而且此实验方法成本低,可以模拟内皮受损后血栓形成和动脉粥样硬化的病理过程,因此也可用于抗血栓药物的研究。 高脂饮食法:目前导致中国人群缺血性心脏病最常见的就是高脂饮食引起的冠状动脉粥样硬化性心脏病,粥样斑块进行性增厚阻塞血管或者斑块破裂血小板聚集后血栓形成阻塞血管,引起心肌缺血甚至心肌梗死。高脂饮食法就是利用此原理进行造模[48],此方法最大的优点就在于可以极大地模拟临床上冠状动脉粥样硬化性心脏病的病理过程,但是此方法造模时间长、成本高,并且由于个体差异,很可能会导致冠状动脉狭窄程度的不可控,结局不可预见,所以常与球囊拉伤法一同使用。刘建勋等[49]在构建这种模型时使用的高脂饲料就是在普通饲料的基础上添加胆固醇、胆盐及猪油等,然后通过导管置入球囊导丝,充气扩张球囊3次封堵左前降支,并同时拉动球囊5次,2个月后,通过冠状动脉造影显示左前降支管径纤细,造模成功。高脂饮食法相较于其他造模方法,是最接近现如今人们患缺血性心脏病病理过程的方法,并且与侵入性手术和介入等有创的方法比,这是无创的方法,不会引起机体的应激,影响真实的实验结果,并可以减少动物的死亡率。 次全结扎法:部分研究表明,将靶血管的部分管腔结扎的次全结扎法是具有可行性的。侯洁等[50]在巴马小型猪上通过这个方法成功构建了慢性心肌缺血模型,在对猪进行麻醉、开胸以及左前降支的游离后先用弹力阻断线悬吊左前降支,观察心肌变化,若未发生急性心肌缺血或梗死,用结扎线在悬吊处将血管与留置针结扎起来,成功后将留置针缓慢抽出。术后数周行多次冠状动脉CT造影和MRI检查,若发现冠脉的慢性不完全梗阻,则证明造模成功。在开胸下的次全结扎法较其他方法的优点是对于狭窄程度的可控性高、结果的可预见性好,但是,此方法的缺点就是需要开胸手术,创伤大。 慢性心肌缺血模型构建方法优缺点对比,见表2。 "

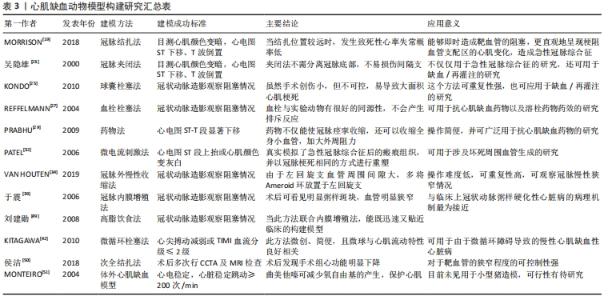
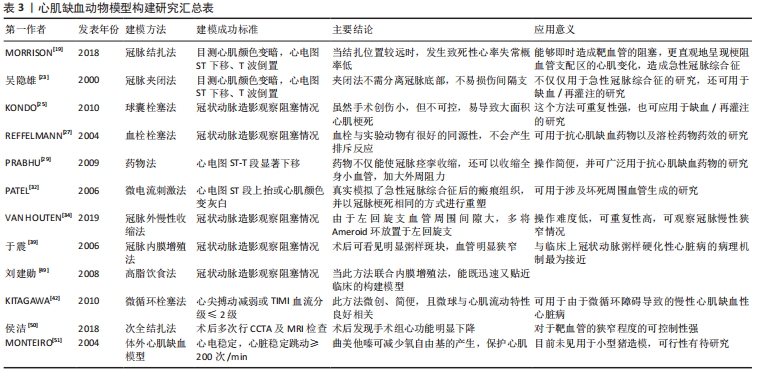
2.2.3 体外心肌缺血动物模型构建方法 体外心肌缺血模型主要用于心肌缺血/再灌注损伤、心肌细胞治疗以及移植心脏保存的研究,并取得了极大的进展。该模型构建是通过Langendorff灌注系统完成,灌流液经冠状动脉入口进入冠状血管营养心脏,达到维持心脏节律性活动的目的,当关闭灌流管时使得心脏缺血,不同时间后再恢复供血,从而研究心肌缺血/再灌注损伤[51],当体外模型在实验过程中心电稳定,心脏跳动保持大于200次/min,未出现持续室性心律失常,甚至心脏停跳的情况,心脏灌注稳定,则证实模型构建成功。高琴等[52]采用体外大鼠心脏灌流方法制作体外模型,通过结扎冠状动脉左前降支30 min模拟心肌缺血,随后松开结扎线恢复灌注120 min,以此来观察心肌缺血/再灌注后心脏各方面的指标;MONTEIRO等[51]通过体外心肌缺血模型发现曲美他嗪对氧化系统(主要对复合物Ⅰ)有优先作用,磷酸化后酶活性增加,O2消耗减少,可以减少氧自由基的产生,增加线粒体的完整性。这些结果使研究者能够更好地了解曲美他嗪对心肌细胞的保护作用。体外模型可以完全排除机体自身代谢对于心肌缺血后的影响,很直观地反映出了心肌细胞的耗氧情况,并且易于控制灌注流量、给药的剂量及浓度。但是,研究表明此模型多用于大鼠,并未见使用小型猪构建相关模型,仍需进一步的研究造模方法应用的可行性。 作者总结了2000-2020年有关心肌缺血动物模型构建方法的文章,见表3。 "
| [1] 王传池,吴珊,江丽杰,等.1990-2020年我国冠心病中医证的流行病学调查研究概况[J].中国中医基础医学杂志,2020,26(12):1883-1893. [2] 胡盛寿,高润霖,刘力生,等.《中国心血管病报告2018》概要[J].中国循环杂志,2019,34(3):209-220. [3] 卜军,陈章炜,崔晓通,等.中国成人代谢异常与心血管疾病防治[J].上海医学,2020,43(3):129-164. [4] JENSEN RV, HJORTBAK MV, BØTKER HE. Ischemic heart disease: an update. Semin Nucl Med. 2020;50(3):195-207. [5] SOROP O, VAN DE WOUW J, CHANDLER S, et al. Experimental animal models of coronary microvascular dysfunction. Cardiovasc Res. 2020; 116(4):756-770. [6] LUNNEY JK. Advances in swine biomedical model genomics. Int J Biol Sci. 2007;3(3):179-184. [7] GÓMEZ FA, BALLESTEROS LE. Morphologic expression of the left coronary artery in pigs: an approach in relation to human heart. Rev Bras Cir Cardiovasc. 2014;29(2):214-220. [8] 北京农业大学实验动物研究所.中国实验用小型猪的培育、开发与应用[J].中国实验动物学杂志,1991(1):15-19. [9] 王达洋,王显.小型猪动脉粥样硬化模型研究进展[J].中国实验动物学报,2020,28(3):410-415. [10] 石兴勇,王吉,陈斌.我国实验小型猪的发展现状及展望[J].中国实验动物学报,2019,27(1):104-109. [11] 田玉龙,钟红珊.五指山小型猪在心血管系统疾病建模中的应用[J].介入放射学杂志,2016,25(4):363-366. [12] 庞琳琳,张会永,杨关林.巴马小型猪在医学研究中的应用进展[J].中国实验动物学报,2014,22(1):94-98. [13] 王超凡,杨关林.小型猪动脉粥样硬化模型研究进展[J].辽宁中医药大学学报,2014,16(5):69-71. [14] 健生.贵州小型香猪实验动物化研究成果通过鉴定[J].上海实验动物科学,1987(4):264. [15] MATTHAN NR, SOLANO-AGUILAR G, MENG H, et al. The ossabaw pig is a suitable translational model to evaluate dietary patterns and coronary artery disease risk. J Nutr. 2018;148(4):542-551. [16] MITSOS S, KATSANOS K, DOUGENI E, et al. A critical appraisal of open- and closed-chest models of experimental myocardial ischemia. Lab Anim (NY). 2009;38(5):167-177. [17] CHIMENTI S, CARLO E, MASSON S, et al. Myocardial infarction: animal models. Methods Mol Med. 2004;98:217-226. [18] 付瑜,姜树民.建立急性冠状动脉综合征动物模型的研究[J].中华中医药学刊,2007,25(1):105-107. [19] MORRISON ML, IWATA A, KEYES CC, et al. Iodide improves outcome after acute myocardial infarction in rats and pigs. Crit Care Med. 2018; 46(11):e1063-e1069. [20] 肖践明,张敏,王中明,等.猪心肌梗死模型的建立[J].云南医药, 2001,22(2):82-84,166. [21] CHOY JS, SVENDSEN M, LU X, et al. Selective autoretroperfusion preserves myocardial function during coronary artery ligation in swine, Acute Card Care. 2011;13(2):99-108. [22] MU YL, XIE YY, WANG FW, et al. Protective Effect of Methylamine Irisolidone, a Novel Compound, on Acute Myocardial Ischemia in Anesthetized Dogs. J Food Drug Analysis. 2009;17(1):11-16. [23] 吴隐雄.用钳夹法制作心肌缺血再灌注损伤模型的研究[J].广西医学,2000,22(3):429-430. [24] OHTSUKA S, ISHIKAWA K, SUZUKI S, et al. A porcine model of ischemic heart failure produced by chronic placement of a tube in a coronary artery. Eur J Heart Fail. 2003;5(5):591-598. [25] KONDO K, SHIBATA R, UNNO K, et al. Impact of a single intracoronary administration of adiponectin on myocardial ischemia/reperfusion injury in a pig model. Circ Cardiovasc Interv. 2010;3(2):166-173. [26] KROMBACH GA, KINZEL S, MAHNKEN AH, et al. Minimally invasive close-chest method for creating reperfused or occlusive myocardial infarction in swine. Invest Radiol. 2005;40(1):14-18. [27] REFFELMANN T, SENSEBAT O, BIRNBAUM Y, et al. A novel minimal-invasive model of chronic myocardial infarction in swine. Coron Artery Dis. 2004;15(1):7-12. [28] LIU JX, YU Z, LI XZ. Effects of shuangshen ningxin capsule on mini-porcine myocardial ischemia model induced by thrombosis via cardiac catheterization intervention. Zhongguo Zhong Xi Yi Jie He Za Zhi. 2006;26(8):728-731. [29] PRABHU S, NARAYAN S, DEVI CS. Mechanism of protective action of mangiferin on suppression of inflammatory response and lysosomal instability in rat model of myocardial infarction. Phytother Res. 2009; 23(6):756-760. [30] Garg M, Khanna D, Exploration of pharmacological interventions to prevent isoproterenol-induced myocardial infarction in experimental models. Ther Adv Cardiovasc Dis. 2014;8(4):155-169. [31] FU XC, WANG X, ZHENG H, et al. Protective effects of orientin on myocardial ischemia and hypoxia in animal models, Nan Fang Yi Ke Da Xue Xue Bao. 2007;27(8):1173-1175. [32] PATEL MK, FACTOR SM, WANG J, et al. Limited myocardial muscle necrosis model allowing for evaluation of angiogenic treatment modalities. J Reconstr Microsurg. 2006;22(8):611-615. [33] ALLAHWALA UK, WEAVER J, BHINDI R, Animal chronic total occlusion models: a review of the current literature and future goals. Thromb Res. 2019;177:83-90. [34] VAN HOUTEN M, YANG Y, HAUSER A, et al. Adenosine stress CMR perfusion imaging of the temporal evolution of perfusion defects in a porcine model of progressive obstructive coronary artery occlusion. NMR Biomed. 2019;32(11):e4136. [35] IKONEN TS, PÄTILÄ T, VIRTANEN K, et al. Ligation of ameroid-stenosed coronary artery leads to reproducible myocardial infarction--a pilot study in a porcine model. J Surg Res. 2007;142(1):195-201. [36] FALLAVOLLITA JA, CANTY JM JR, Ischemic cardiomyopathy in pigs with two-vessel occlusion and viable, chronically dysfunctional myocardium. Am J Physiol Heart Circ Physiol. 2002;282(4):H1370-H1379. [37] CAO X, NAKAMURA Y, AOKI T, et al. Coronary artery vasospasms in a microminipig occurred after placing an ameroid constrictor. J Vet Med Sci. 2016;78(7):1213-1216. [38] 梅卫义,杜志民,胡承恒,等.球囊损伤和早期动脉粥样硬化猪冠状动脉妊娠相关血浆蛋白A和诱导型一氧化氮合酶的表达[J].中国病理生理杂志,2009,25(9):1848-1852. [39] 于震.血栓性心肌缺血模型的建立及双参宁心胶囊的干预作用[D],北京:中国中医科学院,2006. [40] SU LS, WANG XL, MAO JY. Establishment and evaluation on the animal models with coronary microcirculation dysfunction. Zhongguo Yi Xue Ke Xue Yuan Xue Bao. 2014;36(5):542-545. [41] 籍庆余,高扬,王志强,动态CT心肌灌注成像评价猪冠状动脉微循环障碍模型的实验研究[J].中华放射学杂志,2021,55(2):203-208. [42] KITAGAWA K, GEORGE RT, ARBAB-ZADEH A, et al. Characterization and correction of beam-hardening artifacts during dynamic volume CT assessment of myocardial perfusion. Radiology. 2010;256(1):111-118. [43] HEUSCH G, KLEINBONGARD P, BOSE D, et al. Coronary microembolization: from bedside to bench and back to bedside. Circulation. 2009;120(18):1822-1836. [44] BIKOU O, THARAKAN S, YAMADA KP, et al. A novel large animal model of thrombogenic coronary microembolization. Front Cardiovasc Med. 2019;6:157. [45] VENTE MA, NIJSEN JF, DE WIT TC, et al. Clinical effects of transcatheter hepatic arterial embolization with holmium-166 poly (L-lactic acid) microspheres in healthy pigs. Eur J Nucl Med Mol Imaging. 2008;35(7): 1259-1271. [46] TOSHIMA Y, SATOH S, IKEGAKI I, et al. A new model of cerebral microthrombosis in rats and the neuroprotective effect of a Rho-kinase inhibitor. Stroke. 2000;31(9):2245-2250. [47] 叶明芳,陈良龙,陈丹,等.大鼠冠状动脉微血栓模型[J].福建医科大学学报,2003,37(1):58-59,128. [48] 陈民利,潘永明,陈亮,等.小型猪慢性心肌缺血模型的建立与无创遥测技术的应用[J].中国比较医学杂志,2017,27(5):16-18, [49] 刘建勋,于震,李欣志,高脂饲料加球囊拉伤制备小型猪慢性心肌缺血模型的研究[J].中药药理与临床,2008,24(3):108-111, [50] 侯洁,肖俊睿,孙玉,等.次全结扎冠状动脉法构建巴马小型猪心肌缺血模型[J].中国介入影像与治疗学,2018,15(9):561-565. [51] MONTEIRO P, DUARTE AI, GONÇALVES LM, et al. Protective effect of trimetazidine on myocardial mitochondrial function in an ex-vivo model of global myocardial ischemia. Eur J Pharmacol. 2004;503(1-3):123-128. [52] 高琴,姜翠荣,于影,等.线粒体乙醛脱氢酶2在心肌缺血后处理中的作用[J].中国药理学通报,2010,26(8):1088-1092. |
| [1] | Wang Xiaoge, Liu Jiwen, Yang Shuai, Bao Jinyu, Li Cui. Effects of exercise on depression-like behaviors in chronic unpredictable mild stress rodent models: a systematic review and Meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 813-820. |
| [2] | Tan Xinfang, Guo Yanxing, Qin Xiaofei, Zhang Binqing, Zhao Dongliang, Pan Kunkun, Li Yuzhuo, Chen Haoyu. Effect of uniaxial fatigue exercise on patellofemoral cartilage injury in a rabbit [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-6. |
| [3] | Wang Baojuan, Zheng Shuguang, Zhang Qi, Li Tianyang. Miao medicine fumigation can delay extracellular matrix destruction in a rabbit model of knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1180-1186. |
| [4] | Lü Yiyan, Li Hanbing, Ma Xiaoqing, Zhang Han, Zhang Yuhang, Li Genlin. Establishment and characteristic analysis of interior heat and diabetes mouse model using compound factors [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1187-1193. |
| [5] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [6] | Wang Xinmin, Liu Fei, Xu Jie, Bai Yuxi, Lü Jian. Core decompression combined with dental pulp stem cells in the treatment of steroid-associated femoral head necrosis in rabbits [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1074-1079. |
| [7] | Feng Jianbo, Li Chencheng, Liu Jinyue, Wang Xiaomin, Peng Jiachen. Implantation of Kirschner wire with Staphylococcus aureus biofilm establishes a traumatic osteomyelitis model in rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 700-705. |
| [8] | Wang Shihui, Cheng Yang, Zhu Yunjie, Cheng Shaodan, Mao Jianying. Effect of arc edge needle-scalpel therapy on inflammatory factors and histomorphology of the frozen shoulder in rabbit models [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 706-711. |
| [9] | Huang Fan, Di Anqi, Qiu Mingwang, Huang Chuyu, Li Xiaohui, Zhao Siyi, Fan Zhiyong, Wu Shan. Establishing a rat model of intervertebral disc degeneration using X-ray guidance [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(35): 5652-5657. |
| [10] | Gong Yubo, Shi Yuanyuan, Li Yuanchao, Lu Wenjun, Xia Liping, Guo Xiaohua, Luo Ling, Wu Wei. Establishing a mouse model of allergic rhinoconjunctivitis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(32): 5143-5147. |
| [11] | Ma Hailong, Zhao Zhenqun, Liu Wanlin, Sun Jun. Microtubule-associated protein 1 light chain 3 is involved in the occurrence and development of steroid-induced avascular necrosis of the femoral head in a rabbit model [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(32): 5167-5172. |
| [12] | Zhao Lin, Fan Chenxing, Li Kun. Mechanism underlying tanshinone IIA effect on survival and homing ability of myocardial precursor cells under hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(30): 4852-4856. |
| [13] | Liu Ke, Fan Haixia, Wang Hong, Cheng Huanzhi, Geng Haixia. Expression and significance of collagen fiber and matrix metalloproteinase-9 during orthodontic root resorption in rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(27): 4288-4292. |
| [14] | Yang Qian, Zhang Yiou, Jia Lili, Xie Jun, Feng Mali, Li Tingkai. Establishment and disease progression in a rat myocardial infarction model [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(23): 3733-3737. |
| [15] | Su Jianqing, Sun Bo, Ding Yunrong, Liu Guangming, Ji Wei, Jiang Enyu, Yang Jiayu. Preparing a rabbit model of synovitis in knee osteoarthritis based on the “injury-repair-reinjury” method [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(23): 3738-3743. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||