Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (12): 1954-1960.doi: 10.12307/2023.106
Previous Articles Next Articles
Grophene-family nanomaterials in the treatment of periodontal disease: beneficial for osteogenic differentiation and reconstruction of periodontal support tissues
Ren Wenyan, Liu Xue, Wang Yiyu
- School of Stomatology, Jining Medical University, Jining 272067, Shandong Province, China
-
Received:2022-04-05Accepted:2022-05-14Online:2023-04-28Published:2022-07-30 -
Contact:Wang Yiyu, Master, School of Stomatology, Jining Medical University, Jining 272067, Shandong Province, China -
About author:Ren Wenyan, School of Stomatology, Jining Medical University, Jining 272067, Shandong Province, China -
Supported by:Jining Key Research and Development Project, No. 2021YXNS032 (to LX); Student Innovation Training Project of Jining Medical College, No. cx2021131 (to RWY)
CLC Number:
Cite this article
Ren Wenyan, Liu Xue, Wang Yiyu. Grophene-family nanomaterials in the treatment of periodontal disease: beneficial for osteogenic differentiation and reconstruction of periodontal support tissues[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(12): 1954-1960.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
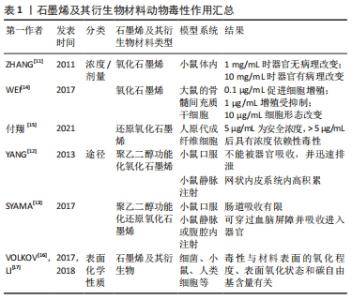
2.1 石墨烯及其衍生物材料的生物性能 良好的生物相容性是植入材料和组织工程支架的基本要求,也是设计和改进新型材料的基础。MUNUERA等[10]将石墨烯纳米薄片与小鼠成纤维细胞共同培养,结果显示石墨烯具有良好的细胞相容性。石墨烯作为植入物与骨组织直接接触,不但不会影响骨结合过程,反而有利于骨细胞的黏附和增殖。虽然石墨烯及其衍生物材料具有相对良好的生物相容性,但仍表现出一定的毒性,为了减少石墨烯及其衍生物对人类健康的不良影响,应评估其生物安全性。 ZHANG等[11]研究了氧化石墨烯在小鼠体内的分布和毒性,发现同样是静脉注射,将1 mg/mL的氧化石墨烯注入小鼠体内14 d后观察体内器官无病理改变;但当质量浓度达到10 mg/mL时则发生了显著的病理学改变,包括炎症细胞浸润、肺水肿及肉芽肿的形成。YANG等[12]发现小鼠口服聚乙二醇功能化氧化石墨烯(GO-PEG),不能被器官吸收,并迅速排泄;而对其静脉注射可发现网状内皮系统(包括肝脏和脾脏)中存在聚乙二醇功能化氧化石墨烯的高积累。SYAMA等[13]研究了聚乙二醇功能化还原纳米石墨烯(RGO-PEG)在白化病小鼠腹腔内和静脉注射后的器官分布、清除和毒性,并对生物分布和血液清除进行了监测,结果表明口服聚乙二醇功能化还原纳米石墨烯肠道吸收有限;10 mg/kg的聚乙二醇功能化还原纳米石墨烯静脉或腹腔内给药可以穿过血脑屏障分布在大脑中,此外,肝脏、肾脏、脾脏和骨髓等器官均有分布。 经过多种研究表明石墨烯及其衍生物对哺乳动物的毒性较低,且其毒性一般是在短期、多量且以溶液的形式直接接触细胞或注射进动物体内时才会表现出来,见表1[11-17]。这与其在牙周组织中应用方式截然不同,其在牙周组织中的作用是一个微量、慢性的过程,目前诸多研究表明,石墨烯及其衍生物在牙周组织中的应用尚未表露出明显的生物安全问题。虽然石墨烯及其衍生物材料对生物体有一定的毒性,但可以采取表面修饰或改性、改变接触途径及控制接触时间等措施来降低毒性,使其能在不损害细胞或生物体的情况下发挥作用。 "
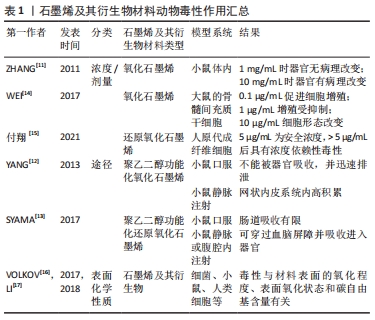
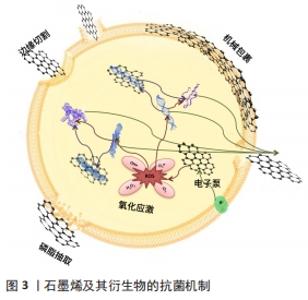
2.2 石墨烯及其衍生物在牙周组织中的应用 目前,石墨烯及其衍生物在牙周组织中的研究主要包含抗菌消炎和引导牙周组织再生2个方面。 2.2.1 石墨烯及其衍生物材料的抗菌性能 牙菌斑是牙周病发生的使动因子,菌斑堆积不仅可以引起牙龈炎,甚至可以进一步导致牙周炎的发生。已有学者对石墨烯及其衍生物的抗菌性能进行过报道,证实了石墨烯及其衍生物对革兰阳性菌和革兰阴性菌均具有较强的抗菌作用,但所采用的细菌模型主要是大肠杆菌或及金黄色葡萄球菌[18-19]。也有学者采用牙周致病菌进行实验,证明石墨烯及其衍生物对于牙周致病菌如伴放线聚集杆菌[20-21]、牙龈卟啉单胞菌等均具有良好的抗菌性能[22]。一方面石墨烯及其衍生物自身具有一定的杀菌抑菌性能,另一方面石墨烯及其衍生物还可作为载体进行载药抗菌。 (1)自身抗菌机制:石墨烯及其衍生物材料所具有的抗菌性能被认为是其物理特性和化学效应协同作用的效果[23],这些物理和化学机制都涉及到石墨烯及其衍生物纳米片穿透细胞膜[24]。与传统的化学抗菌剂使用后会导致机体产生耐药性相比,石墨烯及其衍生物材料不存在耐药性并具有广谱抗菌性。目前被广泛接受的相关抗菌机制有物理破坏学说(边缘切割和机械包裹)、氧化应激学说、磷脂抽取学说,见图3。 "
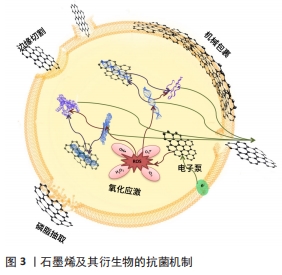
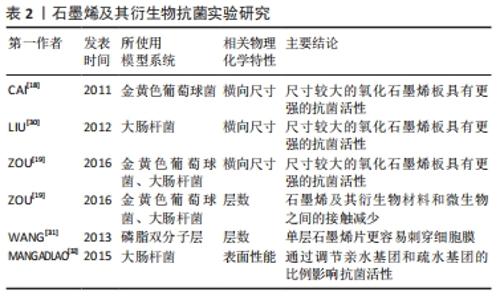
物理破坏学说:①边缘切割学说:通过“穿透模式”,刀片状的石墨烯及其衍生物材料能够刺穿微生物细胞膜,造成细胞内物质泄漏,最终导致细胞死亡。HE等[22]研究了氧化石墨烯纳米片对变形链球菌、牙龈卟啉单胞菌和聚核梭杆菌等常见牙周致病菌的抗菌活性。透射电子显微镜显示氧化石墨烯处理组细胞内密度普遍降低,表明细胞内物质丢失;RNA的流出量测定实验结果也进一步证实了氧化石墨烯对细菌胞膜的破坏作用。石墨烯材料的官能团密度越高、体积越小,与细菌细胞的相互作用机会越大,越容易导致细胞沉积。石墨烯纳米片可以通过破坏细胞膜而引起膜电位降低,导致细胞死亡[25]。②机械包裹学说:石墨烯及其衍生物材料的结构赋予其独特的柔韧性,使其能够充当屏障,将细菌包裹并与周围环境隔离。细菌生存所需的物理化学和营养条件被中断,细菌会逐渐消耗细胞内储存物质,直至死亡。DALLAVALLE等[26]发现石墨烯的包裹性能与尺寸有关,通过研究细菌细胞膜和石墨烯纳米片(尺寸介于0.9-13.3 nm之间)相互作用的模型,证明尺寸大于5.2 nm的石墨烯纳米片能够通过脂质之间强烈的疏水作用部分包裹于细菌表面,最终导致细菌膜受损;而尺寸小于5.2 nm的石墨烯纳米片能够穿透细胞膜而不是将其包裹。石墨烯及其衍生物材料这种独特的包裹性能使其具有显著的抗菌效果。 氧化应激学说:石墨烯及其衍生物材料通过化学途径提高了细胞的氧化应激反应,从而进一步增强了自身抗菌活性[25]。通常,氧化应激通过活性氧依赖性或活性氧非依赖性途径发生,在任何一种情况下,都会破坏细胞功能和机制,导致细胞失活和死亡。活性氧依赖性氧化应激是由细胞内过度累积活性氧引起的,如羟基自由基(OH?)、过氧化氢(H2O2)、单线态分子氧(IO2)和超氧阴离子(O2?-)。这些细胞内积累的活性氧诱导细胞膜变性、脂质过氧化、蛋白质失活、线粒体功能障碍和细胞坏死[27]。活性氧非依赖性途径诱导细胞氧化和破坏,无需活性氧产生,这可能是通过从细胞膜到石墨烯及其衍生物材料的电荷转移而发生的,其中石墨烯及其衍生物材料充当电子泵[27-28]。 磷脂抽取学说:TU等[29]将计算机模拟与实验论证紧密结合,发现了一种新的抗菌机制,通过计算机分子动力学模拟石墨烯独特的二维结构使其可以与细菌细胞膜上的磷脂分子发生强烈的相互作用,从而导致大量的磷脂分子脱离细胞膜并吸附到石墨烯表面。此外,通过扫描电镜直接观察到了细菌细胞膜与氧化石墨烯作用后产生的大范围空腔结构,这也为其理论计算提供了强有力的实验证据。 (2)影响石墨烯及其衍生物抗菌性能的相关物理化学特性:实验结果表明,石墨烯及其衍生物材料的物理化学特性,如横向尺寸、层数和表面性能对其抗菌性能具有十分重要的影响,见表2[18-19,30-32]。 "
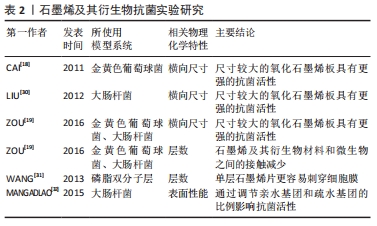
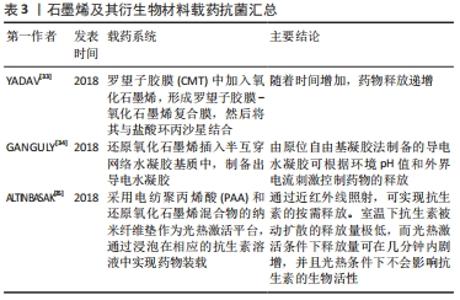
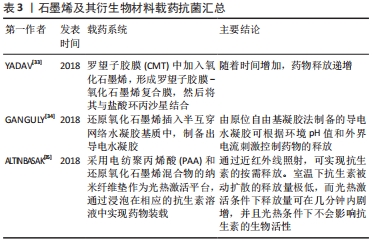
横向尺寸大小是影响石墨烯及其衍生物材料抗菌效果的关键因素。石墨烯及其衍生物的吸附能力、分散性能和边缘的锋利度受颗粒直径的影响非常大;反过来,这些特性对石墨烯及其衍生物的物理化学间的相互作用也具有重要影响[18]。石墨烯及其衍生物材料的横向尺寸越大,吸附能力越强,这归因于其具有较高的表面能[19]。LIU等[30]研究表明,较大的氧化石墨烯板具有更强的抗菌效果。 石墨烯及其衍生物材料的层数是其抗菌活性的重要决定因素:例如,增加石墨烯层数即增加材料的厚度,可使“纳米刀”效应减弱、分散性降低、聚集趋势增加,从而导致石墨烯及其衍生物材料和微生物之间的接触减少[19]。WANG等[31]通过计算石墨烯穿透磷脂双分子层的能力时发现,3层石墨烯片穿透膜的能量势垒约为2.7 KBT,大于单层石墨烯片,因此单层石墨烯片更容易刺穿细胞膜。 MANGADLAO等[32]通过Langmuir-Blodgett(LB)技术将氧化石墨烯片固定于工程塑料基底上,发现表面活性低的疏水的石墨烯只能通过机械切割作用于细胞,而表面活性更高的氧化石墨烯由于具有良好的亲水性,可以贴附于细胞表面而发挥抗菌作用。这也提示可以通过调节石墨烯及其衍生物材料中亲水基团和疏水基团的比例来控制抗菌活性。 2.2.2 载药抗菌 石墨烯及其衍生物材料除自身抗菌外,还可作为载体进行载药抗菌,其载药性能取决于负载药物的位置、时间和浓度。药物在高浓度、短时间内向靶目标释放是最理想的状态,见表3[33-35]。 "
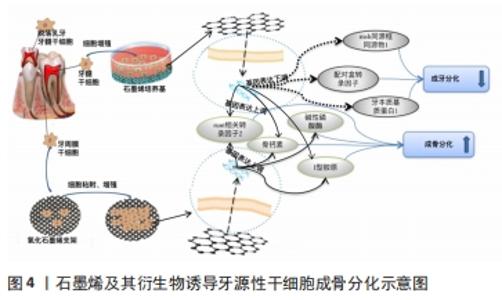
2.2.3 恢复牙周组织生理形态和功能 随着时间的推移,牙周炎所造成的牙周组织破坏会持续叠加,如果不进行干预,牙槽骨会逐渐吸收,可能会导致牙齿松动、脱落,并且很难通过自我修复恢复组织完整性。所以在牙周炎的治疗中,恢复牙周支持组织的形态和功能仍然是研究的热点内容之一。近年来,新型支架材料和牙源性干细胞的研究,为牙周组织再生提供了新的思路。 (1)组织工程支架:牙周组织再生工程的成功在很大程度上取决于支架的功能。支架材料作为牙周组织再生研究的关键,它不仅可为特定的细胞提供合适的环境,还为细胞的迁移、黏附、生长和分化提供生长因子和营养素。目前,许多研究团队进行大量的研究以探索石墨烯及其衍生物作为引导骨再生支架的可能性[36],并尝试将石墨烯及其衍生物作为支架的添加材料[37]、支架材料表面的涂层,进一步改善支架材料的某些性能并赋予其生物活性[38]。 屏障膜被用于引导性牙周组织再生术中,治疗牙周骨缺损,并增强骨再生潜能[39],从而促进牙周病患者病情转归[40]。引导性牙周组织再生术是通过具有适当形状物理屏障膜放置于牙周缺损位置,以覆盖再生过程所在的区域。屏障膜将牙周软组织从缺损区域中隔离,一方面防止牙周软组织进入骨缺损,并提供“引导”骨重建的空间;另一方面作为牙周膜干细胞在其表面黏附、增殖和分化的支架,促进牙骨质、牙周膜及牙槽骨的生长,以实现牙周组织再生的目标。作为牙周再生手术的关键环节,屏障膜的使用一直以来备受关注[41],目前运用于临床的屏障膜主要有第1代不可吸收膜和第2代可吸收膜[42-43]。第1代不可吸收膜性能优异,但需要二次手术取出,增加了感染和再生骨丢失的风险。第2代可吸收膜主要是胶原蛋白膜和壳聚糖膜,具有降解速度过快及生物活性不强等限制,不能满足牙周再生治疗的需求。石墨烯及其衍生物可作为支架的添加材料或表面的涂层材料来改善屏障膜的理化性能,从而增强其促进牙周组织再生的能力。 DE MARCO等[44]将氧化石墨烯的部分含氧官能团通过氢键与胶原蛋白进行非共价结合,获得含氧化石墨烯涂层的胶原膜,将其与人原代牙龈成纤维细胞联合培养发现,氧化石墨烯对胶原膜的机械性能有着一定的改善作用,胶原的易变性能力得到了一定程度的减弱,膜表面的粗糙度略有增加,7 d后牙龈成纤维细胞可在膜表面发生有效的聚合,表明经过氧化石墨烯改性后的胶原膜更有利于细胞黏附、增殖。毕博等[45]将还原氧化石墨烯引入前期制作的三维多孔壳聚糖/β-甘油磷酸钠(CS/GP)支架中以构建针对牙槽骨修复的复合支架(rGO/CS/GP),研究发现经过浓度为0.25%还原氧化石墨烯修饰的壳聚糖/β-甘油磷酸钠支架具有更强的机械性能、更高的吸收率及更低的降解速率,并有利于人牙髓干细胞黏附及增殖,在牙周组织工程中具有极大的潜力。赵彬等[46]合成了负载辛伐他汀的氧化石墨烯/丝素蛋白(GO/SF/SIM)复合屏障膜,这种复合膜可以很好地为成骨前体细胞的黏附、生长与增殖提供支持;辛伐他汀与氧化石墨烯联合使用具有交互作用,协同促进了骨缺损的愈合。 由此发现:石墨烯及其衍生物可为组织工程支架提供有利于细胞黏附的表面进而促进细胞附着和增殖,并能促进支架与周围组织之间的生物整合;石墨烯及其衍生物具有良好的生物相容性和一定的亲水性能,作为支架的添加材料或支架材料表面的涂层材料可以增强支架材料的机械强度;石墨烯及其衍生物可以改善屏障膜的理化性能,增强其骨引导、骨诱导性能。这些新膜有希望作为传统屏障膜的有效替代品用于牙周组织修复。 (2)诱导牙源性干细胞再生和成骨分化:研究者从口腔不同的组织结构中分离出具有干细胞特性的一类细胞群体,包括牙髓干细胞[47]、脱落乳牙牙髓干细胞[48]、牙周膜干细胞等[49]。这类细胞群体被称为牙源性干细胞,具有一般骨髓间充质干细胞的基本特征,其来源广泛、更易获取,并可进行自体移植[50]。已有研究表明氧化石墨烯不仅可以影响细胞形状、黏附、迁移和增殖,还决定了干细胞的分化方向。石墨烯及其衍生物诱导牙源性干细胞成骨分化见图4。 "
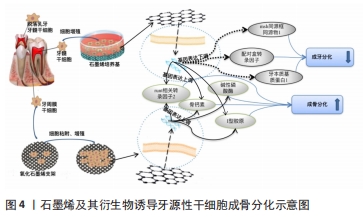

石墨烯及其衍生物诱导牙周膜干细胞分化:目前研究均表明牙周膜干细胞是牙周组织再生的主要功能细胞,牙周膜干细胞通过不断增殖分化来维持牙周组织稳态,促进组织再生,并有能力分化为成骨/牙骨质细胞、成牙本质细胞和成纤维细胞[51],其中成骨/牙骨质细胞最具临床意义。研究表明,石墨烯及其衍生物与牙周膜干细胞联合应用具有良好的骨引导及骨诱导作用,可应用于牙周组织再生领域。 XIE等[52]研究证明2D和3D石墨烯可诱导牙周膜干细胞向更高水平的成骨细胞方向分化。无论是否使用成骨诱导剂,添加石墨烯后成骨相关基因和蛋白质(Ⅰ型胶原、runt相关转录因子2和骨钙素)表达都上调。 氧化石墨烯也被证实可在体外诱导牙周膜干细胞成骨分化[14]。ZHOU 等[53]评估了牙周膜干细胞在添加了氧化石墨烯涂层钛底物与无涂层钛底物上的生物活性,发现氧化石墨烯涂层钛组与对照组相比,牙周膜干细胞中骨生成相关标志物如Ⅰ型胶原、碱性磷酸酶、骨唾液蛋白、runt相关转录因子2和骨钙素等表达明显提高。PARK等[54]通过水溶性四唑盐1(WST-1)法评估了牙周膜干细胞在氧化石墨烯支架上的黏附和增殖,并通过茜素红S染色评估其成骨分化能力,结果表明,在涂有氧等离子体和氧化石墨烯的支架中,牙周膜干细胞的增殖和成骨分化得到了增强。VERA-SáNCHEZ等[55]研究了丝素蛋白和氧化石墨烯复合材料促进人牙周膜干细胞自发分化为骨/成骨细胞的潜力,从培养7,10 d的MTT检测结果来看,那些含有低剂量氧化石墨烯和高剂量丝素蛋白的组合中,牙周膜干细胞的增殖率持续提高。在不添加化学成骨诱导剂的培养基中培养发现:丝素蛋白和氧化石墨烯复合材料能够诱导成骨细胞标记物的过度表达,包括骨形态发生蛋白2、runt相关转录因子2、碱性磷酸酶和Ⅰ型胶原。牙骨质附着蛋白和牙骨质基质蛋白1在牙骨质发育中起着重要作用,是牙周组织再生中的重要趋化蛋白,TORII等[56]研究这2种牙骨质相关基因在早期和后期分化阶段的表达,发现石墨烯及其衍生物和丝蛋白复合材料可以在没有任何生长因子的情况下促进人牙周膜干细胞的增殖和基因表达并诱导人牙周膜干细胞的成牙骨质分化。 虽然牙周膜干细胞是牙周组织再生的主要功能细胞,具有多向分化潜能,但是通过文献综述发现,在添加石墨烯及其衍生物后,牙周膜干细胞只能定向分化为成骨/牙骨质细胞。 石墨烯及其衍生物与其他牙源性干细胞:牙髓干细胞是一个独特的间充质干细胞群体,存在于牙髓的细胞丰富区,能够分化为骨细胞、脂肪细胞和神经样细胞[57]。有研究证明牙髓干细胞可促进动物牙周缺损组织修复和人牙槽骨再生[58]。 XIE等[59]评估了石墨烯在不使用任何化学诱导剂的情况下诱导牙髓干细胞的牙骨质生成或成骨分化。通过比对实验组和对照组中牙髓干细胞有关矿化、成牙和成骨基因的表达以及runt相关转录因子2、Ⅰ型胶原和骨钙素的蛋白表达,证实石墨烯对细胞自发分泌矿化基质有促进作用。石墨烯组msh同源框同源物1、配对盒转录因子和牙本质基质蛋白1等与牙体发育关的基因明显下调;但增加了成骨调控基因runt相关转录因子2、骨钙素和Ⅰ型胶原的表达,表明石墨烯能诱导牙髓干细胞的成骨分化而不是成牙分化。这是由于石墨烯具有较高的弹性模量(1.0-2.4 TPa)[60],而牙髓干细胞通常需要软基质才能实现成分化[61]。氧化石墨烯已被证实可在体外诱导牙髓干细胞成骨分化。魏常博等[62]发现质量浓度为0.1,0.5 μg/mL氧化石墨烯纳米片可以促进脱落乳牙牙髓干细胞的黏附和增殖,并且可以促进成骨相关基因表达。 石墨烯及其衍生物与人牙槽骨中骨髓间充质干细胞:王熙等[63]发现石墨烯能够提高人牙槽骨中骨髓间充质干细胞的增殖活性,并对细胞成骨分化产生促进作用,这可能与石墨烯上调骨形态发生蛋白2、runt相关转录因子2、Ⅰ型胶原等成骨相关因子的基因表达水平有关。 石墨烯及其衍生物对成骨分化的调节作用十分明显,其中氧化石墨烯涂层和还原氧化石墨烯涂层均表现出良好的细胞相容性,并通过上调碱性磷酸酶活性和骨钙素的分泌以及促进相关基因的表达来增强成骨分化[64-65]。 "

| [1] LA WG, PARK S, YOON HH, et al. Delivery of a therapeutic protein for bone regeneration from a substrate coated with graphene oxide. Small. 2013;9(23):4051-4060. [2] DREYER DR, PARK S, BIELAWSKI CW, et al. The chemistry of graphene oxide. Chem Soc Rev. 2010;39(1):228-240. [3] YANG K, WANG J, CHEN B. Facile fabrication of stable monolayer and few-layer graphene nanosheets as superior sorbents for persistent aromatic pollutant management in water. J Mater Chem A. 2014;2: 18219-18224. [4] PARK S, AN J, JUNG I, et al. Colloidal suspensions of highly reduced graphene oxide in a wide variety of organic solvents. Nano Lett. 2009; 9(4):1593-1597. [5] WITHERS N. Graphene oxide: Surfactant sheets. Nat Chem. 2010.https://doi.org/10.1038/nchem.741 [6] ROMERO UAM, SOTO MÁV, JIMÉNEZ LL, et al. Graphene Derivatives: Controlled Properties, Nanocomposites, and Energy Harvesting Applications.G raphene Materials - Structure, Properties and Modifications, 2017. [7] BÁEZ DF, PARDO H, LABORDA I, et al. Reduced Graphene Oxides: Influence of the Reduction Method on the Electrocatalytic Effect towards Nucleic Acid Oxidation. Nanomaterials (Basel). 2017;7(7):168. [8] LU C, LU Z, LI Z, et al. Effect of graphene oxide on the mechanical behavior of strain hardening cementitious composites. Constr Build Mater. 2016; 120(1):457-464. [9] ZHENG Q, HAN B, CUI X, et al. Graphene-Engineered Cementitious Composites: Small Makes a Big Impact. Nanomaterials and Nanotechnology. 2017;7:1-18. [10] MUNUERA JM, PAREDES JI, VILLAR-RODIL S, et al. High quality, low oxygen content and biocompatible graphene nanosheets obtained by anodic exfoliation of different graphite types. Carbon. 2015;94:729-739. [11] ZHANG X, YIN J, CHENG P, et al. Distribution and biocompatibility studies of graphene oxide in mice after intravenous administration. Carbon. 2011;49(3):986-995. [12] YANG K, GONG H, SHI X, et al. In vivo biodistribution and toxicology of functionalized nano-graphene oxide in mice after oral and intraperitoneal administration. Biomaterials. 2013;34(11):2787-2795. [13] SYAMA S, PAUL W, SABAREESWARAN A, et al. Raman spectroscopy for the detection of organ distribution and clearance of PEGylated reduced graphene oxide and biological consequences. Biomaterials. 2017;131:121-130. [14] WEI C, LIU Z, JIANG F, et al. Cellular behaviours of bone marrow-derived mesenchymal stem cells towards pristine graphene oxide nanosheets. Cell Prolif. 2017;50(5):e12367. [15] 付翔,李明新,彭驰伟,等.还原氧化石墨烯对人原代成纤维细胞的毒性研究[J].化学与生物工程,2021,38(2):49-52. [16] VOLKOV Y, MCINTYRE J, PRINA-MELLO A. Graphene toxicity as a double-edged sword of risks and exploitable opportunities: a critical analysis of the most recent trends and developments. 2D Materials. 2017;4(2):22001. [17] LI R, GUINEY LM, CHANG CH, et al. Surface Oxidation of Graphene Oxide Determines Membrane Damage, Lipid Peroxidation, and Cytotoxicity in Macrophages in a Pulmonary Toxicity Model. ACS Nano. 2018;12(2):1390-1402. [18] CAI X, TAN S, LIN M, et al. Synergistic antibacterial brilliant blue/reduced graphene oxide/quaternary phosphonium salt composite with excellent water solubility and specific targeting capability. Langmuir. 2011;27(12):7828-7835. [19] ZOU X, ZHANG L, WANG Z, et al. Mechanisms of the Antimicrobial Activities of Graphene Materials. J Am Chem Soc. 2016;138(7):2064-2077. [20] 吴雨宸,刘凯,苏俭生.添加氧化石墨烯对义齿基托树脂细胞毒性及抗菌性能影响的研究[J].口腔颌面修复学杂志,2020,21(3):129-135. [21] 吴志富,王佐林.氧化石墨烯对牙周致病菌影响的实验研究[J].口腔颌面外科杂志,2019,29(1):23-29. [22] HE J, ZHU X, QI Z, et al. Killing dental pathogens using antibacterial graphene oxide. ACS Appl Mater Interfaces. 2015;7(9):5605-5611. [23] VECITIS CD, ZODROW KR, KANG S, et al. Electronic-structure-dependent bacterial cytotoxicity of single-walled carbon nanotubes. ACS Nano. 2010;4(9):5471-5479. [24] LU X, FENG X, WERBER JR, et al. Enhanced antibacterial activity through the controlled alignment of graphene oxide nanosheets. Proc Natl Acad Sci U S A. 2017;114(46):E9793-E9801. [25] LIU S, ZENG TH, HOFMANN M, et al. Antibacterial activity of graphite, graphite oxide, graphene oxide, and reduced graphene oxide: membrane and oxidative stress. ACS Nano. 2011;5(9):6971-6980. [26] DALLAVALLE M, CALVARESI M, BOTTONI A, et al. Graphene can wreak havoc with cell membranes. ACS Appl Mater Interfaces. 2015;7(7): 4406-4414. [27] WEST JD, MARNETT LJ. Endogenous reactive intermediates as modulators of cell signaling and cell death. Chem Res Toxicol. 2006; 19(2):173-194. [28] LI J, WANG G, ZHU H, et al. Antibacterial activity of large-area monolayer graphene film manipulated by charge transfer. Sci Rep. 2014;4:4359. [29] Tu Y, Lv M, Xiu P, et al. Destructive extraction of phospholipids from Escherichia coli membranes by graphene nanosheets. Nat Nanotechnol. 2013;8(8):594-601. [30] LIU S, HU M, ZENG TH, et al. Lateral dimension-dependent antibacterial activity of graphene oxide sheets. Langmuir. 2012;28(33):12364-12372. [31] WANG J, WEI Y, SHI X, et al. Cellular entry of graphene nanosheets: the role of thickness, oxidation and surface adsorption. Rsc Advances. 2013;3(36):15776-15782. [32] MANGADLAO JD, SANTOS CM, FELIPE MJ, et al. On the antibacterial mechanism of graphene oxide (GO) Langmuir-Blodgett films. Chem Commun (Camb). 2015;51(14):2886-2889. [33] YADAV I, NAYAK SK, RATHNAM VSS, et al. Reinforcing effect of graphene oxide reinforcement on the properties of poly (vinyl alcohol) and carboxymethyl tamarind gum based phase-separated film. J Mech Behav Biomed Mater. 2018;81:61-71. [34] GANGULY S, DAS P, MAITY PP, et al. Green Reduced Graphene Oxide Toughened Semi-IPN Monolith Hydrogel as Dual Responsive Drug Release System: Rheological, Physicomechanical, and Electrical Evaluations. J Phys Chem B. 2018;122(29):7201-7218. [35] ALTINBASAK I, JIJIE R, BARRAS A, et al. Reduced Graphene-Oxide-Embedded Polymeric Nanofiber Mats: An “On-Demand” Photothermally Triggered Antibiotic Release Platform. ACS Appl Mater Interfaces. 2018;10(48):41098-41106. [36] 崔夏青. 氧化石墨烯与石墨烯对成骨细胞增殖分化影响的研究[D].唐山:华北理工大学,2021. [37] 李婷婷,张玉峰,王若茜,等.石墨烯及其衍生物改性复合材料促成骨机制和应用的研究进展[J].国际口腔医学杂志,2018,45(6):673-677. [38] 王楠,周延民.石墨烯材料在口腔医学领域的应用及生物安全性研究[J].口腔医学研究,2020,36(5):410-412. [39] 张敏,周艳,宦泓,等.引导性组织再生联合植骨术对Ⅰ型牙周-牙髓联合病变的临床疗效分析[J].牙体牙髓牙周病学杂志,2018, 28(12):720-723. [40] 许凌.牙周引导组织再生技术治疗牙周病的临床疗效及影响因素分析[J].罕少疾病杂志,2021,28(1):12-14. [41] 张岚,吴燕岷.可吸收生物膜在牙周引导组织再生术中的研究进展[J].口腔医学,2020,40(6):571-575. [42] WANG J, WANG L, ZHOU Z, et al. Biodegradable Polymer Membranes Applied in Guided Bone/Tissue Regeneration: A Review. Polymers (Basel). 2016;8(4):115. [43] CARBONELL JM, MARTÍN IS, SANTOS A, et al. High-density polytetrafluoroethylene membranes in guided bone and tissue regeneration procedures: a literature review. Int J Oral Maxillofac Surg. 2014;43(1):75-84. [44] DE MARCO P, ZARA S, DE COLLI M, et al. Graphene oxide improves the biocompatibility of collagen membranes in an in vitro model of human primary gingival fibroblasts. Biomed Mater. 2017;12(5):055005. [45] 毕博,臧圣奇,何懋典,等.还原氧化石墨烯修饰壳聚糖骨组织工程支架的制备及表征[J].医学研究生学报,2021,34(4):350-356. [46] 赵彬,武峰,白莹莹,等.负载辛伐他汀的氧化石墨烯/丝素蛋白屏障膜的制备及其生物学性能[J].新型炭材料,2018,33(5):460-468. [47] 李鹏,木合塔尔·霍加.牙髓干细胞在再生医学中的应用进展[J].全科口腔医学电子杂志,2018,5(24):24,26. [48] 陈宁馨,赖光云,汪俊.脱落乳牙牙髓干细胞在口腔颌面部组织再生及免疫调节中应用的研究进展[J].中国实用口腔科杂志,2021, 14(2):220-224. [49] 吴博昊,安莹.牙周膜干细胞在牙周组织再生中的研究新进展[J].口腔生物医学,2020,11(4):270-276. [50] CHEN FM, SUN HH, LU H, et al. Stem cell-delivery therapeutics for periodontal tissue regeneration. Biomaterials. 2012;33(27):6320-6344. [51] SEO BM, MIURA M, GRONTHOS S, et al. Investigation of multipotent postnatal stem cells from human periodontal ligament. Lancet. 2004; 364(9429):149-155. [52] XIE H, CAO T, GOMES JV, et al. Two and three-dimensional graphene substrates to magnify osteogenic differentiation of periodontal ligament stem cells. Carbon. 2015;93:266-275. [53] ZHOU Q, YANG P, LI X, et al. Bioactivity of periodontal ligament stem cells on sodium titanate coated with graphene oxide. Sci Rep. 2016;6: 19343. [54] PARK J, PARK S, KIM JE, et al. Enhanced Osteogenic Differentiation of Periodontal Ligament Stem Cells Using a Graphene Oxide-Coated Poly(ε-caprolactone) Scaffold. Polymers (Basel). 2021;13(5):797. [55] VERA-SÁNCHEZ M, AZNAR-CERVANTES S, JOVER E, et al. Silk-Fibroin and Graphene Oxide Composites Promote Human Periodontal Ligament Stem Cell Spontaneous Differentiation into Osteo/Cementoblast-Like Cells. Stem Cells Dev. 2016;25(22):1742-1754. [56] TORII D, TSUTSUI TW, WATANABE N, et al. Bone morphogenetic protein 7 induces cementogenic differentiation of human periodontal ligament-derived mesenchymal stem cells. Odontology. 2016;104(1):1-9. [57] GRONTHOS S, MANKANI M, BRAHIM J, et al. Postnatal human dental pulp stem cells (DPSCs) in vitro and in vivo. Proc Natl Acad Sci U S A. 2000;97(25):13625-13630. [58] JIA L, GU W, ZHANG Y, et al. The Crosstalk between HDPSCs and HUCMSCs on Proliferation and Osteogenic Genes Expression in Coculture System. Int J Med Sci. 2017;14(11):1118-1129. [59] XIE H, CHUA M, ISLAM I, et al. CVD-grown monolayer graphene induces osteogenic but not odontoblastic differentiation of dental pulp stem cells. Dent Mater. 2017;33(1):e13-e21. [60] LEE C, WEI X, KYSAR JW, et al. Measurement of the elastic properties and intrinsic strength of monolayer graphene. Science. 2008; 321(5887):385-388. [61] LU Q, PANDYA M, RUFAIHAH AJ, et al. Modulation of Dental Pulp Stem Cell Odontogenesis in a Tunable PEG-Fibrinogen Hydrogel System. Stem Cells Int. 2015;2015:525367. [62] 魏常博,余智超,李晔,等.氧化石墨烯片对人乳牙牙髓干细胞黏附,增殖及成骨早期相关蛋白表达的影响[J]. 临床口腔医学杂志, 2018,34(7):387-391. [63] 王熙,张淑悦,黄呈森,等.石墨烯对人牙槽骨骨髓间充质干细胞增殖分化的影响[J].卫生职业教育,2020,38(16):117-120. [64] ZHAO C, LU X, ZANDEN C, et al. The promising application of graphene oxide as coating materials in orthopedic implants: preparation, characterization and cell behavior. Biomed Mater. 2015;10(1):015019. [65] LEE JH, SHIN YC, JIN OS, et al. Reduced graphene oxide-coated hydroxyapatite composites stimulate spontaneous osteogenic differentiation of human mesenchymal stem cells. Nanoscale. 2015; 7(27):11642-11651. [66] BREGNOCCHI A, ZANNI E, UCCELLETTI D, et al. Graphene-based dental adhesive with anti-biofilm activity. J Nanobiotechnology. 2017;15(1):89. [67] 何剑亮.氧化石墨烯对变异链球菌的抗菌作用研究[D].上海:上海交通大学,2016. |
| [1] | Nong Fuxiang, Jiang Zhixiong, Li Yinghao, Xu Wencong, Shi Zhilan, Luo Hui, Zhang Qinglang, Zhong Shuang, Tang Meiwen. Bone cement augmented proximal femoral nail antirotation for type A3.3 intertrochanteric femoral fracturalysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-10. |
| [2] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [3] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [4] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [5] | Nie Chenchen, Su Kaiqi, Gao Jing, Fan Yongfu, Ruan Xiaodi, Yuan Jie, Duan Zhaoyuan, Feng Xiaodong. The regulatory role of circular RNAs in cerebral ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1286-1291. |
| [6] | Gao Yu, Han Jiahui, Ge Xin. Immunoinflammatory microenvironment after spinal cord ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1300-1305. |
| [7] | Wang Ji, Zhang Min, Yang Zhongya, Zhang Long. A review of physical activity intervention in type 2 diabetes mellitus with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1272-1277. |
| [8] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [9] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [10] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [11] | Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109. |
| [12] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| [13] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [14] | Bai Siqi, Xiao Zhen, Liu Jing. Application potential of adipose-derived stem cells in female pelvic floor dysfunction diseases [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 921-927. |
| [15] | Zhang Qijian, Xu Ximing. Acquisition and application of ectodermal mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 928-934. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||