中国组织工程研究 ›› 2023, Vol. 27 ›› Issue (33): 5298-5303.doi: 10.12307/2023.514
• 干细胞基础实验 basic experiments of stem cells • 上一篇 下一篇
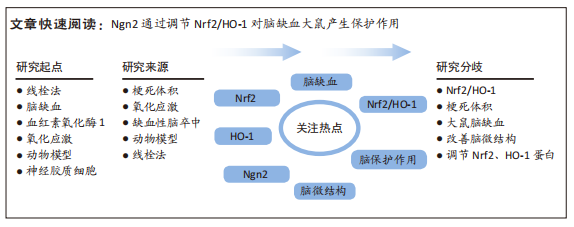
Ngn2调节Nrf2/HO-1对脑缺血模型大鼠脑微结构、角质细胞活性的影响
王明盛1,崔焕喜1,崔红凯1,裴观辉1,李道广1,闫海清2,张 平2
- 新乡医学院第一附属医院,1神经介入科,2神经内科,河南省卫辉市 453100
Ngn2 effects on brain microstructure and keratinocyte activity in cerebral ischemia rats via regulating Nrf2/HO-1
Wang Mingsheng1, Cui Huanxi1, Cui Hongkai1, Pei Guanhui1, Li Daoguang1, Yan Haiqing2, Zhang Ping2
- 1Department of Neurointervention, 2Department of Neurology, The First Affiliated Hospital of Xinxiang Medical University, Weihui 453100, Henan Province, China
摘要:
文题释义:
脑缺血:指由于多种原因导致的局部或多部位的供血不足性疾病。其主要病因与脑动脉狭窄或闭塞、脑动脉栓塞、血流动力学因素、血液学因素有关,主要临床症状包括头痛、呕吐、眩晕、偏瘫、感觉障碍,可导致癫痫、面瘫、语言障碍等并发症。目前主要通过溶栓、手术、药物等多方式治疗,预后与疾病类型有关。脑微结构:脑结构可塑性改变是脑损伤后功能恢复的基础。神经系统中细胞与细胞之间的信号依靠突触结构传递,突触是神经递质和受体作用的功能单位,其结构的完整性是神经元正常生理功能的物质基础。突触超微结构变化也是衡量脑结构可塑性的重要方面。
背景:研究显示,血红素氧化酶1(heme oxidase-1,HO-1)在脑缺血再灌注损伤中具有重要作用;核因子E2相关因子2(nuclear factor-erythroid2-related factor2,Nrf2)能减轻脑缺血再灌注损伤,其作用是通过调控下游抗氧化蛋白实现的;推测Nrf2/HO-1在脑部疾病中均有一定的调控作用。
目的:探究神经源素2(neurogenin 2,Ngn2)通过调节Nrf2/HO-1对脑缺血大鼠脑微结构、角质细胞活性的影响。
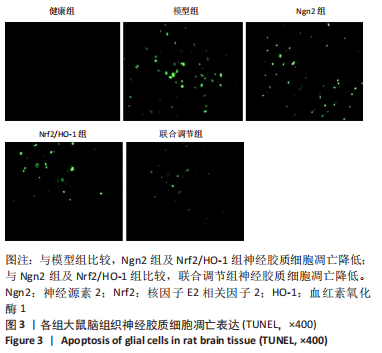
方法:SPF级雄性SD大鼠55只,随机取10只为健康组不进行干预;其余大鼠建立脑缺血模型,将建模成功的40只大鼠随机分为4组:其中模型组大鼠脑内注射生理盐水;Ngn2组大鼠脑内注射Ngn2 10 mg/kg;Nrf2/HO-1组脑内注射HO-1及Nrf2激动剂莱菔硫烷各10 mg/kg;联合调节组脑内注射Ngn2并联合Nrf2/HO-1组用药,均连续给药3 d。分数各向异性图像观察脑微结构,苏木精-伊红染色观察脑组织的病理形态,TUNEL法检测神经胶质细胞凋亡,免疫印迹和PCR分别检测Nrf2、HO-1的蛋白及mRNA表达。
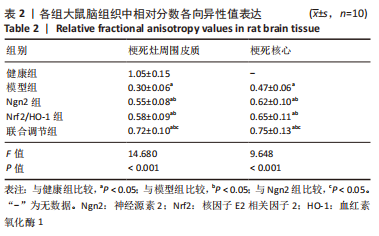
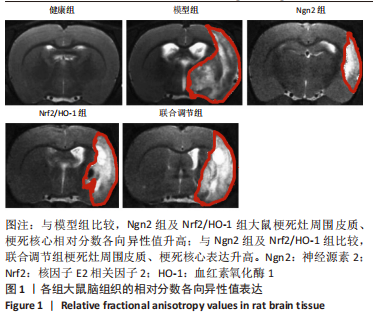
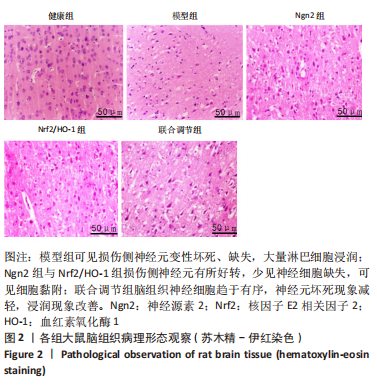
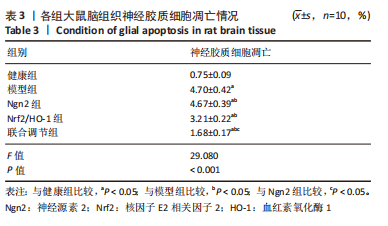
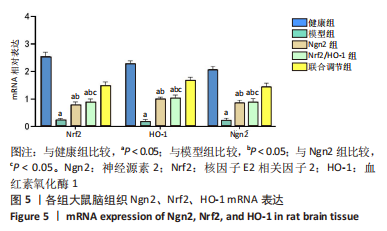
结果与结论:①与健康组比较,模型组大鼠脑组织中梗死灶周围皮质、梗死核心相对分数各向异性值表达较低(P < 0.05);与模型组比较,Ngn2组及Nrf2/HO-1组上述表达升高(P < 0.05);联合调节组上述表达高于Ngn2组及Nrf2/HO-1组(P < 0.05);②模型组大鼠大量损伤神经元,细胞稀疏,排列紊乱,大量浸润;Ngn2组与Nrf2/HO-1组损伤侧神经元好转,仍见神经细胞缺失紊乱及细胞黏附;联合调节组脑组织神经细胞坏死减轻,浸润改善;③与健康组比较,模型组大鼠神经胶质细胞凋亡较高(P < 0.05);与模型组比较,Ngn2组及Nrf2/HO-1组神经胶质细胞凋亡降低(P < 0.05);联合调节组神经胶质细胞凋亡低于Ngn2组及Nrf2/HO-1组(P < 0.05);④与健康组比较,模型组大鼠脑组织Ngn2 mRNA及Nrf2、HO-1的蛋白和mRNA表达较低(P < 0.05);与模型组比较,Ngn2组、Nrf2/HO-1组Ngn2 mRNA及Nrf2、HO-1的蛋白和mRNA表达升高(P < 0.05);联合调节组Ngn2 mRNA及Nrf2、HO-1的蛋白和mRNA表达高于Ngn2组及Nrf2/HO-1组(P < 0.05);⑤结果说明,Ngn2通过调节Nrf2/HO-1对脑缺血大鼠产生保护作用,其机制可能与改善脑微结构、角质细胞活性以及增强Nrf2、HO-1表达等具有一定相关性。
https://orcid.org/0000-0001-6610-0141(王明盛)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号: