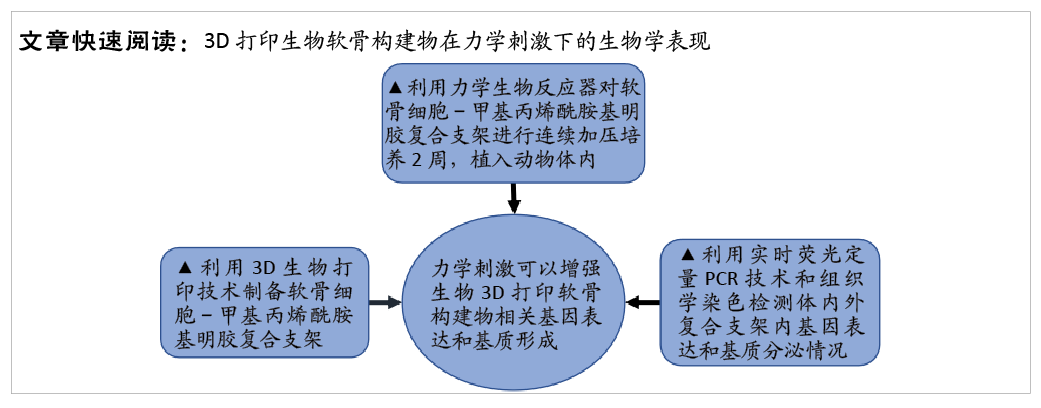
1.1 设计 体内、外比较性观察实验,组内比较采用单因素方差分析,两组间比较采用t检验。
1.2 时间及地点 实验于2020年10月至2021年6月在中国医学科学院整形外科医院研究中心完成。
1.3 材料
1.3.1 实验动物 5月龄健康新西兰白兔2只,体质量2.5-3.0 kg,用于提取兔耳软骨细胞;5周龄健康裸鼠10只,体质量16-18 g,用于复合支架皮下植入实验,均由中国医学科学院整形外科医院实验动物中心提供。动物实验方案通过中国医学科学院整形外科医院实验动物伦理委员会批准(批准号EAEC 2020-09)。
1.3.2 实验试剂 DMEM高糖培养基、青霉素-链霉素-新霉素(PSN)抗生素混合物、胎牛血清、0.25%胰蛋白酶、PBS(GIBCO公司,美国);Ⅱ型胶原酶(Sigma公司,美国);GelMA冻干粉(上普博源北京生物科技有限公司);番红O染液(北京索莱宝科技有限公司,中国);Calcein-AM/PI细胞双染试剂盒(Calcein-AM/PI Double Staining Kit)(东仁化学科技有限公司,中国);抗Ⅰ型胶原抗体(Thermo公司,美国);山羊抗小鼠IgG H&L(HRP)(Abcam公司,英国)。
1.3.3 实验仪器 Bioplotter 3D 生物打印机(Envition tec公司,德国);TC-3F bioreactor、TEB1005 bioreactor(EBERS公司,西班牙);CO2 培养箱(Thermo公司,美国);倒置荧光显微镜(Olympus 公司,日本);共聚焦荧光显微镜(Leica公司,德国);NanoDrop 2000c微量分光光度计(Thermo Fisher Scientific公司,美国);PCR 仪(Eppendorf公司,德国);LightCycler R
96Ⅱ实时荧光定量 PCR(real-time fluorescent quantitative PCR,qRTPCR)系统(Roche 公司,瑞士)。
1.4 实验方法
1.4.1 兔耳软骨细胞的分离、培养和扩增 1%戊巴比妥
50 mg/kg腹腔注射麻醉新西兰白兔,以耳缘静脉空气栓塞法处死,固定于操作台上,以无菌方式取下兔双耳,放入含有1%青霉素-链霉素的PBS中,于低温环境下暂存。将样本送至实验室,于超净工作台中剥离兔耳软骨表面结缔组织,在无菌培养皿中,用眼科剪将软骨剪碎至 1 mm×1 mm×1 mm的小块,移至50 mL离心管内,加5倍体积0.25%胰蛋白,37 ℃
下置于摇床摇30 min(80 r/min);1 000 r/min离心5 min,弃去上清,加 5 倍软骨体积的 0.2%Ⅱ型胶原酶,37 ℃下置于摇床摇8-10 h[14](80 r/min);70 µm细胞滤网过滤,离心,弃上清,洗涤后,调整细胞密度,将细胞接种到含体积分数10%胎牛血清和1%抗生素混合物的DMEM高糖完全培养基中,置于37 ℃、体积分数5%CO2培养箱中培养,每二三天更换一次培养基。软骨细胞为贴壁细胞,一般过夜即可贴壁,于倒置显微镜下观察细胞形态,呈短梭形、多角形,细胞形态不均一。细胞生长达到80%时用0.25%胰蛋白酶消化,按照1∶3的比例进行传代,待第2代细胞贴壁后,于倒置显微镜下观察,软骨细胞呈短梭状,形态较均一。待细胞生长达到80%汇合时,收集第2代软骨细胞进行后续实验。
1.4.2 3D生物打印软骨细胞-GelMA复合支架 打印前,乙醇擦拭3D打印机,实验所需器械均经乙醇浸泡灭菌,开启与3D打印机配套的超净工作台,紫外线照射灭菌,通过可移动式紫外灯对工作台周围环境进行紫外灯照射灭菌。用DMEM高糖培养基将GelMA冻干粉配制为12.5%的墨水溶液,置于70 ℃水浴中使其充分溶解,用0.22 µm过滤器进行过滤除菌。将过滤后的GelMA溶液与第2代兔耳软骨细胞和蓝光引发剂充分混合,配制成细胞终浓度为1×1010 L-1、蓝光引发剂终浓度为0.25%的生物墨水。置入3D打印机中,待墨水状态稳定后,进行逐层打印,选用内径为250μm的针头,温度设置为20 ℃,支架大小设置为10 mm×5 mm,层高0.32 mm,
层数为8层,打印线间距为1.2 mm。每层打印后用405 nm蓝光光照交联3-5 s,使其充分固化,得到含有兔耳软骨细胞的水凝胶复合支架,加入DMEM高糖完全培养基,置于37 ℃、体积分数5%CO2培养箱中培养。
1.4.3 对复合支架进行加压培养 取6孔板中培养5 d的复合支架于TC-3F力学加压生物反应器中,将TC-3F生物反应器置于TEB1005灌流培养箱中,可实现在对生物样本施加的力不变的情况下,培养基循环流动,支持反应器中样本的长期培养,减少污染概率。力学加压设置:频率0.5 Hz,位移
0.50 mm,首次运动方向为下,往返,4 h/d,2周。灌流培养设置:手动模式,LF-318泵头,顺时针灌流,橡胶管内径
1.65 mm,转速8 r/min,实际流速1.200 mL/min。对照组的复合支架仍置于6孔板中培养,每二三天更换一次新鲜DMEM高糖完全培养基。
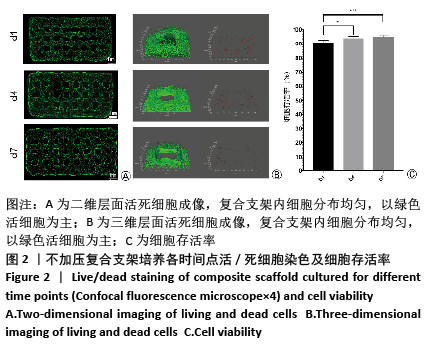
1.4.4 不加压复合支架中细胞存活率检测 培养第1,4,7天,取兔耳软骨复合支架样本,用活死细胞染色试剂盒进行细胞染色,利用共聚焦荧光显微镜进行观察和拍照,在对应波长的光激发下,活细胞呈绿色,死细胞呈红色,对样本进行全景扫描后输出图像,利用共聚焦显微镜分析模块将色彩分类后进行细胞计数,按细胞存活率=活细胞总数/(活细胞总数+死细胞总数)×100%的公式进行计算。另外,选取5个任意区域在Z轴上对复合支架进行层层扫描,图像拟合后输出,观察样品细胞分布及密度变化。
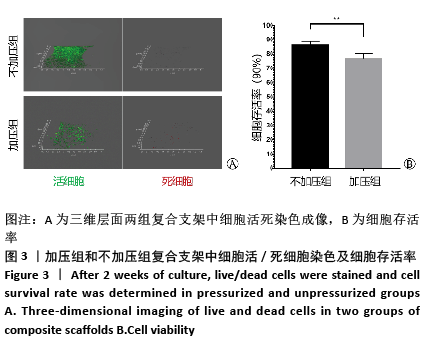
1.4.5 加压组与不加压组复合支架细胞存活率检测 培养2周后,取加压组和不加压组复合支架,活死染色后在Z轴上进行图像采集,检测细胞存活情况,具体方法同上。
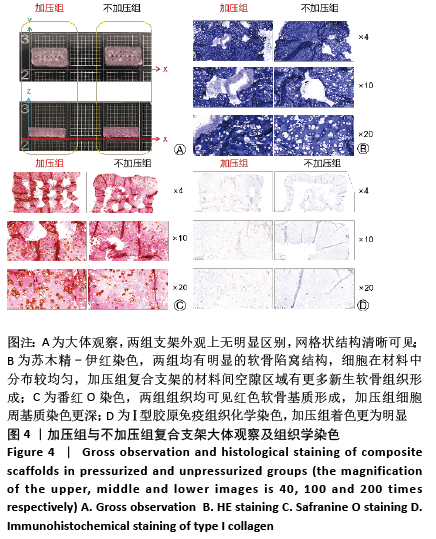
1.4.6 加压组与不加压组复合支架组织切片观察 培养2周后,取加压组和不加压组复合支架,40 g/L多聚甲醛固定,石蜡包埋,切片,切片厚度3μm,常规进行苏木精-伊红、番红O、Ⅰ型胶原免疫组织化学染色。
番红O染色:石蜡切片常规脱蜡至水后,番红O染色液滴染5 min后流水冲洗,常规脱水,二甲苯透明,风干后中性树脂封固。
Ⅰ型胶原免疫组织化学染色:石蜡切片常规脱蜡至水后,PBS充分清洗,内源性过氧化物酶阻断10 min,PBS充分漂洗,复合酶消化(37 ℃,30 min);PBS漂洗,羊血清封闭(37 ℃,30 min),吸除多余血清,一抗孵育(1∶1 000)(4 ℃过夜);PBS充分漂洗,二抗孵育(37 ℃,30 min);PBS充分漂洗,DAB显色,水洗、分化,常规脱水,二甲苯透明,风干后中性树脂封固。
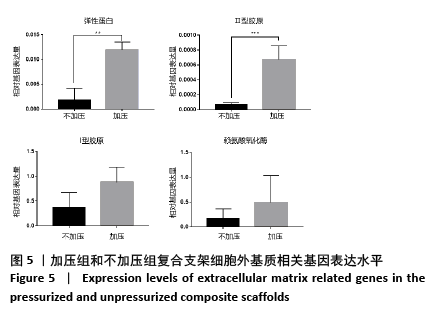
1.4.6 加压组与不加压组复合支架qRT-PCR检测 培养2周后,取加压组和不加压组复合支架,采用Trizol法提取水凝胶支架中的总RNA后,利用NanoDrop 2000c 微量分光光度计检测所提取总RNA的浓度及纯度,达到实验条件后,进行反转录反应(1000 ng RNA),得到的cDNA保存在-20 ℃。SYBR GREEN 的qRT-PCR法检测成软骨相关基因弹性蛋白、Ⅰ型胶原、Ⅱ型胶原、赖氨酸氧化酶的mRNA 相对表达量,以β-actin作为内参对照物,每个样品设3个复孔,反应条件为95 ℃300 s,95 ℃10 s,60 ℃10 s,72 ℃10 s,95 ℃60 s,60 ℃60 s,95 ℃1 s,40 ℃30 s,循环45次,用2-ΔΔCt法计算各基因mRNA的相对表达量。引物在Pubmed上设计并验证,由擎科公司代为合成(中国,北京),基因引物序列见表1。

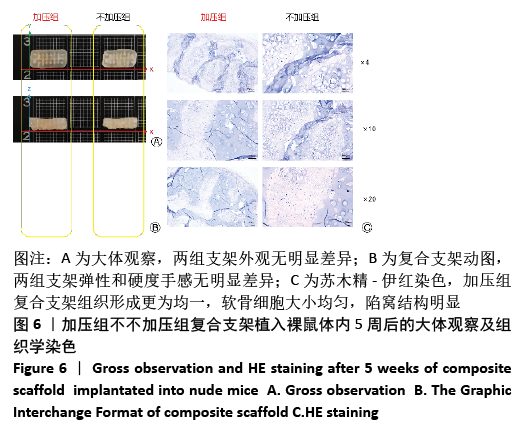
1.4.7 复合支架裸鼠皮下植入 腹膜内注射1%戊巴比妥溶液麻醉裸鼠,沿背部中线剪开一长约1.2 cm
纵切口,将培养2周后的加压组和不加压组复合支架分别植入腹部两侧,缝合切口。5周后,麻醉后脊椎脱臼法处死裸鼠后取材,大体观察两组复合支架的形态、大小和力学特性;40 g/L多聚甲醛固定,石蜡包埋,切片,切片厚度
3 μm,苏木精-伊红染色初步观察裸鼠体内软骨形成情况。
1.5 主要观察指标 加压组与不加压组复合支架的大体形态结构和细胞存活率,以及在体内、体外的软骨形成情况。
1.6 统计学分析 应用 Graphpad Prism 7软件进行统计分析,用x±s来表示各组数据,单因素方差对组内不同时间点间进行比较分析,t检验则用来对两组间数据进行比较,P < 0.05 代表差异有显著性意义。统计学方法已经中国医学科学院整形外科医院生物统计学专家审核。