1.1 设计 随机对照动物实验,体外细胞干预实验,2组数据进行t检验,3组及以上数据进行One-way ANOVA检验。
1.2 时间与地点 实验于2019年7月至2020年8月在南方医科大学第三附属医院中心实验室完成。
1.3 材料
1.3.1 实验动物 8周龄雄性清洁级C57小鼠,共20只,体质量为25-28 g,均由南方医科大学实验动物中心提供,合格证号:No.44007200038731。动物的饲养条件均按照清洁级实验动物管理标准,在恒定25 ℃、标准50%湿度,12 h光照/黑暗循环的昼夜节律条件下,自由获取食物和水,每笼三四只小鼠,每隔5 d更换一次垫料并添加适量的饲料和水,悉心照料。
1.3.2 小鼠原代软骨细胞来源 C57小鼠自我繁殖所得同窝6只出生3 d内的C57BL/6乳鼠,雌雄不限。
1.3.3 实验使用的主要试剂和仪器 乙二胺四乙酸二钠、苏木精粉剂、番红O快速绿购自Sigma;甘油、多聚甲醛、体积分数75%乙醇及二甲苯购自广州化学试剂厂;抗体:PDZK1抗体(23274-1-AP)、Ⅱ型胶原抗体(15943-1-AP)、基质金属蛋白酶13抗体(18165-1-AP)购自Proteintech;兔抗羊、鼠抗羊二抗购自北京锐抗;荧光显微镜、倒置显微镜购自日本Olympus公司。重组鼠源性白细胞介素1β(R&D Systems 美国);0.25%胰蛋白酶、Ⅱ型胶原酶、青霉素-链霉素混合液;胎牛血清;反转录试剂盒、荧光定量PCR试剂盒(艾科瑞生物)。
1.4 方法
1.4.1 动物实验
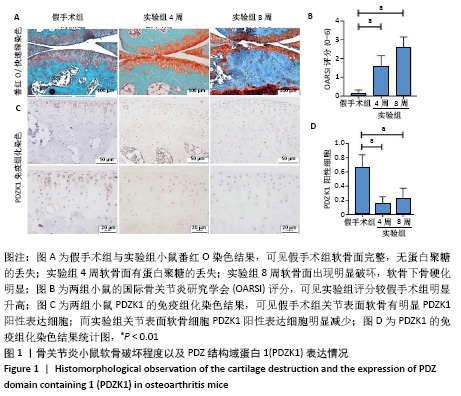
(1)实验动物分组及检测指标:将20只C57/BL6小鼠按随机数字表法分为实验组和假手术组,每组10只;实验组又随机分为4,8周2个亚组,各5只。在术后4,8周取材并进行番红O快速绿染色,通过免疫组织化学染色检测软骨细胞PDZK1的表达量。
(2)小鼠骨关节炎模型建立:实验组小鼠行右侧膝关节内侧半月板胫骨韧带切除,游离内侧半月板。术前小鼠自由摄取食水,每周更换垫料,造模时间在小鼠10周龄、骨骼肌肉发育成熟后进行。麻醉前,利用天平称量每只小鼠的体质量,随后使用1%浓度的异氟烷行气体吸入维持麻醉,数分钟后观察小鼠肌张力,明确麻醉深度。麻醉起效后将小鼠右膝关节周围的鼠毛剔除,并用棉球蘸取碘伏进行消毒。随后在解剖显微镜下将小鼠右膝关节近内侧皮肤切开,沿髌骨韧带内侧纵行切开肌肉,将髌骨外翻后钝性分离肌肉与脂肪等组织,暴露胫骨平台与内侧半月板胫骨韧带。使用高压灭菌的显微剪将内侧半月板胫骨韧带切断,游离内侧半月板,造成膝关节不稳定以诱导骨关节炎[18],最后生理盐水冲洗,并将外翻的髌骨韧带复位,缝合关节囊与切口[19],并将小鼠放置于37 ℃恒温锅进行复苏。待麻醉苏醒后,将小鼠放回原笼中继续饲养,勤换垫料与观察伤口情况,小鼠自由摄取食水、可自由活动。假手术组仅切开关节囊。
(3)关节标本的收集:在术后4,8周将小鼠过量麻醉致死。左手固定小鼠膝关节,利用手术刀切开小鼠右膝关节皮肤,钝性分离皮下组织,利用眼科剪剪断股四头肌肌腱,剪掉多余肌肉和软组织,于股骨中断离断股骨,下方剪断跟腱后于胫骨下端离断胫骨,保留完整的膝关节,为区分上下侧,习惯将股骨保留长度短于胫骨,再利用眼科剪将关节囊周围的肌肉软组织剔除干净,注意不要损伤到关节囊。置于上述配制好的多聚甲醛中,4 ℃冰箱恒温固定36 h。
(4)关节标本的处理:①脱钙:取固定完成后的膝关节,置于去离子水中冲洗1遍,去除多余多聚甲醛;然后更换成14%脱钙液,37 ℃摇床进行脱钙24 d,每三四天换1次,直到针刺检测脱钙完成。②脱水:脱钙完成后的组织放于包埋盒中用去离子水冲洗12 h;梯度乙醇脱水(体积分数依次为50%,70%,80%,95%,95%,100%,100%)60 min。二甲 苯Ⅰ60 min;二甲苯Ⅱ 60 min;软蜡60 min;硬蜡60 min。③石蜡包埋:首先设置预定温度预热石蜡包埋机,使蜡池内蜡块充分溶解。脱水完成后,取出上述各标本,置于液体蜡池中,使用矢状面包埋(尽量保持膝关节内侧面平整贴于包埋盒底面)。待液体蜡覆盖后,将标本放置于低温冰台冷却凝固,蜡块凝固后,取下蜡块,置于-20 ℃冰箱冻存。④切片:切片厚度为10 μm的情况下修整至可以看到内侧半月板开始分离,然后调整切片厚度为4 μm,矢状面切片边切边展片观察,切片至看不到内侧半月板。⑤烘片:将上述切好的石蜡切片置于37 ℃恒温烤箱中烘烤24 h,可以有效防止以后掉片,室温冷却后置于4 ℃冰箱保存,避免组织中的抗原失去活性,影响后续实验结果。
(5)国际骨关节炎研究学会(Osteoarthritis Research Society International,OARSI)评分:根据以往文献报道,利用番红O快速绿染色结果对小鼠骨关节炎严重程度进一步行评估[20]。至少请2位观察者进行双盲观察,在胫骨选取关节面中间进行观察。此次研究只进行关节面中间评分,评分细则大致为:正常(0分);少许番红O染色丢失,没有软骨结构改变(0.5分),没有软骨丢失的少量纤维化(1分);垂直裂缝至表层软骨一下,部分表层丢失(2分);垂直裂缝/侵蚀至钙化软骨层<25%的软骨面(3分);垂直裂缝/侵蚀至钙化软骨层25%-50%的软骨面(4分);垂直裂缝/侵蚀至钙化软骨层51%-75%的软骨面(5分);垂直裂缝/侵蚀至钙化软骨层>75%的软骨面(6分);共6分。
(6)免疫组织化学染色:①取切好的标本,65 ℃恒温烤箱烤片60 min。然后二甲苯脱蜡2遍后,再降梯度乙醇水化,具体过程为:二甲苯Ⅰ,10 min;二甲苯Ⅱ,10 min;无水乙醇Ⅰ,10 min;无水乙醇Ⅱ,10 min;体积分数90%乙醇,5 min;体积分数80%乙醇,5 min;体积分数70%乙醇,5 min;体积分数50%乙醇,5 min;最后用去离子水浸泡 10 min再进行免疫组化实验操作;②切片浸泡在枸橼酸纳溶液60 ℃水浴修复16-36 h,使抗原充分暴露;③用PBS浸泡洗切片3次,5 min/次;用免疫组化笔圈出样品,加入适量体积分数3%的过氧化氢溶液室温放置15 min;④用PBS浸泡洗切片3次,5 min/次;滴加体积分数10%山羊血清封闭液至标本完全覆盖,37 ℃烘箱封闭1 h;⑤根据说明书配制PDZK1相应浓度的一抗工作液,4 ℃过夜放置16-36 h;⑥切片从冰箱拿出复温至室温,用PBS浸泡洗切片3次,5 min/次;现配现用,根据说明书配制一定浓度兔源性二抗工作液,室温条件反应1 h;⑦用PBS浸泡洗切片3次,每次5 min;接着进行DAB显色,待目标区域出现PDZK1的阳性颗粒后用去离子水浸洗干净;随后用苏木精复染细胞核20 s,分化液浸泡1 s,用去离子水将分化液浸洗干净,再将其浸泡在PBS中进行返蓝,在光学显微镜下观察,待细胞核颜色变为蓝色即可;⑧进行脱水透明:体积分数50%乙醇,2 min;体积分数70%乙醇,2 min;体积分数80%乙醇,2 min;体积分数95%乙醇,2 min;无水乙醇Ⅱ,1 min;无水乙醇Ⅰ,1 min;二甲苯Ⅰ,30 s;二甲苯Ⅱ,30 s。最后待切片风干后用中性树胶封固,若有气泡可轻微挤压,利用正置显微镜观察并进行统计PDZK1阳性细胞数。
1.4.2 细胞实验
(1)小鼠原代软骨细胞提取:取出生3 d内的C57/BL6乳鼠逐一称体质量,将1%戊巴比妥钠按照8 μL/g的标准注入麻醉。断颈处死后放入体积分数75%的乙醇中消毒 3-5 min,将消毒后的乳鼠置于超净台中的无菌培养皿中,用已高压消毒过的眼科剪刀和眼科镊子分离出乳鼠的肋软骨。将带有软组织的肋软骨放置于无菌PBS中进行清洗,然后在大体解剖显微镜下将肋软骨进行粗分离,将明显的软组织剥离,尽量只留软骨部分。将其放置于0.25%的胰蛋白酶中 37 ℃恒温消化30 min,取出软骨,放置于新的无菌PBS中清洗,接着在大体解剖显微镜下将肋软骨进行细分离。将分离后的肋软骨放置在胶原酶培养基混合液(0.1%Ⅱ型胶原酶、体积分数10%胎牛血清、1%双抗的DMEM:F12培养基)中进行消化,用无菌封口膜密封离心管,放置于37 ℃恒温水平摇床消化5-8 h,直到大部分肋软骨消化完成,将离心管放置在离心机上1 000 r/min离心10 min,弃上清液,加入适量培养基(体积分数10%胎牛血清、1%双抗的DMEM:F12培养基)重悬软骨细胞,细胞悬液浓度为1×106,种植到6 cm皿中,2只乳鼠的软骨细胞种一个皿,在37 ℃,体积分数5%的CO2条件下孵箱培养,每2 d换液1次,长满后进行传代。原代软骨细胞需在3代以内使用。
(2) 细胞实验分组与检测指标:用白细胞介素1β(10 μg/L)
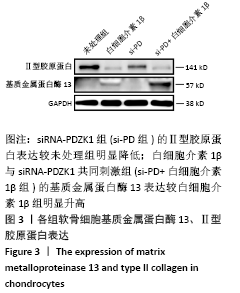
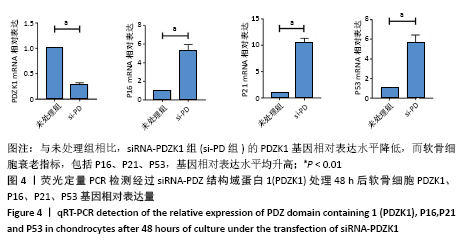
构建骨关节炎的体外细胞模型,并利用siRNA-PDZK1敲低PDZK1,共分为未处理组、白细胞介素1β处理组(白细胞介素1β组)、siRNA-PDZK1组(si-PD组)、白细胞介素1β与siRNA-PDZK1共同刺激组(si-PD+白细胞介素1β组)。检测软骨细胞的PDZK1、Ⅱ型胶原a1、基质金属蛋白酶13以及软骨细胞衰老指标(P16、P21、P53)的表达量。

(3)白细胞介素1β刺激软骨细胞:将小鼠原代软骨细胞培养至第2代,待细胞浓度达60%-70%,进行白细胞介素1β刺激,以6孔板为例,每孔加入10 μg/L,每孔细胞数约为2×106,制作骨关节炎体外模型[21]。
(4)细胞转染实验:将小鼠原代软骨细胞培养至第2代,待细胞浓度达60%-70%,进行转染实验。以6孔板为例,先更换细胞培养液,接着配制转染复合物:4 μL(20 μmol/L)siRNA-PDZK1+4 μL促转染试剂+200 μL无血清培养基。静置30 min后,将转染复合物缓慢滴入孔板中,轻轻震荡后,放入细胞培养箱,培养48 h。siRNA-PDZK1:5’-GCA AUG GCU AUG GCU UCU ATT-3’,5’-UAG AAG CCA UAG CCA UUG CTT-3’。
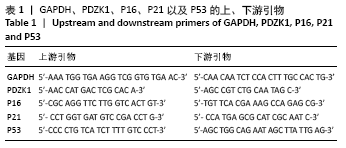
(5)实时荧光定量PCR方法测定PDZK1、P16、P21、P53基因转录水平:取第2代原代软骨细胞,加入1 mL Trizol裂解细胞,静置10 min,加0.2 mL的氯仿,充分混匀后静置5 min再离心,取上层水相加入0.5 mL的异丙醇,轻柔混匀后,离心弃去上清液,用体积分数75%的乙醇清洗离心后自然干燥沉淀RNA,加入DEPC水溶解RNA后,利用紫外分光光度计测量含量及纯度(纯度控制在1.8-2.0)。取Total RNA 1 μg,加入gDNA Clean Reagent 1 μL和 5XgDNA Clean Buffer 2 μL及RNase free H2O,加至液体总量为10 μL,先在42 ℃保温2 min后,再依次加入Evo M-MLVRTase Enzyme Mix 1 μL,RT Primer Mix 1 μL 5X RTase Reaction Buffer Mix I 4 μL RNase free H2O 4 μL。轻轻混匀后,先在37 ℃保温15 min,然后85 ℃保温5 s,得到cDNA 20 μL,选择20 μL的反应体系,分别应用GAPDH、PDZK1、P16、P21以及P53的上、下游引物见表1,对反转录的cDNA进行Real Time PCR反应。反应体系为上、下游引物(10 mol/L)各0.4 μL,模板cDNA 2 μL,ddH2O 7.2 μL,SYBRGreen 10 μL。采用两步法进行PCR反应,反应条件:95 ℃、10 min,1个循环;95 ℃、15 s;60 ℃、1 min,40个循环。反应结束后,采用ABI 7300 Real time PCR软件分析PCR过程,检测样本的Ct值,即PCR扩增过程中扩增产物荧光信号超过基线值(进入指数增长期)时的循环数。以GAPDH为内参照基因,通过2-ΔΔCt法进行相对定量分析。细胞实验结果重复3次。
(6)免疫印迹(Western Blot)
干净的玻璃板准备:使用之前,首先利用体积分数75%乙醇或者去离子水清洗大小2块玻璃板,用吸水滤纸或者干净的眼镜布把液体擦拭干净,然后利用37 ℃的烘箱进行烘干。
SDS-聚丙烯酰胺凝胶的配置:按照厂家说明书的配方,根据所需要胶的数量配制好相应分离胶液体并混匀,将已经混匀的分离胶溶液缓慢加入玻璃板夹层中,尽量不产生气泡,当分离胶的液体顶端距玻璃板上端1.5-2.5 cm时,此时停止添加,并同时加入去离子水覆盖分离胶的顶端,把潜在的气泡去除,将其放在室温中,待分离胶凝固,即去离子水与分离胶之间有一个清晰笔直的边界。然后根据配方和需要的胶数量配制浓缩胶,倾斜玻璃板,倒掉ddH2O,把剩余的ddH2O使用吸水滤纸吸干。将以上配好的浓缩胶液体小心翼翼打入分离胶上,充分覆盖分离胶,把液体加满,将明显的气泡挤出,然后快速轻柔插入用ddH2O洗干净,用吸水滤纸吸干梳子,室温放置40 min左右,等上层浓缩胶凝固后,可以肉眼看到梳子与胶的明显分界。若不马上上样可将配好的胶用去离子水浸湿后包上保鲜膜放于 4 ℃冰箱。
蛋白上样及电泳:从-80 ℃冰箱中取出提取的样品,使用100 ℃金属浴加热5 min,随后快速离心2 min,离心后的样品在加样前先用移液枪充分吹打混匀,根据BCA测得的各个样品浓度,定量上样入上述胶的对应孔中(首次均加入 10 μL),以恒定电流16 mA/胶的条件电泳90-120 min,根据所需目的蛋白的大小,控制好电泳时间,保证蛋白不要跑出泳道。期间使用去离子水和甲醇溶液稀释配置1X的转移液,切记要将其放入-20 ℃冰箱进行预冷。
转膜:将上述电泳完成的胶上的蛋白质转移至PVDF膜上,转膜过程中注意避免产生气泡,造成实验结果条带不清晰,而且夹板的黑色面对着胶,夹板的白色面对着膜,做到胶膜夹的充分贴合。以恒定电压150-220 V的条件转膜 90-120 min,转膜电压和转膜时间要根据目的蛋白大小来调整。
封闭:将转膜完成的PVDF膜放置于封闭液(5%牛奶)中,室温条件下慢摇床封闭1 h,减少抗体的非特异性结合。
孵育一抗:封闭结束后,用1X的TBST涮洗PVDF膜数
秒,按照Ⅱ型胶原a1、基质金属蛋白酶13蛋白分子量裁剪条带,并对应加入配制好的Ⅱ型胶原a1、基质金属蛋白酶13一抗抗体稀释液,稀释比例参考抗体的说明书,在 4 ℃条件下慢摇摇床孵育16-24 h,使抗体与目的蛋白充分结合。
孵育二抗:回收一抗,用1X的TBST清洗液,室温下在快摇摇床上进行3次洗膜,5 min/次。根据二抗说明书配制相应浓度的二抗抗体稀释液,切记二抗抗体稀释液要现配现用,二抗孵育在室温下慢摇床孵育1 h。
软件曝光:用1X的TBST清洗液,室温下在快摇摇床上进行5次洗膜,3 min/次。一般1个条带需要100-200 μL曝光液,取等体积的显示A和显示B工作液,在避光1.5 mL EP管中混匀,配制适量的ECL工作液。软件设置条件下按时间梯度进行曝光。
分析结果:根据内参分析条带的灰度值,来调整下一次上样量。
1.5 主要观察指标 ①建立小鼠骨关节炎模型,分别在实验4,8周取材,首先通过番红O快速绿染色对小鼠进行OARSI评分;接着利用PDZK1免疫组化染色确定骨关节炎中的表达情况;②分离培养C57/BL6乳鼠原代软骨细胞,利用白细胞介素1β与siRNA-PDZK1处理后,通过免疫印迹实验检测PDZK1表达情况以及软骨细胞代谢改变。
1.6 统计学分析 统计学处理均由第一作者进行。采用Microsoft Excel工作表整理汇总实验结果和资料,Adobe Photoshop 2020软件处理图片,GraphPad Prism 8.0.1软件制作统计图,SPSS 20.0软件对数据进行统计分析。对2组数据进行t检验,对3组及以上数据进行One-way ANOVA检验,P < 0.05为差异有显著性意义。