中国组织工程研究 ›› 2018, Vol. 22 ›› Issue (24): 3792-3797.doi: 10.3969/j.issn.2095-4344.0313
• 口腔组织构建 oral tissue construction • 上一篇 下一篇
OTX2基因对hFOB1.19成骨细胞增殖和分化的影响
王 晶1,2,田玉楼2
- 1中国医科大学临床一系,辽宁省沈阳市 110122;2中国医科大学口腔医学院正畸教研室,辽宁省沈阳市 110002
Effect of OTX2 gene on the proliferation and differentiation of hFOB1.19 osteoblasts
Wang Jing1, 2, Tian Yu-lou2
- 1the First Clinical Department of China Medical University, Shenyang 110122, Liaoning Province, China; 2Department of Orthodontics, School of Stomatology, China Medical University, Shenyang 110002, Liaoning Province, China
摘要:
文章快速阅读:
.jpg)
.jpg)
文题释义:
OTX2 基因:定位于染色体14q22.23 区,共含3个外显子,编码由 289个氨基酸构成的转录因子,包含N末端结构域,1个高度保守的同源结构域和C末端转录激活域。其中高度保守的同源结构域为DNA结合域,与 DNA 序列相结合,可形成螺旋-转角-螺旋结构。
基因沉默:RNA干扰技术可以特异性剔除或关闭特定基因的表达,即引起基因沉默,是基因表达调控的一种重要方式,是生物体在基因调控水平上的一种自我保护机制。可利用基因沉默在基因治疗中有效抑制有害基因的表达,达到治疗疾病的目的。
摘要
背景:研究成骨细胞的表达及分化有助于阐明骨性反牙合畸形下颌骨发育过度的分子机制。
目的:应用RNA干扰技术下调成骨细胞系hFOB1.19中OTX2基因的表达,进一步研究OTX2基因对成骨细胞增殖及分化的影响。
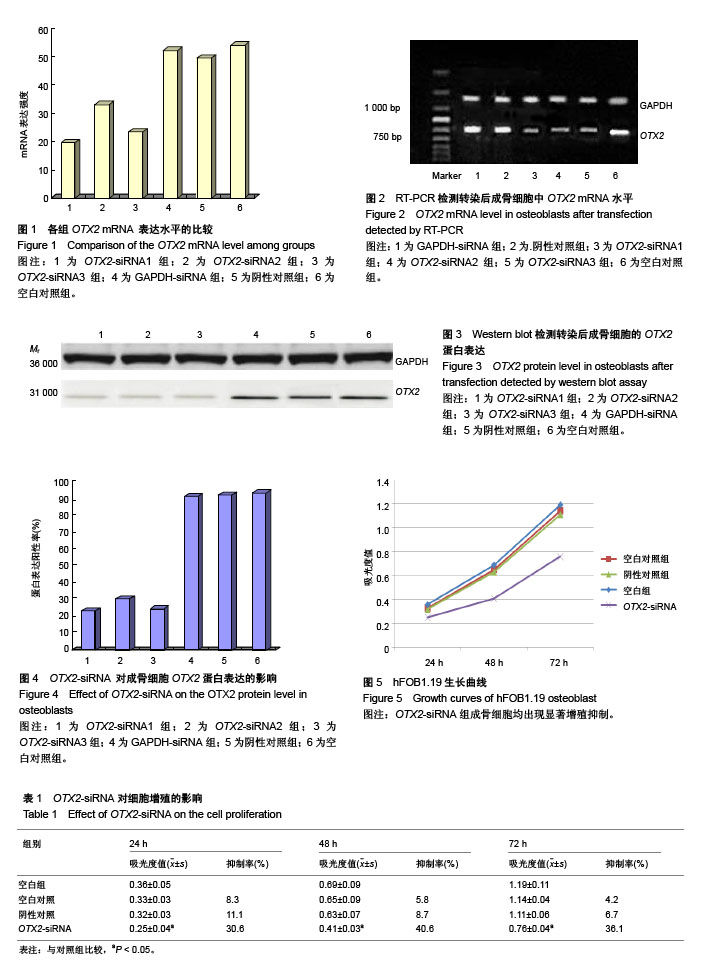
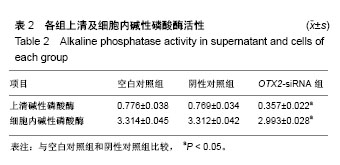
方法:实验分为6组:特异性OTX2-siRNA1、OTX2-siRNA2、OTX2-siRNA3组,GAPDH-siRNA组,阴性对照组和空白对照组。设计3个靶序列的小干扰RNA(iRNA),转染人成骨细胞hFOB 1.19。RT-PCR检测转染后成骨细胞中OTX2 mRNA水平的变化;Western Blot检测蛋白质表达水平;MTT法评估OTX2-siRNA对成骨细胞增殖的抑制作用;化学比色法检测细胞碱性磷酸酶活性。
结果与结论:①转染后,出现OTX2 mRNA水平下调,蛋白表达水平下调;②倒置显微镜下观察漂浮细胞OTX2-siRNA组明显多于各对照组,细胞增殖抑制率明显高于各对照组,OTX2-siRNA组碱性磷酸酶活性明显降低;③结果提示,化学合成的特异性OTX2-siRNA 转染人成骨细胞系hFOB1.19,能有效下调OTX2 mRNA水平;OTX2基因表达下调能够抑制hFOB1.19成骨细胞增殖;OTX2基因表达下调可降低hFOB1.19成骨细胞碱性磷酸酶活性,抑制其分化。
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
ORCID: 0000-0002-9399-4467(王晶)
中图分类号:
.jpg)