1 材料和方法 Materials and methods
1.1 设计 体外和体内分组对照观察实验。
1.2 时间及地点 实验于2014年10月至2016年1月在泰山医学院附属医院骨科研究所完成。
1.3 材料
实验动物:比格犬18只,12月龄,体质量13-15 kg,雌雄不限,北京玛斯生物技术有限公司提供。
试剂及仪器:Ficoll分离液(G&E,瑞士);DMEM、 Hank’s液、胎牛血清、0.25% 胰蛋白酶、双抗(GIBCO,美国);地塞米松、β-磷酸甘油钠、维生素C、MTT(Sigma,美国);CM-Dil(Molecular Probes,美国);碱性磷酸酶 ELISA KIT (96t) DRE-9001、骨钙素ELISA KIT (96t) DRE-9002(优博奥生物科技有限公司,北京);Trizol (Invitrogen,美国);PCR Marker、RNA酶抑制剂(MBI)、焦碳酸二乙酯(DEPC)、反转录酶(M-MLV)、PCR反应缓冲液(10×)、TAE buffer(10×)、dNTPs(4×)、Oligo dT、溴化乙锭(EB)、琼脂糖(Promega, 美国);天然珊瑚(西沙群岛,海南);磷酸三钙(β-TCP)(贝奥路生物材料有限公司,上海);倒置相差显微镜(Olympus,日本);酶标仪(Thermo Electron Corporation, 芬兰);组织匀浆机(GLas-Col Homogenizer, 美国);数控超声波细胞粉碎机(KBS-900)(昆山超声仪器厂,江苏);PCR仪(Bio-Rad,美国);紫外分光光度计(Ultrospec 2100)(GE Healthcare, 瑞典);全自动数码凝胶成像分析系统(UVP BioSpectrum AC,美国);高速恒温冷冻离心机(Hitachi, 日本);激光扫描共聚焦显微镜(TCS-SP2)(徕卡,德国)。
1.4 实验方法
1.4.1 生物支架材料的制备和灭菌消毒
珊瑚支架制备:选取西沙群岛产致密橙黄滨珊瑚,加工成体积为8 mm×6 mm×3 mm大小。用5%次氯酸钠溶液浸泡2周,3 d换液1次,然后用三蒸水冲洗,煮沸10 min×3次,超声清洗(5次,每次10 min)后80 ℃烘干24 h,高温高压灭菌后备用。
β磷酸三钙支架制备:加工成体积为8 mm×6 mm× 3 mm大小,超声清洗后烘干,高温高压灭菌。
1.4.2 骨髓间充质干细胞的分离培养 比格犬以0.12 mL/kg剂量肌注氯胺酮/速眠新(两者2∶1混合)麻醉,常规备皮、消毒、铺巾,用骨穿针于髂后上嵴穿入骨髓腔,然后用含1 mL肝素(50 U/mL)的20 mL注射器负压抽取骨髓液4 mL,加入4 mL Hank’s液混匀,小心加入含4 mL Ficoll淋巴细胞分离液的15 mL离心管中, 2 000 r/min离心20 min,吸取中间白色云雾状的有核细胞层,DMEM洗涤2次,离心后细胞计数,将细胞悬液按1.0×109 L-1细胞浓度接种于直径10 cm的培养皿,置于37 ℃、体积分数5%CO2培养箱内培养,48 h后换液,清除未贴壁细胞,7 d后细胞克隆达80%融合,胰酶消化,按5.0×107 L-1细胞浓度传代。选取第2代细胞备用。
1.4.3 三系诱导分化及鉴定 ①成骨诱导:成骨诱导培养基(10-8 mol/L地塞米松、0.01 mol/L β-磷酸甘油钠、0.05 g/L 维生素C、体积分数10%胎牛血清、1%双抗)培养骨髓间充质干细胞21 d,40 g/L多聚甲醛固定,碱性磷酸酶染色试剂盒染色;体积分数为95%的乙醇固定1 h,2%茜素红染色;40 g/L多聚甲醛固定,加入抗骨桥蛋白一抗和二抗,免疫荧光检测。②成软骨诱导:成软骨诱导培养基(10 μg/L转化生长因子β1、40 μg/L地塞米松、50 μg/L维生素C、体积分数10%胎牛血清、1% 双抗)诱导培养14 d,40 g/L多聚甲醛固定,甲苯胺蓝、番红O染色;40 g/L多聚甲醛固定,加入抗Ⅱ型胶原一抗和二抗,免疫细胞化学检测。③成脂诱导:成脂诱导培养基(0.5 mmol/L IBMX、10-5 mol/L胰岛素、0.2 mmol/L吲哚美辛、10-6 mol/L地塞米松、体积分数10% 胎牛血清、1% 双抗)诱导培养14 d,40 g/L多聚甲醛固定,60% 异丙醇处理,油红O染色。
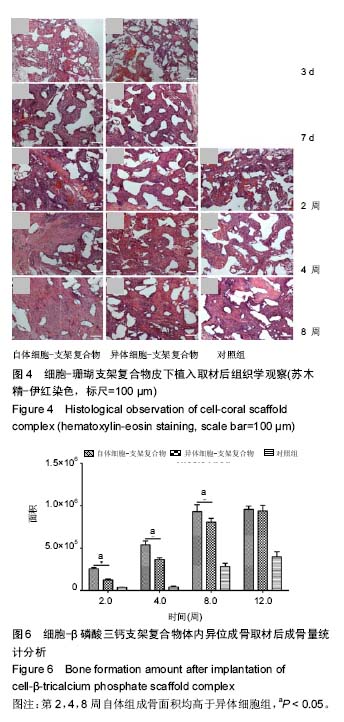
1.4.4 CM-Dil标记骨髓间充质干细胞 收集P2代骨髓间充质干细胞制成细胞浓度为1.0×1010 L-1细胞悬液(PBS悬浮),每1 mL细胞悬液中加入40 μL CM-Dil(1 g/L),此时CM-Dil的终浓度为40 μmol/L。细胞悬液置于37 ℃,3 min,然后冰浴15 min,洗涤后按5.0×107 L-1的细胞浓度接种到培养皿中。24 h后,荧光显微镜下观察标记后的细胞,MTT法检测细胞的增殖能力。
1.4.5 细胞接种珊瑚、β磷酸三钙支架材料 收集CM-Dil标记的骨髓间充质干细胞,分别以2.0×1010 L-1的细胞浓度接种珊瑚、β磷酸三钙支架,成骨诱导培养基体外培养3 h、3 d、7 d,2.5%戊二醛固定,乙醇脱水干燥,扫描电镜观察材料的孔隙率和接种后细胞-材料的黏附情况。复合物成骨诱导培养7 d后比格犬皮下植入(植入前12 h更换无胎牛血清的培养基,以减少外源性胎牛蛋白植入后对受体造成的影响)。
1.4.6 细胞-支架复合物比格犬背部皮下植入及检测 比格犬术前12 h禁食,并肌肉注射青霉素预防感染(剂量为80×104 U)。氯胺酮/速眠新(两者以体积比2∶1混合)以0.12 mL/kg的剂量肌肉注射进行诱导麻醉后,动物俯卧位放置并固定到手术台上,常规备皮、消毒、铺无菌巾,暴露手术视野。确定切口位置,犬背部正中上次齐平肩关节,下侧与两侧髂前上棘水平,在正中线上平均做3个约4 cm的纵行切口,电凝充分止血,掀起皮肤,用大血管钳和组织剪分别向两侧分层分离皮下、浅筋膜,达到脂肪层浅层,血管钳扩大范围形成约5 cm×5 cm的皮下腔隙(皮袋)。体外成骨诱导培养的细胞-支架复合物用0.9 %的盐水小心将表面的培养基冲洗干净,放入预先形成的皮袋中。用庆大霉素和生理盐水冲洗切口及周围皮下组织,逐层关闭切口,医用缝线分层缝合。术后肌肉注射青霉素(每次80×104 U,每天2次,连续5 d)以预防感染。
1.4.7 实验分组 根据比格犬供、受体配对的情况,按照比格犬植入的骨髓间充质干细胞来源不同,实验分为3组,自体细胞-支架复合物组(autologous BMSCs- tissue engineering bone,Auto-TEB)、异体细胞-支架复合物组(allogeneic BMSCs-tissue engineering bone,Allo-TEB)和空白支架材料对照组。每组3只比格犬,每只犬背部6个皮袋,每个皮袋中放入2块细胞-支架复合物。
1.4.8 取材及检测 分别于术后3 d及术后1,2,4,8,12周对每组3只犬背部皮下植入的组织进行取材(由于珊瑚支架降解速率快,术后取材进行到第8周),手术方法同上。每个时间点取出每只犬一个皮袋内的2块细胞-支架复合物,用生理盐水将表面的血液冲洗干净,手术刀小心平均切为2块,其中一块放入体积分数4%的中性甲醛中固定,另外一块快速投入液氮中,然后转移到 -80 ℃低温冰箱中冷冻保存。
1.5 主要观察指标
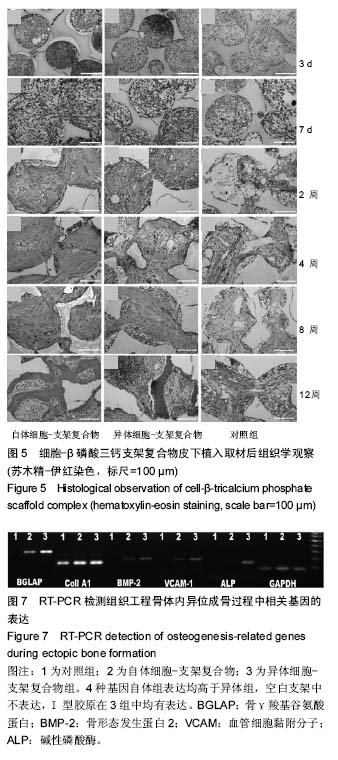
1.5.1 苏木精-伊红染色及成骨面积分析 标本甲醛固定后行石蜡连续切片、苏木精-伊红染色,倒置相差显微镜下下观察自体和异体骨髓间充质干细胞构建的组织工程骨在比格犬皮下异位成骨的情况,以及局部淋巴细胞的浸润。
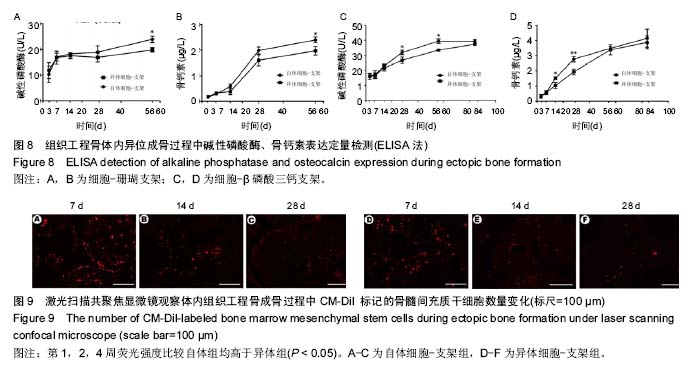
骨髓间充质干细胞-β磷酸三钙在体内2,4,8和12周异位构建的组织工程骨,于高倍镜下(200×)对每个标本随机选取20个视野,应用软件Image-Pro Plus 6.0.计算其成骨面积并对数据进行统计学分析。
1.5.2 RT-PCR检测组织工程骨植入体内相关基因的表达
组织中总RNA的提取:细胞-珊瑚支架复合物植入体内4周后取材,快速投入液氮中。硬组织置于含有1 mL Trizol的离心管中,用组织匀浆器进行匀浆,直至匀浆液呈无颗粒透明状,将细胞裂解液转移到eppendorf 管中。室温下静置5 min后,4 ℃12 000×g离心10 min,取上清液,加入200 μL四氯甲烷,剧烈振荡15 s后室温下静置10 min,4 ℃ 12 000×g离心15 min。此时管中液体分为3层(无色的上清水相、中间白色层和粉红色下层有机相),小心转移上层水相到另一eppendorf管中,加入等体积的异丙醇,混匀后室温放置10 min,4 ℃ 12 000×g离心10 min。弃上清,加入1 mL体积分数75%的乙醇,轻轻混匀后4 ℃ 12 000×g离心5 min,重复2次。小心移走上清,室温下干燥沉淀,加入ddH2O溶解沉淀后-70 ℃保存。
RNA的反转录(cDNA):取提取的RNA样品,用1×组织工程骨 Buffer稀释样品100倍,测定样品在260 nm和280 nm的吸光度值,以确定提取RNA的质量,并计算RNA的浓度,调整各组RNA浓度为200 mg/L。反转录反应体系为20 μL。反转录反应程序为:65 ℃ 5 min,37 ℃ 2 min,37 ℃ 60 min,70 ℃ 15 min。
聚合酶链式反应(PCR):PCR反应程序及产物电泳检测同上,并应用软件对电泳条带进行灰度扫描和半定量分析。
1.5.3 细胞-支架复合物成骨过程中碱性磷酸酶、骨钙素体内表达定量检测 用酶联免疫吸附测定(ELISA)的方法对犬体内组织工程骨成骨过程中的碱性磷酸酶、骨钙素表达进行检测。标本从-80 ℃低温冰箱中取出,解冻后用精密电子天平称质量,使每块标本质量为0.05 g,放置于EP管中,PBS冲洗干净后加入Tris-HCl缓冲液(pH=7.4) 0.5 mL,研磨标本,超声震荡粉碎(45 s,间隔9 s,4 ℃),然后取混合震荡液用ELISA试剂盒进行检测。具体步骤如下(以碱性磷酸酶为例):①稀释标准品(10,20,40,80,120 U/L);②加样:空白孔只加入显色剂A、B和终止液;标准品孔加入标准品50 μL和链霉素亲和-HRP 50 μL;待测样品孔加入样品40 μL、抗碱性磷酸酶抗体10 μL和链霉素亲和-HRP50 μL (注意设置足够的复孔)。盖上封板膜后轻轻振荡混匀,37 ℃温浴60 min;③洗涤:揭开封板膜,弃去液体并甩干,每孔内加满洗涤液(30×浓缩洗涤液用蒸馏水稀释30倍),静置30 s后弃去,重复5次,甩干;④显色和终止:每孔依次加入显色剂A 50 μL、显色剂B 50 μL,振荡混匀后37 ℃ 避光显色10 min。每孔加入终止液50 μL终止反应(液体颜色由蓝色变为黄色);⑤测定:应用酶标仪检测,空白孔调零,450 nm波长下测量各孔的吸光度值(A值)。根据标准品浓度和对应的A值绘制标准曲线并计算其直线回归方程(应用软件CurveExpert 1.3),再根据待测样品的A值在回归方程上计算出对应的样品浓度。
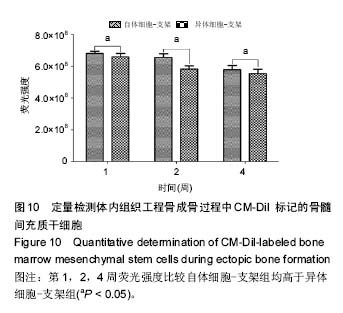
1.5.4 比格犬体内植入骨髓间充质干细胞(CM-Dil 标记)的示踪观察 取石蜡切片标本(选取1,2,4周3个时间点),彻底脱蜡(温度控制在37 ℃)后用DAPI染核,置于激光扫描共聚焦显微镜下观察。以空白对照切片(骨髓间充质干细胞未标记)进行荧光调零,除去其他组织细胞的荧光干扰,CM-Dil标记的骨髓间充质干细胞在波长488 nm处被激发出红色荧光,结合光镜下图像和DAPI染核后的蓝色细胞核,应用显微镜配置软件Volocity Demo5.4 (32bit) 进行荧光强度分析。
1.6 统计学分析 应用SPSS 16.0统计软件包对实验数据进行统计学分析。所测数据以x±s表示,各样本总体进行正态性检验和方差齐性检验,多样本均数比较采用单因素方差分析,组间两两比较采用Post Hoc分析的LSD、Bonferroni检验,以及两独立样本的t检验,P < 0.05认为两组间差异有显著性意义。
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
.jpg) 文题释义:
同种异体移植:是指同种不同基因型个体之间的移植,是临床最常见的移植类型,也是移植免疫学研究的重点所在。
磷酸三钙:又称磷酸钙。化学式Ca3(PO4)2。白色晶体或无定形粉末。存在多种晶型转变,主要分为低温β相(β-TCP)和高温α相(α-TCP),相转变温度为1 120-1 170 ℃,熔点1 670 ℃;溶于酸,不溶于水和乙醇。在人的骨骼中普遍存在,是一种良好的骨修复材料。
文题释义:
同种异体移植:是指同种不同基因型个体之间的移植,是临床最常见的移植类型,也是移植免疫学研究的重点所在。
磷酸三钙:又称磷酸钙。化学式Ca3(PO4)2。白色晶体或无定形粉末。存在多种晶型转变,主要分为低温β相(β-TCP)和高温α相(α-TCP),相转变温度为1 120-1 170 ℃,熔点1 670 ℃;溶于酸,不溶于水和乙醇。在人的骨骼中普遍存在,是一种良好的骨修复材料。.jpg) 文题释义:
同种异体移植:是指同种不同基因型个体之间的移植,是临床最常见的移植类型,也是移植免疫学研究的重点所在。
磷酸三钙:又称磷酸钙。化学式Ca3(PO4)2。白色晶体或无定形粉末。存在多种晶型转变,主要分为低温β相(β-TCP)和高温α相(α-TCP),相转变温度为1 120-1 170 ℃,熔点1 670 ℃;溶于酸,不溶于水和乙醇。在人的骨骼中普遍存在,是一种良好的骨修复材料。
文题释义:
同种异体移植:是指同种不同基因型个体之间的移植,是临床最常见的移植类型,也是移植免疫学研究的重点所在。
磷酸三钙:又称磷酸钙。化学式Ca3(PO4)2。白色晶体或无定形粉末。存在多种晶型转变,主要分为低温β相(β-TCP)和高温α相(α-TCP),相转变温度为1 120-1 170 ℃,熔点1 670 ℃;溶于酸,不溶于水和乙醇。在人的骨骼中普遍存在,是一种良好的骨修复材料。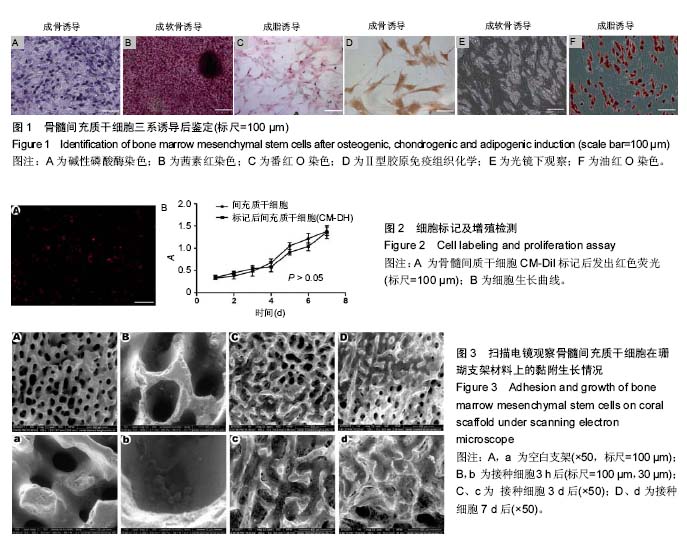
.jpg) 文题释义:
同种异体移植:是指同种不同基因型个体之间的移植,是临床最常见的移植类型,也是移植免疫学研究的重点所在。
磷酸三钙:又称磷酸钙。化学式Ca3(PO4)2。白色晶体或无定形粉末。存在多种晶型转变,主要分为低温β相(β-TCP)和高温α相(α-TCP),相转变温度为1 120-1 170 ℃,熔点1 670 ℃;溶于酸,不溶于水和乙醇。在人的骨骼中普遍存在,是一种良好的骨修复材料。
文题释义:
同种异体移植:是指同种不同基因型个体之间的移植,是临床最常见的移植类型,也是移植免疫学研究的重点所在。
磷酸三钙:又称磷酸钙。化学式Ca3(PO4)2。白色晶体或无定形粉末。存在多种晶型转变,主要分为低温β相(β-TCP)和高温α相(α-TCP),相转变温度为1 120-1 170 ℃,熔点1 670 ℃;溶于酸,不溶于水和乙醇。在人的骨骼中普遍存在,是一种良好的骨修复材料。