前交叉韧带重建是治疗前交叉韧带损伤是的主要手段,采用肌腱移植物做为前交叉韧带重建的材料是目前的主流选择;其中移植物与骨隧道牢固的愈合是前交叉韧带重建手术成功的关键之一。但是,许多动物实验研究发现,肌腱移植物与骨隧道达到完全可靠的腱-骨愈合需要12-24个月甚至更长时间
[6-9]。
在美国每年前交叉韧带重建的手术约10万例以上,但每年翻修手术高达3 000-10 000例,其中肌腱移植物在骨隧道内延迟愈合就是主要原因之一[10-11]。此外,术后为了使移植物经历坏死、重新血管化、胶原纤维爬行替代、塑型等过程,最后成为类似于交叉韧带生物特性的替代韧带以及腱移植物与骨隧道的牢固愈合,膝关节需要较长时间的限制活动,从而引起后期关节功能康复锻炼的困难、甚至关节功能恢复的不理想。
如何早日使腱移植物与骨隧道牢固愈合以及移植物尽快完成爬行替代、塑型过程,减少患者膝关节固定时间,使其早日进行功能锻炼并恢复关节功能是临床骨科研究的热点之一。
目前,促进腱移植物与骨隧道愈合的方法主要包括:骨膜包裹肌腱移植物、生物活性因子、磷酸钙、骨髓间充质干细胞、低强度脉冲超声波、体外冲击波及基因工程治疗等[12-26]。以上各种促进腱骨愈合的方法均对移植物在骨隧道内的愈合起一定作用,但作用机制还需更深入的研究。
如骨膜内多能干细胞的质量和数量直接影响骨膜对腱骨愈合的促进作用,如何最大程度发挥骨膜内多能干细胞的活性对腱骨愈合起重要作用;关节腔内注射生物活性因子受关节活动和关节内滑液稀释影响,如何保证生物活性因子的有效浓度是其发挥促进腱骨愈合作用的关键;而如何保证骨髓间充质干细胞在腱骨界面更长时间存留,尚需寻找更合适的载体,防止间充质干细胞从腱骨界面流失及减少载体对移植物愈合的影响;低强度脉冲超声波和体外冲击波均存在作用强度、作用频率及作用部位和时间的选择;基因技术及组织工程的应用可能是肌腱移植重建交叉韧带后促进腱骨愈合的一个研究方向,但离临床应用还很遥远。以上各种促进 腱-骨界面愈合的方法均对移植物在骨隧道内的愈合起积极作用,但作用机制仍需更深入的研究。所以,目前尚无经济、安全、可靠并大规模应用于临床促进腱-骨愈合的方法。
这次实验在兔前交叉韧带重建的关节内施加间歇性的低强度负压,通过观察腱-骨界面组织学改变、移植物的强度及关节内滑液中白细胞介素1β的水平,初步研究负压对腱-骨界面愈合肌腱移植物强度的影响。
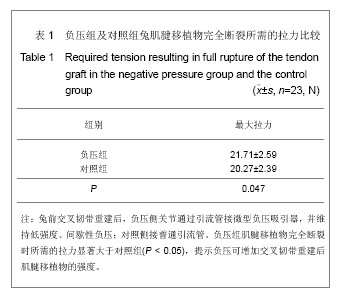
本实验结果提示,术后6周,负压组腱-骨界面成骨细胞显著多于对照组;拉力测定中,负压组肌腱移植物自骨隧道拉出数目少于对照组,同时移植物的强度显著高于对照组。这些结果证实,间歇性负压可能会促进交叉韧带重建后腱-骨愈合及移植物的塑性替代过程。这主要可能与负压所形成的机械性刺激和缺氧有关,机械性刺激是细胞生长过程中受到的基本刺激之一,它可以对细胞分化和增殖产生重要的影响,许多体外实验已经证实机械刺激可以促进细胞成骨分化[27-29],应力刺激也 能通过促进成骨细胞增殖、分化等多种途径促进骨的形成[30]。另外,关节内维持负压环境势必造成组织细胞缺氧,研究发现低氧能提高大鼠骨髓间充质细胞骨形成能力[31]。
在以往的研究中证实低强度间歇性负压可以成功的诱导人骨髓间充质干细胞向成骨细胞定向分化,诱导的细胞具有典型的成骨细胞特性[1];同时间歇性负压具有抑制骨吸收、促进成骨的作用[2]。
作者推测,与正常对照相比,当关节腔内维持间歇性负压,更多的骨髓间充质干细胞间歇进入关节腔侧的腱-骨界面并向成骨细胞转化;同时负压抑制腱-骨界面的骨吸收,促进其成骨,从而促进了腱-骨界面愈合。
此外,本文发现,负压组关节液中白细胞介素1β水平显著低于对照组。关节液由滑膜细胞产生分泌,含胶原蛋白、透明质酸、蛋白多糖、滑液内正常细胞和一些脱落的滑膜表皮细胞、酶等物质,不含凝血因子和纤维蛋白,正常关节液的主要功能是润滑和向软骨细胞提供营养物质,同时降解和清除关节内的软骨碎屑。前交叉韧带重建术后,由于手术创伤的刺激引起关节内严重的炎症反应,关节液异常增多,而重建肌腱移植物内无血液供应,也没有腱膜和结缔组织包裹覆盖,关节液中异常增多的大量炎性细胞和炎症因子等直接与之接触,不利于韧带的愈合,抑制了肌腱移植物的爬行替代,所以韧带强度急剧下降。同时,理化性质异常的关节液进入肌腱与骨隧道之间的缝隙,其中的炎症因子,白细胞介素1、肿瘤坏死因子α及基质金属蛋白酶等可降解骨组织,抑制了腱-骨愈合[32]。
Cameron等[33]研究也认为关节液是引起骨隧道内骨质溶解,隧道扩大的重要因素之一。也有学者认为关节滑液对腱-骨愈合无显著影响[34]。但最新的研究发现股骨隧道内腱-骨愈合优于胫骨端骨隧道,提示关节滑液不利于了腱-骨界面愈合[35],本实验结果支持此结论。
白细胞介素1由单核细胞、巨噬细胞和滑膜缅胞等细胞产生[36],是关节组织损伤的重要介质。此外,白细胞介素1可以刺激肿瘤坏死因子α、白细胞介素6、白细胞介素8及基质金属蛋白酶的分泌[37-38],加重关节内结构的损伤。Henderson等[39]研究认为白细胞介素1抑制剂能够抑制滑膜炎症和软骨破坏,提示关节液内的白细胞介素1会破坏关节内结构,对腱-骨愈合产生不利影响。
作者认为,间歇性的负压吸引不仅可以减少关节液的量,特别是使重要的炎症白细胞介素1β水平的明显降低,间接减少了其他炎症递质的释放,抑制了骨和肌腱移植物的破坏及降解,从而促进了腱-骨界面愈合及肌腱移植物的爬行替代。
在负压大小和模式的选择方面,根据前期的文献提示60-80 kPa的负压有利于缩小创面,促进肉芽组织迅速生长,有利于创面愈合[40],负压通过刺激血管生成、改善组织血供,促进细胞及肉芽组织生长,从而加速软组织创面愈合[41]。50 kPa 体外间断性负压可以抑制骨保护素配体的表达,同时促进骨髓基质细胞骨保护素 mRNA的表达[1]。在一项研究中发现,在没有负压的情况下血管内皮细胞迁移受限,而负压条件下血管内皮细胞的增殖和迁移明显增加,间歇性负压效果优于连续性负压[42]。
此外,作者认为,兔前交叉韧带重建关节内创伤较大,术后持续性负压必然会导致大量的血液及体液的丧失,不利于兔前交叉韧带重建术后创伤的愈合,故本实验选择50 kPa 体外间断性负压施加干预。
关于负压维持时间,作者这次实验选择5 d,因为引流管放置时间过长容易引起关节感染,实验中就发生了1只兔关节感染导致前交叉韧带重建失败,故选择引流管放置5 d。
到目前为止,未见将间歇性负压技术应用到前交叉韧带重建动物模型的研究报道。本实验发现,负压组 腱-骨界面成骨细胞显著多于对照组,同时移植物的强度显著高于对照组;并且负压组关节液中白细胞介素1β水平显著低于对照组。
总之文章结果提示,间歇性负压可能在前交叉韧带重建术后腱-骨界面愈合、肌腱移植物的塑性及爬行替代中扮演着积极作用,其作用机制是多方面的,这需要进一步深入研究其具体机制及筛选更适宜的负压大小及频率。


.jpg)