Chinese Journal of Tissue Engineering Research ›› 2014, Vol. 18 ›› Issue (21): 3391-3397.doi: 10.3969/j.issn.2095-4344.2014.21.020
Previous Articles Next Articles
Degradable materials for bone tissue engineering and their vascularization: existing problems and application prospects
Cen Chao-de, Luo Cong
- Department of Orthopedics, Children Hospital of Chongqing Medical University, Chongqing 400014, China
-
Online:2014-05-21Published:2014-05-21 -
Contact:Luo Cong, Associate chief physician, Department of Orthopedics, Children Hospital of Chongqing Medical University, Chongqing 400014, China -
About author:Cen Chao-de, Studying for master’s degree, Department of Orthopedics, Children Hospital of Chongqing Medical University, Chongqing 400014, China -
Supported by:the Foundation for Sci & Tech Research Project of Chongqing, No. CSTC2011ggB1004; the National Key Clinical Specialist Construction Programs of China
CLC Number:
Cite this article
Cen Chao-de, Luo Cong. Degradable materials for bone tissue engineering and their vascularization: existing problems and application prospects[J]. Chinese Journal of Tissue Engineering Research, 2014, 18(21): 3391-3397.
share this article

2.1 可降解支架材料 人体骨是胶原蛋白与羟基磷灰石的天然复合物,皮质骨的孔隙率为10%-30%,松质骨的孔隙率为30%-90%。微孔的直径也大小不一,小径微孔直径小于20 µm,大径微孔直径大于100 µm。皮质骨的杨氏模量为15-20 GPa,松质骨为0.1-2.0 GPa。皮质骨的抗压强度为100-200 MPa,松质骨为2-20 MPa[2]。理想的支架材料除了机械参数与人体骨相似外,还应具备以下条件[3]:材料表面结构及性质有利于细胞吸附、增殖和分化;良好的生物相容性;降解速度与新组织的产生相匹配,降解产物无毒、易被人体吸收或排出体外;易制成三维多孔状及加工成不同的几何形态以满足临床的应用;能保持对细胞的分化,不会使细胞产生变异;具备生物活性,即支架材料能与活体骨化学键合产生生物性羟基磷灰石层;具备骨传导性;具备骨诱导性。 如表1所示,目前常用的材料可分为高分子材料与可吸收陶瓷。此外,近年来,随着研究的深入,金属材料在骨组织工程材料中的应用也日益广泛。"

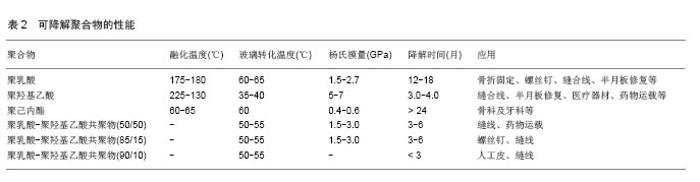
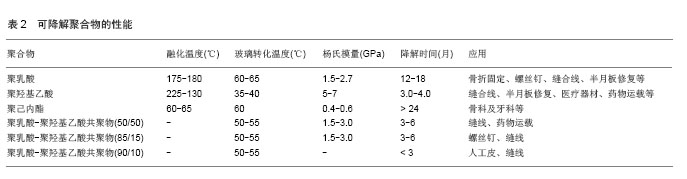
2.1.1 可降解高分子材料 可降解高分子材料根据来源不同可分为天然高分子材料与合成高分子材料。多糖类如壳聚糖、海藻酸盐及透明质酸的衍生物,蛋白质类如胶原、丝素蛋白及纤维蛋白等都属于天然高分子材料,由于它们较高的生理活性,降解速率不可控,机械性能较差等因素限制了其在研究中的应用。合成高分子材料可弥补天然高分子材料的不足适合于各方面的应用。 目前常用的可降解合成高分子材料包括聚乳酸、聚羟基乙酸、聚乳酸-聚羟基乙酸共聚物、聚β-羟基丁酯、聚己内酯、聚富马酸羟基丙酯、聚对二氧六环酮等,其性能见表2。聚乳酸、聚羟基乙酸及其二者的复合物因具备良好的生物相容性、机械性能,降解产物无毒等优点已获得美国FDA的批准用于临用缝线、暂时性支架及药物控释载体。聚乳酸-聚羟基乙酸共聚物可通过肝肾代谢,其终产物为CO2和H2O。然而有研究表明,作为聚乳酸-聚羟基乙酸共聚物降解中间产物的羟基乙酸,在局部聚集可导致局部酸度增大,这又会加速聚乳酸-聚羟基乙酸共聚物的降解速度,从而形成恶性循环,最终引发无菌性炎症[4]。 聚己内酯是一类可降解的脂肪族聚酯,具备良好的力学性能、热稳定性和生物相容性,其降解产物对人体无害,目前被广泛应用于组织工程支架材料领域。由于聚己内酯具有较高的结晶度,导致其相比于聚乳酸及聚羟基乙酸更不易降解,仅通过改变其分子量大小难以控制其降解速率。因此,聚己内酯适合于充当长期的移植物。聚己内酯具有药物渗透性,可用作药物缓释载体。 聚富马酸羟基丙酯是一种不饱和线型聚酯,其重复单位中包含一个不饱和双键,可以进行共价交联反应,含有两个脂基团,可以水解生成富马酸和丙二醇,其降解产物可通过正常新陈代谢排出体外,并且对体内系统如pH值等没有影响[5]。由于聚富马酸羟基丙酯可生物降解并在体温下能任意塑型,以及固化前具有良好的流动性,因此可将其作为一种可注射式填充材料用于骨缺损部位修复和重建,其缺陷是反应条件不易控制。 聚对二氧六环酮是另一类可降解的高分子材料,由于其良好的生物相容性及机械性能被广泛应用于骨折内固定及药物控释。随着聚对二氧六环酮的降解,新骨可沉积于支架表面。通过控制其结晶度、分子量及融化温度可调整其降解时间在180-200 d[6] 。 聚β-羟基丁酯也是一类可降解材料,是微生物在不平衡生长条件下储存于细胞内的一种天然高分子材料。人工合成聚β-羟基丁酯也可降解,具有较高的立构规整度,已作为可降解树脂被广泛应用于医学领域。但脆性较大,可与其他高分子材料复合使用降低其脆性及融化温度。在体内降解产物为3-羟基丁酸,是人体血液内的固有成分,其最终经酮酵解为CO2和H2O,体内降解时间为1/2-2年[7] 。 2.1.2 可降解镁合金 自Sir Humphrey Davy 1808年发现金属元素镁以来,镁已被广泛应用于研究,如缝线、血管吻合器、动脉瘤介入及移植材料等。金属镁生物相容性好,机械性能较佳,易被机体侵蚀后重吸收或排除体外。相比于钛合金、钴合金等,它与生理骨有相似的弹性模量及密度,可避免材料与人体骨弹性模量不匹配导致的应力效应[8] 。目前常用的镁合金有Mg-Ca合金,Mg-Zn合金等。锌离子是骨形成过程中重要的微量元素,可通过提高Mg的电荷转移电阻增加Mg的耐腐蚀性能[9] 。Mg-6%Zn的抗张强度和拉伸率分别为279.5 MPa和18.8%,以2.32 mm/年降解速率的降解,降解产物可被机体吸收。而钙是骨骼发育的基本原料,大部分以羟基磷酸钙的形式存在,人体骨的硬度与骨钙的含量有直接的关系。Mg-1%Ca无细胞毒性,植入兔股骨缺损模型可观察到支架周围成骨细胞活性增强,表现出了良好的生物相容性和生物活性[10] 。 "

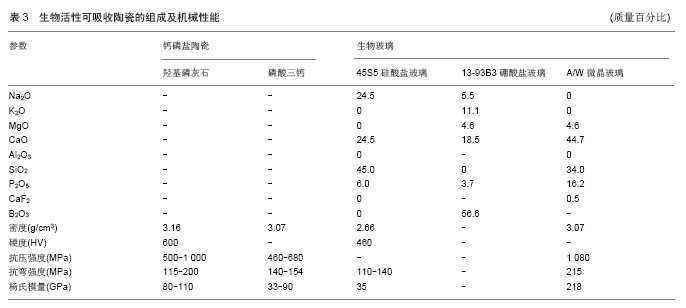
2.1.3 可降解生物活性玻璃 生物活性玻璃首次由Hench制造出来,是生物活性玻璃通过控制微晶化处理制得的单晶或多晶磷灰石晶体,具有致密的微晶结构、较高的机械强度、较低的溶解度及较好的生物亲和性。将其植入人体或动物体后,可逐渐形成与骨组织能够化学键合的生物性羟基磷灰石层,其组成及机械性能见表3。 生物玻璃按其成分可分为硅酸盐玻璃(45S5)、硼酸盐玻璃(13-93B3)及磷酸盐玻璃,生物玻璃可通过调整其组成成分的种类及比例控制其降解速率。研究发现45S5可促进新骨在骨与移植物之间界面的生长,也可促进新骨向偏离界面的移植物中生长,故其既具有骨传导性又具有骨诱导性。13-93B3是将B2O3替代了45S5中的SiO2而制成的生物玻璃,随着B2O3比例的增加,生物玻璃转化为羟基磷灰石的比例越大,其中13-93B3可以完全转化为羟基磷灰石[11]。 A/W微晶玻璃是含磷灰石、硅灰石晶相及玻璃相,成分为MgO-CaO-SiO2-P2O5-CaF2的微晶玻璃陶瓷,具有良好的生物相容性、生物亲和性、一定的生物降解性和较高的生物力学性能。溶胶-凝胶法可制备多孔A/W微晶玻璃,利于细胞组织生长,改善其物降解性能和骨传导性,目前被广泛应用于承重骨替代,脊椎假体、胸、额骨修复和骨缺损修复。 2.1.4 可降解钙磷盐陶瓷 钙磷盐陶瓷的结构成分与人骨组织中的无机质相似,故其生物相容性和骨传导性良好。钙磷盐陶瓷研究最多的是羟基磷灰石、磷酸三钙及二者的复合物双相磷酸钙陶瓷。脆性大,不易成形,体内降解困难,而β-磷酸三钙在体内的降解速度较快,与新骨生长速度不匹配。双相磷酸钙陶瓷的骨传导效应优于单一的羟基磷灰石或磷酸三钙,它是羟基磷灰石的强度与磷酸三钙生物降解的结合。(80±3)%的羟基磷灰石与(20±3)%的β-磷酸三钙通过聚合复型法可制备出孔隙率为70%的支架,其中68%微孔直径为400 nm,2%为0.7 μm,该类结合大径与小径微孔的支架植入免疫缺陷小鼠体内可明显促进骨的生成[12]。通过微波烧结3D打印技术制备的孔隙>60%的磷酸三钙支架,不仅可以加速成骨细胞的增殖,还可促进新骨组织在微孔的沉积[13]。目前研究显示在钙磷盐陶瓷中添加掺杂物可改善支架的机械性能、降解速率及生物相容性,如将SiO2 (0.5%)和ZnO (0.25%)加入β-磷酸三钙支架后可以使其压缩强度增大2.5倍,11 d后种子细胞存活率仍可高达92%[14]。 2.1.5 复合支架 复合支架是由不同类型的两种或两种以上材料制备而得,如陶瓷与高分子材料的复合。高分子材料可增加钙磷盐陶瓷的韧度与压缩强度,使其更接近天然骨的特点,而钙磷盐陶瓷较低的磨耗率可改善高分子材料的机械性能及生物活性。Roohani-Esfahani等[15]研究示,经羟基磷灰石/聚己内酯复合材料表面修饰后的双向磷酸钙陶瓷多孔支架可表现出更佳的压缩强度。Fu等[16]将聚己内酯-聚乙二醇-聚己内酯与30%的纳米羟基磷灰石复合,通过静电纺丝技术制备而得的聚己内酯-聚乙二醇-聚己内酯/纳米羟基磷灰石具备良好的骨引导生成能力。由于金属元素可改善钙磷盐陶瓷的压缩强度,因此将两者复合的研究也较多。Song等[17]将碱性金属Na、K、Sr引入聚磷酸钙支架,制备K/Sr-聚磷酸钙或Na/Sr-聚磷酸钙支架。与纯聚磷酸钙支架组相比,体外实验发现碱性金属可促进聚磷酸钙支架的降解,成骨细胞增殖明显。扫描电子显微镜观察到支架表面有磷灰石样矿物质沉积,支架的压缩强度也得到了提高。 在药物缓释方面,高分子材料涂层常用于陶瓷支架表面以控释支架表面药物。近年来,研究者发现高分子材料涂层可改善材料的亲和性,使材料与药物得以共价结合,增强材料与药物之间的相互作用[18]。Xue等[19]观察到用聚己内酯涂层的β-磷酸三钙不仅强度得到了改善,而且还观察到吸附于材料表面的血清蛋白可持久、可控地释放。 2.2 支架的血管化策略 骨移植后修复的基本过程是组织工程骨血管化、骨再生及骨端融合[20]。支架植入体内后,体积较小支架可通过周围组织血管长入,使其与周围组织建立血液循环并获得营养,但这种供养范围仍很有限,因为种子细胞的存活范围仅在血供弥散150-200 μm内[21];而体积较大支架植入后很难依靠周围组织血管的长入建立血液供应,由于缺血缺氧,种子细胞会很快坏死而导致移植物失效。 人体内新生血管形成基于血管生成和血管形成两个过程[22]。前者是指血管的生长来源于已经存在的微血管内皮细胞,通过已经存在的血管通过出芽及微血管融合生长等方式来进行的。后者指血管内皮细胞来源于其前体细胞—内皮祖细胞,由内皮祖细胞发育成成熟的内皮细胞,进而细胞在无血管的区域增殖并创造血管网络。过去一般认为此种方式只存在于胚胎期,后来Asahara等[23]从动物实验模型中提取出内皮祖细胞,证实了组织工程骨两种血管化机制共存的理论。基于以上理论,目前可通过以下几个方面来促进组织工程骨的血管化。 2.2.1 支架构建 组织工程骨支架的多孔性、孔径大小及孔隙率对血管新生有很大影响。松质骨内血管生长速率是0.2-0.4 mm/d,皮质骨再血管化的最大速度为 0.15-0.3 mm/d,这是因为松质骨有开放性的结构。研究表明,孔径大于50 μm的支架有利于氧气与营养物质的交换并排除代谢废物,但细胞的黏附率及细胞之间信号传递会因此降低,而孔径小于10 μm时可取得相反的效果。因此,大径与小径微孔的结合更能促进血管的新生和骨的生成[24]。Bai等[25]实验证实多孔材料促进血管化和成骨细胞黏附、增殖、分化的最佳孔径是400 μm,大于该尺度的孔径对血管新生无显著影响。在孔径90-120 μm的羟基磷灰石中先诱导软骨形成然后再骨化,而在大于350 μm的羟基磷灰石中可以直接诱导骨组织形成。支架孔隙率可影响新生血管的数量及尺寸,而增大孔径只能使新生血管尺寸相应地变大。一般现在对组织工程材料的要求是孔隙率70%左右,孔径100-500 μm,因为较高的孔隙率会降低支架的机械性能。为使支架具备较好的三维结构,目前常用的技术包括纳米静电纺丝、微流控及快速成型技术等。 2.2.2 生长因子 目前已知的促血管化因子主要有血管内皮生长因子、碱性成纤维细胞生长因子、肝细胞生长因子等;另外一些细胞因子,如血小板源性生长因子、转化生长因子β、Ang等,作为间接血管生成因素参与内皮细胞的再生,加速血管化进程。其中研究比较深入的是血管内皮生长因子和碱性成纤维细胞生长因子。血管内皮生长因子家族由多个成员组成,其中VEGF121和VEGF165是主要的分泌成分和效应分子,对内皮细胞的体外增殖和血管生成作用最强。血管内皮生长因子通过旁分泌和自分泌形式产生后,与相应的受体VEGFR-1(Flt-1)、VEGFR-2 (KDR/Flk-1)、VEGFR-3(Flt-4)及NRP结合产生促进血管生成的效应。血管内皮生长因子促进新生血管生成的主要机制有[26]:①产生血管基底膜分解所需要的蛋白酶及特定的整合素,促进内皮细胞的增殖与迁移。②促进骨髓源性的内皮祖细胞聚集和活化。而bFGF的血管生成作用是通过PKC-p44/p42 MAP kinase(MAPK)途径诱导血管内皮生长因子及其受体的表达来实现的[27]。骨形态发生蛋白是一类能促进骨生成的蛋白质,首次由Urist于脱钙骨中提取,被认为是引导成骨过程的启动因子,其中骨形态发生蛋白2,7研究较多,已被美国FDA批准用于临床,但国内学者Kang[28]在美国研究对比了14中骨形态发生蛋白成骨作用的强弱,发现骨形态发生蛋白9的成骨作用最强。 支架的血管化成骨是一系列因子相互作用、共同介导的过程,生长因子多数已被证实具有协同作用,单一的因子不能模拟体内骨再生的复杂过程[29]。传统的向靶区快速注射生长因子的方法也不能很好地模拟体内细胞之间信号的传递,不能在局部根据细胞的功能调节有效的释放细胞因子,快速注射的生长因子容易经体液扩散后被机体分解降低其作用[30]。此外,因子浓度是最关键的问题之一,因子浓度过高可导致肿瘤、动脉粥样硬化及增生性视网膜病的发生,甚至可导致新生血管畸形及阻碍血管生成[31]。 随着分子生物学研究的深入和药物输送技术的提高,生长因子的缓释与控释是目前研究的热点。Solorio等[32]将骨形态发生蛋白2封装入交联的明胶微球,发现人骨髓间充质干细胞表达的骨唾液酸糖蛋白明显升高。然而,因封装的生长因子量有限,无法确保细胞因子持续、持久的释放。将能表达血管内皮生长因子的质粒DNA转染细胞,使细胞能持续表达血管内皮生长因子,是当前促进人工骨血管化的一种乐观的方法。Jabbarzadeh等[33]将载有编码血管内皮生长因子的cDNA通过腺病毒转染人脂肪间充质干细胞,将细胞与PLGA复合,体外实验发现支架内有明显的血管生成。Luo等[34]研究振荡磁场下超顺磁性壳聚糖质粒(pDsVEGF165Red1-N1)明胶控释微球对体内人工骨血管化的影响,发现振荡磁场较静磁场及无磁场条件下血管内皮生长因子释放量及释放时间有增加趋势,初步实现了对生长因子的控释,人工骨支架内部的磁性微动、营养物质交换能有效促进人工骨血管化。 2.2.3 血管内皮祖细胞 血管化的关键环节是内皮细胞的增殖、分化、迁移与聚集。成熟的内皮细胞可从脐带、皮肤、脂肪组织和隐静脉中提取,然而其增殖能力较低,不易获取[35]。此外,大血管上衰老的内皮细胞可能导致细胞信号传导通路中断,降低细胞对成血管生长因子正确的反应能力[36]。目前,骨组织工程研究最多的成血管细胞是内皮祖细胞。内皮祖细胞可通过CD133、CD34和VEGFR2这三种细胞标记物识别出来,该细胞存在于骨髓、脂肪组织和外周血,能分化成为成熟的内皮细胞,参与血管形成和血管生成过程[37]。 内皮祖细胞具有很强的增殖能力及自我更新能力,已被成功用于骨折的修复。Matsumoto等[38]报道了一项内皮祖细胞用于治疗延迟性骨不连的实验。内皮祖细胞可通过骨折区域释放的趋化因子转移并定植该区域,促进该区域血管和骨的生成。为避免内皮祖细胞局部大量增殖分化潜在的不良反应,研究者优化了以上实验方案,将内皮祖细胞种植于股骨骨不连区域,通过粒细胞集落刺激因子的局部释放动员内皮祖细胞的增殖与分化,促进骨愈合。同样地,为使内皮祖细胞能够稳定和持续的发挥作用,需要组成血管其他部件的参与。如将内皮祖细胞种植于PGA-聚左旋乳酸支架,体外观察细胞可保留其分化能力,但只有在培养基中加入血管平滑肌后才观察到支架中微血管网络的形成[39]。` 2.2.4 共培养 在体内骨的形成过程中,血管化与骨生成之间有着复杂的联系。研究发现,单纯内皮细胞生成的微血管网络较内皮细胞与间充质前体细胞共培养时不成熟及不稳定[40]。Wang等[41]将类成骨细胞与人脐静脉内皮细胞共培养,阐明了内皮细胞与成骨细胞的关系。类成骨细胞与人脐静脉内皮细胞共培养可导致成骨细胞数量及碱性磷酸酶活性增加,而1,25-二羟维生素D3又可促进内皮细胞上血管内皮生长因子受体的表达,但是这种现象只存在于类成骨细胞与人脐静脉内皮细胞共培养时,类成骨细胞与人脐静脉内皮细胞单独培养时不出现以上情况。结果证实了osteoblasts 和内皮细胞在骨形成过程相互作用的重要性。Zhou等[42]将间充质干细胞诱导分化的内皮细胞与间充质干细胞共培养于多孔的β-磷酸三钙支架中,然后植入兔尺骨缺损区,发现内皮细胞不仅促进局部血管化,而且加速间充质干细胞的成骨分化。可见血管化是成骨的先决条件,成骨过程可促进血管的生成,细胞共培养无疑是促进组织工程骨血管化的一个重要渠道。 血管内皮细胞和成骨细胞之间复杂的联系贯穿骨折愈合的全过程,共培养系统为微细毛细血管结构形成提供了良好的物理与化学条件,因此可避免外源性血管生成刺激因子的供应。Marina等[43]将成骨细胞与人表皮微血管内皮细胞共培养于SPCL纤维网支架,发现支架可诱发Ⅰ型胶原蛋白mRNA及蛋白的合成,因此证实了Ⅰ型胶原蛋白是为内皮细胞的迁移与分化提供物理与化学信号的关键分子。此外,内皮细胞可上调碱性磷酸酶的表达,促进成骨细胞的分化。共培养的另一个重要的问题是具备直接的细胞接触。实验发现将成骨细胞的条件培养基加入内皮细胞或在共培养时于二者之间用过滤装置隔开,未发现微细毛细血管的形成。Connexin-43 (Cx43)被认为是内皮细胞和成骨细胞之间介导胞内调节离子和小分子交换的缝隙连接蛋白[44]。为更好地模拟人体骨折的修复环境,目前常用的共培养系统包括备皮细胞/成骨细胞,人脐静脉内皮细胞/间充质干细胞、内皮祖细胞/成骨细胞及人表皮微血管内皮细胞/成骨细胞等。 2.2.5 显微外科技术 组织工程骨预制为其血管化提供了可能。“骨瓣预构”是一种通过血管生成的“外部模式”来促进人工骨血管化,包括两个主要阶段:首先将组织工程支架包埋于血管丰富的组织,如皮下、肌内及腹膜下,待支架有充分的微血管网生成时,将支架带蒂游离并植入骨缺损区域,支架血管蒂与骨缺损区血管通过显微外科技术吻合,实现整个支架的瞬间灌注。此类预构骨瓣具有以下明显优点:①可以按照受区形状制成相应的模式。②植入受区后可较快实现与宿主骨的连接。③移植骨内部塑形快,能较快的适应宿主骨的力学环境。④有独立的血供,即使在感染或血液循环差的部位也可存活。⑤能够修复大段骨缺损。然而,此技术也存在一定的缺陷,如需3次手术,花费高,随机的血管化生成模式,血管生成程度高度依赖供区血管条件,供区功能缺失等[45]。 另外一种较可靠的方法是通过血管生成的“内部模式”来促进人工骨血管化,即将适合于显微外科转移的大血管如颈动脉、颈静脉分支、动静脉血管束等植入支架,通过显微外科技术与骨缺损区血管吻合。也可在受区解剖出非主干血管植入材料内,保留近端的血供,不需专门分离血管蒂和行血管吻合。此方法较“骨瓣预构”有更多优点,只需二次手术、不依赖于供区血管条件、定向的血管化生成模式等。但目前支架血管束植入仍存在一定的挑战,如多数负重骨支架不易根据血管束的形状塑形、显微外科吻合技术要求高等。"
| [1]Crane GM,Ishaug SL,Mikos AG.Bone tissue engineering.Nat Med.1995;1(12):1322-1324. [2]Bose S,Roy M,Bandyopadhyay A,et al.Recent advances in bone tissue engineering scaffolds.Trends Biotechnol. 2012; 30(10):546-554. [3]Rahaman MN,Day DE,Sonny Bal B,et al.Bioactive glass in tissue engineering. Acta Biomaterialia.2011;7(6):2355-2373. [4]Lu L,Zhu X,Valenzuela RG,et al.Biodegradable polymer scafoldsfor cartilage tissue engineering.Clin Orthop Relat Res.2001;391(Supp1):251-270. [5]He S,Yaszemski MJ,Yasko AW,et al. Injectable biodegradable polymer composites based on poly (propylene fumarate) crosslinked with poly (ethylene glycol) –dimethacrylate. Biomaterials.2000;21(23):2389-2394. [6]Tan L,Yu X,Wan P,et al.Biodegradable Materials for Bone Repairs: A Review. J Mater Sci Technol.2013;29(6):503-513. [7]Novikova LN,Pettersson J,Brohlin M,et al.Biodegradable poly -β-hydroxybutyrate scaffold seeded with Schwann cells to promote spinal cord repair. Biomaterials. 2008;29(9): 1198-1206. [8]Yamaguchi M .Review Role of nutritional zinc in the prevention of osteoporosis. Mol Cell Biochem. 2010;338(1-2):241-254. [9]Zhang XN,Zhang SX,Zhao CL,et al.Research on a Mg−Zn alloys as a biodegradable biomaterial.Acta Biomaterialia. 2010;6(2):626−640. [10]Zheng YF,Li ZJ,Gu XN,et al.The development of binary Mg-Ca alloys for use as biodegradable materials within bone.Biomaterials.2008;29(10):1329-1344. [11]Dietrich E,Oudadesse H,Lucas-Girot A,et al.In vitro bioactivity of melt derived glass 46S6 doped with magnesium.J Biomed Mater Res A.2009;88(4):1087-1096. [12]Teixeira S,Fernandes H,Leusink A,et al.In vivo evaluation of highly macroporous ceramic scaffolds for bone tissue engineering.J Biomed Mater Res.2010;93(2):567-575. [13]Tarafder S,Balla VK,Davies NM,et al.Microwave-sintered 3D printed tricalcium phosphate scaffolds for bone tissue engineering.J Tissue Eng Regen Med.2013;7(8):631-641. [14]Fielding GA,Bandyopadhyay A,Bose S.Effects of silica and zinc oxide doping on mechanical and biological properties of 3D printed tricalcium phosphate tissue engineering scaffolds. Dent Mater.2012;28(2):113-122. [15]Roohani-Esfahani SI,Nouri-Khorasani S,Lu Z,et al.The influence hydroxyapatite nanoparticle shape and size on the properties of biphasic calcium phosphate scaffolds coated with hydroxyapatite–PCL composites. Biomaterials. 2010; 31(21):5498-5509. [16]Fu S,Ni P,Wang B,et al.In vivo biocompatibility and osteogenesis of electrospun poly (ε- caprolactone) - poly (ethylene glycol)-poly(ε-caprolactone)/nano-hydroxyapatite composite scaffold.Biomaterials.2012;33(33):8363-8371. [17]Song W,Wang Q,Wan C,et al.A novel alkali metals/strontium co-substituted calcium polyphosphate scaffolds in bone tissue engineering. J Biomed Mater Res B Appl Biomater. 2011;98 (2):255-262. [18]Mattanavee W,Suwantong O,Puthong S,et al.Immobilization of biomolecules on the surface of electrospun polycaprolactone fibrous scaffolds for tissue engineering. ACS Appl Mater Interfaces.2009;1(5):1076-1085. [19]Xue W,Bandyopadhyay A,Bose S.Polycaprolactone coated porous tricalcium phosphate scaffolds for controlled release of protein for tissue engineering. J Biomed Mater Res Part B: Appl Biomater.2009;91(2):831-838. [20]Gross TO,Cox QG,Jinnah RH.History and current application of bone transplantation. Orthopedics.1993; 16(8): 895-900. [21]Colton CK.Implantable biohybrid artificial organs.Cell Transplant.1995;4(4):415-436. [22]Carmeliet P.Mechanism s of angiogenesis and arteriogenesis. Nat Med.2000; 6(4):389-395. [23]Asahara T,Takahashi T,Masuda H,et al.VEGF contributes to post-natal neovascularization by mobilizing bone marrow-rived endothelial progenitor cells. EMBO J. 1999; 18(14):3964-3972. [24]Karageorgiou V,Kaplan D.Review Porosity of 3D biomaterial scaffolds and osteogenesis. Biomaterials. 2005;26(27): 5474-5491. [25]Bai F,Wang Z,Lu J,et al.The correlation between the internal structure and vascularization of controllable porous bioceramic materials in vivo: a quantitative study.Tissue Eng Part A.2010;16(12):3791-3803. [26]Ferrara N.Molecular and biological properties of vascular endothelial growth factor.J Mol Med.1999;77(7):527-543. [27]Hata Y,Rook SL,Aiello LP.Basic fibroblast growth factor induces expression of VEGF receptor KDR through a protein kinase C and p44/p42 mitogen-activated protein kinase-dependent pathway.Diabetes.1999;48(5):1145-1155. [28]Kang Q,Sun MH,Cheng H,et al.Characterization of the distinct orthotopic bone-forming activity of 14 BMPs using recombinant adenovirus-mediated gene delivery.Gene Ther.2004;11(17):1312-1320. [29]Kempen DH,Creemers LB,Alblas J,et al.Review Growth factor interactions in bone regeneration.Tissue Eng Part B Rev.2010;16(6):551-566. [30]Nguyen LH,Annabi N,Nikkhah M,et al.Vascularized Bone Tissue Engineering: Approaches for Potential Improvement. Tissue Eng Part B Rev.2012;18(5):363-382. [31]Davies N,Dobner S,Bezuidenhout D,et al.The dosage dependence of VEGF stimulation on scaffold neovascularisation. Biomaterials.2008;29(26):3531-3538. [32]Solorio L,Zwolinski C,Lund AW,et al.Gelatin microspheres crosslinked with genipin for local delivery of growth factors.J Tissue Eng Regen Med.2010;4(7):514-523. [33]Jabbarzadeh E,Starnes T,Khan YM,et al.Induction of angiogenesis in tissue-engineered scaffolds designed for bone repair: A combined gene therapy–cell transplantation approach.Proc Natl Acad Sci U S A.2008;105(32): 11099-11104. [34]Luo C,An H,Li T,et al.Regulation of plasmid release from super paramagnetic gelatin microspheres in implant of porosity cage under oscillating magnetic field. WAC Congress Series.2008;22(1):337-343. [35]KimS ,von Recum H.Endothelial Stem Cells and Precursors for Tissue Engineering: Cell Source, Differentiation, Selection, and Application.Tissue Eng. Part B Rev. 2008; 14(1):133-147. [36]Nomi M,Atala A,De Coppi P,et al.Principals of neovascularization for tissue engineering.Mol Aspects Med.2002;23(6):463-483. [37]Hristov M,Erl W,Weber PC.Endothelial progenitor cells: isolation and characterization.Trends Cardiovasc Med. 2003; 13(5):201-206. [38]Matsumoto T,Mifune Y,Kawamoto A,et al.Fracture induced mobilization and incorporation of bone marrow-derived endothelial progenitor cells for bone healing. Am J Pathol. 2008;215(1):232-242. [39]Wu X,Rabkin-Aikawa E,Guleserian J,et al.Tssue –engineered microvessels on three-dimensional degradable scaffolds using human endothelial progenitor cells. Am J Physiol Heart Circ Physiol.2004;287(2):H480-487. [40]Koike N,Fukumura D,Gralla O,et al.Tissue engineering: creation of long-lasting blood vessels. Nature. 2004;428 (6979): 138-139. [41]Wang DS,Miura M,Demura H,et al.Anabolic effects of 1,25-dihydroxyvitamin D3 on osteoblasts are enhanced by vascular endothelial growth factor produced by osteoblasts and by growth factors produced by endothelial cells. Endocrinology.1997; 138(7):2953-2962. [42]Zhou J,Lin H,Fang T,et al.The repair of large segmental bone defects in the rabbit with vascularized tissue engineered bone. Biomaterials.2010;31(6):1171-1179. [43]Marina I,Santos,Rui L,et al.Vascularization in Bone Tissue Engineering:Physiology, Current Strategies, Major Hurdles and Future Challenges. Macromol Biosci.2010;10(1):12-27. [44]Guillotin B,Bourget C,Remy-Zolgadri M.et al.Human primary endothelial cells stimulate human osteoprogenitor cell differentiation.Cell Physiol Biochem.2004;14(4-6):325-332. [45]Cassell OC,Hofer SO,Morrison WA,et al.Vascularisation of tissue-engineered grafts: the regulation of angiogenesis in reconstructive surgery and in disease states.Br J Plast Surg. 2002;55(8):603-610. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [3] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [4] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [5] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [6] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [7] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||