Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (5): 747-752.doi: 10.12307/2024.312
Previous Articles Next Articles
Mechanism and influencing factors in molecular weight degradation of non-cross-linked hyaluronic acid
Li Jiaqi1, 2, Huang Yuanli1, Li Yan3, Wang Chunren1, Han Qianqian1
- 1National Institutes for Food and Drug Control, Beijing 102629, China; 2China Pharmaceutical University, Nanjing 210000, Jiangsu Province, China; 3Beijing MeiYan Kong Jian Biology Medicine Co., Ltd., Beijing 100025, China
-
Received:2023-02-11Accepted:2023-04-28Online:2024-02-18Published:2023-08-16 -
Contact:Han Qianqian, PhD, Researcher, National Institutes for Food and Drug Control, Beijing 102629, China -
About author:Li Jiaqi, Master candidate, National Institutes for Food and Drug Control, Beijing 102629, China; China Pharmaceutical University, Nanjing 210000, Jiangsu Province, China Huang Yuanli, National Institutes for Food and Drug Control, Beijing 102629, China -
Supported by:Key Research & Development Project of the Ministry of Science and Technology during the “14th Five-Year Plan” Period, No. 2022YFC2401800 (to WCR)
CLC Number:
Cite this article
Li Jiaqi, Huang Yuanli, Li Yan, Wang Chunren, Han Qianqian. Mechanism and influencing factors in molecular weight degradation of non-cross-linked hyaluronic acid[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 747-752.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
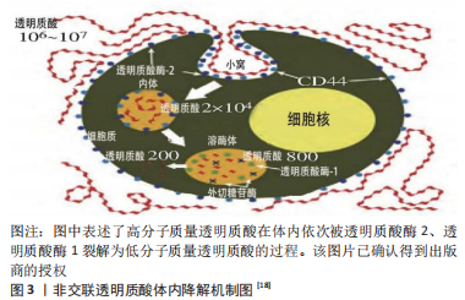
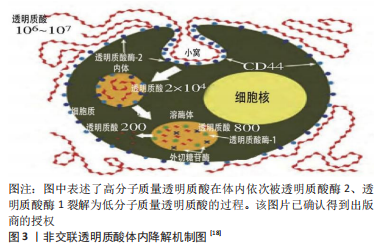
非交联透明质酸在机体内的降解机制如图3所示[18],与糖苷键的断裂形成有关,主要通过特异性的酶解作用和非特异性的自由基降解作用这两种不同的机制实现体内降解。非交联透明质酸在机体内的酶解作用主要通过透明质酸酶家族完成。透明质酸酶是指能够将透明质酸及部分糖胺聚糖降解成二糖或小分子寡糖的一类糖苷酶[19],目前透明质酸酶家族中已被确认的成员包括透明质酸酶1、透明质酸酶2、透明质酸酶3、透明质酸酶4、透明质酸酶P1和人类膜结合型透明质酸酶6种,其中透明质酸酶1和透明质酸酶2是降解透明质酸的酶中最重要的成员,在酸性pH值条件下具有最佳活性。在非交联透明质酸的降解过程中,位于细胞膜上的透明质酸酶2主要分布于机体的心脏、骨骼肌、脾脏、肾脏、肺部、结肠和胎盘中[20],可将超过1 000 kD的高分子质量透明质酸裂解为20 kD的中分子质量透明质酸,然后这些中分子质量透明质酸被主要分布于肝脏(这也是透明质酸降解的主要部位)的透明质酸酶1在溶酶体中裂解为四糖[20],随后这些四糖会在β-N-乙酰葡萄糖胺酶、β-葡萄糖醛酸酶等其他酶的作用下转化为单糖。除此之外,研究者近年来发现存在于细胞膜上的跨膜蛋白2也在细胞外基质中发挥透明质酸酶的作用,可在溶酶体内化和降解前将高分子质量透明质酸和中分子质量透明质酸降解为低分子质量透明质酸[21]。因此,非交联透明质酸在机体内的酶解作用可以说是由透明质酸酶1、透明质酸酶2和跨膜蛋白2协同作用完成的。此外,透明质酸也可被组织炎症、组织损伤和癌症产生的自由基切断糖苷键发生氧化降解作用,由高分子质量透明质酸降解为低分子质量透明质酸,在进一步降解代谢后被机体消除。"
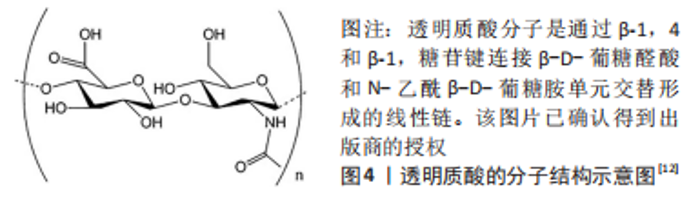
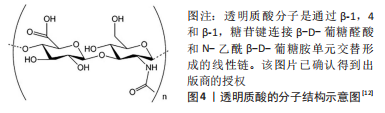
2.2 分子质量降解对非交联透明质酸结构和流变性质的影响 分子质量降解会改变非交联透明质酸的三维结构,降低其零切变黏度、黏弹性、假塑性等流变性质,进而影响临床应用。透明质酸的一级结构如图4所示[12],是由包含β-D-葡糖醛酸和N-乙酰β-D-葡糖胺的重复二糖单元形成的线性链,由于两种单糖都处于β构型,结构能量稳定,具有刚性构象的特点[2-3]。由此可见,透明质酸的一级结构并不受分子质量的影响[22]。透明质酸及其盐具有高度亲水性,在水分子的作用下可形成分子间氢键,进而形成表现出具有反平行左向链特点的每圈有2个二糖残基的双螺旋结构,即透明质酸的二级结构[23]。在疏水作用和分子间氢键的影响下,透明质酸的双螺旋结构形成聚合物双链,即β-片状三级结构,并且随着透明质酸分子质量和浓度的增加,聚合物链缠绕并形成三维网络结构[24-25]。"

非交联透明质酸分子质量的大小关系到其三维网络结构的建立,进而造成性能上的差异。比如随着非交联透明质酸分子质量的增加,其单个透明质酸分子形成的氢键个数增多,聚合物链的缠绕逐渐变大,从而易于形成并强化聚合物三维网络结构[22],具体表现为即使在1 μg/mL质量浓度的极低浓度下高分子质量透明质酸也会以三维网络结构形式存在[24,26],而低分子质量透明质酸则是以团簇形式存在,并不会形成三维网络结构[27],同时,由于水分子可与其中的氢键结合牢牢固定在这种三维网络结构中减少流失[28],高分子质量透明质酸常表现出高度的保湿性,而低分子质量透明质酸则具有良好的吸湿性能,体现出不同分子质量的非交联透明质酸结构不同对性能的影响。 此外,不同分子质量的非交联透明质酸因结构不同还会影响到其流变性质(包括零切变黏度、黏弹性及假塑性等)。流变性质作为非交联透明质酸的特殊理化性质,对于其在关节疾病、美容医学等领域的应用有至关重要的作用。比如在生产过程中,良好的流变性质可以减少产品灌注、分装的时间,保证产品装量的准确性;在进行面部填充和治疗关节疾病时,良好的流变性质能够保证内容物通过针头推入组织的顺利性以及注射剂量的准确性;作为凝胶等外用制剂使用时适宜的流变性质使其易于涂布等。因此明确非交联透明质酸分子质量与流变性质之间的关系对于非交联透明质酸的实际生产、应用具有重要意义。非交联透明质酸的流变性质与其分子质量大小成正比,即分子质量越高,其流变性质越强[22],这是因为随着分子质量的增加,其聚合物链的缠绕程度逐渐变大,展现出黏性行为所需的时间变长,因此其黏弹性增加,流变性质增强。比如在相同浓度下,分子质量大于1×106 Da的高分子质量透明质酸溶液的与分子质量在5×103和5×105 Da之间的低分子质量透明质酸溶液相比,其黏度要高出几个数量级[27]。此外,FALCONE等[29]通过对3种不同分子质量(350 kDa、680 kDa和1 800 kDa)非交联透明质酸的流变性质研究也证实了随着非交联透明质酸分子质量的增加,聚合物三维网络结构得到强化,其黏性及黏弹性等流变性质得到加强。 总之,非交联透明质酸分子质量与其结构和流变性质息息相关,分子质量的降解会使得其结构发生改变,三维网络结构解开,进而导致黏性、黏弹性等流变性质降低,力学性质改变,机械性能下降,最终影响非交联透明质酸产品的实际应用效果。例如在关节治疗时注射的非交联透明质酸需要具有良好的黏弹性以保护骨关节避免磨损,因此应注射具有高黏弹性的高分子质量透明质酸[10],同时高分子质量透明质酸还可通过降低神经冲动与敏感性来减轻疼痛发挥软骨保护作用[11]。但若是非交联透明质酸产品在放置过程中已发生分子质量降解,患者被注射黏弹性不足的低分子质量透明质酸,或者关节腔内的高分子质量透明质酸注射液发生降解,低分子质量透明质酸的机械性能不足以隔绝关节间的摩擦,难以起到减震和润滑关节减少关节磨损的作用,无法达到治疗效果,并且由于不同分子质量透明质酸的生物活性差异,低分子质量透明质酸的促炎性还会促进炎性因子的释放,引发组织炎症,加重患者关节的疼痛。然而,目前关于非交联透明质酸分子质量降解与其结构、流变性质的关联的研究较为浅表,对于分子质量降解改变其结构、流变性质后对人体生物功能造成的影响,以及在如组织工程等的应用中所引发的后续反应等尚不明确,有待研究者进一步探索研究。"

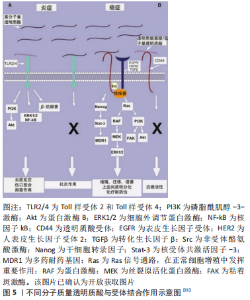
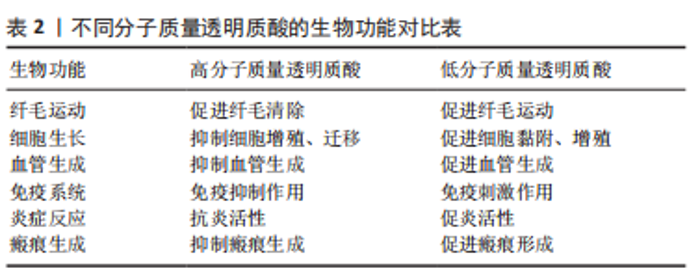
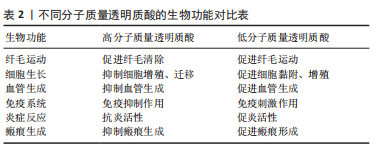
2.3 分子质量降解对非交联透明质酸生物活性的影响 非交联透明质酸作为细胞外基质的主要组成成分,具有优异的生物相容性、抗炎活性与低免疫原性,可通过与不同的细胞表面蛋白受体结合参与到细胞增殖分化、血管生成、炎症反应及伤口愈合等多个生物学过程中[3,5-8]。换而言之,非交联透明质酸的生物活性与其和不同受体的结合有关。而现有研究表明,非交联透明质酸分子质量的不同会影响到细胞对其摄取能力的强弱以及受体亲和力的大小,进而影响非交联透明质酸的生物活性[30]。图5表述了不同分子质量透明质酸与受体结合后的表现出的生物功能[11]。从图5中可以看出,透明质酸的生物活性很大程度上取决于其分子质量的大小,比如分子质量为0.4-4.0 kDa的透明质酸具有非凋亡特性,可作为热休克蛋白的诱导剂;分子质量为6-20 kDa范围内的透明质酸具有免疫刺激、促血管生成和抑菌作用;分子质量为20-200 kDa的透明质酸则可参与胚胎发育、伤口愈合等生物学过程[12,30-33]。与此同时,不同分子质量的透明质酸其生物活性甚至可能是相反的,表2对比了高分子质量透明质酸和低分子质量透明质酸在血管生成、免疫刺激及炎症反应等方面生物功能的差异。"
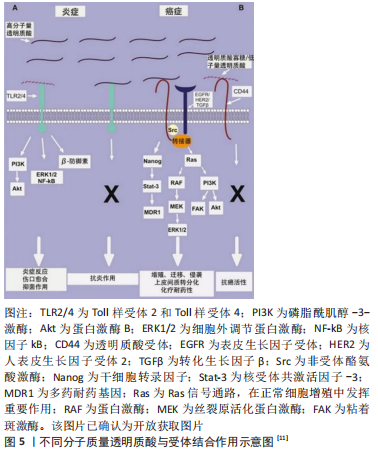

目前关于透明质酸分子质量影响其生物活性的机制尚未完全清楚,已有研究证明高分子质量透明质酸是通过使细胞停滞在有丝分裂G1期来抑制血管平滑肌细胞的增殖起到抗血管生成作用,而低分子质量透明质酸则是作用于G1期促进细胞增殖以促进新生血管生成[34]。对于炎症反应,研究认为低分子质量透明质酸可以激活Toll样受体2,4[30],诱导Toll样受体介导的炎症反应,而高分子质量透明质酸虽然也可通过Toll样受体进行信号传导,但并不能起到促炎作用[20]。但同时也有研究者认为,早期发现的低分子质量透明质酸对炎症反应的诱导作用可能是由于Toll样受体配体被内毒素(特别是脂多糖)污染导致的,而并非是低分子质量透明质酸引起的[20]。 综上所述,非交联透明质酸的生物活性与其分子质量大小密切相关,不同分子质量透明质酸的生物活性不同,甚至高分子质量透明质酸和低分子质量透明质酸与同一受体结合会表达出完全相反的生物效应。因此,在临床应用中非交联透明质酸分子质量的降解会改变其生物活性,导致非交联透明质酸产品功效降低,无法达到预期的治疗效果而延误病情,甚至因降解后的生物活性相反而诱发炎症反应、超敏反应等不良反应加重患者病情。例如非交联高分子质量透明质酸凝胶在临床中常被用于烧伤、整形、植皮以及深度创面的外科疗法等以抑制瘢痕增生[35-36],一旦在临床中使用了分子质量降解程度过大的非交联透明质酸凝胶,含量过多的低分子质量透明质酸会促进炎性因子释放与瘢痕形成,不仅无法达到抑制瘢痕的治疗效果,甚至可能加重瘢痕形成,引发急性炎症、肉芽肿等不良反应,为患者的康复与日常生活带来困扰。由此可知,深入阐明透明质酸生物活性与分子质量之间的关联以保障非交联透明质酸在临床应用的安全性是至关重要的。在非交联透明质酸原料或产品的放置过程应密切关注其分子质量的降解程度,以免因高分子质量透明质酸与低分子质量透明质酸生物活性的差异影响产品作用效果的发挥,特别是在美容医学和药物递送等领域,更要避免分子质量降解导致透明质酸生物活性发生截然相反的变化而加重病情的情况。"


2.4 分子质量降解对非交联透明质酸应用的影响 不同分子质量的非交联透明质酸在结构、性质与生物活性方面的显著差异决定了其在临床中的用途不同。例如,高分子质量透明质酸与低分子质量透明质酸相比其三维网络结构得到强化,水分子与其中的氢键结合后可被牢牢固定在结构中,水合作用得到增强[28]。因此非交联透明质酸在用于化妆品时,高分子质量透明质酸主要起到保湿作用,加速聚合物在皮肤上成膜,减少水分流失,而低分子质量透明质酸则因其具有良好的吸湿性能,可以调节皮肤水分平衡与代谢,用于抗衰老及美白产品。此外,非交联透明质酸在用于软组织修复时,小于250 kDa的低分子质量透明质酸可以促进细胞的黏附、增殖以及新生血管的形成,因此可作为创面敷料以促进创面的修复愈合,而当1 000 kDa以上的高分子质量透明质酸用作敷料时,由于其具有抗炎活性,可以抑制炎症反应的发生且具有良好的黏弹性,常用于术后创面以起到防粘连、抑制瘢痕形成和抗炎作用。与此同时,高分子质量透明质酸良好的流变性质使其能够在延长药液滞留时间的同时起到一定的润滑与保护作用,因此在临床上尤其是眼部疾病和炎症反应(如膀胱炎、阴道炎和骨关节炎等)的治疗中被广泛应用。比如在治疗干眼症的滴眼液中常加入1 000-1 500 kDa的高分子质量透明质酸以增加滴眼液在眼部的滞留时间,延长药物的作用时间,缓解患者眼部不适;3 000 kDa以上的高分子质量透明质酸在眼科手术中可作为黏弹性保护剂撑起前房,保护眼内组织以及降低术后炎症发生的可能; 5 000 kDa以上的高分子质量透明质酸因其高黏弹性可作为骨关节注射液注射入关节腔内,促进软骨修复的同时起到机械保护作用,减少关节磨损与患者疼痛。 但与此同时,与交联透明质酸相比,非交联透明质酸的半衰期短、稳定性差,产品在放置及应用过程中易受到外界因素(如温度、储存条件、pH值、超声波以及紫外光和过氧化氢等因素)的影响发生降解,导致分子质量降低的同时其结构、性质和生物活性亦随之改变,透明质酸的有效含量降低,产品应用时的有效性下降。不仅如此,在高分子质量透明质酸降解为低分子质量透明质酸后,低分子质量透明质酸具有的促炎活性、免疫刺激活性以及透明质酸降解产生的降解产物对机体细胞、组织和生物功能的作用可能会引发机体的炎症反应或加速肿瘤进展,引起局部疼痛、急性炎症、超敏反应、形成肉芽肿等不良反应的发生[37-41],增加患者应用产品时的安全风险。ALTMAN等[42]通过对大量的关节内注射透明质酸以治疗膝骨关节炎的随机试验进行统计分析发现,与低分子质量透明质酸产品相比,高分子质量透明质酸产品在治疗膝骨关节炎方面具有更高的安全性与有效性,这也进一步证实了非交联透明质酸分子质量降解会为临床应用带来安全性风险。 随着非交联透明质酸降解的发生,其分子质量分布系数会随着高分子质量透明质酸降解为低分子质量透明质酸而逐渐变大,加速透明质酸降解速率的同时降低透明质酸的机械性能,进而影响产品的使用寿命与应用性能。比如在组织工程中,非交联透明质酸可作为组织工程支架材料植入体内用于骨组织修复,而支架材料的应用性能与非交联透明质酸的分子质量大小以及其在基质材料中的分布息息相关,理想的透明质酸降解速率应与组织再生同步,但实际应用中随着支架材料使用时间的增长,透明质酸分子质量降解,分子质量分布系数变大,非交联透明质酸分子质量的降解速率常过快,使得植入的支架材料机械性能迅速下降,植入材料破裂并引发炎症等并发症,不利于患者骨组织修复的治疗。综上所述,分子质量降解会降低非交联透明质酸原料及产品的安全性、有效性,影响产品的使用寿命与应用性能,最终影响临床应用效果。 非交联透明质酸用于药物载体时可采用无菌分装的方法避免分子质量降解。有研究采用的旋转水浴灭菌法与传统湿热灭菌法相比,能够使透明质酸凝胶在灭菌过程中的降解程度大幅降低[43]。在产品的运输过程中,应要求冷链运输并及时登记入库,防止透明质酸分子质量受环境温度变化影响发生降解,降低产品有效性。在临床应用中,对于需要临用新配的非交联透明质酸样品应在低温、4 < pH值< 11的条件下进行,避免暴露于超声波与活性氧中,如果是长期储存应放置于冰箱中4 ℃冷藏条件下保存,同时要积极关注产品的货架寿命,注意产品在效期内的稳定性,避免因分子质量降解影响产品的有效性与安全性。 文章总结了非交联透明质酸在温度、储存方式、pH值以及超声波等影响因素条件下的降解实验情况[10,44-47],见表3。非交联透明质酸易受到温度、储存条件、pH值和超声波等多重因素的影响发生降解,在低温、4 < pH值< 11且未受到超声波影响的条件下分子质量最为稳定,降解程度最低。因此,为尽可能避免在临床应用中非交联透明质酸分子质量降解带来的有效性与安全性风险,延长产品的使用寿命,保障产品的应用性能,在非交联透明质酸原料与产品的贮存、生产、运输及使用过程中应按照规定要求操作,严格控制产品分子质量。比如在制备非交联透明质酸产品的前期应严格把控原料质量,在4 ℃冷藏条件下贮存,以防受温度影响非交联透明质酸分子质量降解造成主成分含量下降影响成品的有效性。在生产过程中,要严格把控车间环境温度,进行工艺优化,设置适宜的加工温度及pH值,避免或减少产品暴露于超声波与活性氧中的时间,尽可能地减少非交联透明质酸在生产过程中的降解。在灭菌阶段,常用的紫外灭菌、辐照灭菌和湿热灭菌等灭菌方法会显著降低非交联透明质酸分子质量,不利于产品的有效性,可采用过滤除菌、环氧乙烷灭菌等方法,并在灭菌后再次测定透明质酸分子质量以评估降解情况。"

| [1] 杨卫,徐呈祥,陈则胜,等.基于生物聚合物伤口敷料的研究及应用进展[J].材料导报,2022,36(S1):523-527. [2] SHOU Y, ZHANG J, YAN S, et al. Thermoresponsive chitosan/DOPA-based hydrogel as an injectable therapy approach for tissue-adhesion and hemostasis. ACS Biomater Sci Eng. 2020;6(6):3619-3629. [3] THAPA RK, DIEP DB, TØNNESEN HH. Topical antimicrobial peptide formulations for wound healing: current developments and future prospects. Acta Biomater. 2020;103:52-67. [4] AIDA TM, OSHIMA M, SHARMIN T, et al. Controlled conversion of sodium hyaluronate into low-molecular-weight polymers without additives using high-temperature water and fast-heating-rates. J Supercrit Fluids. 2020;155:104638. [5] ZHANG A, LIU Y, QIN D, et al. Research status of self-healing hydrogel for wound management: a review. Int J Biol Macromol. 2020;164:2108-2123. [6] ABATANGELO G, VINDIGNI V, AVRUSCIO G, et al. Hyaluronic acid: redefining its role. Cells. 2020;9(7):1743. [7] HINTZE V, SCHNABELRAUCH M, ROTHER S. Chemical modification of hyaluronan and their biomedical applications. Front Chem. 2022;10:830671. [8] SKANDALIS SS, KARALIS T, HELDIN P. Intracellular hyaluronan: importance for cellular functions. Semin Cancer Biol. 2020;62:20-30. [9] 殷悦,李潼,王师平,等.富血小板血浆联合非交联透明质酸钠复合溶液填充治疗上睑凹陷疗效分析[J].中国美容医学,2020,29(10):6-10. [10] SIMULESCU V, KALINA M, MONDEK J, et al. Long-term degradation study of hyaluronic acid in aqueous solutions without protection against microorganisms. Carbohydr Polym. 2016;137:664-668. [11] TAVIANATOU AG, CAON I, FRANCHI M, et al. Hyaluronan: molecular size‐dependent signaling and biological functions in inflammation and cancer. FEBS J. 2019;286(15):2883-2908. [12] GRAÇA MFP, MIGUEL SP, CABRAL CSD, et al. Hyaluronic acid-based wound dressings: a review. Carbohydr Polym. 2020;241:116364. [13] FALLACARA A, BALDINI E, MANFREDINI S, et al. Hyaluronic acid in the third millennium. Polymers (Basel). 2018;10(7):701. [14] 许磊,韩晓强,张锦涛,等.关节软骨细胞周围透明质酸产生、转化和功能特征[J].中国组织工程研究,2022,26(5):768-773. [15] LIU L, LIU Y, LI J, et al. Microbial production of hyaluronic acid: current state, challenges, and perspectives. Microb Cell Fact. 2011;10:99. [16] 刘晖,刘爱峰,张宇,等.透明质酸支架在软骨修复工程中的优势和应用策略[J].中国组织工程研究,2022,26(34):5518-5524. [17] BALAZS EA. Ultrapure hyaluronic acid and the use thereof. US: US4141973,1979-02-27. [18] DICKER KT, GURSKI LA, PRADHAN-BHATT S, et al. Hyaluronan: a simple polysaccharide with diverse biological functions. Acta Biomater. 2014;10(4):1558-1570. [19] 雷曦,张蕊,黄遵锡,等.透明质酸酶的研究进展[J].微生物学通报,2021,48(3):882-895. [20] GARANTZIOTIS S. Modulation of hyaluronan signaling as a therapeutic target in human disease. Pharmacol Ther. 2022;232:107993. [21] SCHINZEL RT, HIGUCHI-SANABRIA R, SHALEM O, et al. The hyaluronidase, TMEM2, promotes ER homeostasis and longevity independent of the UPRER. Cell. 2019;179(6):1306-1318.e18. [22] SNETKOV P, ZAKHAROVA K, MOROZKINA S, et al. Hyaluronic acid: the influence of molecular weight on structural, physical, physico-chemical, and degradable properties of biopolymer. Polymers (Basel). 2020;12(8):1800. [23] HEATLEY F, SCOTT JE. A water molecule participates in the secondary structure of hyaluronan. Biochem J. 1988;254(2):489-493. [24] SCOTT JE, CUMMINGS C, BRASS A, et al. Secondary and tertiary structures of hyaluronan in aqueous solution, investigated by rotary shadowing-electron microscopy and computer simulation. Biochem J. 1991;274(3):699-705. [25] SCOTT JE, HEATLEY F. Hyaluronan forms specific stable tertiary structures in aqueous solution: a 13C NMR study. Proc Natl Acad Sci U S A. 1999;96(9):4850-4855. [26] SCOTT JE. Supramolecular organization of extracellular matrix glycosaminoglycans, in vitro and in the tissues. FASEB J. 1992;6(9):2639-2645. [27] ROSA DM, D’AGOSTINO A, GATTA LA, et al. Hybrd cooperative complexes of hyaluronic acid. US: US2013165404, 2013-6-27. [28] 张堃,简军,张政朴.透明质酸的结构、性能、改性和应用研究进展[J].高分子通报, 2015,197(9):217-226. [29] FALCONE SJ, PALMERI DM, BERG RA. Rheological and cohesive properties of hyaluronic acid. J Biomed Mater Res A. 2006;76A(4):721-728. [30] JUNCAN AM, MOISĂ DG, SANTINI A, et al. Advantages of hyaluronic acid and its combination with other bioactive ingredients in cosmeceuticals. Molecules. 2021;26(15):4429. [31] 蔡同凯,刘谋治,邓婕,等.透明质酸的作用机制及临床应用研究进展[J].药学实践杂志,2022,40(2):103-107,131. [32] HOARAU A, POLETTE M, CORAUX C. Lung hyaluronasome: Involvement of low molecular weight Ha (Lmw-Ha) in innate immunit. Biomolecules. 2022;12(5):658. [33] ROWLEY JE, AMARGANT F, ZHOU LT, et al. Low molecular weight hyaluronan induces an inflammatory response in ovarian stromal cells and impairs gamete development in vitro. Int J Mol Sci. 2020;21(3):1036. [34] CUFF CA, KOTHAPALLI D, AZONOBI I, et al. The adhesion receptor CD44 promotes atherosclerosis by mediating inflammatory cell recruitment and vascular cell activation. J Clin Invest. 2001;108(7):1031-1040. [35] 王彤,成亚飞,陈诚,等.透明质酸在烧伤整形美容外科中的应用进展[J].中国美容医学,2020,29(2):170-173. [36] HUSSAIN SN, GOODMAN GJ, RAHMAN E. Treatment of a traumatic atrophic depressed scar with hyaluronic acid fillers: a case report. Clin Cosmet Investig Dermatol. 2017;10:285-287. [37] MORAN M, NIETO-LOPEZ F, RUEDA-CARRASCO J. Lipoteichoic acid and molecular weight of hyaluronic acid could explain the late inflammatory response trigger by hyaluronic acid fillers. J Cosmet Dermatol. 2022;21(11):5610-5613. [38] OWCZARCZYK-SACZONEK A, ZDANOWSKA N, WYGONOWSKA E, et al. The immunogenicity of hyaluronic fillers and its consequences. Clin Cosmet Investig Dermatol. 2021;14:921-934. [39] 林建云,罗时荷,杨崇岭,等.生物基高分子型止血材料和伤口敷料[J].化学进展, 2021,33(4):581-595. [40] WANG HC, YU N, WANG X, et al. Cerebral embolism as a result of facial filler injections: a literature review. Aesthet Surg J. 2022;42(3):NP162-NP175. [41] KOKOSKA RE, LIMA AM, KINGSLEY MM. Review of delayed reactions to 15 hyaluronic acid fillers. Dermatol Surg. 2022;48(7):752-757. [42] ALTMAN RD, BEDI A, KARLSSON J, et al. Product differences in intra-articular hyaluronic acids for osteoarthritis of the knee. Am J Sports Med. 2016;44(8):2158-2165. [43] 刘志雯,黄慧娟,张军东,等.一种透明质酸钠凝胶的灭菌方法[P].上海: CN106139178A,2016-11-23. [44] CHEN H, QIN J, HU Y. Efficient degradation of high-molecular-weight hyaluronic acid by a combination of ultrasound, hydrogen peroxide, and copper ion. Molecules. 2019;24(3):617. [45] SIMULESCU V, MONDEK J, KALINA M, et al. Kinetics of long-term degradation of different molar mass hyaluronan solutions studied by SEC-MALLS. Polym Degrad Stab. 2015;111: 257-262. [46] MALEKI A, KJØNIKSEN A-L, NYSTRÖM B. Effect of PH on the behavior of hyaluronic acid in dilute and semidilute aqueous solutions. Macromol Symp. 2008;274(1):131-140. [47] HAFSA J, CHAOUCH MA, CHARFEDDINE B, et al. Effect of ultrasonic degradation of hyaluronic acid extracted from rooster comb on antioxidant and antiglycation activities. Pharm Biol. 2017;55(1):156-163. |
| [1] | Yu Weijie, Liu Aifeng, Chen Jixin, Guo Tianci, Jia Yizhen, Feng Huichuan, Yang Jialin. Advantages and application strategies of machine learning in diagnosis and treatment of lumbar disc herniation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1426-1435. |
| [2] | Weng Rui, Lin Dongxin, Guo Haiwei, Zhang Wensheng, Song Yuke, Lin Hongheng, Li Wenchao, Ye Linqiang. Abnormal types of intervertebral disc structure and related mechanical loading with biomechanical factors [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1436-1442. |
| [3] | Lin Zeyu, Xu Lin. Research progress in gout-induced bone destruction mechanism [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1295-1300. |
| [4] | Ma Shuwei, He Sheng, Han Bing, Zhang Liaoyun. Exosomes derived from mesenchymal stem cells in treatment of animals with acute liver failure: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1137-1142. |
| [5] | Zhang Kefan, Shi Hui. Research status and application prospect of cytokine therapy for osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 961-967. |
| [6] | Cheng Jinhui, Wu Quan, Peng Min, Huang Changli, Tian Huimin, Li Yang. Preparation and properties of selective laser melting of porous titanium at a low energy density [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 664-668. |
| [7] | Li Wenlan, Wang Wenyuan, Ren Wenxiu, Zhang Yupei, Yang Xiaoyan, Wang Zhigang, Xia Jizhu. Preparation of a near-infrared photoresponsive biomimetic nanoprobe and its application in photothermal detection and treatment of breast cancer [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 669-675. |
| [8] | Lan Weiwei, Yu Yaodong, Huang Di, Chen Weiyi. In vitro degradation behavior of Mg-Zn-Ca alloys [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 717-723. |
| [9] | Xu Rong, Wang Haojie, Geng Mengxiang, Meng Kai, Wang Hui, Zhang Keqin, Zhao Huijing. Research advance in preparation and functional modification of porous polytetrafluoroethylene artificial blood vessels [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 759-765. |
| [10] | Yin Tong, Yang Jilei, Li Yourui, Liu Zhuoran, Jiang Ming. Application of core-shell structured nanofibers in oral tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 766-770. |
| [11] | Wang Yeyuan, Du Yilang, Yu Dehao, Ning Fengting, Bai Bing. Effect of micro-arc oxidation treatment on biological activity of medical metals [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 771-776. |
| [12] | Chen Xiaofang, Zheng Guoshuang, Li Maoyuan, Yu Weiting. Preparation and application of injectable sodium alginate hydrogels [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 789-794. |
| [13] | Liu Chuang, Shan Shuo, Yu Tengbo, Zhou Huan, Yang Lei. Advantages, discomfort and challenges of clinical application of orthopedic hemostatic materials [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 795-803. |
| [14] | Zhang Ming, Wang Bin, Jia Fan, Chen Jie, Tang Wei. Application of brain-computer interface technology based on electroencephalogram in upper limb motor function rehabilitation of stroke patients [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 581-586. |
| [15] | He Yuanjie, Chen Yuheng, Zhao Yongchao, Wang Zhenglong. Progress in epigenetic regulation of vascular smooth muscle cell remodeling in the occurrence and development of aortic aneurysms [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 602-608. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||