Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (33): 5377-5384.doi: 10.12307/2023.716
Previous Articles Next Articles
Action mechanism of traditional Chinese medicine combined with bone marrow mesenchymal stem cells in regulating blood-brain barrier after cerebral ischemia reperfusion injury
Wang Shaona1, Liu Feixiang1, 2, Ying Chunmiao1, Gao Chen1, Zhang Yunke1, 2
- 1Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China; 2First Affiliated Hospital of Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China
-
Received:2022-10-11Accepted:2022-11-18Online:2023-11-28Published:2023-03-30 -
Contact:Zhang Yunke, Professor, Chief physician, Doctoral supervisor, Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China; First Affiliated Hospital of Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China -
About author:Wang Shaona, Master candidate, Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China -
Supported by:National Natural Science Foundation of China, No. 81974564 (to ZYK); National Natural Science Foundation of China, No. 82104730 (to LFX); Central Plains Talent Plan-Science and Technology Innovation Leading Talent Project, No. 224200510027 (to ZYK)
CLC Number:
Cite this article
Wang Shaona, Liu Feixiang, Ying Chunmiao, Gao Chen, Zhang Yunke. Action mechanism of traditional Chinese medicine combined with bone marrow mesenchymal stem cells in regulating blood-brain barrier after cerebral ischemia reperfusion injury[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(33): 5377-5384.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

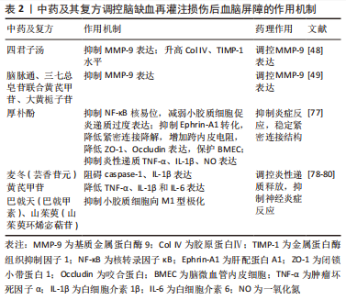
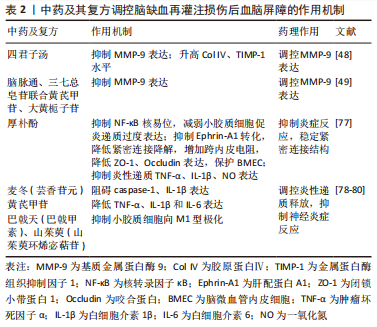
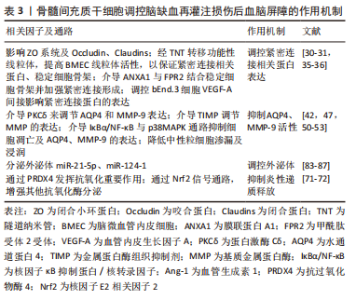
2.1 血脑屏障生理结构 血脑屏障主要是由脑微血管内皮细胞构成血管壁,周围绕以周细胞、基底膜以及星形胶质细胞轴突所形成的一道维持脑内平衡的高调节性半透膜,进而将中枢神经系统和血液分隔开来,调控分子进入和流出来确定物质交换与营养供应,保护大脑免受毒性物质侵害,维持大脑稳态。 2.1.1 特定组件结构 血脑屏障特定组件包括基本细胞结构和主要连接结构。脑微血管内皮细胞是血脑屏障核心要素,其独有的高跨内皮电阻使得其对跨膜物质具备高度选择性,其异常破坏将增大血脑屏障通透性引起外周物质进入中枢神经系统[6]。星形胶质细胞是血脑屏障关键诱导剂,其足突末端水通道蛋白4管控两侧离子与水平衡,进而调控血脑屏障通透性[7]。周细胞基本覆盖大脑内毛细血管基底膜外腔,其与脑微血管内皮细胞共用同一基底膜,两者之间相互作用经细胞旁转运、影响紧密连接产生、改善脑血流量等途径发挥协同作用促进血脑屏障成熟,若被异常破坏将引起毒性物质进入脑组织、再灌注受损及神经退行性病变[8]。闭合蛋白(Claudins)、咬合蛋白(Occludin)、连接黏附分子(JAM)、闭合小环蛋白(ZO)和细胞骨架相关蛋白构成紧密连接复杂的跨膜蛋白网,是血脑屏障通透性改变的最敏感指标。紧密连接与脑微血管内皮细胞联系在一起,成为限制传播物质移动至大脑的第一道屏障,也是影响血脑屏障通透性的关键因素[9]。黏附连接存在于内皮细胞中是调节血管通透性的重要物质,由受Ca2+调节的VE-钙黏蛋白构成,其与紧密连接一起调节小分子运动进而发挥稳定内皮层、限制细胞旁交换、保持血管完整性的作用。邻近细胞膜中闭合蛋白经相互作用而封闭细胞间隙达到维持高跨内皮电阻作用[10],其异常表达将选择性开放紧密连接;咬合蛋白与临近细胞间特殊环状结构可封闭细胞旁空间,且其包含C端结构可募集闭合小环蛋白家族起到稳定内皮屏障的作用,其包含N端起到维持紧密连接完整性的作用,若缺失不仅影响细胞旁通透性,也引起更低跨内皮电阻。DIAZ等[11]研究表明咬合蛋白表达降低时,血脑屏障通透性将增加;连接黏附分子1是最早出现在细胞间接触位点的分子,具备唤醒其他蛋白启动并稳定紧密连接结构,降低细胞旁通路通透性等特点,其表达降低与紧密连接完整性被破坏密切相关[12];闭锁小带蛋白1是紧密连接复合体中的重要枢纽蛋白,可经SH3结构交联各种紧密连接蛋白并连接到肌动蛋白细胞骨架上,其磷酸化为影响血脑屏障通透性的决定性因素[13]。上述相关蛋白起到屏障及栅栏作用,它们之间存在紧密且复杂的联系,其中任何表达异常将破坏主要连接结构完整性,继而破坏血脑屏障完整性。 2.1.2 相关因子及信号通路 血脑屏障形成需要各种相关因子参与及细胞内信号通路微调。血小板衍生生长因子BB主要影响周细胞数量,并与其细胞上受体结合激活多种信号传导,若异常表达则致血脑屏障渗透性增加[14];血管内皮生长因子-血管内皮生长因子受体2信号传导促进血管生成;Wnt信号通路参与血管发育和血脑屏障形成;音猬因子是主要来源于星形胶质细胞的一种信号,对脑微血管内皮细胞至关重要,一方面可抑制其中白细胞介素8、细胞间黏附分子1等多种炎性因子表达,进而阻碍外周炎症渗入至血脑屏障;另一方面可调节紧密连接相关蛋白和VE-钙黏蛋白表达[15]。目前对血脑屏障基本细胞之间相互作用的信号通路研究较少,尤其是支持血脑屏障稳定的周细胞与脑微血管内皮细胞,现有研究仅有2种信号通路[16]:一为周细胞对脑微血管内皮细胞的血管生成素Tie-2信号通路;二为脑微血管内皮细胞对周细胞的转化生长因子β相关通路,未来将致力于研究每一个细胞间通路。 2.2 脑缺血再灌注损伤后血脑屏障的病理变化 2.2.1 炎性因子释放 相比于其他任何部位毛细血管,血脑屏障更微细、缺乏窗孔的特点严格控制有毒物质进入大脑,神经血管单元任何有效成分缺失均会引起血脑屏障缺失或渗漏。缺血缺氧发生后,神经炎症存在是破坏血脑屏障完整性的极大危险因素,释放如自由基、白细胞介素1、肿瘤坏死因子α、类花生酸等炎性因子。脑缺血数小时内,中性粒细胞呈指数增长并黏附到脑微血管内皮细胞上阻碍血流,与P-选择素糖蛋白配体1/P选择素、巨噬细胞抗原复合物1/细胞间黏附分子1之间相互作用加重上述过程,增加细胞旁通透性[17];此外,中性粒细胞可通过影响活性氧、基质金属蛋白酶、中性粒细胞胞外诱捕网及脂质运载蛋白2等多种因素降解血脑屏障结构[18]。活性氧产生后激活基质金属蛋白酶、调控紧密连接、改变血管张力控制脑血流量及干扰部分转运蛋白破坏血脑屏障通透性,最终使得血脑屏障打开。研究表明,含有环氧化酶1、环氧化酶2的类花生酸释放前列腺素、白三烯在体外实验中对血脑屏障具有高渗性[19]。基质金属蛋白酶9、基质金属蛋白酶2可通过VE-钙黏蛋白、基底膜蛋白直接降解内皮紧密连接及脑微血管内皮细胞,两者过表达是引起脑缺血再灌注损伤后血脑屏障中断的重要原因,且前者造成不可逆改变。此外,活性氧可激活基质金属蛋白酶分泌,基质金属蛋白酶又可激活白细胞介素1β、肿瘤坏死因子α,由此形成恶性循环并促进血脑屏障打开。由此可见,抗炎、抗氧化、下调基质金属蛋白酶表达、调控紧密连接和黏附连接是治疗脑缺血再灌注后血脑屏障泄露的重要方向[20]。 2.2.2 细胞结构功能破坏 脑缺血发生时,各细胞正常形态结构及其之间相互协同关系将遭到破坏,其中星形胶质细胞对稳定血脑屏障通透性具有至关重要的作用。脑缺血再灌注损伤发生时星形胶质细胞肿大、增生、肥大成为反应性星形胶质细胞,并促进诱导型一氧化氮合成酶表达进一步生成高浓度一氧化氮加重脑损伤。正常情况下,水通道蛋白4位于最外层血管周围末端,脑缺血情况下则分散在整个反应性星形胶质细胞的细胞质中。研究发现,水通道蛋白4表达上调,不仅导致星形胶质细胞肿胀、脑积水增多,还可诱发促炎因子(白细胞介素1β,肿瘤坏死因子α)释放,加大血脑屏障通透性[21]。此外,反应性星形胶质细胞释放的血管内皮生长因子A诱导并加重紧密连接分解、诱导咬合蛋白磷酸化、引发炎性因子浸润从而参与破坏血脑屏障[22]。实验研究表明,脑损伤小鼠血管内皮生长因子A表达上调,但在使用其抗体阻断后被破坏的血脑屏障得到明显减轻[23]。由此可见,调控星形胶质细胞、水通道蛋白4、血管内皮生长因子A表达是治疗脑缺血再灌注后血脑屏障泄露的重要方向。 2.3 中药联合骨髓间充质干细胞调控血脑屏障的机制 2.3.1 调控紧密连接相关蛋白表达 脑微血管内皮细胞中紧密连接相关蛋白表达异常可引起血脑屏障损害继而加重缺血后脑组织损害。因此,上调紧密连接相关蛋白成为保护脑缺血再灌注损伤后血脑屏障的关键方向之一。已有多数研究均统一证实,紧密连接破坏是导致缺血后血脑屏障障碍的最主要原因之一,且闭锁小带蛋白1、咬合蛋白、闭合蛋白发挥绝对性作用[24]。骨髓间充质干细胞调节紧密连接蛋白表达的机制主要有3个方面:①影响闭合小环蛋白系统及咬合蛋白、闭合蛋白;②经隧道纳米管转移功能性线粒体,提高脑微血管内皮细胞上线粒体活性,以保证紧密连接相关蛋白表达,稳定细胞骨架;③介导膜联蛋白A1(ANXA1)与甲酰肽受体2受体结合稳定细胞骨架并加强紧密连接形成;④调控bEnd.3细胞血管内皮生长因子A间接影响紧密连接蛋白的表达。 不同于其他结构组织,血脑屏障中脑微血管内皮细胞具有高线粒体密度,可见脑脉管系统对三磷酸腺苷有更高需求[25]。线粒体是细胞内能量加油站,主要调节钙信号、细胞凋亡、维持氧化还原平衡[26],此外其衍生的ATP可通过调节肌动蛋白动力学而稳定细胞骨架接连结构。肌动蛋白细胞骨架经闭合小环蛋白系统与紧密连接结构相互作用,并连接脑微血管内皮细胞共同支持血脑屏障功能稳定性。研究发现,脑微血管内皮细胞中线粒体ATP对血脑屏障完整性至关重要,若其缺失或减少,将影响肌动蛋白细胞骨架之间相互作用,破坏紧密连接机制和血脑屏障完整性[27]。隧道纳米管是一种新的细胞与细胞通讯机制,介导线粒体在连接细胞之间交换,虽然绝大多数体外研究证实了隧道纳米管存在,但其在体内的存在也得到有关证据支持[28]。隧道纳米管可转移健康细胞中线粒体,一则弥补受损脑微血管内皮细胞上的线粒体及功能紊乱的线粒体,二则防止脑血管内皮细胞、周细胞、星形胶质细胞成分之间串扰,稳定组织形态、修复受损组织[29]。研究发现,间充质干细胞可利用隧道纳米管结构交换完整功能的线粒体,使得迁移至脑内皮细胞上以发挥正常功能[30]。间充质干细胞移植后,显著提高宿主细胞上线粒体活性、促进脑微血管系统中血管生成也在研究中得到证实[31]。 膜联蛋白A1与脑微血管内皮细胞表达密切相关,也是维持血脑屏障完整性的关键内源性因子之一[32],常为甲酰肽受体激动剂。缺血缺氧情况下,RhoA被激活,而后β-肌动蛋白遭到破坏,破坏后细胞骨架结构稳定性和脑微血管内皮细胞上紧密连接蛋白表达均显著下降,表现为血脑屏障更高渗透性[33]。膜联蛋白A1可与甲酰肽受体2受体结合,两者作用后明显抑制RhoA活性,避免β-肌动蛋白被破坏,最终促进细胞骨架形成并增强紧密连接来稳定血脑屏障完整性[34]。然而脑血管系统若发生缺血时,膜联蛋白A1表达下降,其阻碍炎症破坏紧密连接和阻碍炎症细胞进入脑实质的能力降低,血脑屏障内源性保护作用也随之丧失。研究发现,间充质干细胞或其衍生的细胞外囊泡富含膜联蛋白A1,并经膜联蛋白A1可与甲酰肽受体轴保护血脑屏障[35]。此外,研究表明骨髓间充质干细胞可通过调控bEnd.3细胞中血管内皮生长因子A来间接调节内皮细胞紧密连接表达[36]。 中药联合骨髓间充质干细胞调控脑缺血再灌注损伤后血脑屏障通透性可通过上述机制且表现出较单独治疗更明显的协调作用。KIM等[37]研究发现,当归毛状根水提物(AG)可通过促进闭锁小带蛋白1表达,降低血脑屏障通透性,且将其与骨髓间充质干细胞联合使用,达到对血脑屏障的保护作用明显优于单独使用骨髓间充质干细胞。扎里奴思方通过干预咬合蛋白和闭合蛋白mRNA动态表达进而改善脑缺血再灌注损伤后血脑屏障通透性,重点是联合骨髓间充质干细胞改善脑水肿的效果大于单独使用[38]。补阳还五汤联合骨髓间充质干细胞通过上调缺血脑组织中咬合蛋白、闭合蛋白、连接黏附分子、闭锁小带蛋白1表达来维持紧密连接完整性,达到脑保护作用[39]。 2.3.2 抑制水通道蛋白4、基质金属蛋白酶9活性 脑缺血再灌注损伤后在病程急性期由于血脑屏障通透性增加促发脑水肿形成,其主要机制涉及跨细胞隔间进行水交换的水通道蛋白4表达上调及基质金属蛋白酶9活性增强;体外实验中,敲除水通道蛋白4表现为减缓细胞肿胀,而水通道蛋白4过度表达更显著表现细胞肿胀[40];基质金属蛋白酶具有降解紧密连接相关蛋白及破坏脑微血管内皮细胞的功能,尚可激活其他基质金属蛋白酶导致瀑布效应,加重脑损伤。一项实验研究表明,缺血性脑损伤后血脑屏障通透性发生显著下降,得益于益母草碱具备抑制水通道蛋白4上调的特性[41];先前大多研究已经确立基质金属蛋白酶9表达会引起血脑屏障不可逆破坏之间的相关性,再灌注损伤发生24 h内基质金属蛋白酶9表达达到峰值且维持5 d,此时血脑屏障遭到最大破坏[42]。刘旋辉等[43]发现丁苯酞可下调脑组织水通道蛋白4和基质金属蛋白酶9表达,减轻脑水肿,对缺血再灌注引起的血脑屏障损伤起到保护作用。因此,抑制水通道蛋白4、基质金属蛋白酶9的活性成为保护脑缺血再灌注损伤后血脑屏障的另一方向。骨髓间充质干细胞抑制水通道蛋白4、基质金属蛋白酶9活性的机制为:①介导蛋白激酶Cδ来调节水通道蛋白4和基质金属蛋白酶9表达;②介导金属蛋白酶组织抑制剂调节基质金属蛋白酶的表达;③介导IκBα/NF-κB与p38MAPK通路抑制细胞凋亡及水通道蛋白4、基质金属蛋白酶9的表达;④降低中性粒细胞渗漏及浸润。 蛋白激酶Cδ是调控血脑屏障通透性的关键影响因子之一[44],其表达增加可加剧脑缺血再灌注损伤。蛋白激酶Cδ激活会导致ERK1/2磷酸化或者易位继而刺激转录因子Ets 样转录因子1与基质金属蛋白酶9启动因子结合,从而诱导基质金属蛋白酶9转录[45];但抑制其激活不仅可阻止闭锁小带蛋白1磷酸化而减弱紧密连接渗漏,还可加强其和咬合蛋白同肌动蛋白细胞骨架的关联[46]。基质金属蛋白酶9与血脑屏障中水通道蛋白4正交阵列模式结构之间有联系,其含量增加后引起水通道蛋白4正交阵列模式结构退化、血脑屏障不可逆破坏和血管性水肿。DATTA等[42]研究表明,间充质干细胞显著缓解血脑屏障损伤且减轻血管源性水肿是通过介导蛋白激酶Cδ来调节水通道蛋白4和基质金属蛋白酶9的表达。 金属蛋白酶组织抑制剂是基质金属蛋白酶的内源性抑制剂,与基质金属蛋白酶一样是调节血脑屏障完整性的关键因素,通过其半胱氨酸残基与基质金属蛋白酶中锌离子活性中心相结合进而抑制基质金属蛋白酶同底物结合,而达到抑制细胞外基质降解的作用。LOZITO等[47]研究表明骨髓间充质干细胞可通过分泌金属蛋白酶组织抑制剂抑制高水平基质金属蛋白酶,成为抑制内外源性基质金属蛋白酶的可靠来源,更重要的是即使在病理状态下也能保护血管免受基质金属蛋白酶9损害。 研究表明,四君子汤[48]、脑脉通、三七总皂苷联合黄芪甲苷和大黄栀子苷可抑制基质金属蛋白酶9表达和细胞凋亡[49],同时也可升高胶原蛋白、金属蛋白酶组织抑制因子1水平,而四君子汤尤以高剂量明显。LI等[50]发现骨髓间充质干细胞移植能够降低脑膜通透性、减缓脑缺血大鼠基底膜胶原蛋白的降解,源于大黄苷元增加金属蛋白酶组织抑制因子9表达而调节了基质金属蛋白酶9的平衡。研究表明,骨髓间充质干细胞移植不仅能够减弱中性粒细胞外渗,还能下调基质金属蛋白酶9表达[51]。同样,WANG等[52]研究表明骨髓间充质干细胞能够减弱中性粒细胞浸润进而控制基质金属蛋白酶9的表达。当脑缺血发作后,中性粒细胞迁移并通过细胞内黏附分子 1 ,在脑内皮中释放巨量基质金属蛋白酶9,但骨髓间充质干细胞可激发AMP活化激酶(AMPK)的磷酸化进而抑制细胞内黏附分子 1。汤光辉[53]研究发现骨髓间充质干细胞能通过下调水通道蛋白4表达维持血脑屏障完整性。 中药联合骨髓间充质干细胞调控脑缺血再灌注损伤后血脑屏障通透性可通过上述机制表现出较单独治疗更明显的作用。补阳还五汤联合骨髓间充质干细胞运用于大脑中动脉闭塞大鼠实验中,更显著抑制基质金属蛋白酶9/基质金属蛋白酶2表达且下调水通道蛋白4表达[39]。脑脉通联合骨髓间充质干细胞可下调基质金属蛋白酶9表达并上调金属蛋白酶组织抑制因子1表达,阻碍胶原蛋白降解,进而减轻微血管基底膜成分分解,尤以联合28 d效果全面且突出,进而维持血脑屏障血管成分稳定[54]。同样,扎里奴思方联合骨髓间充质干细胞同各自单独使用比较,联合使用干预水通道蛋白4表达而减轻脑水肿的作用更显著[38]。 2.3.3 促进血管新生,挽救缺血半暗带 血管新生是以原有血管网为基础通过血管内皮细胞出芽而形成新生血管的一系列病理过程。多数证据表明,血管新生不仅可以缓解血脑屏障渗漏,而且还有助于改善脑组织血流、神经元代谢和重塑及清除坏死组织。 血管内皮生长因子是一种多效性生长因子,与血管生成及血管通透性有关[55],其主要与酪氨酸激酶受体(血管内皮细胞生长因子受体1、血管内皮细胞生长因子受体2)结合,使得酪氨酸残基磷酸化,协同刺激血管内皮细胞激活参与血管新生[56]。血管内皮生长因子的作用有2个:一则激发细胞外基质降解;二则促进血管内皮细胞增殖存活,诱导新血管形成,是血管新生的关键调控因子。血管内皮生长因子信号通路在急性脑缺血再灌注损伤后的血脑屏障损伤中起重要作用,既往研究发现,由于血管内皮生长因子在急性期脑缺血发生后立即表达上调[57],并促进炎症反应引发血脑屏障渗漏性增加。研究发现,血管生成素可拮抗血管内皮生长因子有害作用[58],若在脑缺血再灌注损伤后24 h抑制脑脉管系统中血管内皮生长因子表达,会降低基质金属蛋白酶2,9表达,升高胶原蛋白Ⅳ水平,增加咬合蛋白表达,维持紧密连接闭合,进而稳定基底层结构[59]。间隙连接介导的间充质干细胞移植可与脑微血管内皮细胞之间相互作用,抑制血管内皮生长因子的摄取和炎症反应,确保血脑屏障的稳定性[60]。 血管生成素为内皮细胞中特异性表达的促血管生成因子,与酪氨酸激酶受体Tie结合促发血管新生。血管生成素1、血管生成素2为研究热点,影响有2个:一是降低血管内皮生长因子诱导血脑屏障通透性,并与基质金属蛋白酶9活性降低密切相关;二是降低内皮细胞通透性,介导信号经血管内皮细胞表达的Tie2诱导血管重塑及稳定。血管生成素1调控信号通路:①经Tie2分别激活PI3K-AKt通路,抑制细胞凋亡,进而起到稳定并保持脑微血管内皮细胞连续性[61];②脑缺血再灌注损伤后胶原蛋白Ⅳ降解与血脑屏障渗透持续增加相一致;而血管生成素1经DII4/Notch通路提高胶原蛋白Ⅳ表达,促进主要血管稳定性和基底膜稳定从而降低血脑屏障渗透性[62];③血管生成素1经转化生长因子β通路抑制血管纤维化。研究发现,薏苡仁对血脑屏障的保护作用是通过转化生长因子β通路促进血管生成而发生的,与其协同阻止血管纤维化[63]。但血管生成素2作为天然拮抗剂对抗血管生成素1信号通路保护血脑屏障通透性有待更深研究。 川芎嗪[64]、清热化瘀方[65]、脑脉通1号联合骨髓间充质干细胞起协同作用上调标记物CD31或血管内皮生长因子表达且改善缺血半暗带血管新生较骨髓间充质干细胞组更为显著[66]。补阳还五汤联合骨髓间充质干细胞通过PI3K-Akt信号通路发挥协同增效作用对血管再生效果强于单独移植组[67]。灯盏花素[68]、补阳还五汤联合骨髓间充质干细胞通过升高胶质纤维酸性蛋白表达促进血管新生[69]。黄芪甲苷与三七总甲苷联合骨髓间充质干细胞输注对提高血管生成素1与转化生长因子β表达修复受损血管效应优于单用药物或骨髓间充质干细胞输注[70]。 2.3.4 抑制炎性递质释放 脑缺血再灌注损伤后活性氧产生为脑损伤第一步,主要来源于线粒体,并在传递过程中产生超氧阴离子自由基,参与氧化应激反应和细胞毒性物质的释放,是造成紧密连接破坏、血脑屏障损伤的关键因素;另一方面,血脑屏障常驻细胞群分泌炎症递质通过核因子κB、丝裂原活化蛋白激酶及激活蛋白1等炎症信号通路激活转录因子,使得细胞因子、趋化因子、黏附因子和促炎递质聚集释放,导致脑缺血再灌注损伤向炎性损伤转化,产生大量蛋白水解酶等效应分子,破坏脑微血管内皮细胞及基底膜,诱发脑水肿;然而,血脑屏障受损后又反过来加重上述复杂神经炎症级联反应。可见,抑制活性氧来源、直接清除自由基、提高组织抗氧化能力、抑制炎性递质释放的药物替代疗法为治疗方向又一靶点。现有研究对于中药和骨髓间充质干细胞抗氧化作用、阻断炎性递质释放已有共识。中药联合骨髓间充质干细胞的抗炎、抗氧化机制主要有4个方面:①通过抗过氧化物酶4发挥抗氧化作用;②通过核因子E2相关因子2(nuclearfactor erythroidderived 2-like 2,Nrf2)信号通路,增强其他抗氧化酶分泌;③抑制小胶质细胞M1表型,促进M2表型,减弱促细胞因子表达,抑制神经炎症;④抑制TXNIP/NLRP3炎症激活减轻血脑屏障功能障碍。 过氧化物酶4是一种高效抗氧化酶,在脑微血管内皮细胞中高度表达,并作为膜相关过氧化酶在内皮中发挥重要作用。脑缺血再灌注损伤期间,过量活性氧激活酶和脂质等信号级联,使基质金属蛋白酶表达上调,通过肿瘤坏死因子α、白细胞介素1等促炎细胞因子,导致血脑屏障功能障碍,但相反过氧化物酶4可清除活性氧,抑制转录因子NF-κB激活,发挥血脑屏障抗氧化保护作用。HUANG等[71]研究发现,过氧化还原蛋白过氧化物酶于骨髓间充质干细胞治疗后高度表达,可见骨髓间充质干细胞治疗起到稳定血脑屏障通透性的作用。 Nrf2是广泛存在于细胞内重要的脑保护转录因子,可识别且结合300个抗氧化反应元件以启动目的基因表达,调节下游多种解毒酶及抗氧化酶表达,研究证实其介导Nrf2/HO-1信号通路是对炎症、氧化应激至关重要的细胞防御机制。正常生理状态下,负性调节蛋白Keap1与Nrf2以复合体形式存在并无活性,脑缺血再灌注后活性氧大量产生,一方面Keap1半胱胺酸残基氧化,构象改变,Nrf2降解减少,复合体结构解离;另一方面研究表明骨髓间充质干细胞分泌活性因子对Nrf2信号通路有两方面的作用[72]:一是其受到氧化应激刺激从胞质转移至细胞核,激发醌氧化还原酶等抗氧化反应;二是其能经Nrf2信号通路消除活性氧等有害物质,从而提高组织活细胞抗氧化能力。Nrf2保护作用机制在体外实验敲除Nrf2后其作用明显抑制得到证实[73];重要的是,Nrf2的靶基因血红素加氧酶1将促炎游离血红素分解为抗炎化合物和胆红素以发挥重要抗炎作用[74]。此外,一些Nrf2激活剂如富马酸二甲酯、萝卜硫酸,无论是体内实验证实其激活后阻止紧密连接破坏、缝隙连接形成、降低基质金属蛋白酶活性,还是体外实验证实其激活稳定紧密连接、降低炎性细胞因子释放、白细胞迁移,均表现出对脑缺血再灌注损伤后血脑屏障的保护作用[75]。 小胶质细胞是具有吞噬活性的免疫监控细胞,其活化后迅速启动炎症程序,使得表面抗原、形态改变。活化后小胶质细胞表现为2种功能分型:促炎型M1或抗炎型M2,神经炎性损伤尤以M1型为主导;脑缺血再灌注损伤后,M1型快速增殖迁移到受损区域,继而释放促炎细胞因子(白细胞介素1β、肿瘤坏死因子α、白细胞介素6)及趋化因子,募集白细胞、分泌活性氧、升高基质金属蛋白酶,破坏脑微血管内皮细胞,加重血脑屏障损害。可溶性Robo4蛋白由M1型小胶质细胞分泌,为内皮细胞特异性抗体,主要调控内皮细胞增殖、迁移,研究表明其可经Src-Erk1/2-MMP9信号通路干扰内皮细胞紧密连接正常表达,增加血脑屏障通透性[76];另一方面,跨膜酪氨酸激酶受体稳定脑微血管内皮细胞中紧密连接,当其与Ephrin-A1结合时自身磷酸化,破坏紧密连接,增加血脑屏障通透性;同时,小胶质细胞中NF-κB核移位增加脑缺血再灌注损伤后M1型过度表达肿瘤坏死因子α,引起内皮细胞程序性死亡,破坏血脑屏障。 厚朴酚保护脑缺血再灌注损伤后血脑屏障功能作用机制包括[77]:①抑制NF-κB核易位,减弱小胶质细胞促炎递质过度表达;②抑制肝配蛋白A1转化,降低紧密连接降解,增加跨内皮电阻,降低闭锁小带蛋白1、咬合蛋白表达,保护脑微血管内皮细胞;③抑制炎性递质肿瘤坏死因子α、白细胞介素1β、一氧化氮表达。 麦冬含有的芸香苷元成分可经TXNIP/NLRP3炎性体阻碍caspase-1、白细胞介素1β表达,调节血脑屏障及炎性小体[78]。靳晓飞等[79]建立大脑中动脉闭塞大鼠脑缺血再灌注损伤模型,黄芪甲苷组酶联免疫吸附实验检测到脑组织炎症因子肿瘤坏死因子α、白细胞介素1β和白细胞介素6含量均明显下降,表明其对血脑屏障保护与抗炎机制密切相关。郑娜[80]表明补肾中药如巴戟天、山茱萸及其两者有效成分巴戟甲素、山茱萸环烯宓萜苷均对小胶质细胞向M1型极化具有抑制作用。 中药联合骨髓间充质干细胞调控脑缺血再灌注损伤后血脑屏障通透性可通过上述机制且表现出较单独治疗更明显的协调作用。刘雪[81]研究发现,应用酶联免疫吸附剂测定大脑中动脉闭塞模型中炎性因子表达,结果显示:在骨髓间充质干细胞治疗组与铁皮石斛主要成分铁皮石斛多糖共培养的神经样细胞组均低,更重要的是,联合共同培养组肿瘤坏死因子α、白细胞介素1β和白细胞介素6表达显著低于其他单独治疗组。 2.3.5 调控外泌体 外泌体广泛分布于体液中,是细胞释放到外部的脂质双层膜包裹的囊泡,具备免疫原性低、耐受性好、递送效率高等特点,其包括蛋白质、mRNA、miRNA、DNA片段等成分,既可介导细胞间通讯,又在调控缺血再灌注损伤、血管炎症反应、细胞凋亡分化发挥关键作用。其中miRNA是外泌体核心物质,也作为调节脑缺血再灌注损伤后血脑屏障的重要调节分子,几乎涵盖影响血脑屏障结构和功能的各个病理损伤形式,如破坏紧密连接、基质金属蛋白酶9、水通道蛋白4,凋亡和神经炎症,而这些病理过程可能会加剧血脑屏障功能障碍,同时病理条件下,血脑屏障能够加速对外泌体摄取[82]。 介于miRNA种类繁多,且对血脑屏障具有双向调节作用,研究也层出不穷,GE等[83]研究发现骨髓间充质干细胞来源外泌体中miR-21-3p增加介导靶向MAT2B促进细胞凋亡和炎症,从而加重血脑屏障损伤。但最新研究验证出骨髓间充质干细胞来源外泌体中miR-21-5p对血脑屏障保护机制有4个方面[84]:①调控NF-κB信号通路传导或炎症因子来抑制炎症;②调节细胞凋亡因子和Akt信号通路来抑制细胞凋亡;③促进稳定血脑屏障相关的Ang-1/Tie轴活化;④外泌体中miR-21-5p水平上调可减轻内皮屏障损伤和紧密连接损失。另外,miR-29b被认为是血脑屏障功能障碍调节器,调节基质金属蛋白酶9、水通道蛋白4表达稳定血脑屏障并减轻脑水肿[85-86];骨髓间充质干细胞来源外泌体介导的miR-124-1调控小胶质细胞向M2型极化[87]。可见,干预miRNA可经不同机制成为保护血脑屏障有前景的因子,在未来研究鉴定可预测血脑屏障损伤的miRNA是非常必要和可能的。 姜黄素(cur)与其他抗氧化剂相比,独有抗氧化活性强、抗凋亡、清除自由基等优势稳定血脑屏障完整性,同时,其稳定性差及难以穿过血脑屏障的缺点使得其难以发挥更好的抗氧化损伤作用。研究发现外泌体包裹姜黄素组(Ex-cur)与单独姜黄素组相比[88]:①姜黄素积累且活性、稳定性更强;②消除活性氧生成;③维持线粒体膜电位,减少线粒体介导的细胞凋亡;④抑制紧密连接降解,诱导咬合蛋白、紧密连接蛋白5更高表达,减轻脑缺血再灌注损伤后血脑屏障破坏而发挥神经保护作用。 中药联合骨髓间充质干细胞可经外泌体调控脑缺血再灌注损伤后血脑屏障通透性,芎归方联合骨髓间充质干细胞来源外泌体对血脑屏障作用均可通过以下机制[89-90]:①明显减轻脑水肿;②抑制炎症细胞及肿瘤坏死因子α、诱导型一氧化氮合成酶mRNA表达而降低M1型小胶质细胞表达;上调抗炎因子白细胞介素13表达而促进M2型小胶质细胞表达;③抑制神经元凋亡,重塑突触。 中药及有效成分联合骨髓间充质干细胞调控脑缺血再灌注损伤后血脑屏障作用机制总结见表1;中药及其复方调控脑缺血再灌注损伤后血脑屏障作用机制见表2;骨髓间充质干细胞调控脑缺血再灌注损伤后血脑屏障作用机制见表3。"

| [1] OTERO-ORTEGA L, LASO-GARCÍA F, GÓMEZ-DE FRUTOS M, et al. Role of Exosomes as a Treatment and Potential Biomarker for Stroke. Transl Stroke Res. 2019;10(3):241-249. [2] THRIFT AG, HOWARD G, CADILHAC DA, et al. Global stroke statistics: An update of mortality data from countries using a broad code of “cerebrovascular diseases”. Int J Stroke. 2017;12(8): 796-801. [3] YARYGIN KN, NAMESTNIKOVA DD, SUKHINICH KK, et al. Cell Therapy of Stroke: Do the Intra-Arterially Transplanted Mesenchymal Stem Cells Cross the Blood-Brain Barrier? Cells. 2021; 10(11):2997. [4] LALU MM, MONTROY J, DOWLATSHAHI D, et al. From the Lab to Patients: a Systematic Review and Meta-Analysis of Mesenchymal Stem Cell Therapy for Stroke. Transl Stroke Res. 2020; 11(3):345-364. [5] 刘抒雯,杨丽华,马春,等.中医药保护脑缺血再灌注损伤后神经血管单元的作用[J].中国实验方剂学杂志,2018,24(23):225-234. [6] SWEENEY MD, SAGARE AP, ZLOKOVIC BV. Blood-brain barrier breakdown in Alzheimer disease and other neurodegenerative disorders. Nature Rev Neurol. 2018;14(3):133-150. [7] JIA W, LU R, MARTIN TA, et al. The role of claudin-5 in blood-brain barrier (BBB) and brain metastases (review). Mol Med Rep. 2014;9(3):779-785. [8] SWEENEY MD, AYYADURAI S, ZLOKOVIC BV. Pericytes of the neurovascular unit: key functions and signaling pathways. Nat Neurosci. 2016;19(6):771-783. [9] LV J, HU W, YANG Z, et al. Focusing on claudin-5: A promising candidate in the regulation of BBB to treat ischemic stroke. Prog Neurobiol. 2018;161:79-96. [10] LIAO Z, YANG Z, PIONTEK A, et al. Specific binding of a mutated fragment of Clostridium perfringens enterotoxin to endothelial claudin- 5 and its modulation of cerebral vascular permeability. Neuroscience. 2016;327:53-63. [11] DIAZ R, MIGUEL PM, DENIZ BF, et al. Environmental enrichment attenuates the blood brain barrier dysfunction induced by the neonatal hypoxia- ischemia. Int J Dev Neurosci. 2016;53:35-45. [12] 张楠.王思迪.涂盼春.等.紧密连接相关蛋白对血脑屏障通透性影响的研究进展[J].沈阳医学院学报,2017,19(1):72-75. [13] XIONG R, ZHOU XG, TANG Y, et al. Lychee seed polyphenol protects the blood-brain barrier through inhibiting Aβ(25-35)-induced NLRP3 inflammasome activation via the AMPK/mTOR/ULK1-mediated autophagy in bEnd.3 cells and APP/PS1 mice. Phytother Res. 2021;35(2):954-973. [14] NIKOLAKOPOULOU AM, ZHAO Z, MONTAGNE A, et al. Regional early and progressive loss of brain pericytes but not vascular smooth muscle cells in adult mice with disrupted platelet-derived growth factor receptor-β signaling. PLoS One. 2017;12(4):e0176225. [15] ALVAREZ JI, DODELET-DEVILLERS A, KEBIR H, et al. The Hedgehog pathway promotes blood-brain barrier integrity and CNS immune quiescence. Science. 2011;334(6063):1727-1731. [16] OBERMEIER B, DANEMAN R, RANSOHOFF RM. Development, maintenance and disruption of the blood-brain barrier. Nat Med. 2013;19(12):1584-1596. [17] MA Y, YANG X, CHATTERJEE V, et al. Role of Neutrophil Extracellular Traps and Vesicles in Regulating Vascular Endothelial Permeability. Front Immunol. 2019;10:1037. [18] QIU YM, ZHANG CL, CHEN AQ, et al. Immune Cells in the BBB Disruption After Acute Ischemic Stroke: Targets for Immune Therapy? Front Immunol. 2021;12:678744. [19] ZHAO Y, GAN L, REN L, et al. Factors influencing the blood-brain barrier permeability. Brain Res. 2022;1788:147937. [20] CHEN R, SONG Z, DENG M, et al. TIMP-2 Polymorphisms Define Subtypes of Hypertensive Intracerebral Hemorrhage with Distinct Perihematomal Edema Development Patterns. Curr Neurovasc Res. 2020;17(1):44-49. [21] KATADA R, AKDEMIR G, ASAVAPANUMAS N, et al. Greatly improved survival and neuroprotection in aquaporin-4-knockout mice following global cerebral ischemia. FASEB J. 2014;28(2):705-714. [22] SHEN Y, GU J, LIU Z, et al. Inhibition of HIF-1α Reduced Blood Brain Barrier Damage by Regulating MMP-2 and VEGF During Acute Cerebral Ischemia. Front Cell Neurosci. 2018;12:288. [23] MICHINAGA S, KIMURA A, HATANAKA S, et al. Delayed Administration of BQ788, an ETB Antagonist, after Experimental Traumatic Brain Injury Promotes Recovery of Blood-Brain Barrier Function and a Reduction of Cerebral Edema in Mice. J Neurotrauma. 2018;35(13):1481-1494. [24] 张伟,吴晓丹,刘海旭,等.中医药对缺血性中风后血脑屏障保护作用的研究进展[J].中国医药,2021,16(1):149-152. [25] SALMINA AB, KHARITONOVA EV, GORINA YV, et al. Blood-Brain Barrier and Neurovascular Unit In Vitro Models for Studying Mitochondria-Driven Molecular Mechanisms of Neurodegeneration. Int J Mol Sci. 2021;22(9):4661. [26] 苏晓梅,张丹参.细胞间线粒体转移治疗缺血性脑卒中研究进展[J].中国药理学与毒理学杂志,2021,35(6):462-470. [27] LEE MJ, JANG Y, HAN J, et al. Endothelial-specific Crif1 deletion induces BBB maturation and disruption via the alteration of actin dynamics by impaired mitochondrial respiration. J Cereb Blood Flow Metab. 2020;40(7):1546-1561. [28] DUPONT M, SOURIANT S, LUGO-VILLARINO G, et al. Tunneling Nanotubes: Intimate Communication between Myeloid Cells. Front Immunol. 2018;9:43. [29] PISANI F, CASTAGNOLA V, SIMONE L, et al. Role of pericytes in blood-brain barrier preservation during ischemia through tunneling nanotubes. Cell Death Dis. 2022;13(7):582. [30] LIU K, JI K, GUO L, et al. Mesenchymal stem cells rescue injured endothelial cells in an in vitro ischemia-reperfusion model via tunneling nanotube like structure-mediated mitochondrial transfer. Microvasc Res. 2014;92:10-18. [31] LIU K, GUO L, ZHOU Z, et al. Mesenchymal stem cells transfer mitochondria into cerebral microvasculature and promote recovery from ischemic stroke. Microvasc Res. 2019;123:74-80. [32] SHEIKH MH, SOLITO E. Annexin A1: Uncovering the Many Talents of an Old Protein. Int J Mol Sci. 2018;19(4):1045. [33] CRISTANTE E, MCARTHUR S, MAURO C, et al. Identification of an essential endogenous regulator of blood-brain barrier integrity, and its pathological and therapeutic implications. Proc Natl Acad Sci U S A. 2013;110(3):832-841. [34] PARK JC, BAIK SH, HAN SH, et al. Annexin A1 restores Aβ1-42 -induced blood-brain barrier disruption through the inhibition of RhoA-ROCK signaling pathway. Aging Cell. 2017;16(1):149-161. [35] GUSSENHOVEN R, KLEIN L, OPHELDERS DRMG, et al. Annexin A1 as Neuroprotective Determinant for Blood-Brain Barrier Integrity in Neonatal Hypoxic-Ischemic Encephalopathy. J Clin Med. 2019;8(2):137. [36] TANG G, LIU Y, ZHANG Z, et al. Mesenchymal stem cells maintain blood-brain barrier integrity by inhibiting aquaporin-4 upregulation after cerebral ischemia. Stem Cells. 2014;32(12):3150-3162. [37] KIM R, KIM P, LEE CY, et al. Multiple Combination of Angelica gigas Extract and Mesenchymal Stem Cells Enhances Therapeutic Effect. Biol Pharm Bull. 2018;41(12):1748-1756. [38] 刘敬霞,任非非,刘会贤,等.回药扎里奴思方联合BMSCs移植对脑缺血再灌注大鼠BBB紧密连接蛋白的影响[J].中风与神经疾病杂志,2016,33(1):54-59. [39] 张运克,车志英,李可.补阳还五汤联合骨髓间充质干细胞移植脑缺血再灌注大鼠脑组织紧密连接蛋白的表达[J].中国组织工程研究,2019,23(1):55-60. [40] LISJAK M, POTOKAR M, RITUPER B, et al. AQP4e-Based Orthogonal Arrays Regulate Rapid Cell Volume Changes in Astrocytes. J Neurosci. 2017;37(44):10748-10756. [41] 祝连明.益母草碱对缺血性脑损伤大鼠脑组织抗氧化应激及AQP4蛋白表达的影响[J].内蒙古中医药,2018,37(11):96-97. [42] DATTA A, SARMAH D, KAUR H, et al. Post-stroke Impairment of the Blood-Brain Barrier and Perifocal Vasogenic Edema Is Alleviated by Endovascular Mesenchymal Stem Cell Administration: Modulation of the PKCδ/MMP9/AQP4-Mediated Pathway. Mol Neurobiol. 2022;59(5):2758-2775. [43] 刘旋辉,容鹏飞,黄远桃,等.丁苯酞对脑缺血再灌注大鼠AQP4和MMP9表达及磁共振扩散成像的影响[J].老年医学与保健,2019, 25(5):605-609+632. [44] TANG Y, SOROUSH F, SUN S, et al. Protein kinase C-delta inhibition protects blood-brain barrier from sepsis-induced vascular damage. J Neuroinflammation. 2018;15(1):309. [45] HSIEH HL, WU CY, YANG CM. Bradykinin induces matrix metalloproteinase-9 expression and cell migration through a PKC-delta-dependent ERK/Elk-1 pathway in astrocytes. Glia. 2008; 56(6):619-632. [46] CHOU WH, MESSING RO. Hypertensive encephalopathy and the blood-brain barrier: is deltaPKC a gatekeeper? J Clin Invest. 2008;118(1):17-20. [47] LOZITO TP, TUAN RS. Mesenchymal stem cells inhibit both endogenous and exogenous MMPs via secreted TIMPs. J Cell Physiol. 2011;226(2): 385-396. [48] YANG P, TIAN YM, DENG WX, et al. Sijunzi decoction may decrease apoptosis via stabilization of the extracellular matrix following cerebral ischaemia-reperfusion in rats. Exp Ther Med. 2019;18(4):2805-2812. [49] 涂华,胡光强,陈碧琼,等.栀子苷预处理对脑缺血再灌注大鼠血脑屏障的保护作用[J].中风与神经疾病杂志,2015,32(6):508-510. [50] LI JS, LIU JX, SUN J, et al. Effects of rhubarb aglycone on matrix metalloproteinase in cerebral ischemic tissue in rats with bone marrow mesenchymal stem cell transplantation. Zhong Xi Yi Jie He Xue Bao. 2008;6(8):810-816. [51] CHENG Z, WANG L, QU M, et al. Mesenchymal stem cells attenuate blood-brain barrier leakage after cerebral ischemia in mice. J Neuroinflammation. 2018;15(1):135. [52] WANG C, BÖRGER V, SARDARI M, et al. Mesenchymal Stromal Cell-Derived Small Extracellular Vesicles Induce Ischemic Neuroprotection by Modulating Leukocytes and Specifically Neutrophils. Stroke. 2020; 51(6):1825-1834. [53] 汤光辉.骨髓间充质干细胞抑制水通道蛋白4的上调减轻脑缺血诱发的脑水肿的分子机理研究[D].上海:上海交通大学,2014. [54] 孙捷.脑脉通联合骨髓间充质干细胞移植对脑缺血再灌注大鼠微血管损伤的保护作用[D].郑州:河南中医学院,2007. [55] GREENBERG DA, JIN K. Vascular endothelial growth factors (VEGFs) and stroke. Cell Mol Life Sci. 2013;70(10):1753-1761. [56] ZHENG H, LIU C, OU Y, et al. Total saponins of Panax notoginseng enhance VEGF and relative receptors signals and promote angiogenesis derived from rat bone marrow mesenchymal stem cells. J Ethnopharmacol. 2013;147(3):595-602. [57] ZHANG ZG, ZHANG L, JIANG Q, et al. VEGF enhances angiogenesis and promotes blood-brain barrier leakage in the ischemic brain. J Clin Invest. 2000;106(7):829-838. [58] VALABLE S, MONTANER J, BELLAIL A, et al. VEGF-induced BBB permeability is associated with an MMP-9 activity increase in cerebral ischemia: both effects decreased by Ang-1. J Cereb Blood Flow Metab. 2005;25(11):1491-1504. [59] ZHANG HT, ZHANG P, GAO Y, et al. Early VEGF inhibition attenuates blood-brain barrier disruption in ischemic rat brains by regulating the expression of MMPs. Mol Med Rep. 2017; 15(1):57-64. [60] KIKUCHI-TAURA A, OKINAKA Y, SAINO O, et al. Gap junction-mediated cell-cell interaction between transplanted mesenchymal stem cells and vascular endothelium in stroke. Stem Cells. 2021;39(7):904-912. [61] 王延,钱海兵. Ang-1/Tie-2信号通路与缺血性脑卒中的相关性研究述评[J].中国中医基础医学杂志,2021,27(1):170-172,177. [62] 春花,黄骥翀,赵凤艳,等.血管生成素2对血脑屏障的调控作用与相关机制研究[J].高原科学研究,2022,6(1):76-81. [63] DU J, YIN G, HU Y, et al. Coicis semen protects against focal cerebral ischemia-reperfusion injury by inhibiting oxidative stress and promoting angiogenesis via the TGFβ/ALK1/Smad1/5 signaling pathway. Aging (Albany NY). 2020;13(1):877-893. [64] LI L, CHU L, REN C, et al. Enhanced Migration of Bone Marrow-Derived Mesenchymal Stem Cells with Tetramethylpyrazine and Its Synergistic Effect on Angiogenesis and Neurogenesis After Cerebral Ischemia in Rats. Stem Cells Dev. 2019;28(13):871-881. [65] 秦红玲,农必华,陈炜,等.清热化瘀方联合骨髓间充质干细胞移植对脑缺血再灌注损伤大鼠血管新生的影响[J].现代中西医结合杂志,2017,26(25):2747-2750. [66] 陈朝.脑脉一号联合骨髓间充质干细胞移植对缺血中风大鼠脑微血管生成的影响[D].广州:广州中医药大学,2010. [67] 王燃冰,胡红艳,刘颖,等.益气活血类中药及骨髓间充质干细胞对脑血管新生相关血管内皮生长因子及其受体影响的研究进展[J].中医临床研究,2015,7(4):144-145+148. [68] 周瑸,于筠,袁鲁,等.灯盏花素联合骨髓间充质干细胞治疗鼠脑梗塞模型的研究[C].上海:中国中西医结合学会神经外科专业委员会第四届学术大会论文集,2017. [69] 张运克,高峰,张丹,等.补阳还五汤联合骨髓间充质干细胞移植对脑缺血再灌注大鼠脑组织NSE和GFAP表达的影响[J].中医杂志,2013,54(23):2043-2045. [70] 李艳玲,丁煌,杨芙蓉,等.黄芪甲苷配伍三七总皂苷对脑缺血大鼠BMSCs移植后血管新生的影响[J].中国实验方剂学杂志,2021,27(21):73-79. [71] HUANG Y, WANG J, CAI J, et al. Targeted homing of CCR2-overexpressing mesenchymal stromal cells to ischemic brain enhances post-stroke recovery partially through PRDX4-mediated blood-brain barrier preservation. Theranostics. 2018;8(21):5929-5944. [72] CHEN X, LIANG H, XI Z, et al. BM-MSC Transplantation Alleviates Intracerebral Hemorrhage-Induced Brain Injury, Promotes Astrocytes Vimentin Expression, and Enhances Astrocytes Antioxidation via the Cx43/Nrf2/HO-1 Axis. Front Cell Dev Biol. 2020;8:302. [73] ZHOU F, WANG M, JU J, et al. Schizandrin A protects against cerebral ischemia-reperfusion injury by suppressing inflammation and oxidative stress and regulating the AMPK/Nrf2 pathway regulation. Am J Transl Res. 2019;11(1):199-209. [74] 张昊悦,赵蓓,王业皇,等.大黄素通过调节Nrf2/HO-1和MAPKs抑制炎症和氧化应激机制研究[J].中国免疫学杂志,2021,37(9): 1063-1068. [75] MAO L, YANG T, LI X, et al. Protective effects of sulforaphane in experimental vascular cognitive impairment: Contribution of the Nrf2 pathway. J Cereb Blood Flow Metab. 2019;39(2):352-366. [76] 黄锦龙,李宸,杨亮亮,等.脑缺血再灌注小鼠M1极化的小胶质细胞分泌的可溶性Robo4对血脑屏障完整性的破坏作用[J].生理学报,2022,74(4):513-524. [77] LIU X, CHEN X, ZHU Y, et al. Effect of magnolol on cerebral injury and blood brain barrier dysfunction induced by ischemia-reperfusion in vivo and in vitro. Metab Brain Dis. 2017;32(4): 1109-1118. [78] CAO G, JIANG N, HU Y, et al. Ruscogenin Attenuates Cerebral Ischemia-Induced Blood-Brain Barrier Dysfunction by Suppressing TXNIP/NLRP3 Inflammasome Activation and the MAPK Pathway. Int J Mol Sci. 2016;17(9):1418. [79] 靳晓飞,张彐宁,周晓红,等.黄芪甲苷对脑缺血再灌注大鼠炎症因子及超微结构的影响[J].中国比较医学杂志,2020,30(4):1-6. [80] 郑娜.补肾中药有效成分对小胶质细胞极化的调节及机制研究[D].广州:广州中医药大学,2017. [81] 刘雪.铁皮石斛多糖对骨髓间充质干细胞向神经样细胞分化及MCAO模型大鼠预后的影响[D].合肥:安徽医科大学,2020. [82] 李祺,王秀,杜丽娜.外泌体在脑靶向递送中的应用[J].药学学报,2022,57(3):658-669. [83] GE X, LI W, HUANG S, et al. Increased miR-21-3p in Injured Brain Microvascular Endothelial Cells after Traumatic Brain Injury Aggravates Blood-Brain Barrier Damage by Promoting Cellular Apoptosis and Inflammation through Targeting MAT2B. J Neurotrauma. 2019;36(8):1291-1305. [84] GE X, HUANG S, GAO H, et al. miR-21-5p alleviates leakage of injured brain microvascular endothelial barrier in vitro through suppressing inflammation and apoptosis. Brain Res. 2016; 1650:31-40. [85] KALANI A, KAMAT PK, FAMILTSEVA A, et al. Role of microRNA29b in blood-brain barrier dysfunction during hyperhomocysteinemia: an epigenetic mechanism. J Cereb Blood Flow Metab. 2014;34(7):1212-1222. [86] WANG Y, HUANG J, MA Y, et al. MicroRNA-29b is a therapeutic target in cerebral ischemia associated with aquaporin 4. J Cereb Blood Flow Metab. 2015;35(12):1977-1984. [87] 郝磊,金戈,杨涌涛,等.骨髓间充质干细胞外泌体介导miR-124-1对小胶质细胞M2型极化调控的影响[J].上海交通大学学报(医学版),2022,42(3):323-330. [88] HE R, JIANG Y, SHI Y, et al. Curcumin-laden exosomes target ischemic brain tissue and alleviate cerebral ischemia-reperfusion injury by inhibiting ROS-mediated mitochondrial apoptosis. Mater Sci Eng C Mater Biol Appl. 2020;117:111314. [89] 姜萌萌.芎归方协同BMSCs-exosomes干预脑卒中神经炎症的效应研究[D].天津:天津中医药大学,2021. [90] 白晓丹.芎归方协同BMSCs-exosomes干预缺血性脑损伤神经重塑的作用研究[D].天津:天津中医药大学,2020. [91] CHEN L, LI Y, CHEN W, et al. Enhanced recruitment and hematopoietic reconstitution of bone marrow-derived mesenchymal stem cells in bone marrow failure by the SDF-1/CXCR4. J Tissue Eng Regen Med. 2020;14(9):1250-1260. [92] 胡跃强,陈海峰,甘业贤,等.缺氧预处理MSCs移植对脑缺血再灌注损伤大鼠SDF-1/CXCR4表达的影响及清热化瘀方的干预作用[J].中药新药与临床药理,2016,27(6):779-784. [93] 陆吴超,钱伟宏,姚志宏,等.补肾、活血中药及补肾活血复方对骨髓间充质干细胞增殖、定向迁移及成骨分化的影响及作用机制的研究进展[J].中医正骨,2018,30(7):36-38. [94] 李琳.川芎嗪预处理促进骨髓间充质干细胞向损伤区迁移提高脑缺血的治疗作用[D].杭州:浙江中医药大学,2015. [95] 曲铁兵.川芎嗪预处理促进骨髓间充质干细胞迁移的体外研究[D].杭州:浙江中医药大学,2014. [96] 汪禹,陈铁龙,梁翠,等.黄芪甲苷提高骨髓间充质干细胞缺氧微环境下耐受性的作用机制研究[J].中国现代应用药学,2021,38(7): 814-819. [97] 包翠芬,包翠芳,李磊,等.人参皂苷Rg1联合BMSCs对大鼠脑缺血再灌注损伤的保护作用[J].山东医药,2012,52(25):9-11. |
| [1] | Nong Fuxiang, Jiang Zhixiong, Li Yinghao, Xu Wencong, Shi Zhilan, Luo Hui, Zhang Qinglang, Zhong Shuang, Tang Meiwen. Bone cement augmented proximal femoral nail antirotation for type A3.3 intertrochanteric femoral fracturalysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-10. |
| [2] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [3] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [4] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [5] | Wang Ji, Zhang Min, Yang Zhongya, Zhang Long. A review of physical activity intervention in type 2 diabetes mellitus with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1272-1277. |
| [6] | Nie Chenchen, Su Kaiqi, Gao Jing, Fan Yongfu, Ruan Xiaodi, Yuan Jie, Duan Zhaoyuan, Feng Xiaodong. The regulatory role of circular RNAs in cerebral ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1286-1291. |
| [7] | Gao Yu, Han Jiahui, Ge Xin. Immunoinflammatory microenvironment after spinal cord ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1300-1305. |
| [8] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [9] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [10] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [11] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| [12] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [13] | Liu Wentao, Feng Xingchao, Yang Yi, Bai Shengbin. Effect of M2 macrophage-derived exosomes on osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 840-845. |
| [14] | Long Yanming, Xie Mengsheng, Huang Jiajie, Xue Wenli, Rong Hui, Li Xiaojie. Casein kinase 2-interaction protein-1 regulates the osteogenic ability of bone marrow mesenchymal stem cells in osteoporosis rats [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 878-882. |
| [15] | Li Qicheng, Deng Jin, Fu Xiaoyang, Han Na. Effects of bone marrow mesenchymal stem cells-derived exosomes on hypoxia-treated myoblasts [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 853-859. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||