Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (15): 2385-2394.doi: 10.12307/2023.361
Previous Articles Next Articles
Action mechanism of traditional Chinese medicine to regulate neural stem cells in treatment of Alzheimer’s disease
Ying Chunmiao1, Ma Yucheng1, Fan Feiyan1, Gao Chen1, Wang Shaona1, Yang Xing1, Zhang Yunke1, 2
- 1Henan University of Chinese Medicine, Zhengzhou 450046, Henan Province, China; 2First Affiliated Hospital of Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China
-
Received:2022-05-05Accepted:2022-06-25Online:2023-05-28Published:2022-10-18 -
Contact:Zhang Yunke, MD, Professor, Chief physician, Doctoral supervisor, Post-doctoral cooperative supervisor, Henan University of Chinese Medicine, Zhengzhou 450046, Henan Province, China; First Affiliated Hospital of Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China -
About author:Ying Chunmiao, Master candidate, Henan University of Chinese Medicine, Zhengzhou 450046, Henan Province, China -
Supported by:the National Natural Science Foundation of China, No. 81974564 (to ZYK); the Zhongyuan Talent Program - Science and Technology Innovation Leading Talent Project, No. 224200510027 (to ZYK)
CLC Number:
Cite this article
Ying Chunmiao, Ma Yucheng, Fan Feiyan, Gao Chen, Wang Shaona, Yang Xing, Zhang Yunke. Action mechanism of traditional Chinese medicine to regulate neural stem cells in treatment of Alzheimer’s disease[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(15): 2385-2394.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
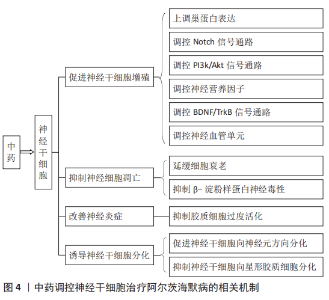
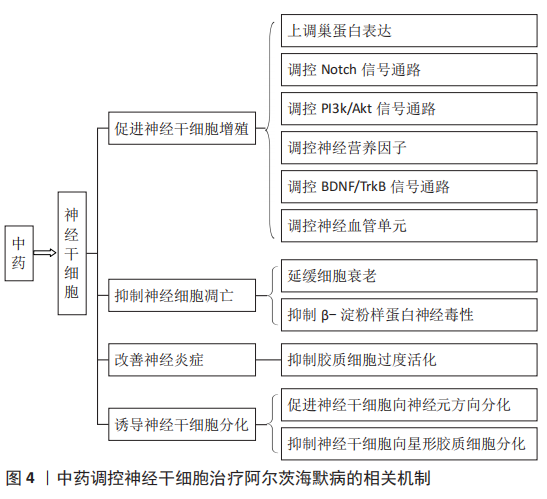
2.2 中药促进神经干细胞增殖 2.2.1 中药上调巢蛋白表达 巢蛋白(Nestin)又被称为神经上皮干细胞蛋白,来自成人大脑的巢蛋白阳性细胞能够在体外形成神经球并产生神经元和星形细胞谱系的分化细胞[20]。研究发现,海马神经发生与巢蛋白阳性细胞的改善呈正相关[21],巢蛋白基因的缺失会造成神经干细胞自我更新、代谢能力下降,增殖能力减弱,增加细胞死亡率[22]。巢蛋白在周围和中枢神经系统增殖强烈的前体细胞中表达,因此常作为神经干细胞的分子标记及增殖标志物[23]。 研究发现,石菖蒲[24-25]、草苁蓉[26]、蛇床子素[27-28]、山茱萸环烯醚萜苷[29]、酸枣仁苷A[30]、槲皮素[31]、灵芝多糖[32]、人参皂苷和黄芩苷[33]、穿心莲内酯[34]、补肾活血方[35]、黄精丸[36]、开心散等均可增加脑组织中巢蛋白表达[37]。石菖蒲可显著增加小鼠大脑内巢蛋白的含量,增加小鼠脑内成神经细胞和未成熟神经元的数量,提高新生细胞存活率[24-25]。草苁蓉提取物可明显增强大鼠海马中巢蛋白的免疫活性表达[26],参与阿尔茨海默病大鼠神经缺损的修复。蛇床子素能够增强巢蛋白阳性表达[27-28], 显著增加小鼠脑室下区、颗粒下区和脑损伤区域的Nestin/BrdU和Sox2/BrdU阳性细胞数量,通过促进内源性神经干细胞的增殖改善并恢复神经元,提高神经干细胞活力[38]。山茱萸环烯醚萜苷能够促进海马齿状回颗粒细胞下层的BrdU阳性细胞数目显著增多[29]。灵芝多糖能够显著增加阿尔茨海默病小鼠海马颗粒下区BrdU/NeuN双阳性细胞的数量,且呈剂量依赖型增加[32]。人参皂苷和黄芩苷能够增强阿尔茨海默病小鼠脑内巢蛋白和神经元特异性烯醇化酶的表达水平[33],并且人参皂苷能够提高细胞活性,促进神经元存活。黄精丸促进巢蛋白表达呈现明显的量效关系,同时小鼠海马形态结构也有所恢复[36]。 2.2.2 中药增强微管相关蛋白阳性表达 皮质神经元微管相关蛋白是一种微管和肌动蛋白丝相关蛋白,其在发育中以及成人大脑许多区域的神经前体和新生成的未成熟神经元中特异性表达,微管相关蛋白常被用做神经前体和未成熟神经元的特异性标记,用来评估成人大脑内神经发生[39]。 石菖蒲挥发油可以上调阿尔茨海默病模型小鼠脑内微管相关蛋白的表达[24],且小鼠脑内积分吸光度值显著增加,海马齿状回细胞层出现清晰可见的神经元突起和胞体。槲皮素可以显著增加成年齿状回中微管相关蛋白阳性细胞的数量[31]。穿心莲内酯能够显著增加齿状回中微管相关蛋白细胞数量[34],促进成年小鼠海马齿状回中新颗粒神经元的生成。 2.2.3 中药调控Notch信号通路 Notch信号通路通过旁分泌作用于邻近细胞,是调节神经干细胞增殖和分化平衡的主要分子机制之一[40]。Notch信号通路是由Notch受体、Notch配体(Delta和Jagged)和细胞内效应器分子(CSL-DNA结合蛋白)组成,还包括一些调节分子,如糖基转移酶Fringe、Mam蛋白、膜相关蛋白Numb及TLE蛋白等。当配体与受体结合后,Notch分子活化,释放受体胞内段活性结构域,启动Notch下游靶基因Hes1等的转录而发挥调控作用,阻断Notch信号通路后,NICD、Hes1的表达均降低,同时神经干细胞的增殖明显减少[41]。 研究表明,蛇床子素[27,42]、姜黄素[43]、黄芪甲苷均能够上调自我更新基因Notch1和Hes1的表达[44],增加NICD的蛋白表达,激活Notch信号通路,促进内源性神经干细胞增殖。姚璎珈等[28]体外培养神经干细胞研究证实,蛇床子素可通过上调Notch1、Hes1,激活Notch通路,促进神经干细胞增殖。姜黄素能够增加细胞周期蛋白依赖性激酶4、细胞周期素D1(CyclinD1)的蛋白表达共同启动Notch通路,促进内源性神经干细胞增殖和海马神经发生、减少神经元凋亡,有效改善阿尔茨海默病小鼠模型的认知障碍[43]。黄芪甲苷能够刺激早老素1基因下调,延缓衰老,促进神经细胞存活[44]。 2.2.4 中药调控PI3k/Akt信号通路 PI3K/Akt信号通路广泛存在于细胞中,是膜受体信号向细胞内转导的重要途径,在细胞增殖、代谢、凋亡等过程中发挥着关键作用[45]。研究表明,Toll样受体4、补体受体3和成纤维细胞生长因子受体1等膜受体具有介导多糖的作用。成纤维细胞生长因子受体1和血管内皮生长因子受体是碱性成纤维细胞生长因子和表皮生长因子的受体,这是海马中神经祖细胞增殖和自我更新的2个关键生长因子。MEK/ERK和PI3K/AKT级联是成纤维细胞生长因子受体1激活后负责神经祖细胞增殖的2条下游信号通路[46]。 灵芝多糖能够促进细胞ERK磷酸化和AKT磷酸化,激活成纤维细胞生长因子受体1 [32],促进成纤维细胞生长因子受体信号传导影响神经发生。石菖蒲提取物可以作用于MEK/ERK级联,使得ERK活化增强进而促进神经细胞的增殖[25]。穿心莲内酯通过激活PI3K/Akt信号传导刺激神经发生,诱导新生神经元的存活[47]。突触囊泡膜蛋白和突触后致密物95是与调节突触传递和突触可塑性相关的2个重要蛋白质标志物,脑内突触囊泡膜蛋白不足会导致学习记忆障碍,突触后致密物95参与树突棘形成、突触连接及信号转导,并维持突触可塑性[48-49]。蛇床子素能够改善突触囊泡膜蛋白和突触后致密物95的表达,从而有利于神经元功能和突触重构[50]。 2.2.5 中药调控神经干细胞增殖及其他途径 尼氏体是神经元的代表结构,由大量粗面内质网和游离核糖体组成,在蛋白质合成中起着至关重要的作用[51]。远志提取物能够增加成年大鼠海马CA1区神经干细胞的数量,其有效成分3,6’-二萘基蔗糖(DISS)能够增加尼氏体的数量,促进神经干细胞增殖[52-53]。浦肯野细胞形态的改变是阿尔茨海默病的病理特征之一,阿尔茨海默病患者早期出现的认知、学习功能降低和手指协调运动障碍与小脑浦肯野神经细胞的丢失有关[54]。秦川等[55]研究发现,给予灵芝治疗后,阿尔茨海默病小鼠小脑出现新兴的浦肯野神经细胞,且成长的神经细胞增多,细胞体积、核团增大。钟佩茹等[56]研究发现,给予黄芪皂苷后小鼠脑内神经球数目明显增多,在体外能够促进神经干细胞增殖,发挥治疗阿尔茨海默病的作用。 2.3 中药改善脑内微环境 2.3.1 中药调控神经营养因子 在中枢神经系统中,成熟神经元和神经细胞前体的不同功能、突触活动和可塑性的许多不同方面都受到大脑神经营养因子的调节。神经生长因子、神经营养因子3、脑源性神经营养因子、胶质细胞源性神经营养因子均是中枢神经系统发育和功能的重要调节剂,能够减少宿主内源性神经元的死亡,促进轴突连接并增强移植的神经干细胞存活和植入[57]。脑源性神经营养因子在皮质和海马体中表达,在认知表现中发挥关键作用,是海马和其他大脑区域突触传递和长时程增强的重要调节因子,对突触的正常生长、发育和可塑性有重要作用,参与调节神经元分化[58-59]。神经营养因子3主要在齿状回中表达,在齿状回-CA3突触前末端具有增强作用,参与长时程增强,可以通过阻止胆碱能神经元的退变来改善阿尔茨海默病等神经退行性疾病的学习、记忆功能障碍[60]。缺乏神经营养因子3表达的小鼠会出现齿状回内的神经发生缺陷,并且齿状回-CA3突触处的长时程增强也存在缺陷,使得小鼠在空间记忆方面表现出严重受损[61]。 人参皂苷预处理能够逆转急性固定应激大鼠海马中脑源性神经营养因子蛋白的减少[61],进而对中枢神经系统和周围神经系统发挥作用。槲皮素能够促进参与调节神经发生的脑源性神经营养因子、神经生长因子、环磷腺苷效应元件结合蛋白(cAMP Response Element Binding Protein,CREB)和EGR-1基因的表达[31],增加神经营养因子改善脑内环境。胶质细胞源性神经营养因子是支持神经元存活和发育的重要神经营养因子,在阿尔茨海默病患者中胶质细胞源性神经营养因子水平下调。蛇床子素能够显著提高阿尔茨海默病小鼠脑内胶质细胞源性神经营养因子水平[50],促进神经元存活。山茱萸环烯醚萜苷能够增强穹窿海马伞切断大鼠模型和局灶性脑缺血大鼠模型脑内神经营养因子的表达[62]。石菖蒲挥发油可明显增加小鼠大脑海马区神经营养因子3阳性细胞的表达量[24]。神藻健脑口服液能够显著上调阿尔茨海默病样小鼠齿状回区的脑源性神经营养因子水平,改善小鼠脑内微环境,促进神经元存活[63]。 2.3.2 中药调控脑源性神经营养因子/TrkB信号通路 神经营养因子通过2种受体类型对下游信号级联产生影响:p75神经营养因子受体(p75NTR)和原肌球蛋白受体激酶(Trk)。脑源性神经营养因子是CREB下游效应因子,与TrkB结合,通过激活细胞内区域的酪氨酸激酶活性,引起TrkB自身磷酸化增加,进而激活下游Akt和ERK信号通路,促进神经元生长、生存与分化并对β-淀粉样蛋白引起的阿尔茨海默病神经元损伤起到保护作 用[64-65]。神经生长因子是胆碱能神经元发育中的关键神经营养因子,TrKA是神经生长因子的特异性高亲和力受体。神经生长因子与TrkA结合,能够激活多种信号通路,诱导神经元发育、存活和分化[66]。 石菖蒲挥发油可上调脑源性神经营养因子、TrkB表达,激活脑源性神经营养因子/TrkB信号通路,促进受损神经元恢复功能,延长神经元存活时间[24]。淫羊藿苷能够增加阿尔茨海默病小鼠的pTrkB/TrkB比率,上调阿尔茨海默病大鼠海马中脑源性神经营养因子及其受体TrkB的蛋白表达以及Akt和CREB的磷酸化,通过脑源性神经营养因子/TrkB/Akt途径改变突触可塑性和功能,促进海马神经干细胞的增殖和分化[67-68]。黄芪甲苷能上调脑源性神经营养因子/TrkB通路促进海马齿状回神经发生[69]。远志中的有效成分DISS可以通过CaMKII和ERK1/2途径增加脑源性神经营养因子的表达并促进CREB的磷酸化,促进阿尔茨海默病小鼠模型脑内海马神经发生[70]。蛇床子素能够上调脑源性神经营养因子的表达,并在CREB磷酸化增加后,促进脑源性神经营养因子受体TrkB的活化,刺激APP/PS1转基因小鼠的脑源性神经营养因子/TrkB/CREB信号传导改善神经发生[71]。开心散可促进小鼠长时程增强形成,通过激活环磷酸腺苷依赖的信号通路,使神经生长因子和脑源性神经营养因子表达增加,进而上调突触素的表达,改善小鼠认知障碍[37]。 中药调控神经干细胞治疗阿尔茨海默病的相关机制,见图4。 "

2.4 中药抑制神经元细胞凋亡 2.4.1 中药调控Wnt/β-catenin信号通路 Wnt/β-catenin信号通路是调节成年海马神经发生的关键信号机制。Wnt 通路的激活会减少 tau 磷酸化、β-淀粉样蛋白形成,防止细胞凋亡。它可以通过Wnt靶基因细胞周期素D1的表达来控制神经祖细胞的增殖,细胞周期素D1作为细胞周期蛋白是人类基因CCND1编码蛋白,在正常细胞增殖和生长中起重要作用[72]。糖原合成激酶3β是Wnt/β-catenin信号通路上重要的媒介,能够下调β-淀粉样前体蛋白的非淀粉样蛋白切割。此外,糖原合成激酶3β能够降低β-分泌酶BACE1介导的β-淀粉样前体蛋白切割。在阿尔茨海默病患者大脑中发现Wnt/β-catenin信号途径被抑制,β-catenin水平下降,糖原合成激酶3β水平升高,造成β-淀粉样蛋白大量积累,导致阿尔茨海默病的发生[73]。Wnt-3a是Wnt配体之一,可促进神经干细胞的增殖、存活和分化,星形胶质细胞Wnt-3a表达减少与神经发生减少有关。 蛇床子素能够下调糖原合成激酶3β的mRNA表达,增加β-catenin的mRNA表达,激活Wnt/β-catenin信号通路,促进神经干细胞的增殖和存活,减少神经元凋亡[74]。XIAO等[75]研究发现,淫羊藿苷Ⅱ能够显著上调Wnt-3a表达,增加糖原合酶激酶3β的磷酸化并增强β-连环蛋白的核转移;淫羊藿苷Ⅱ还促进星形胶质细胞分泌Wnt-3a,正向调节Wnt/β-catenin信号通路,促进神经干细胞增殖和神经元分化,呈剂量依赖性地抑制细胞凋亡并提高转染β-淀粉样前体蛋白基因的神经干细胞活力。黄芪甲苷通过Wnt通路下调白细胞介素17的表达来刺激海马神经发生,并且促进海马区神经干细胞的增殖、迁移和分化[69]。姜黄素通过增强β-catenin的核转位和增加糖原合酶激酶3β的磷酸化,激活Wnt/β-catenin信号,并通过与Wnt/β-catenin信号通路抑制基因Wif-1、Dkk-1和糖原合酶激酶3β相互作用调节神经发生,抑制阿尔茨海默病大鼠模型β-淀粉样蛋白神经毒性[76]。穿心莲内酯通过抑制糖原合酶激酶3β减少β-淀粉样蛋白沉积来刺激神经发生[47]。p21是一种参与细胞生长和分化的细胞周期蛋白依赖性激酶抑制剂,能够通过抑制Sox2基因表达来调节神经干细胞自我更新[77]。淫羊藿苷能够增加p21及细胞周期素D1的表达,促进神经干细胞的增殖与更新[78]。 2.4.2 中药抑制β-淀粉样蛋白神经毒性 阿尔茨海默病的病理特征之一是β-淀粉样蛋白斑块聚集形成老年斑,导致脑神经细胞的凋亡,这在阿尔茨海默病患者脑神经元损失中起到至关重要的作用。β-淀粉样蛋白最丰富的形式是40和42残基肽变体β-淀粉样蛋白1-40和β-淀粉样蛋白1-42,在体外和体内直接或间接诱导神经元凋亡[79]。细胞凋亡部分受抗凋亡蛋白Bcl-2和促凋亡蛋白Bax这两种蛋白的调节,如果Bax/Bcl-2的比例过高,DNA的修复能力就会减弱,最终导致细胞解体和凋亡[80]。半胱天冬酶(Caspase)是细胞凋亡的关键介质,其中Caspase-3是一种频繁激活的死亡蛋白酶,可催化许多关键细胞蛋白的特异性切割。Caspase-3参与淀粉样蛋白β前体蛋白的切割,这与阿尔茨海默病的神经元死亡有关[81]。β-淀粉样蛋白1-42诱导阿尔茨海默病小鼠海马中的Bax/Bcl-2比值升高,上调Caspase-3蛋白,导致神经细胞凋亡[82]。热休克蛋白75主要在线粒体中表达,对氧化损伤、局灶性缺血有反应[83],其在维持线粒体功能和细胞存活方面发挥着至关重要的作用,特别是其能够对β-淀粉样蛋白1-42因子诱导的神经毒性发挥保护作用,抑制神经干细胞的凋亡[84- 85]。 丹参提取物通过抑制氧化应激和线粒体依赖性凋亡途径保护SH-SY5Y细胞免受β-淀粉样蛋白25-35诱导的神经毒性[82],对β-淀粉样蛋白25-35诱导的细胞凋亡起到神经保护作用,丹参酮IIA可以降低缺血皮质中caspase-3蛋白表达,增加Bcl-2蛋白表达,减弱大脑中动脉闭塞诱导的细胞凋亡。人参皂苷Rb1可以通过降低阿尔茨海默病大鼠的Bax/Bcl-2比值来抑制神经细胞凋亡,保护神经元[86]。淫羊藿苷能够抑制受到β-淀粉样蛋白影响的大鼠神经元凋亡[87]。雌激素具有多重神经保护及营养作用,研究表明雌激素受体β主要与情绪调节和认知有关。雌激素可以阻止细胞色素C激活Caspase-3,降低Caspase-3、Bcl-2基因相关蛋白和蛋白激酶的表达,下调这些酶类启动的细胞凋亡程序[88-89]。补骨脂异黄酮可以与雌激素受体结合,诱导Bcl-2蛋白上调,在线粒体凋亡中起到抑制因子的作用,阻止细胞色素C的释放,从而阻断线粒体凋亡通路,对β-淀粉样蛋白损伤神经细胞发挥保护作用[90]。梓醇和阿克苷是六味地黄汤的有效成分,梓醇可以降低促凋亡蛋白Bax的表达,增加抗凋亡蛋白Bcl-2的表达,阿克苷可以降低caspase-3表达,减少细胞凋亡[91-92]。蛇床子素通过对Caspase-3的靶向抑制,减弱β-淀粉样蛋白诱导的细胞凋亡[38]。神藻健脑口服液能够显著下调Bax并上调Bcl-2水平,进一步减少齿状回区域中Caspase-3标记的凋亡神经元的数量,抑制神经元凋亡[63]。开心散可以提高β-淀粉样蛋白1-42损伤的神经干细胞存活率,发挥神经保护作用[37]。山茱萸环烯醚萜苷能够通过抑制Tau蛋白过度磷酸化起到神经保护作用[29]。益肾化浊方能够明显提高β-淀粉样蛋白25-35损伤的细胞活力,提高细胞存活率[93]。 2.4.3 中药调控衰老细胞的清除 细胞衰老也被认为是阿尔茨海默病认知能力下降的主要原因。大脑衰老是由神经细胞衰老累积引起的,免疫功能衰退、氧化应激及神经退行性改变是衰老的重要成因,主要表现为线粒体功能障碍、能量代谢受损、衰老相关分泌表型和慢性神经炎症。清除衰老细胞可以防止阿尔茨海默病小鼠的β-淀粉样蛋白沉积、Tau病理学改变和认知能力下降[94]。 刺五加提取液可以抑制β、γ-分泌酶活性,促进α-分泌酶表达,进而减少β-淀粉样蛋白1-42的产生,增加具有保护作用的可溶性淀粉样前体蛋白生成,达到预防阿尔茨海默病的目的[95]。何首乌可提高血清及组织中超氧化物歧化酶活性,降低丙二醛水平,以延缓D-半乳糖大鼠衰老[96]。灵芝可改善老年免疫功能低下状态,拮抗氧化应激所致的组织损伤, 抑制阿尔茨海默病的发生和发展[97]。梓醇可提高超氧化物歧化酶、谷胱甘肽过氧化物酶和过氧化氢酶的活性,降低丙二醛水平,提高Na+-K+-ATP酶和Ca2+-Mg2+ATP酶的活性,通过促进内源性抗氧化酶的活性、降低自由基的产生和改善能量紊乱发挥抗老化作用[98-99]。 2.4.4 中药抑制神经干细胞凋亡 远志有效成分DISS可提高细胞活力并保护SH-SY5Y细胞免受谷氨酸和H2O2诱导的细胞凋亡,改善患有慢性轻度应激大鼠的海马可塑性[100-101]。六味地黄汤中透过血脑屏障的成分梓醇和阿克苷可抑制阿尔茨海默病来源诱导多能干细胞分化的神经干细胞(iPSCd-NSC)凋亡[102]。 2.5 中药减轻神经炎症 2.5.1 中药抑制NF-κB因子 NF-κB是一种诱导型转录因子,在免疫反应、炎症反应、细胞分化以及正常和恶性细胞存活中起核心作用。在哺乳动物中,NF-κB由Rel家族的5个成员的同二聚体和异二聚体组成,包括NF-κB1(p105/p50)、NF-κB2(p100/p52)、RelA(p65)、RelB和c-Rel。促炎转录因子NF-κB是一种非常有效的促炎基因激活剂[103]。 穿心莲内酯通过抑制NF-κB26、85的激活改善炎症,抑制神经细胞凋亡[34]。黄芪多糖能够抑制NF-κB通路的激活,减少下游NF-κB进入细胞核转录,最后降低炎症因子白细胞介素1β和肿瘤坏死因子α的表达,促进神经细胞存活[104]。 2.5.2 中药抑制神经胶质细胞过度活化 小胶质细胞和星形胶质细胞的激活在引发参与阿尔茨海默病的炎症信号通路中起重要作用。反应性星形胶质细胞和小胶质细胞存在于阿尔茨海默病患者的大量老年斑附近[105]。在成人大脑中,小胶质细胞参与调节更高的认知功能,如学习和记忆[106],大脑中有害刺激导致小胶质细胞活化,产生炎症递质,包括趋化因子、细胞因子、诱导型一氧化氮合酶、环氧合酶2和活性氧等自由基,干扰神经元功能并造成细胞损伤。小胶质细胞的持续激活则会导致神经毒性及神经退行性病变,进而发展表现为阿尔茨海默病的临床特征[107]。在被β-淀粉样蛋白激活或出现损伤信号后,星形胶质细胞也会参与分泌炎性细胞因子,包括白细胞介素1、白细胞介素6和肿瘤坏死因子α,从而加速阿尔茨海默病的神经退行性过程[105]。 研究发现,六味地黄汤(LW)及其有效成分六味地黄苷糖(LW-AFC)和寡糖(CA-30)均可减少阿尔茨海默病小鼠脑内小胶质细胞的数量,抑制小胶质细胞的活化[102]。黄芪甲苷可以抑制脑缺血或脑出血急性期星形胶质细胞的过度增生活化和胶质纤维酸性蛋白的过度表达,利于损伤后的神经功能恢复[108]。穿心莲内酯能够降低星形胶质细胞的活化,减少β-淀粉样蛋白刺激的小胶质细胞中促炎细胞因子的表达[47]。 2.6 中药诱导神经干细胞神经向分化的作用 神经干细胞具有分化为神经元的潜力和功能,在一定条件下可以增殖并分化为成熟的神经细胞,补充丢失的神经元,是神经干细胞移植后受损中枢神经系统功能恢复再生的来源[26]。中药可以通过多途径调控神经干细胞向神经元分化,抑制其向星形胶质细胞分化的趋势,进而改善阿尔茨海默病患者脑中神经元缺失状态,达到治疗阿尔茨海默病的目的。 蛇床子素[28]、酸枣仁苷[30]、何首乌[109]、开心散[37]、益肾化浊方均对神经干细胞分化具有双向调节作用[93,110],既能促进神经干细胞向神经元方向分化,同时又具有抑制其向星形胶质细胞分化的趋势,补充阿尔茨海默病条件下神经元的缺失。远志中的有效成分DISS和OB可以有效挽救转染β-淀粉样前体蛋白基因的神经干细胞的分化缺陷,促进其向神经元分化[111]。蛇床子素能够显著上调齿状回和CA3区microRNA-9进而促进转染β-淀粉样前体蛋白的神经干细胞分化成更多的神经元[28]。石菖蒲挥发油可以提高转染β-淀粉样前体蛋白的神经干细胞的增殖能力,并促进其向神经元分化[24]。山茱萸环烯醚萜苷能够促进体外培养的神经干细胞增殖及向神经元分化,并且长期应用能够明显增加海马齿状回颗粒下区新生神经元的数量[29]。补肾活血方促进海马区NeuN细胞数明显增多,蛋白表达上升,促进小鼠海马区神经干细胞向成熟的神经元分化[35]。神藻健脑口服液处理后,小鼠脑组织出现更多被巢蛋白染色的神经干细胞和被BrdU染色的增殖细胞,并且小鼠皮质和海马区成熟神经元数量和突触囊泡膜蛋白的表达均显著增加[63]。益肾化浊方能够降低信号转导和转录激活因子3 、磷酸化信号转导和转录激活因子3、Smad1、胶质纤维酸性蛋白表达[98,110]。在神经系统发育过程中,Neurogenin1(Ngn1)在神经前体细胞中被诱导表达,Ngn1能促进神经细胞分化,并抑制神经胶质细胞分化,是一种神经细胞分化过程中关键的调控蛋白[112]。益肾化浊方同时能够上调Ngn1基因表达,调控JAK/STAT通路,促进神经干细胞向神经元分化。转录激活因子和信号转导因子3和碱性螺旋-环-螺旋家族蛋白是决定神经干细胞分化的重要细胞信号转导因子,黄芩苷能够通过促进转录激活因子和信号转导因子3、碱性螺旋-环-螺旋家族蛋白的磷酸化诱导神经祖细胞向神经元的分化[33,113]。 2.7 中药调控血管神经单元 中枢神经系统的生理过程涉及神经元、血管和神经胶质细胞系统及多种分泌因子的相互协同作用[114]。神经血管单元是一个结构和功能相互依赖的多细胞复合体,主要由神经元、血管内皮细胞、基底膜、周细胞和星形胶质细胞组成,构成了一个解剖和功能的整体,通过血脑屏障的开合调节脑血流及营养物质和代谢废物的出入,维持大脑微环境的稳态平衡,在支持大脑功能方面发挥着重要作用[115]。以血管内皮生长因子为核心的一大类促血管生成因子在调控血管生成过程中起到核心作用。血管内皮生长因子能促进内皮细胞的增殖和迁移,增加血管通透性,促进新生血管的形成。可通过调节血管内皮功能、改善微循环、增加脑血流量等机制,改善脑内氧化应激、神经元凋亡和胆碱能系统损伤[116]。阿尔茨海默病患者脑内血管内皮生长因子伴随β-淀粉样蛋白大量沉积,且以很高的亲和度直接与β-淀粉样蛋白相结合;血管内皮生长因子持续与β-淀粉样蛋白共沉积,导致脑内活性血管内皮生长因子水平下降。脑内活性血管内皮生长因子水平不足,导致血管生成水平降低、新血管数量减少、微循环障碍、脑灌注不足等,这些变化加重了阿尔茨海默病的进展[117]。 梓醇通过特异性上调血管内皮生长因子及血管内皮生长因子受体2表达,促进人静脉内皮细胞增殖、迁移,发挥促进血管新生的作用[118]。养血清脑颗粒可以提高血管内皮生长因子水平,促进血管生成,增加脑内微血管密度,从而改善微循环及灌注,改善患者认知功能[119]。晚期糖基化终末产物受体在神经血管单元中尤其是β-淀粉样蛋白富集条件下表达增多,六味地黄丸可能通过调节RAGE/LRP1系统,降低P-Selection和vWF的表达,增加血管内皮生长因子A和CD34的表达[120]。血管内皮生长因子含量越低,阿尔茨海默病神经退行性变越严重,通过调控碱性成纤维细胞生长因子的表达可促进神经干细胞增殖,提高动物的认知功能,补脑Ⅰ号可上调海马脑源性神经营养因子、血管内皮生长因子蛋白及碱性成纤维细胞生长因子mRNA表达,从而改善阿尔茨海默病[121]。 中药有效成分、中药复方调控神经干细胞的作用机制及药效作用,见表2和表3。"

| [1] HAN F, BI J, QIAO L, et al. Stem Cell Therapy for Alzheimer’s Disease. Adv Exp Med Biol. 2020;1266:39-55. [2] KNOPMAN DS, AMIEVAH, PETERSEN RC, et al. Alzheimer disease. Nat Rev Dis Primers. 2021;7(1):33. [3] KUMAR A, SIDHU J, GOYAL A, et al. Alzheimer Disease. Treasure Island (FL): StatPearls Publishing, 2022. [4] 殷贺,刘广志. 银杏叶提取物治疗阿尔茨海默病的作用机制研究进展[J].中国医药,2020,15(1):151-154. [5] HUANG L, ZHANG L. Neural stem cell therapies and hypoxic-ischemic brain injury. Prog Neurobiol. 2019;173:1-17. [6] VASIC V, BARTH K, SCHMIDT M. Neurodegeneration and Neuro-Regeneration-Alzheimer’s Disease and Stem Cell Therapy. Int J Mol Sci. 2019;20(17):4272. [7] FANG CY, WU XS, ZHANG H, et al. Research advances in endogenous neural stem cells promoting neural repair after ischemic stroke. Sheng Li Xue Bao. 2019;71(3):454-462. [8] RODA AR, SERRA-MIR G, MONTOLIU-GAYA L, et al. Amyloid-beta peptide and tau protein crosstalk in Alzheimer’s disease. Neural Regen Res. 2022;17(8):1666-1674. [9] ZHENG J. Hippocampal neurogenesis and pro-neurogenic therapies for Alzheimer’s disease. Animal Model Exp Med. 2022;5(1):3-14. [10] 聂志玲,周小莉.阿尔茨海默病的中医病因病机探析[J].时珍国医国药,2020,31(6):1443-1444. [11] 罗刘军,祝美珍,陈兰,等.基于“肾-脑髓-干细胞”轴探讨缺血性卒中及神经再生[J].辽宁中医药大学学报,2020,22(3):104-107. [12] 李鑫,邵瑞,王彧.中药调节神经干细胞增殖分化的研究进展[J].中国实验方剂学杂志,2019,25(9):221-227. [13] ZHU Q, ZHANG N, HU N, et al. Neural stem cell transplantation improves learning and memory by protecting cholinergic neurons and restoring synaptic impairment in an amyloid precursor protein/presenilin 1 transgenic mouse model of Alzheimer’s disease. Mol Med Rep. 2020;21(3):1172-1180. [14] BLURTON-JONES M, KITAZAWA M, MARTINEZ-CORIA H, et al. Neural stem cells improve cognition via BDNF in a transgenic model of Alzheimer disease. Proc Natl Acad Sci U S A. 2009;106(32):13594-13599. [15] CHENG Z, BOSCO DB, SUN L, et al. Neural Stem Cell-Conditioned Medium Suppresses Inflammation and Promotes Spinal Cord Injury Recovery. Cell Transplant. 2017;26(3):469-482. [16] JIA G, DIAO Z, LIU Y, et al. Neural stem cell-conditioned medium ameliorates Aβ25-35-induced damage in SH-SY5Y cells by protecting mitochondrial function. Bosn J Basic Med Sci. 2021;21(2):179-186. [17] WANG L, GU S, GAN J, et al. Neural Stem Cells Overexpressing Nerve Growth Factor Improve Functional Recovery in Rats Following Spinal Cord Injury via Modulating Microenvironment and Enhancing Endogenous Neurogenesis. Front Cell Neurosci. 2021;15:773375. [18] RYU S, LEE SH, KIM SU, et al. Human neural stem cells promote proliferation of endogenous neural stem cells and enhance angiogenesis in ischemic rat brain. Neural Regen Res. 2016;11(2): 298-304. [19] 孙孟军,郭建美,周更苏,等.ICR小鼠神经干细胞的诱导分化及鉴定[J].医学动物防制,2021,37(5):467-470. [20] BERNAL A, ARRANZ L. Nestin-expressing progenitor cells: function, identity and therapeutic implications. Cell Mol Life Sci. 2018;75(12): 2177-2195. [21] ZHANG W, GU GJ, ZHANG Q, et al. NSCs promote hippocampal neurogenesis, metabolic changes and synaptogenesis in APP/PS1 transgenic mice. Hippocampus. 2017;27(12):1250-1263. [22] 汪建成.中间丝蛋白Nestin调节细胞内环境稳态的作用机理研究[D].广州:中山大学,2016. [23] KULKARNI S, MICCI MA, LESER J, et al. Adult enteric nervous system in health is maintained by a dynamic balance between neuronal apoptosis and neurogenesis. Proc Natl Acad Sci U S A. 2017;114(18): E3709-E3718. [24] 高宁辛.石菖蒲挥发油对AD模型小鼠神经元损伤的保护作用及机制探讨[D].广州:广东药科大学,2018. [25] MAO J, HUANG S, LIU S, et al. A herbal medicine for Alzheimer’s disease and its active constituents promote neural progenitor proliferation. Aging Cell. 2015;14(5):784-796. [26] 李彩峰,王晓琴,刘勇,等.草苁蓉化学成分及药理活性研究进展[J].中草药,2014,45(7):1016-1023. [27] YAN Y, KONG L, XIA Y, et al. Osthole promotes endogenous neural stem cell proliferation and improved neurological function through Notch signaling pathway in mice acute mechanical brain injury. Brain Behav Immun. 2018;67: 118-129. [28] 姚璎珈,胡昱,李少恒,等.蛇床子素可促进体外培养神经干细胞的增殖[J].中国组织工程研究,2014,18(32):5184-5189. [29] 张丽,赵丽红,张兰,等.山茱萸环烯醚萜苷促进成体大鼠海马神经干细胞增殖和分化的影响[J].中国新药杂志,2015,24(5):550-553. [30] 陈吉聪,邓艳,肖洪贺,等.酸枣仁皂苷A促进阿尔茨海默病神经干细胞模型增殖和分化作用的研究[J].现代中药研究与实践,2021, 35(6):17-21. [31] KARIMIPOUR M, RAHBARGHAZI R, TAYEFI H, et al. Quercetin promotes learning and memory performance concomitantly with neural stem/progenitor cell proliferation and neurogenesis in the adult rat dentate gyrus. Int J Dev Neurosci. 2019;74:18-26. [32] HUANG S, MAO J, DING K, et al. Polysaccharides from Ganoderma lucidum Promote Cognitive Function and Neural Progenitor Proliferation in Mouse Model of Alzheimer’s Disease. Stem Cell Reports. 2017;8(1): 84-94. [33] ZHAO J, LU S, YU H, et al. Baicalin and ginsenoside Rb1 promote the proliferation and differentiation of neural stem cells in Alzheimer’s disease model rats. Brain Res. 2018;1678:187-194. [34] VARELA-NALLAR L, ARREDONDO SB, TAPIA-ROJAS C, et al. Andrographolide Stimulates Neurogenesis in the Adult Hippocampus. Neural Plast. 2015;2015:935403. [35] 刘盼兴,高媛媛,任璐,等.补肾活血方对SAMP8小鼠学习记忆及海马神经干细胞影响实验研究[J].中华中医药学刊,2020,38(2): 50-53. [36] 杨晶莹.黄精丸治疗阿尔茨海默病小鼠痴呆的作用与机制研究[D].南昌:江西中医药大学,2021. [37] 邓艳,时悦,肖洪贺,等.开心散含药血清对Aβ_(1-42)损伤的神经干细胞增殖和分化能力的影响[J].中国现代中药,2021,23(6):999-1004. [38] KONG L, HU Y, YAO Y, et al. The Coumarin Derivative Osthole Stimulates Adult Neural Stem Cells, Promotes Neurogenesis in the Hippocampus, and Ameliorates Cognitive Impairment in APP/PS1 Transgenic Mice. Biol Pharm Bull. 2015;38(9):1290-1301. [39] LIU RX, MA J, WANG B, et al. No DCX-positive neurogenesis in the cerebral cortex of the adult primate. Neural Regen Res. 2020;15(7): 1290-1299. [40] 王珍珍,鲁海,王媛卓,等.调神开窍针刺法与Notch信号通路、内源性神经干细胞在卒中后抑郁治疗中相关性的理论探讨[J].针灸临床杂志,2021,37(1):98-101. [41] ESKANDARI S, SAJADIMAJD S, ALAEI L, et al. Targeting Common Signaling Pathways for the Treatment of Stroke and Alzheimer’s: a Comprehensive Review. Neurotox Res. 2021;39(5):1589-1612. [42] 陶震宇.蛇床子素联合神经干细胞移植治疗机械性脑损伤的实验研究[D].沈阳:辽宁中医药大学,2017. [43] LI J, HAN Y, LI M, et al. Curcumin Promotes Proliferation of Adult Neural Stem Cells and the Birth of Neurons in Alzheimer’s Disease Mice via Notch Signaling Pathway. Cell Reprogram. 2019;21(3):152-161. [44] HAIYAN H, RENSONG Y, GUOQIN J, et al. Effect of Astragaloside IV on Neural Stem Cell Transplantation in Alzheimer’s Disease Rat Models. Evid Based Complement Alternat Med. 2016;2016:3106980. [45] 汪宏锦,李晶晶,柯慧,等.中药对神经干细胞增殖分化信号通路的综合调控作用分析[J].中国中药杂志,2017,42(21):4093-4103. [46] ALAM R, MRAD Y, HAMMOUD H, et al. New insights into the role of fibroblast growth factors in Alzheimer’s disease. Mol Biol Rep. 2022; 49(2):1413-1427. [47] ARREDONDO SB, REYES DT, HERRERA-SOTO A, et al. Andrographolide promotes hippocampal neurogenesis and spatial memory in the APPswe/PS1ΔE9 mouse model of Alzheimer’s disease. Sci Rep. 2021; 11(1):22904. [48] 夏星,徐治强,彭翔.姜黄素对APP/PS1双转基因小鼠认知功能、炎症反应及海马区突触素表达的影响[J].中国临床神经外科杂志, 2018,23(9):609-612. [49] 陈艳清,陈峥,王伟,等.神经元中PSD-95的研究[J].脑与神经疾病杂志,2019,27(11):723-727. [50] XIAO H, WANG Y, WU Y, et al. Osthole ameliorates cognitive impairments via augmenting neuronal population in APP/PS1 transgenic mice. Neurosci Res. 2021;164:33-45. [51] LI J, WEN PY, LI WW, et al. Upregulation effects of Tanshinone IIA on the expressions of NeuN, Nissl body, and IκB and downregulation effects on the expressions of GFAP and NF-κB in the brain tissues of rat models of Alzheimer’s disease. Neuroreport. 2015;26(13):758-766. [52] ZHOU H, XUE W, CHU SF, et al. Polygalasaponin XXXII, a triterpenoid saponin from Polygalae Radix, attenuates scopolamine-induced cognitive impairments in mice. Acta Pharmacol Sin. 2016;37(8):1045-1053. [53] 姚辛敏,周晓洁,周妍妍,等.远志化学成分及药理作用研究进展[J].中医药学报,2022,50(2):103-107. [54] MAVROUDIS I, PETRIDIS F, KAZIS D, et al. Purkinje Cells Pathology in Alzheimer’s Disease. Am J Alzheimers Dis Other Demen. 2019;34(7-8): 439-449. [55] 秦川,吴善球,陈保生,等.灵芝制剂治疗APP/PS-1阿尔茨海默病转基因小鼠模型的病理学改变[J].中国医学科学院学报,2017, 39(4):552-561. [56] 钟佩茹,王秀云,柴丽娟,等.黄芪甲苷对体外培养胚胎神经干细胞增殖作用的影响[J].中国中医药信息杂志,2013,20(5):42-44. [57] DE GIOIA R, BIELLA F, CITTERIO G, et al. Neural Stem Cell Transplantation for Neurodegenerative Diseases. Int J Mol Sci. 2020; 21(9):3103. [58] COLUCCI-D’AMATO L, SPERANZA L, VOLPICELLI F. Neurotrophic Factor BDNF, Physiological Functions and Therapeutic Potential in Depression, Neurodegeneration and Brain Cancer. Int J Mol Sci. 2020;21(20):7777. [59] YAN YH, LI SH, GAO Z, et al. Neurotrophin-3 promotes proliferation and cholinergic neuronal differentiation of bone marrow- derived neural stem cells via notch signaling pathway. Life Sci. 2016;166:131-138. [60] SIMS SK, WILKEN-RESMAN B, SMITH CJ, et al. Brain-Derived Neurotrophic Factor and Nerve Growth Factor Therapeutics for Brain Injury: The Current Translational Challenges in Preclinical and Clinical Research. Neural Plast. 2022;2022:3889300. [61] KANG X, HONG W, XIE K, et al. Ginsenoside Rb1 pretreatment reverses hippocampal changes in BDNF/TrkB mRNA and protein in rats subjected to acute immobilization stress. Drug Des Devel Ther. 2019;13:2127-2134. [62] KIM J, LEE S, CHOI BR, et al. Sulforaphane epigenetically enhances neuronal BDNF expression and TrkB signaling pathways. Mol Nutr Food Res. 2017;61(2):10. [63] XIAO H, LI H, SONG H, et al. Shenzao jiannao oral liquid, an herbal formula, ameliorates cognitive impairments by rescuing neuronal death and triggering endogenous neurogenesis in AD-like mice induced by a combination of Aβ42 and scopolamine. J Ethnopharmacol. 2020; 259:112957. [64] ARAGONA M, PORCINO C, GUERRERA MC, et al. The BDNF/TrkB Neurotrophin System in the Sensory Organs of Zebrafish. Int J Mol Sci. 2022;23(5):2621. [65] CHEN XQ, LI CF, CHEN SJ, et al. The antidepressant-like effects of Chaihu Shugan San: Dependent on the hippocampal BDNF-TrkB-ERK/Akt signaling activation in perimenopausal depression-like rats. Biomed Pharmacother. 2018;105:45-52. [66] NORMAN BH, MCDERMOTT JS. Targeting the Nerve Growth Factor (NGF) Pathway in Drug Discovery. Potential Applications to New Therapies for Chronic Pain. J Med Chem. 2017;60(1):66-88. [67] SHENG C, XU P, ZHOU K, et al. Icariin Attenuates Synaptic and Cognitive Deficits in an Aβ(1-42)-Induced Rat Model of Alzheimer’s Disease. Biomed Res Int. 2017;2017:7464872. [68] LU Q, ZHU H, LIU X, et al. Icariin sustains the proliferation and differentiation of Aβ(25-35)-treated hippocampal neural stem cells via the BDNF-TrkB-ERK/Akt signaling pathway. Neurol Res. 2020;42(11): 936-945. [69] NI GX, LIANG C, WANG J, et al. Astragaloside IV improves neurobehavior and promotes hippocampal neurogenesis in MCAO rats though BDNF-TrkB signaling pathway. Biomed Pharmacother. 2020;130:110353. [70] HU Y, LIU MY, LIU P, et al. Neuroprotective effects of 3,6’-disinapoyl sucrose through increased BDNF levels and CREB phosphorylation via the CaMKII and ERK1/2 pathway. J Mol Neurosci. 2014;53(4):600-607. [71] LIU H, XUE X, SHI H, et al. Osthole Upregulates BDNF to Enhance Adult Hippocampal Neurogenesis in APP/PS1 Transgenic Mice. Biol Pharm Bull. 2015;38(10):1439-1449. [72] MA X, XIANG F, PEI Z, et al. Circ-Smad5 retards the G1/S transition of cell cycle via inhibiting the activity of wnt/lef/cyclind1 signaling in JB6 cells. Genes Dis. 2021;8(3):364-372. [73] 许蓬娟,蔡青,谭俊珍,等.Wnt/β-catenin信号通路在阿尔茨海默病神经元变性中的研究进展[J].重庆医科大学学报,2019,44(4):419-423. [74] 姚璎珈,孔亮,教亚男,等.蛇床子素通过Wnt/β-catenin信号通路促进转染APP基因的神经干细胞分化为更多神经元且减少神经元凋亡[J].中国药理学通报,2015,31(11):1516-1523. [75] XIAO HH, ZHANG MB, XU JT, et al. Icarisid II promotes proliferation and neuronal differentiation of neural stem cells via activating Wnt/β-catenin signaling pathway. Phytother Res. 2021. doi: 10.1002/ptr.7022. Online ahead of print. [76] TIWARI SK, AGARWAL S, SETH B, et al. Correction to Curcumin-Loaded Nanoparticles Potently Induce Adult Neurogenesis and Reverse Cognitive Deficits in Alzheimer’s Disease Model via Canonical Wnt/β-Catenin Pathway. ACS Nano. 2019;13(6):7355. [77] ZHU Q, CHEN L, LI Y, et al. Rack1 is essential for corticogenesis by preventing p21-dependent senescence in neural stem cells. Cell Rep. 2021;36(9):109639. [78] FU X, LI S, ZHOU S, et al. Stimulatory effect of icariin on the proliferation of neural stem cells from rat hippocampus. BMC Complement Altern Med. 2018;18(1):34. [79] THAL DR, WALTER J, SAIDO TC, et al. Neuropathology and biochemistry of Aβ and its aggregates in Alzheimer’s disease. Acta Neuropathol. 2015;129(2):167-182. [80] DADSENA S, KING LE, GARCÍA-SÁEZ AJ. Apoptosis regulation at the mitochondria membrane level. Biochim Biophys Acta Biomembr. 2021; 1863(12):183716. [81] 康传依,赵娜,ASIYAMAVLIKHANOVA,等.神经节苷脂对慢性酒精中毒小鼠海马Caspase-3、Bax、Bcl-2蛋白表达水平的影响[J].中华精神科杂志,2020,53(5):426-430. [82] ZHANG XZ, QIAN SS, ZHANG YJ, et al. Salvia miltiorrhiza: A source for anti-Alzheimer’s disease drugs. Pharm Biol. 2016;54(1):18-24. [83] RAMOS REGO I, SANTOS CRUZ B, AMBRÓSIO AF, et al. TRAP1 in Oxidative Stress and Neurodegeneration. Antioxidants (Basel). 2021; 10(11):1829. [84] WANG Y, LIN J, CHEN QZ, et al. Overexpression of mitochondrial Hsp75 protects neural stem cells against microglia-derived soluble factor-induced neurotoxicity by regulating mitochondrial permeability transition pore opening in vitro. Int J Mol Med. 2015;36(6):1487-1496. [85] 朱江华,范焕琼.白藜芦醇通过上调Hsp75蛋白表达改善Aβ对C17.2细胞增殖的抑制作用[J].今日药学,2017,27(7):475-478. [86] 曹梦园,赵月鸣,张晶,等.人参皂苷Rb1对Aβ25-35诱导痴呆大鼠海马神经元凋亡的影响[J].中国现代医学杂志,2015,25(35):33-36. [87] Yan L, Deng Y, Gao J, et al. Icariside II Effectively Reduces Spatial Learning and Memory Impairments in Alzheimer’s Disease Model Mice Targeting Beta-Amyloid Production. Front Pharmacol. 2017;8:106. [88] 李沁轩,王一枝,徐艳,等.地塞米松联合雌激素干预脊髓钝挫伤大鼠白细胞介素6、Caspase3和Bcl-2的表达[J].中国组织工程研究,2020,24(17):2680-2685. [89] 黄颖,周艳华,崔海峰,等.雌激素调节作用机制研究进展[J].中国医药导报,2010,7(5):7-8. [90] 肖韩艳,付东莹,袁春华,等.补骨脂异黄酮对β-淀粉样肽_(25-35)损伤的神经干细胞存活及调亡的影响[J].中国医院用药评价与分析,2016,16(12):1613-1615. [91] 韩飞飞,刘亚群,廖晶,等.梓醇对高糖诱导SH-SY5Y细胞凋亡的Bcl-2蛋白和YAP蛋白的影响[J].锦州医科大学学报,2021,42(5):10-14. [92] JIANG B, SHEN RF, BI J, et al. Catalpol: a potential therapeutic for neurodegenerative diseases. Curr Med Chem. 2015;22(10):1278-1291. [93] 韩文文,张玉莲,周震,等.益肾化浊方对Aβ_(25-35)介导神经干细胞增殖与分化的影响[J].中国实验方剂学杂志,2015,21(20):99-102. [94] WANG Q, DUAN L, LI X, et al. Glucose Metabolism, Neural Cell Senescence and Alzheimer’s Disease. Int J Mol Sci. 2022;23(8):4351. [95] 朱雯菲,付朝旭,代霖,等.刺五加提取液对小鼠学习记忆障碍和淀粉样前体蛋白酶解通路影响及作用机制[J]. 中国老年学杂志, 2019,39(12):2976-2981. [96] 邹佳益,杨江权,徐林,等.何首乌提取液对衰老小鼠脑组织DNA甲基化和基因转录的影响[J].第三军医大学学报,2020,42(1):9-17. [97] 林志彬.灵芝的抗衰老与抗阿尔茨海默病的药理研究进展[J].神经药理学报,2018,8(1):9-15. [98] SEO HW, CHEON SM, LEE MH, et al. Catalpol Modulates Lifespan via DAF-16/FOXO and SKN-1/Nrf2 Activation in Caenorhabditis elegans. Evid Based Complement Alternat Med. 2015;2015:524878. [99] Huang JZ, Wu J, Xiang S, et al. Catalpol preserves neural function and attenuates the pathology of Alzheimer’s disease in mice. Mol Med Rep. 2016;13(1):491-496. [100] 王琳,金桂芳,余河汉,等.细叶远志皂苷在Aβ_(23-35)诱导SH-SY5Y 细胞氧化损伤中的作用及机制研究[J].天然产物研究与开发, 2019,31(9):1537-1542. [101] 桑旭星,杨依,唐晓丽,等.远志寡糖酯抗β淀粉样蛋白25-35诱导的SH-SY5Y细胞损伤的作用研究[J].中国药学杂志,2018,53(11): 876-881. [102] 李孟宇.六味地黄汤及其活性部位对阿尔茨海默病模型小鼠神经发生的作用研究[D].南宁:广西医科大学,2018. [103] SHAO P. MiR-216a-5p ameliorates learning-memory deficits and neuroinflammatory response of Alzheimer’s disease mice via regulation of HMGB1/NF-κB signaling. Brain Res. 2021;1766:147511. [104] 马金昀,王金英,孙宇,等.黄芪多糖抑制小鼠EAE及调控BV-2神经小胶质细胞活化的实验研究[J].中国免疫学杂志,2018,34(3): 381-387. [105] FAKHOURY M. Microglia and Astrocytes in Alzheimer’s Disease: Implications for Therapy. Curr Neuropharmacol. 2018;16(5):508-518. [106] PIERRE WC, SMITH P, LONDONO I, et al. Neonatal microglia: The cornerstone of brain fate. Brain Behav Immun. 2017;59:333-345. [107] SARLUS H, HENEKA MT. Microglia in Alzheimer’s disease. J Clin Invest. 2017;127(9):3240-3249. [108] 于婧文,郭敏芳,张婧,等.黄芪甲苷对体外由脂多糖诱导的星形胶质细胞炎性反应及其作用机制的研究[J].中华微生物学和免疫学杂志,2018,38(11):829-834. [109] 张玉莲,周震,韩文文,等.何首乌有效成分二苯乙烯苷对Aβ_(25-31)诱导神经干细胞定向分化的影响[J].中医杂志,2014,55(4):323-327. [110] 韩文文,张玉莲,张琳琳,等.益肾化浊方条件培养基对神经干细胞增殖分化影响的研究[J].时珍国医国药,2015,26(10):2339-2342. [111] 王琦,刘瑜琦.中药远志对阿尔茨海默病的病理作用机制[J].中国老年学杂志,2016,36(2):505-509. [112] AN J, CHEN B, TIAN D, et al. Regulation of Neurogenesis and Neuronal Differentiation by Natural Compounds. Curr Stem Cell Res Ther. 2021. doi: 10.2174/1574888X16666210907141447. [113] 崔猛,冯世庆,范宁建,等.黄芩苷下调p-STAT3诱导神经干细胞向神经元分化[J].天津医药,2013,41(8):786-788. [114] 陆露,刘秀秀,李政懋,等.脑血管源性细胞间通讯异常与脑疾病机制研究[J].中国药理学通报,2021,37(5):597-601. [115] SWEENEY MD, ZHAO Z, MONTAGNE A, et al. Blood-Brain Barrier: From Physiology to Disease and Back. Physiol Rev. 2019;99(1):21-78. [116] TAKEDA H, YAMAGUCHI T, YANO H, et al. Microglial metabolic disturbances and neuroinflammation in cerebral infarction. J Pharmacol Sci. 2021;145(1):130-139. [117] MUCHE A, BIGL M, ARENDT T, et al. Expression of vascular endothelial growth factor (VEGF) mRNA, VEGF receptor 2 (Flk-1) mRNA, and of VEGF co-receptor neuropilin (Nrp)-1 mRNA in brain tissue of aging Tg2576 mice by in situ hybridization. Int J Dev Neurosci. 2015;43: 25-34. [118] 周霞,张文倩,刘炬,等.从血管内皮生长因子及其受体调控角度探讨地黄梓醇促血管新生作用及分子机制研究[J].实用心脑肺血管病杂志,2020,28(2):64-68. [119] 黄丽,莫林宏,刘爱贤.养血清脑颗粒治疗阿尔茨海默病的疗效及对血管内皮生长因子的影响[J].中国实验方剂学杂志,2022, 28(14):121-126. [120] 贾亚泉,宋军营,袁永,等.六味地黄丸通过RAGE/LRP1受体介导对SAMP8小鼠脑微血管的调节作用[J/OL].中国实验方剂学杂志. https://kns.cnki.net/kcms/detail/detail.aspx?dbcode= CAPJ&dbname=CAPJLAST&filename=ZSFX20220210004& uniplatform=NZKPT&v=CBx30l9aYtTm44kIlz6MbCWErXX A78rGtTx1jBSqc0VdDRfnMmKU01OKdTkUc6ER(2022/06/03) [121] 杨辉,钟方敏,陈燕,等.补脑Ⅰ号对阿尔茨海默病模型小鼠脑内移植骨髓间充质干细胞后海马VEGF、BDNF表达及超微结构的影响[J].中医杂志,2021,62(15):1349-1355. |
| [1] | Fang Xingyan, Tian Zhenli, Zhao Zheyi, Wen Ping, Xie Tingting. Effects of sodium arsenite on human umbilical vein endothelial cell injury and sphingosine kinases 1/sphingosine 1-phosphate signaling axis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-7. |
| [2] | Nong Fuxiang, Jiang Zhixiong, Li Yinghao, Xu Wencong, Shi Zhilan, Luo Hui, Zhang Qinglang, Zhong Shuang, Tang Meiwen. Bone cement augmented proximal femoral nail antirotation for type A3.3 intertrochanteric femoral fracturalysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-10. |
| [3] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [4] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [5] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [6] | Nie Chenchen, Su Kaiqi, Gao Jing, Fan Yongfu, Ruan Xiaodi, Yuan Jie, Duan Zhaoyuan, Feng Xiaodong. The regulatory role of circular RNAs in cerebral ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1286-1291. |
| [7] | Gao Yu, Han Jiahui, Ge Xin. Immunoinflammatory microenvironment after spinal cord ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1300-1305. |
| [8] | Wang Ji, Zhang Min, Yang Zhongya, Zhang Long. A review of physical activity intervention in type 2 diabetes mellitus with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1272-1277. |
| [9] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [10] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [11] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [12] | Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109. |
| [13] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| [14] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [15] | Li Qicheng, Deng Jin, Fu Xiaoyang, Han Na. Effects of bone marrow mesenchymal stem cells-derived exosomes on hypoxia-treated myoblasts [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 853-859. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||



