Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (11): 1758-1764.doi: 10.12307/2022.362
Previous Articles Next Articles
Chinese herbal prescriptions for tonifying kidney and promoting blood circulation in the intervention of steroid-induced avascular necrosis of the femoral head: relevant signal pathways and targets
Han Jie1, Ren Guowu2, Mo Jian1, Zhang Xiaoyun1, Wen Shuaibo2, Wu Yukun2
- 1Ruikang Hospital Affiliated to Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China; 2Guangxi University of Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China
-
Received:2021-01-28Revised:2021-01-30Accepted:2021-03-12Online:2022-04-18Published:2021-12-13 -
Contact:Mo Jian, Associate chief physician, Master’s supervisor, Department of Joint and Sports Medicine, Ruikang Hospital Affiliated to Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China -
About author:Han Jie, Master, Associate chief physician, Master’s supervisor, Ruikang Hospital Affiliated to Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China -
Supported by:Guangxi Medical and Health Appropriate Technology Development and Promotion Application Project, No. S2019070 (to HJ); Guangxi University Scientific Research Basic Ability Enhancement Project for Young and Middle-aged Teachers, No. 2020KY07017 (to HJ); Hospital Preparation Quality Improvement Project of Chinese Zhuang Yao Medicine, No. GZZJ202011 (to HJ); The Self-Funded Research Project of Guangxi Zhuang Autonomous Region Administration of Traditional Chinese Medicine, No. GZZC2020081 (to MJ); University-level Scientific Research Project of Guangxi University of Chinese Medicine, No. 2020MS040 (to MJ)
CLC Number:
Cite this article
Han Jie, Ren Guowu, Mo Jian, Zhang Xiaoyun, Wen Shuaibo, Wu Yukun. Chinese herbal prescriptions for tonifying kidney and promoting blood circulation in the intervention of steroid-induced avascular necrosis of the femoral head: relevant signal pathways and targets[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(11): 1758-1764.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
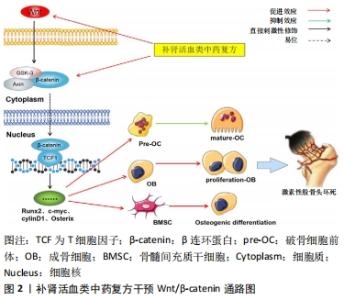
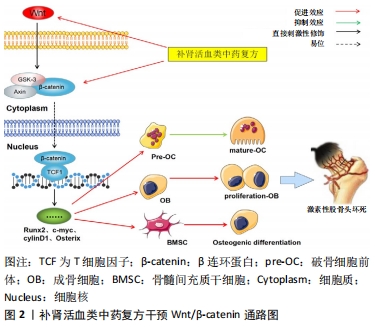
通过检索活血补肾类中药复方干预激素性股骨头坏死信号通路相关文献,符合纳入标准共54篇文献,分析文献内容得出活血补肾类中药复方可能通过影响Wnt/β-catenin、缺氧诱导因子1α、RANK、Notch、过氧化物酶体增殖物激活受体γ、转化生长因子β/Smad、腺苷酸活化蛋白激酶等多信号通路,起到改善股骨头血运障碍、脂肪代谢紊乱、骨重塑与吸收失衡等作用,进而干预激素性股骨头坏死的进展。 2.1 Wnt/β-catenin信号通路 Wnt/β-catenin通路对骨组织动态平衡具有调控作用,该通路通过多种机制正向调节骨髓间充质干细胞分化、骨细胞增殖和多种细胞因子的表达[10]。Wnt/β-catenin通路的激活:活化的Wnt与胞膜表面卷曲蛋白受体(Frizzled)、低密度脂蛋白受体相关蛋白5/6结合后,包膜信号复合体转入到胞内阻碍糖原合成酶激酶3β复合体对β-catenin的降解,β-catenin与T细胞因子、淋巴增强因子结合形成激活复合体,启动下游靶基因如Runx2、c-myc、cylinD1、Osterix等的表达[11],而下游基因的表达是影响骨髓间充质干细胞成骨分化、成骨细胞与破骨细胞骨代谢平衡和上调血管内皮生长因子表达促进血管生成的重要因素[12]。大量、长期、不规律使用糖皮质激素会诱导Wnt信号抑制因子Dickkopf-1(DKK-1)分泌,使Wnt/β-catenin通路信号传导受阻、下游基因表达下调[13];进而导致股骨头、颈部的成骨细胞生成减少、破骨细胞活性增强、骨髓间充质干细胞向脂质细胞异常分化,骨结构遭到破坏,干骺端修复能力下降,最终导致股骨头坏死。 ZHANG等[14]通过右归饮治疗激素性股骨头坏死模型兔,发现在局部骨组织形态上,相对于对照组,经右归饮防治的干预组激素性股骨头坏死兔造模率降低,骨小梁断裂或变薄的骨组织减少,骨细胞的空骨陷窝及骨髓细胞包围的固缩核破坏减少。通过检测相关蛋白和细胞染色发现,右归饮可上调坏死股骨头骨组织中的骨钙素、β-catenin和糖原合成酶激酶3β活性抑制剂(p-Ser9GSK-3β)蛋白表达;以此逆转激素对Wnt信号的抑制作用,促进骨细胞成骨,减少骨质破坏,上调成骨细胞/破骨细胞比例,改善骨小梁微结构,增强骨骼承载能力达到修复股骨头坏死的目的。施乐等[15]通过研究《伤科大成》中的补肾活血汤对股骨头坏死局部血管得影响,发现补肾活血汤干预组股骨头坏死区域的 Wnt、β-catenin和血管内皮生长因子蛋白水平升高,局部骨小梁较为整齐、清晰,血管微结构清晰、呈现网状供血;且血管坏死面积减少、血管体积分数增加、血管厚度增粗。此外,谢磊等[16]研究发现,采用具有祛瘀强骨功效的强骨胶囊与引导骨再生技术结合修复股骨头骨缺陷,骨缺损处骨组织碱性磷酸酶、Runx2、血管内皮生长因子、骨形态发生蛋白2等基因的mRNA表达上调;以补肾活血类制剂配合骨再生技术,可促进生物膜屏障创造出对骨组织更具优势的微环境生长环境,使具有修复能力的骨细胞更易进入骨缺损腔进行修复。补肾活血类中药复方可通过逆转激素对Wnt/β-catenin信号的抑制、促进下游靶点基因表达,来促进血管新生、骨组织重建修复骨坏死,见图2。"
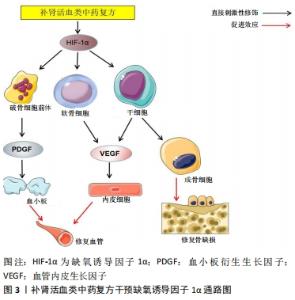
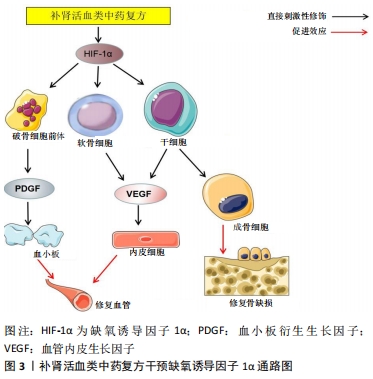
2.2 缺氧诱导因子1α信号通路 缺氧诱导因子是一类DNA结合转录因子,在某些情况下能够激活一系列与缺氧相关的基因,并产生适应性反应以降低氧张力。缺氧诱导因子由α、β两个亚基构成。细胞中缺氧诱导因子1β通常过量存在,而不稳定型缺氧诱导因子1α的分解是缺氧诱导因子1活性的关键。在股骨头坏死局部骨组织出现缺血、缺氧环境,脯氨酸羟化酶自身缺氧以及骨细胞内呼吸链中代谢产物堆积抑制了脯氨酸羟化酶的活性,阻断缺氧诱导因子1α降解活化过程,阻碍了其参与调节血管生成、骨细胞增殖、能量代谢等过程。目前发现大约100种缺氧诱导因子,包括血管内皮生长因子,血红素氧合酶1和葡萄糖转运蛋白1等,其中血管内皮生长因子作为缺氧诱导因子1α族中的强力靶向因子,具有诱导内皮细胞增殖、迁移形成血管的功能[17]。有研究表明,血管内皮生长因子作为调节骨信号网络中的一个关键因子,在血管形成-成骨耦合中具有重要功能[18];血管内皮生长因子可通过影响破骨细胞的成熟和分化,募集骨髓间充质干细胞和骨祖细胞、促进干细胞血管分化,进而影响骨形成与重塑过程[19]。 刘锌等[20]研究发现运用右归饮治疗剂量依赖性干预激素性股骨头坏死,相较于模型组和低剂量组,高剂量组股骨头坏死处新生骨修复活跃、大量血管新生、骨小梁虽有部分断裂但整体结构完整;在细胞结构上脂肪细胞浸润减少,骨髓间充质干细胞保持正常数量。高剂量右归饮可通过增强成骨碱性磷酸酶活性促进骨新生,上调血管内皮生长因子改善股骨头坏死区域血液微循环,升高骨髓间充质干细胞凋亡时产生的自噬保护反应蛋白(LC3Ⅱ、P53、beclin-1等自噬蛋白)的表达,防止干细胞凋亡,同时诱导其向成骨分化。王江伟等[21]研究发现,经过以活血化瘀、滋补肝肾为主要功效的通血健骨丸处理过的激素性股骨头坏死兔的骨坏死区域缺氧诱导因子1α、血管内皮生长因子、骨形态发生蛋白2的 mRNA和蛋白表达明显增加,表明缺氧诱导因子1α作为血管-骨组织网络的调节因子可促进骨组织成骨。张岩等[22]对80例股骨头患者进行随机分组研究,发现通过服用桃仁汤联合温针灸可改善中期股骨头坏死患者的临床症状,同时上调患者血清中血管内皮生长因子的水平,为血管化营造一个有利环境。补肾活血类中药复方通过缺氧诱导因子1α/血管内皮生长因子通路参加血管生成-成骨耦合网络,影响股骨头坏死骨组织中的骨髓间充质干细胞、成骨细胞、破骨细胞生命活动过程,见图3。"
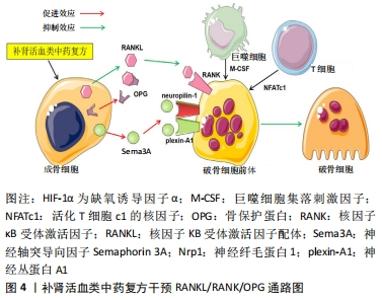
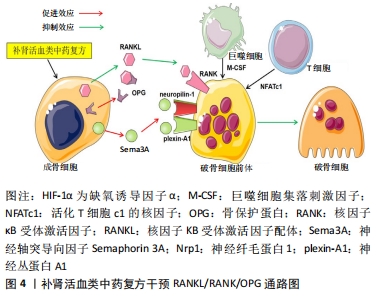
2.3 RANKL/RANK/OPG通路 OPG/RANKL/RANK三聚体主要成分有骨保护蛋白(osteoprotegerin,OPG),核因子κB受体激活剂(receptor activator of nuclear factor-κB,RANK),核因子κB受体激活剂配体(receptor activator of nuclear factor-κB ligand,RANKL)。骨保护蛋白具有抑制破骨细胞分化、促进成骨细胞增殖成骨的作用。RANKL作为一种Ⅱ型跨膜蛋白可直接与分布于破骨细胞前体胞膜的RANK结合,产生诱导前体破骨细胞分化、成熟及减缓成熟破骨细胞凋亡的作用[23]。而在RANKL/RANK/OPG通路中骨保护蛋白可通过与RANK竞争性结合占据靶点,来减少RANK与其配体的结合,产生降低破骨细胞增殖分化和破骨活性的作用。因此,OPG/RANKL/RANK通路是一个维持骨吸收与重塑平衡的调节系统[24]。生理情况下骨组织出现缺损时,巨噬细胞受到巨噬细胞集落刺激因子、活化T细胞c1的核因子、RANK等破骨细胞分化所必需的共刺激信号的激活,分化为成熟破骨细胞产生吸收局部坏死骨组织的作用。尽管糖皮质激素会降低炎症反应,但大量激素会促进Dickkopf-1、RANK分泌,阻碍Wnt、骨保护蛋白信号的表达,使骨吸收与重建功能失衡;且激素会诱导肾脏对钙的排泄、对抗维生素D、降低胃肠对钙的吸收,骨原料缺失、阻碍骨基质矿化;导致局部骨组织代谢紊乱、加快骨量丢失,引起骨小梁骨质疏松,骨强度下降、骨组织结构形态不稳定,局部微细骨折导致股骨头坏死[25]。 宋红梅等[26]研究发现温阳补肾方能升高血清中钙、磷、骨钙素、成骨标志物骨碱性磷酸酶水平,为骨重塑提供原料;并且增加骨保护蛋白mRNA及蛋白在股骨头坏死区域的表达,抑制RANK及RANKL mRNA和蛋白的表达,增加骨保护蛋白与RANK的比例,促进成骨细胞分化,降低破骨活性,同时保持了骨细胞内的细胞器、线粒体和内质网形态,胞质间的胶原纤维分布密集和排列整齐。 在骨动态平衡过程中除了受到骨保护蛋白与RANK竞争性结合的调控外,成骨细胞会分泌一种神经轴突信号蛋白——臂板蛋白3A参与抑制RANK的表达。臂板蛋白3A通过与其受体神经纤毛蛋白1(Nrp1)的结合,竞争性的减少了其与神经丛蛋白A1(plexin-A1)的结合,减少plexin-A1-TREM2-DNAX激活蛋白12(DAP12)复合物生成,该复合物与RANK协同诱导活化T细胞核因子1,具有激活破骨细胞特异性基因转录的作用。成骨细胞能正常分泌臂板蛋白3A时,使单核巨噬细胞处于“待令”状态来抑制破骨活性,并保持成骨。而在激素的诱导作用下抑制成骨细胞分泌臂板蛋白3A,激活RANKL表达;使神经纤毛蛋白1下调、促进神经丛蛋白A1释放并形成DAP12,单核巨噬细胞转为“激活”状态分化为成熟的破骨细胞[27]。LIU等[28]对具有补肾强骨功效的中药复方二至丸研究发现,二至丸的主要成分可通过诱导增强臂板蛋白3A与细胞表面受体形成Sema3A-plexinA1-Nrp1复合物,促进成骨细胞增殖、干细胞向成骨分化,同时可通过减少DAP12的形成来抑制RANKL诱导的破骨细胞增殖分化。补肾活血类中药复方通过刺激骨保护蛋白、臂板蛋白3A信号的表达参与RANKL/RANK/OPG通路,影响成骨、破骨细胞的活动状态,改善股骨头坏死区域的骨质流失、促进骨质生成,见图4。"
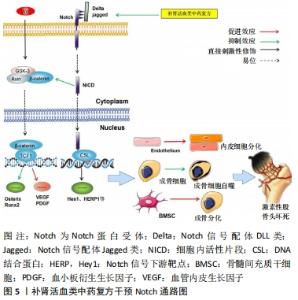
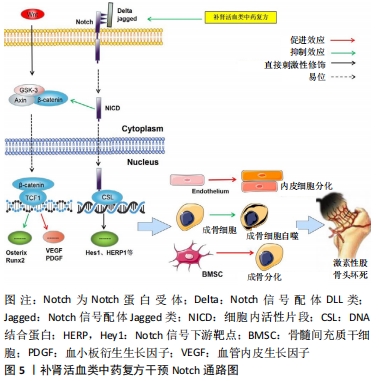
2.4 Notch信号通路 Notch信号在哺乳动物的多种类型细胞和组织的发育中起着联系上下信号的作用,Notch信号通路有4个受体(Notch1-4)、5种配体(jagged1-2,DLL1,3,4)及下游靶点因子(Hes1,5,6,7,HERP,Hey1,2,L等)组成[29]。Notch信号依靠细胞间接触激活,Notch受体与附近细胞表面表达的Notch配体结合,引导γ-分泌酶复合物对Notch受体进行蛋白水解切割,从而释放Notch受体到细胞基质形成活性片段,细胞内活性片段迁移至细胞核内与DNA结合蛋白RBPjK/CBF1相互作用形成激活物复合体,进而诱导下游基因表达产生调控细胞活动的作用。诸多研究表明,Notch信号通路在骨细胞的分化及活性调控过程中呈现出既促进又抑制的双向作用,这种双向调节作用可能与Notch信号通路中不同受体及配体表达水平有关[30]。有研究表明,Notch1/3受体高表达时DLL3、jagged1配体明显增多,但DLL1/4、jagged2配体无明显变化,Notch1/3信号表达时增加骨保护蛋白的表达促进成骨细胞分化、而对RANKL诱导破骨细胞的增殖分化产生抑制作用。当Notch1失活、Notch2表达增强时,骨保护蛋白减少、核因子κB表达增加,则诱导破骨细胞活跃[31]。受体Notch1、配体Jag1和下游靶点Hes1表达升高时会促进骨髓间充质干细胞成骨分化、抑制其增殖和成脂分化,而当受体Notch1、配体Jag1和下游靶Hes1/5表达降低时则促进骨髓间充质干细胞向神经元分化、抑制成骨分化[32]。此外,Notch信号会与其他信号通路相互影响,如Notch与Wnt/β-Catenin相互作用时Notch会抑制Wnt/β-catenin信号传导,Notch1信号的激活时下游靶点HES、HEY会抑制Wnt下游基因Osterix、Runx2的表达。但Notch1不会抑制骨形态发生蛋白信号转导,骨形态发生蛋白族通过Smad信号诱导Notch下游靶点基因促进干细胞成骨分化。Notch信号亦可与Wnt/β-Catenin相互作用诱导血管内皮生长因子、血小板衍生生长因子的表达、促进造血祖细胞扩增生成血管[33-34]。 糖皮质激素可能通过抑制股骨头骨组织中Notch信号通路受体Notch1、配体Jagged1、DLL1、DLL4及下游基因HES1的表达,并上调受体Notch2、配体DLL3、下游基因Herp1的表达,抑制成骨细胞的成骨能力,增强破骨细胞骨吸收、骨髓间充质干细胞的成脂能力,导致股骨头缺血坏死的发生。王敏等[35-37]的实验发现,有补肾活血功效的活血通络汤可通过降低Notch1、Notch2、Notch3受体及相关配体DLL1、DLL3、DLL4、Jagged1的表达,下调下游靶点Hes1、HERP1等细胞自噬基因表达水平;同时促进血管内皮生长因子、血小板衍生生长因子、骨形态蛋白2、骨钙素的表达刺激血管再生、诱导骨髓间充质干细胞成骨分化、增加成骨细胞与破骨细胞比例,改善骨坏死区域微结构。肾活血类中药复方可以通过抑制Notch信号治疗股骨头坏死,但目前关于Notch信号传导机制和下游靶点的作用效果仍未阐明,未来仍值得继续探索,见图5。"
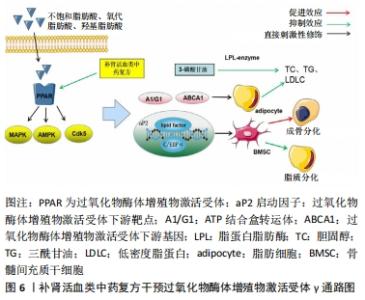
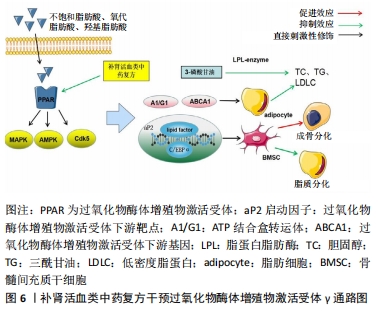
2.5 过氧化物酶体增殖物激活受体γ信号通路 过氧化物酶体增殖物激活受体在脂肪细胞分化、脂质储存及代谢过程具有重要意义。过氧化物酶体增殖物激活受体存在3种亚型即过氧化物酶体增殖物激活受体α、过氧化物酶体增殖物激活受体β、过氧化物酶体增殖物激活受体γ,过氧化物酶体增殖物激活受体α可以降低血清中胆固醇、三酰甘油、低密度脂蛋白等脂质水平,过氧化物酶体增殖物激活受体β调控作用脂类代谢过程为骨骼、肌肉细胞活动提供能量,过氧化物酶体增殖物激活受体γ不仅能调控干细胞向脂质分化,同时兼具降血脂、血糖的功能[38]。在过氧化物酶体增殖物激活受体亚型结构中,过氧化物酶体增殖物激活受体γ亚型研究较为广泛;过氧化物酶体增殖物激活受体γ可以被不饱和脂肪酸、氧代脂肪酸、羟基脂肪酸等脂质能量代谢物质激活,过氧化物酶体增殖物激活受体γ可通过丝裂原活化蛋白激酶、细胞周期素依赖的蛋白激酶5、腺苷酸活化蛋白激酶通路产生磷酸化。aP2启动因子包含C/EBPα和过氧化物酶体增殖物激活受体γ脂质转录因子结合部位,过氧化物酶体增殖物激活受体γ磷酸化诱导下游靶点基因aP2启动因子、ATP结合盒转运体A1/G1、ABCA1基因的表达[39]。 激素诱导脂质代谢紊乱使过氧化物酶体增殖物激活受体γ和C/EBPα在aP2基因结合后的表达异常调,导致坏死骨组织中骨髓间充质干细胞脂质分化增加,骨细胞数量减少,脂肪细胞取代髓腔内红骨髓,使骨内压力增高出现骨内间室综合征,破坏股骨头的骨密度和骨质量;异常高表达过氧化物酶体增殖物激活受体γ在脂蛋白脂肪酶作用下诱导3-磷酸甘油合成胆固醇,同时激活下游靶点基因A1/G1、ABCA1转录促进细胞中胆固醇的流出,使血清胆固醇、低密度脂蛋白水平增加,血液黏度升高使股骨头微循环凝血,出现骨组织坏死[40]。李晓敏等[41]认为健脾活骨方能够抑制骨髓间充质干细胞脂质分化的相关基因——过氧化物酶体增殖物激活受体γ、aP2及相关作用蛋白酶脂蛋白脂肪酶的表达,同时促进成骨标志物血清碱性磷酸酶、D1x5、Runx2、骨形态发生蛋白2、血清骨钙素的表达。KONG等[42]亦证明了由健脾活骨方减桂枝组成的活骨Ⅰ号,可下调股骨头坏死局部过氧化物酶体增殖物激活受体γ蛋白及miRNA的表达,减少脂肪细胞占据的骨髓面积,降低骨内高压力;同时抑制了下游基因对胆固醇、三酰甘油和低密度脂蛋白合成的作用,改善血脂水平,促进微循环供血。此外,孙海忠等[43]的临床研究发现,通过活血生骨汤联合打压支撑植骨术治疗早中期股骨头坏死患者,可有效降低血清三酰甘油和低密度脂蛋白水平,提高血清骨钙素水平,更有利于术后患者髋关节功能恢复,降低术后股骨头塌陷率。经过临床疗效和实验研究证明了补肾活血中药复方可以抑制过氧化物酶体增殖物激活受体γ信号激活,改善骨细胞分化和血脂水平;但检测的信号以过氧化物酶体增殖物激活受体γ为主、尚不能明确过氧化物酶体增殖物激活受体α、过氧化物酶体增殖物激活受体β信号对股骨头坏死的作用机制,中药复方治疗股骨头坏死脂质调控机制仍需要更进一步的探究和思考,见图6。"
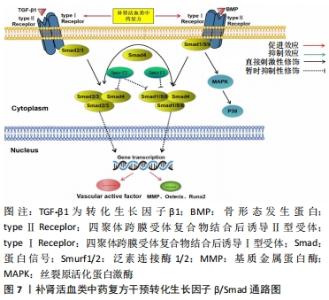
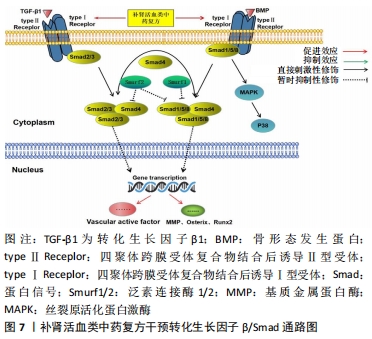
2.6 转化生长因子β/Smad信号通路 转化生长因子β超家族本质上是一种具有调节细胞生长活性的多肽类物质,可以通过结合特异的细胞膜受体参与调控骨细胞增殖分化、代谢及凋亡的生物过程[44]。转化生长因子β超家族系含有40多种细胞因子,如转化生长因子β、骨形态发生蛋白、激活素和抑制素。转化生长因子β1是人体骨组织中含量最多的生长因子,转化生长因子β1在细胞表面与特定的四聚体跨膜受体复合物结合后诱导Ⅱ型受体Ⅰ激酶结构域的磷酸化,从而激活Smad蛋白信号,该信号转运到细胞核来完成控制靶基因的转录。转化生长因子β/Smad信号通路可以调节成骨细胞增殖分化,抑制基质金属蛋白酶活性,防止骨形成基质分子的降解,刺激新骨的形成。此外,转化生长因子β/Smad信号通路亦能激活血管活性因子,诱导内皮细胞修复血管。骨形态发生蛋白是诱导成骨分化的重要因子,在骨形态发生蛋白家族中的骨形态发生蛋白2至骨形态发生蛋白16亚型中骨形态发生蛋白2诱导成骨作用最强,但它不是直接启动靶基因,而是通过丝裂原活化蛋白激酶信号诱导磷酸化和乙酰化,使Runx2、Osterix与磷酸化Smad蛋白形成复合物启动成骨细胞靶向基因的表达[45]。 有研究表明,相较于正常人,股骨头坏死患者的病理结果显示转化生长因子β1表达明显下调;且随着骨坏死严重程度,坏死区转化生长因子β1的表达量越低。有实验表明,肌注转化生长因子β1治疗激素性股骨头坏死兔,影像学结果显示双侧股骨头表面稍不平滑,但无明显股骨头塌陷;病理组织显示局部坏死病理无明显大量脂肪细胞增生和嗜酸性粒细胞聚集[46-47]。蛋白泛素-蛋白酶体通路可以特异性降解细胞内Smad蛋白;Smad泛素化调节因子Smurf1/2可选择性降解Smad蛋白和调控骨形态发生蛋白信号传导,来影响骨细胞增殖和分化。黄春元等[48]发现华山壮骨散通过诱导骨形态发生蛋白/Smad信号通路,增加骨形态发生蛋白2、骨形态发生蛋白4、Smad2、Smad4表达,进而上调Smurf1/2和降低26 蛋白水解酶复合体(26S-PSM)、蛋白泛素-蛋白酶体通路的表达,促进骨髓间充质干细胞成骨分化、成骨细胞增殖影响股骨头坏死。袁斓等[49]发现,活血通络汤能通过上调转化生长因子β1、骨形态发生蛋白2激活转化生长因子β1/Smad信号通路,增加碱性成纤维细胞生长因子、血小板衍生生长因子、骨钙素的表达水平,促进骨髓腔内成骨细胞增殖成骨、造血细胞形成血管,修复局部骨组织;抑制激素诱导的骨破坏,使骨小梁总体结构保持完整。补肾活血中药复方可以通过复合性激活转化生长因子β/Smad通路修复股骨头局部坏死组织,但该信号的传导涉及多个信号亚型、通路及相关蛋白,其中的机制尚待进一步明确,见图7。"
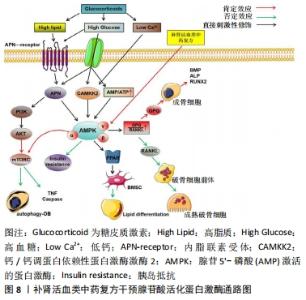
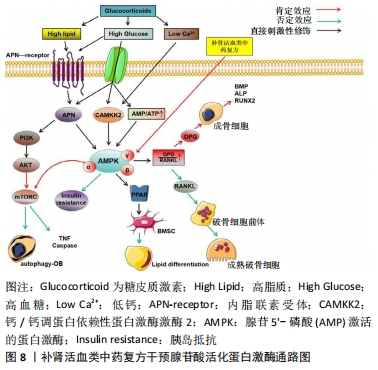
2.7 腺苷酸活化蛋白激酶信号通路 腺苷5’-磷酸激活的蛋白激酶本质上是一种进化保守的丝氨酸/苏氨酸蛋白激酶,其作为一种能量传感器通过调节分解、合成代谢过程的速率,来维持细胞能量代谢的动态平衡。腺苷酸活化蛋白激酶通路可被多个上游激酶激活磷酸化而激活,如内脂联素、肿瘤抑制肝激酶B1、钙/钙调蛋白依赖性蛋白激酶激酶2,腺苷酸活化蛋白激酶磷酸化后可调整腺苷5’-磷酸/ATP和ADP/ATP比率的变化,从而微调ATP消耗与合成之间的平衡[50]。腺苷酸活化蛋白激酶与腺苷5’-磷酸或ADP整合后活化,活化后形成的化合物可以通过磷酸化多种相关蛋白受体或下路调节转录因子完成监控细胞能量状态及细胞增殖、分化和自噬。肿瘤抑制肝激酶B1和钙/钙调蛋白依赖性蛋白激酶激酶2上游激酶可诱导腺苷酸活化蛋白激酶通路刺激成骨细胞分泌骨形态发生蛋白、血清碱性磷酸酶、RUNX2促进成骨细胞分化和骨基质形成,肿瘤抑制肝激酶B1又可诱导腺苷酸活化蛋白激酶通路刺激造血干细胞分化成不同的细胞后代。腺苷酸活化蛋白激酶是介入不同关键细胞信号通路的十字路口,如腺苷酸活化蛋白激酶活化化合物可磷酸化过氧化物酶体增殖物激活受体γ调控间充质干细胞的分化,磷酸化RANKL增加破骨细胞的分化和活性,也可通过下游靶点哺乳动物雷帕霉素复合物、PIK3C3调控PI3K/AKT通路影响成骨细胞增殖分化和自噬凋亡[51-52]。由于腺苷酸活化蛋白激酶通路具有调控细胞内能量的动态平衡功能,当激素引发血液、脂质、血糖等紊乱时即可影响整个腺苷酸活化蛋白激酶信号通路的传导使骨细胞发生炎症、自噬、凋亡,如激素可通过抑制腺苷酸活化蛋白激酶通路对下游靶点哺乳动物雷帕霉素复合物的激活,诱导骨髓间充质干细胞凋亡,同时激素紊乱产生的高血脂、血糖又可促进腺苷酸活化蛋白激酶磷酸化与过氧化物酶体增殖物激活受体γ、RANKL信号结合诱导骨髓间充质干细胞脂质分化、破骨细胞活性增强等[53]。张翔等[54]发现补肾活血方通过激活内脂联素-腺苷酸活化蛋白激酶信号传导通路,上调内脂联素、骨保护蛋白、Bcl-2基因等抗脂、成骨因子、抑制细胞凋亡基因的表达,下调肿瘤坏死因子α、半胱氨酸蛋白酶3等细胞自噬因子的表达,来减缓骨坏死局部的骨细胞凋亡。尽管研究证明补肾活血方可以通过激活腺苷酸活化蛋白激酶信号影响细胞能量代谢,调节骨坏死区域细胞的活动状态,但由于腺苷酸活化蛋白激酶结构复杂是α、β、γ亚基组成的三聚体且亚基又存在不同亚型,而腺苷酸活化蛋白激酶信号传导涉及多个上下游靶点和多条通路,因此中药复方对腺苷酸活化蛋白激酶的靶点影响尚不能完全明确,见图8。"
| [1] PETEK D, HANNOUCHE D, SUVA D. Osteonecrosis of the femoral head: pathophysiology and current concepts of treatment. EFORT Open Rev. 2019; 4(3):85-97. [2] 唐涛,苟远涛,唐俊,等.成都地区成人股骨头坏死流行病学研究[J].中国康复理论与实践,2018,24(8):970-974. [3] LIU F, WANG W, YANG L, et al.An epidemiological study of etiology and clinical characteristics in patients with nontraumatic osteonecrosis of the femoral head. J Res Med Sci. 2017;22(1):15. [4] IKEUCHI K, HASEGAWA Y, SEKI T, et al. Epidemiology of nontraumatic osteonecrosis of the femoral head in Japan. Mod Rheumatol. 2015;25(2):278-281. [5] 李子荣.股骨头坏死临床诊疗规范[J].中国矫形外科杂志,2016, 24(1):49-54. [6] 李雅男,覃彬森.股骨头坏死中医病名考辨[J].国际中医中药杂志, 2019(7): 769-771. [7] 郭雪峰,侯德才.股骨头坏死中医辨证客观化研究探讨[J].中华中医药学刊:1-7[2020-12-01] [8] 汪小敏,曹林忠,张晓刚,等.激素性股骨头坏死中医“证”的三大组学研究进展[J].中国骨质疏松杂志,2018,24(7):966-970. [9] 朱蜀云,杨康,王巍,等.股骨头坏死中医治法应用分析[J].中医正骨, 2020,32(1):40-42. [10] ZUO R, LIU M, WANG Y, et al. Correction to: BM-MSC-derived exosomes alleviate radiation-induced bone loss by restoring the function of recipient BM-MSCs and activating Wnt/β-catenin signaling. Stem Cell Res Ther. 2020;11(1):33. [11] WANG LJ, CAI HQ. Let-7b downgrades CCND1 to repress osteogenic proliferation and differentiation of MC3T3-E1 cells: An implication in osteoporosis. Kaohsiung J Med Sci. 2020;36(10):775-785. [12] HE X, HAN Z, JIANG W, et al. Hypoxia improved vasculogenesis in distraction osteogenesis through Mesenchymal-Epithelial transition (MET), Wnt/β-catenin signaling pathway, and autophagy. Acta Histochem. 2020;122(6):151593. [13] NIE Z, CHEN S, PENG H. Glucocorticoid induces osteonecrosis of the femoral head in rats through GSK3β-mediated osteoblast apoptosis. Biochem Biophys Res Commun. 2019;511(3):693-699. [14] ZHANG P, XU H, WANG P, et al. Yougui pills exert osteoprotective effects on rabbit steroid-related osteonecrosis of the femoral head by activating β-catenin. Biomed Pharmacother. 2019;120:109520. [15] 施乐,张超,季文辉,等.补肾活血汤通过抑制Wntβ-catenin信号通路对激素性股骨头坏死大鼠疗效及血管形态、VEGF的影响[J].四川中医, 2020, 38(2):59-62. [16] 谢磊,张严,姜自伟,等.引导骨再生技术结合补肾法修复大鼠股骨骨缺损[J].中国组织工程研究,2020,24(26):4106-4111. [17] LI D, HU Q, TAN G, et al. Erythropoietin Enhances Bone Repair Effects via the Hypoxia-Inducible Factor Signal Pathway in Glucocorticoid-Induced Osteonecrosis of the Femoral Head. Am J Med Sci. 2018; 355(6):597-606. [18] DASHTIMOGHADAM E, FAHIMIPOUR F, TONGAS N, et al. Microfluidic fabrication of microcarriers with sequential delivery of VEGF and BMP-2 for bone regeneration. Sci Rep. 2020;10(1):11764. [19] 胡亮,王军海,王志烈,等.骨形态发生蛋白2联合突变型低氧诱导因子1α修复激素性股骨头缺血性坏死[J].中国组织工程研究, 2018,22(28):4440-4446. [20] 刘锌,金翔,杜斌,等.右归饮加减方对兔激素性股骨头坏死的干预作用及其机制研究[J].江苏中医药,2019,51(9):81-85. [21] 王江伟,魏道德,王丽,等.通血健骨丸对兔缺血性坏死股骨头HIF-1α, VEGF和BMP-2表达的影响[J].临床与病理杂志,2017,37(12): 2625-2632. [22] 张岩,张志伟,叶宝飞.桃仁汤联合温针灸对中期股骨头缺血性坏死患者的临床疗效[J].中成药,2020,42(10):2820-2822. [23] LIU Y, XU Z, WANG Q, et al. Selective regulation of RANKL/RANK/OPG pathway by heparan sulfate through the binding with estrogen receptor β in MC3T3-E1 cells. Int J Biol Macromol. 2020;161:1526-1534. [24] ZHENG H, WANG C, HE JW, et al. OPG, RANKL, and RANK gene polymorphisms and the bone mineral density response to alendronate therapy in postmenopausal Chinese women with osteoporosis or osteopenia. Pharmacogenet Genomics. 2016;26(1):12-19. [25] AZETSU Y, CHATANI M, DODO Y, et al. Treatment with synthetic glucocorticoid impairs bone metabolism, as revealed by in vivo imaging of osteoblasts and osteoclasts in medaka fish. Biomed Pharmacother. 2019;118:109101. [26] 宋红梅,魏迎辰,李楠,等.温阳补肾方对兔激素性股骨头坏死组织中骨保护素和核因子-κB受体活化因子及其配体mRNA表达的影响[J].中国康复理论与实践,2019,25(2):178-183. [27] ZHENG L. Luteolin stimulates proliferation and inhibits late differentiation of primary rat calvarial osteoblast induced by high-dose Dexamethasone via Sema3A/NRP1/Pleixin A1. Curr Pharm Biotech. 2020.doi: 10.2174/1389201021666201216150442. [28] LIU YQ, HAN XF, BO JX, et al. Wedelolactone Enhances Osteoblastogenesis but Inhibits Osteoclastogenesis through Sema3A/NRP1/PlexinA1 Pathway. Front Pharmacol. 2016;7:375. [29] 袁斓,陈惠娜,江蓉星,等.活血通络汤基于Notch信号通路对家兔激素性股骨头缺血性坏死治疗作用机制研究[J].时珍国医国药, 2016,27(10):2305-2308. [30] YOUNGSTROM DW, HANKENSON KD. Contextual Regulation of Skeletal Physiology by Notch Signaling. Curr Osteoporos Rep. 2019;17(4):217-225. [31] 平依林,娄锋,杨肖,等.Notch1蛋白高表达抑制破骨细胞增殖和分化[J].华西口腔医学杂志,2016,34(2):121-124. [32] 雷乐,张玲莉,杨杰.Notch信号通路在骨髓间充质干细胞及骨代谢疾病中的功能研究进展[J].中国骨质疏松杂志,2020,26(9):1364-1369. [33] MICHALICKA M, BOISJOLI G, JAHAN S, et al. Human Bone Marrow Mesenchymal Stromal Cell-Derived Osteoblasts Promote the Expansion of Hematopoietic Progenitors Through Beta-Catenin and Notch Signaling Pathways. Stem Cells Dev. 2017;26(24):1735-1748. [34] CAO J, WEI Y, LIAN J, et al. Notch signaling pathway promotes osteogenic differentiation of mesenchymal stem cells by enhancing BMP9/Smad signaling. Int J Mol Med. 2017;40(2):378-388. [35] 王敏,江蓉星,李涛,等.活血通络汤对SANFH兔造模过程中Notch2/DLL1/Hes1表达的影响[J].中国中西医结合杂志,2018, 38(11):1384-1388. [36] 陈子锴,江蓉星,方锐洁,等.活血通络汤对激素性股骨头坏死造模兔PDGF、BMP-2及Notch3的影响[J].辽宁中医杂志,2019, 46(1):186-190+225. [37] 蔡万翔,江蓉星,王敏,等.活血通络汤在家兔激素性股骨头缺血性坏死模型中对Notch1、DLL3和HERP1的影响[J].中华中医药杂志,2018,33(1):300-303. [38] KIM DH, KIM DH, HECK BE, et al. PPAR-δ agonist affects adipo-chondrogenic differentiation of human mesenchymal stem cells through the expression of PPAR-γ. Regen Ther. 2020;15:103-111. [39] LI T, ZHANG L, JIN C, et al. Pomegranate flower extract bidirectionally regulates the proliferation, differentiation and apoptosis of 3T3-L1 cells through regulation of PPARγ expression mediated by PI3K-AKT signaling pathway. Biomed Pharmacother. 2020;131:110769. [40] YUAN N, LI J, LI M, et al. BADGE, a synthetic antagonist for PPAR gamma, prevents steroid - related osteone-crosis in a rabbit model.BMC Musculoskelet Disord.2018;19(1):129. [41] 李晓敏,孔祥英,张村,等.健脾活骨方不同提取部位对骨髓间充质干细胞增殖和分化的影响[J].中国中医药信息杂志,2015,27(7): 63-67. [42] KONG X, LI X, ZHANG C, et al. Ethyl acetate fraction of Huogu formula inhibits adipogenic differentiation of bone marrow stromal cells via the BMP and Wnt signaling pathways. Int J Biol Sci. 2017;13(4):480-491. [43] 孙海忠,韦标方.活血生骨汤配合打压支撑植骨术治疗塌陷前期股骨头坏死研究[J].时珍国医国药,2019,30(8):1911-1913. [44] YANG X, CHEN Z, CHEN C, et al. Bleomycin induces fibrotic transformation of bone marrow stromal cells to treat height loss of intervertebral disc through the TGFβR1/Smad2/3 pathway. Stem Cell Res Ther. 2021;12(1):34. [45] YU S, GUO J, SUN Z, et al. BMP2-dependent gene regulatory network analysis reveals Klf4 as a novel transcription factor of osteoblast differentiation. Cell Death Dis. 2021;12(2):197. [46] TAO J, DONG B, YANG LX, et al. TGF-β1 expression in adults with non-traumatic osteonecrosis of the femoral head. Mol Med Rep. 2017;16: 9539-9544. [47] 吴成玉,许克庆,葛迅,等.TGF-β1对兔激素性股骨头缺血坏死治疗的实验研究[J].锦州医科大学学报,2020,41(3):31-35. [48] 黄春元,刘英雪,谢晚晴,等.华山壮骨散对激素性股骨头坏死大鼠BMP/Smad/UPP通路的作用机制[J].中国骨质疏松杂志,2019, 25(11):1533-1536. [49] 袁斓,陈惠娜,江蓉星,等.活血通络汤对激素性股骨头缺血性坏死模型兔股骨细胞因子表达的影响[J].中医杂志,2016,57(24): 2130-2133. [50] KIM TJ, KIM HJ, KANG M, et al. Ginsenoside F2 induces cellular toxicity to glioblastoma through the impairment of mitochondrial function. Phytomedicine. 2021;83:153483. [51] LEE J, HONG SW, KIM MJ, et al. Metformin, resveratrol, and exendin-4 inhibit high phosphate-induced vascular calcification via AMPK-RANKL signaling. Biochem Biophys Res Commun. 2020;530(2):374-380. [52] JACQUEL A, LUCIANO F, ROBERT G, et al. Implication and Regulation of AMPK during Physiological and Pathological Myeloid Differentiation. Int J Mol Sci. 2018; 19(10):2991. [53] WANG L, ZHANG HY, GAO B, et al. Tetramethylpyrazine Protects Against Glucocorticoid-Induced Apoptosis by Promoting Autophagy in Mesenchymal Stem Cells and Improves Bone Mass in Glucocorticoid-Induced Osteoporosis Rats. Stem Cells Dev. 2017;26(6):419-430. [54] 张翔,吴泱,董晓俊,等.补肾活血方调控兔激素性股骨头坏死APN-AMPK信号通路的实验研究[J].中国中西医结合杂志,2019, 39(10):1234-1239. |
| [1] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhou Qian, Zhang Qiang, Chen Qiu. Human salivary components and osteoporosis/osteopenia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1439-1444. |
| [2] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| [3] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| [4] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [5] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [6] | Liang Xuezhen, Yang Xi, Li Jiacheng, Luo Di, Xu Bo, Li Gang. Bushen Huoxue capsule regulates osteogenic and adipogenic differentiation of rat bone marrow mesenchymal stem cells via Hedgehog signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1020-1026. |
| [7] | Wang Jifang, Bao Zhen, Qiao Yahong. miR-206 regulates EVI1 gene expression and cell biological behavior in stem cells of small cell lung cancer [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1027-1031. |
| [8] | Guo Jia, Ding Qionghua, Liu Ze, Lü Siyi, Zhou Quancheng, Gao Yuhua, Bai Chunyu. Biological characteristics and immunoregulation of exosomes derived from mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1093-1101. |
| [9] | Wu Weiyue, Guo Xiaodong, Bao Chongyun. Application of engineered exosomes in bone repair and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1102-1106. |
| [10] | Zhou Hongqin, Wu Dandan, Yang Kun, Liu Qi. Exosomes that deliver specific miRNAs can regulate osteogenesis and promote angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1107-1112. |
| [11] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [12] | Huang Chenwei, Fei Yankang, Zhu Mengmei, Li Penghao, Yu Bing. Important role of glutathione in stemness and regulation of stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1119-1124. |
| [13] | Hui Xiaoshan, Bai Jing, Zhou Siyuan, Wang Jie, Zhang Jinsheng, He Qingyong, Meng Peipei. Theoretical mechanism of traditional Chinese medicine theory on stem cell induced differentiation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1125-1129. |
| [14] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [15] | Fan Yiming, Liu Fangyu, Zhang Hongyu, Li Shuai, Wang Yansong. Serial questions about endogenous neural stem cell response in the ependymal zone after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1137-1142. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||