Chinese Journal of Tissue Engineering Research ›› 2019, Vol. 23 ›› Issue (34): 5479-5485.doi: 10.3969/j.issn.2095-4344.1923
Previous Articles Next Articles
The competitive situation of tissue engineering and regenerative medicine based on patent analysis
-
Received:2019-07-02Online:2019-12-08Published:2019-12-08 -
Contact:Ouyang Zhaolian, Associate Researcher, Institute of Medical Information / Medical Library, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100020, China -
About author:Zhang Ting, PhD, Associate Researcher, Master’s supervisor, Institute of Medical Information / Medical Library, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100020, China -
Supported by:the Fundamental Research Funds for the Central Universities, No. 2017PT63006 (to ZT), Chinese Academy of Medical Sciences Innovation Fund for Medical Sciences (CIFMS), No. 2016-I2M-2-004 (to CH); the National Key Research and Development Program of China, No. 2016YFC0104805 (Ouyang ZL)
CLC Number:
Cite this article
share this article
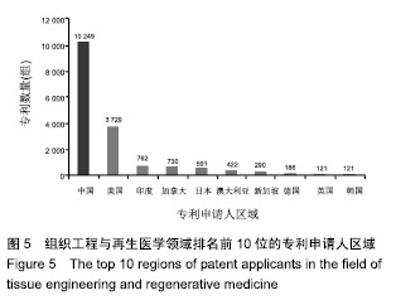
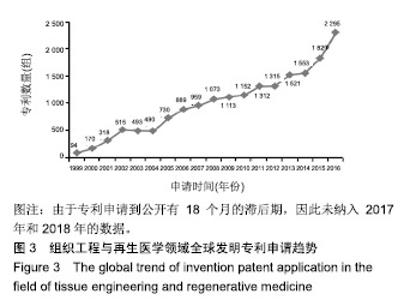
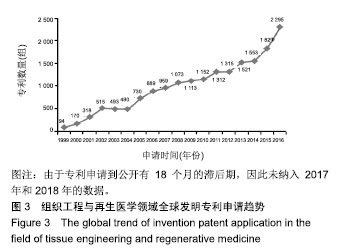
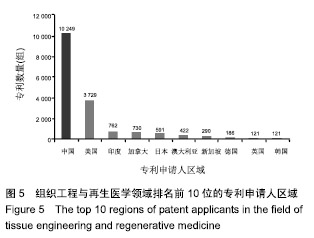
组织器官缺损及功能缺陷的修复与替代需求旺盛,组织工程与再生医学创新活跃,是最具发展潜力的高新技术生物产业之一。全球许多国家和地区通过设立国家科技战略、规划及持续投入支持相关科研工作,组织工程与再生医学成为多个国家和地区的优先发展领域。因此,全球组织工程与再生医学的技术开发活动十分活跃,专利申请和授权都呈现快速增长的态势,尤其是近10年发展迅速。 2.2 专利申请人区域分布 专利申请人区域分布可以从一定程度上反映一个领域的技术来源地[10]。全球组织工程与再生医学领域专利申请共55 328件,有22 799组简单同 族,专利申请数量排名前10位的申请人区域见图5,反映出该领域居前列的技术来源地。中国有10 249组,处于第1位,占全球该领域专利申请总量的44.95%,接近1/2,是主要的技术来源地;其次是美国,专利申请数量3 729组,全球占比16.36%;其他技术来源地专利数量均在1 000组以下,分别是印度(762组)、加拿大(730组)、日本(591组)、澳大利亚(422组)、新加坡(290组)、德国(186组)、英国(121组)和韩国(121组)。组织工程与再生医学领域的技术来源地以中国和美国为主,中国是全球第一大技术来源地。从专利数量上看,中国占有巨大的优势,但由于近些年中国对专利申请的大力推进及政策引导,存在大量政策催生情况,实际的中美差异并没有如此悬殊,且此次分析采用了简单同族的合并规则,由于中国和其他专利发达国家的申请特征有所差异,中国大多采用本国申请,同族专利数量较少,发达国家多采用跨国布局的方法,同族专利的数量较多,这也是此次分析使差距显著拉大的主要原因。"
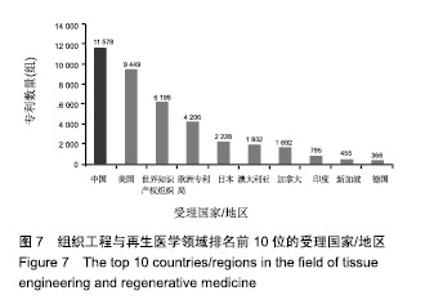
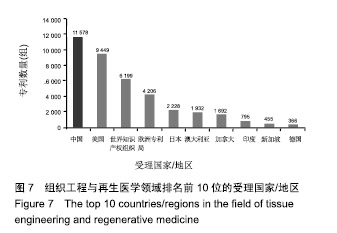
2.3 专利受理国家/地区分布 专利受理国家/地区可以一定程度上反映一个领域的目标市场分布情况[10]。全球组织工程与再生医学领域专利申请共55 328件,从专利受理国家/地区分布来看,有40 755组简单同族,专利申请数量排名前10位的受理国家/地区见图7,反映出该领域的主要目标市场情况。中国排在第1位,专利申请数量有11 578组,全球专利布局数量最多,占全球本领域专利申请总量的28.41%,是全球最受关注的目标市场。美国排在第2位,专利申请数量9 449组,与中国差距不大,全球占比为23.18%,也是全球重要的目标市场。世界知识产权组织排在第3位,专利申请数量6 199组,占比为15.21%,反映出各国都在争夺国际市场。欧洲专利局排在第4位,专利申请数量4 206组,占比10.32%,表明欧洲市场也是各国关注的焦点。其他目标市场的专利申请数量均不及3 000组,分别是日本(2 228组)、澳大利亚(1 932组)、加拿大(1 692组)、印度(795组)、新加坡(455组)和德国(366组)。组织工程与再生医学领域的主要目标市场以中国和美国为主,中国是全球最受关注的目标市场,此外,国际市场和欧洲市场也是该领域重点关注的目标市场。"
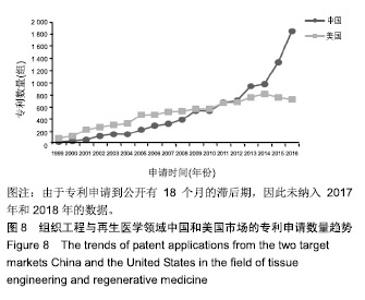
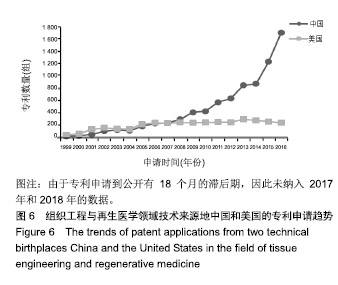
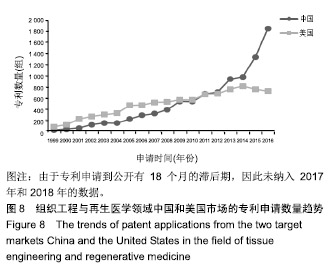
中国和美国是组织工程与再生医学领域的主要目标市场,近20年的专利申请趋势见图8。中国是全球第一大目标市场,2012年的专利申请数量达到699组,首次超过美国(667组),从2014年开始,专利申请增长趋势明显,且领先优势明显,2014年专利申请数量达到975组,并持续增长至2016年的1 854组,近10年复合增长率22.16%,发展速度很快。美国每年的专利申请数量均在1 000组以下,近几年维持在800组左右,近10年复合增长率3.92%。从以上分析可以发现,美国作为老牌发达国家,从1999年开始就是该技术主要青睐的目标市场,随着中国市场的逐渐扩大,以及改革开放政策成效的逐渐显现,中国作为目标市场逐渐成为技术投资者的统一认识,因此才呈现出专利数量的激增,进而在2012年超过了美国,于2016年达到了当前峰值,这与中国市场的逐渐增加及中国在世界上的经济地位密不可分,因此中国市场具有极大的挖掘潜力。"
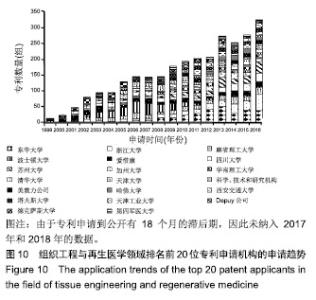
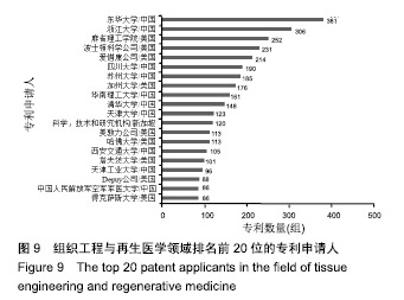
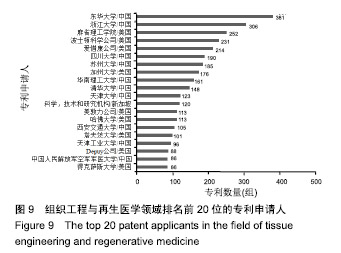
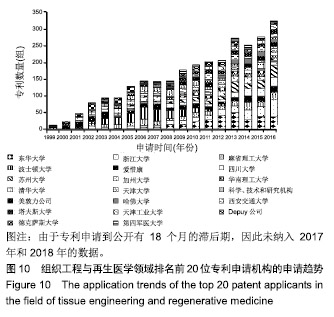
组织工程与再生医学领域排名前20位的专利申请机构近20年专利申请趋势见图10。美国的波士顿科学公司在2004至2009年间,每年的专利申请数量均在20组以上,与其他机构相比处于较明显的领先地位。2010至2013年间,东华大学的专利申请数量呈现明显的增长趋势,且远远领先于其他机构,专利申请数量由2010年的25组,增长至2013年的51组。此后,东华大学的年专利申请数量稍有回落,但仍维持在40组左右,于2017年达到峰值53组。浙江大学从2014年开始与东华大学专利申请数量呈现不相上下,2014年专利申请数量30组,2016年达到50组,超过了东华大学的年专利申请数量,此后专利申请数量有所回落,但每年的申请数量仍维持在30组左右。"

2.5 发明人 组织工程与再生医学领域专利申请数量排名前20位的发明人见表1,大部分都是国内发明人,国外发明人只有1个。专利申请数量最多的3个发明人分别是朱明(四川师范大学)、蒋燕妮(四川师范大学)和王一飞(广州赛莱拉干细胞科技股份有限公司、广东美赛尔细胞生物科技有限公司和广州赛莱拉生物基因工程有限公司),专利申请数量72组。 2.6 技术领域分布 专利由审查员依据其对技术方案的理解赋予若干代表其创新点的国际专利分类号(IPC),通过IPC可了解该专利涉及的相关技术创新点[10,20-21]。通过对组织工程与再生医学领域专利的国际专利分类号进行分析,来揭示其技术分布情况。表2是组织工程与再生医学领域专利数量排名前20位的国际专利分类号,技术领域主要涉及组织工程支架[22-23]、支架材料[24-25]、材料分析方法[26-27]、细胞或组织培养技术与装置[28]、高分子材料[29]、细胞测定或检查方法[30]、药物组合物的制备方法等技术点[31]。 专利数量最多的技术领域是A61L27,专利数量6 636组,主要涉及组织工程及再生医学领域相关支架材料,例如:CN101766837B(标题:仿生多孔微球组织工程支架及其制作方法)是关于支架及其制作方法的专利,US20140314824A1(标题:Porous Scaffold For Tissue Engineering And Preparation Method Thereof)是用于组织工程的多孔支架及其制备方法。专利数量排在第2位的是C12N5,有3 707组,主要涉及相关细胞及组织的培养,例如:US8637065(标题:Dermis-derived cells for tissue engineering applications)是用于组织工程应用的真皮衍生细胞,EP2412799B1(标题:Method For Reconstructing Tissue Engineered Human)是关于重建组织工程人角膜内皮细胞的方法。专利数量排在第3位的是A61F2,有2 991组,主要涉及相关植入物,例如:DE102005018643A1(标题:Osteogenes Matrixkomposit, Verfahren zu dessen Herstellung sowie Implantat und Scaffold für das Tissue Engineering mit einer Beschichtung aus einem osteogenen Matrixkomposit)是有关涂布组织工程植入物或支架的成骨基质复合物,WO2010117389A1(标题:Advanced Bio-Compatible Nanocomposite Surface Coatings For Implants And Tissue Engineering Scaffolds)是用于植入物和组织工程支架的生物兼容性纳米复合表面涂层。"

| [1]Abzan N, Kharaziha M, Labbaf S. Development of three-dimensional piezoelectric polyvinylidene fluoride-graphene oxide scaffold by non-solvent induced phase separation method for nerve tissue engineering. Materials & Design.2019;167:107636.[2]Kenar H, Ozdogan CY, Dumlu C, et al. Microfibrous scaffolds from poly(l-lactide-co-ε-caprolactone) blended with xeno-free collagen/hyaluronic acid for improvement of vascularization in tissue engineering applications. Materials Science and Engineering:C.2019;97:31-44.[3]Nabavinia M, Khoshfetrat AB, Naderi-Meshkin H. Nano-hydroxyapatite-alginate-gelatin microcapsule as a potential osteogenic building block for modular bone tissue engineering. Mater Sci Eng C Mater Biol Appl. 2019;97: 67-77.[4]王春仁,白东亭.中国组织工程与再生医学的最新研究进展[J].药物分析杂志,2010,30(7):1370-1372.[5]曹谊林,崔磊,刘伟.中国组织工程研究回顾与发展[J].医学研究通讯,2005,3(2):5-6.[6]罗远,黄远亮.脂肪干细胞生物学特性及在口腔再生医学中的应用[J].中国组织工程研究,2017,21(5):795-801.[7]李大为,何进,何凤利,等.丝素蛋白/壳聚糖复合材料在组织工程中应用的研究进展[J].中国生物工程杂志,2017,37(10): 111-117.[8]Przekora A. The summary of the most important cell-biomaterial interactions that need to be considered during in vitro biocompatibility testing of bone scaffolds for tissue engineering applications. Mater Sci Eng C Mater Biol Appl.2019;97:1036-1051.[9]Zhu H, Kimura T, Swami S, et al. Pluripotent stem cells as a source of osteoblasts for bone tissue regeneration. Biomaterials.2019;196:31-45.[10]张婷,欧阳昭连.基于专利分析及可视化的抗肿瘤药竞争态势研究[J].中国新药杂志,2018,27(20):2337-2345.[11]Zhang T, Chen J, Jia X. Identification of the Key Fields and Their Key Technical Points of Oncology by Patent Analysis. PLoS One.2015;10(11):e0143573.[12]Chen DZ, Chang HW, Huang MH, et al. Core technologies and key industries in Taiwan from 1978 to 2002: A perspective from patent analysis. Scientometrics.2005; 64(1):31-53.[13]Qu J, Lu J, Hu Y. Research and development of anti-Parkinson's drugs: an analysis from the perspective of technology flows measured by patent citations. Expert Opin Ther Pat.2019;29(2):127-135.[14]Jeong Y, Yoon B. Development of patent roadmap based on technology roadmap by analyzing patterns of patent development. Technovation.2015;39-40:37-52.[15]赵晓宇.药物研发相关的专利策略研究[D].北京:中国人民解放军军事医学科学院,2007.[16]张婷,晏仁义,崔胜男,等.药学科研领域几种常用仪器的专利计量分析[J].中国药业,2014,23(2):12-15.[17]张婷,贾晓峰.基于专利计量分析的抗HIV药物发展趋势研究[J].现代生物医学进展,2015,15(8):1540-1546.[18]张婷,贾晓峰.基于专利分析的天然抗肿瘤药制剂技术发展态势研究[J].现代生物医学进展,2016,16(8):1546-1550.[19]池慧.中国医疗器械创新力发展报告[M].北京:科学出版社, 2018.[20]张婷,欧阳昭连.中国肿瘤领域重点技术的识别研究[J].中国肿瘤,2018,27(5):393-400.[21]张婷.基于专利分析和社会网络分析的天然抗肿瘤药研究[J].中国肿瘤,2017,26(8):642-649.[22]何凤利,何进,尹大川.静电纺丝制备组织工程支架的研究进展[J].材料导报,2014,28(23):1-7.[23]曹雪飞,宋朋杰,乔永杰,等. 3D打印骨组织工程支架的研究与应用[J]中国组织工程研究,2015,19(25):4076-4080.[24]Wang Y, Wang X, Shi J, et al. A Biomimetic Silk Fibroin/Sodium Alginate Composite Scaffold for Soft Tissue Engineering. Sci Rep.2016;6:39477.[25]Rogozhnikov D, O'Brien PJ, Elahipanah S, et al. Scaffold Free Bio-orthogonal Assembly of 3-Dimensional Cardiac Tissue via Cell Surface Engineering. Sci Rep.2016;6: 39806.[26]张志强,黄向华,赵林远.微环境对细胞的影响以及仿生学在组织工程支架中的应用[J].中国生物工程杂志,2014,34(4): 101-109.[27]陈希亮,陈庆华,庄颖,等.KGM/明胶/nano HAP椎间盘纤维环组织工程支架的制备与研究[J].无机材料学报,2018,33(1): 60-66.[28]李正茂.生物活性玻璃组织工程支架的制备及细胞相容性研究[D].广州:华南理工大学,2013.[29]Hatamzadeh M, Najafi-Moghadam P, Baradar-Khoshfetrat A, et al. Novel nanofibrous electrically conductive scaffolds based on poly(ethylene glycol)s-modified polythiophene and poly(epsilon-caprolactone) for tissue engineering applications. Polymer.2016;107(19):177-190.[30]蒋涛.大鼠脱细胞脊髓支架的优化改性及相关特性研究[D].重庆:第三军医大学,2013.[31]卫兰.基于功能性聚肽共聚物及高分子水凝胶的载药体系及组织工程支架的制备和研究[D].上海:华东理工大学,2011. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Li Jun, Zuo Xinhui, Liu Xiaoyuan, Zhang Kai, Han Xiangzhen, He Huiyu, . Effect of over expression of miR-378a on osteogenic and vascular differentiation of bone marrow mesenchymal stem cell sheet [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(31): 4939-4944. |
| [11] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [12] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [13] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [14] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [15] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||