Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (30): 4849-4854.doi: 10.3969/j.issn.2095-4344.0985
Previous Articles Next Articles
Current situation and development progress of vascular grafts
Yan Tuo1, Liu Ya-wen1, Wu Can1, Zhou Feng1, Liu Si-shi1, Liu Yuan1, Ouyang Chen-xi2
- 1Wuhan Yangsen Biotechnology Co., Ltd., Wuhan 430079, Hubei Province, China; 2Department of Vascular Surgery, Fuwai Hospital, Chinese Academy of Medical Sciences, Beijing 100037, China
-
Received:2018-05-29Online:2018-10-28Published:2018-10-28 -
Contact:Ouyang Chen-xi, Associate chief physician, Department of Vascular Surgery, Fuwai Hospital, Chinese Academy of Medical Sciences, Beijing 100037, China -
About author:Yan Tuo, Master, Wuhan Yangsen Biotechnology Co., Ltd., Wuhan 430079, Hubei Province, China -
Supported by:the National Key Research and Development Plan of China, No. 2017YFC1104100
CLC Number:
Cite this article
Yan Tuo, Liu Ya-wen, Wu Can, Zhou Feng, Liu Si-shi, Liu Yuan, Ouyang Chen-xi. Current situation and development progress of vascular grafts[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(30): 4849-4854.
share this article
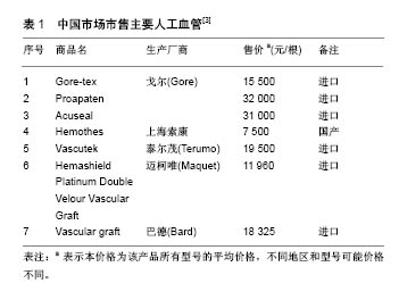
2.1 人工血管市场情况分析 目前在临床上使用的人工血管可分为织造型和非织造型,内径范围一般在4- 36 mm。非织造型人工血管一般由膨体聚四氟乙烯组成,内径范围多在4-10 mm之间,膨体聚四氟乙烯是由聚四氟乙烯经由糊膏挤出、膨化拉伸等工艺后得到,具有独特的节-纤维微观结构,能够产生大量的中空空间[3],人体组织细胞及血管可长入其微孔,形成组织连接,如同自体组织一样,可以有效提高人工血管的长期通畅率。目前市场上应用较多的非织造型人工血管主要来自国外,这些产品都具有高孔隙率、稳定性好、应用广泛等特点,据报道,Gore-Tex人工血管的孔隙率可达到76%[4]。 近年来,Gore公司在其纯膨体聚四氟乙烯Gore-tex基础上又开发出来了两款改进型产品Proapaten和Acuseal,并获得了国家食品药品监督管理局批准上市。两款产品在人工血管材料纯膨体四氟乙烯表面采用涂层技术,引入了肝素抗凝涂层CBAS(Carmeda BioActive Surface,Carmeda),极大提高了人工血管的抗血栓性和通畅率。其中Acuseal人工血管还在聚四氟乙烯材料中间引入了硅胶层,增加了人工血管的耐穿刺性。Proapaten人工血管于2000年第一次植入人体,截至目前全世界已经植入超过100 000根[5]。有报道指出,Proapaten人工血管在膝下的植入一年通畅率达到70%以上[6-8]。 织造型人工血管一般由聚酯涤纶材料经过编织而成,内径多在10-36 mm之间。聚酯涤纶化学名称为聚对苯二甲酸乙二醇酯,相对分子质量为15 000-20 000,为高度结晶性聚合物,具有高强度、高柔软性、回弹性优异、吸水率极低等特点。 截止到2017年,已有数十个人工血管产品在中国获得了批准,表1列举了目前中国市场主要的人工血管供应商。"
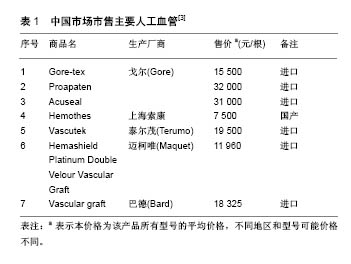
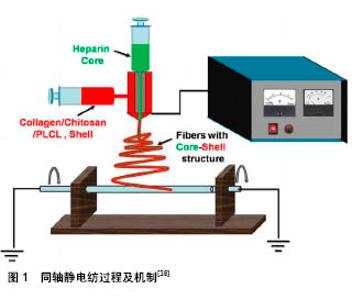
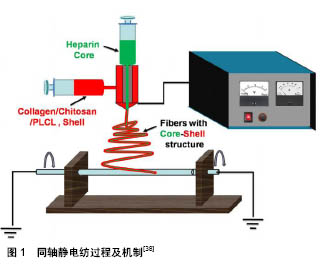
从表1可以看出,目前中国市场上人工血管产品主要依赖于进口,市场完全由国外厂商主导,售价均在 1万-4万元人民币之间不等,总体而言市场价格偏高,中国仅有上海索康一家企业能够生产。 2.2 人工血管材料 人工血管作为三类植入医疗器械,应该对机体无毒性,生物及血液相容性良好,具有良好的力学强度及可促进细胞黏附增长的多孔结构。按来源不同,人工血管材料可分为动物源脱细胞基质、天然材料及高分子合成材料3大类。 2.2.1 动物源脱细胞基质 将同种或者异种来源的动物血管或肠系膜,通过酶处理、超声或离心技术处理成脱细胞基质后制备成组织工程人工血管,是近年来人工血管研究的热点。脱细胞技术可有效保留动物源血管细胞外基质蛋白,又可避免脱细胞人工血管移植血管后引起免疫反应。这种材料在人工血管领域具有广泛的应用前景。 涂秋芬等[9]用多聚环氧化合物对犬主动脉进行了一系列的脱细胞处理,制备出一种脱细胞血管支架,随后在其表面接种平滑肌细胞及血管内皮细胞。研究表明这种脱细胞人工血管能够有效保持血管力学性能,且具有优良的细胞相容性,平滑肌细胞及血管内皮细胞能在其上生长良好,可形成密度均匀的细胞层。 冉峰等[10]利用酶处理的方法将兔主动脉制备成脱细胞血管支架,在其上体外培养兔骨髓间充质干细胞,构建出一种新型组织工程血管。研究表明,这种组织工程人工血管具有与正常动脉结构类似的3层结构,内皮细胞能完整覆盖其上,将这种兔脱细胞人工血管移植进同种异体大白兔体内3个月后,血管通畅率高达90%。 武欣等[11]用去垢剂及酶处理的方法将猪颈动脉进行脱细胞处理制备成血管支架,在其上培养犬骨髓间充质干细胞诱导分化的血管内皮细胞。实验结果表明,这种脱细胞人工血管的孔隙率高达94.93%,显著性高于天然血管,且该血管支架具有良好的力学性能,爆破强度及缝合耐受强度与天然血管无统计学差异。 2.2.2 天然高分子材料 天然高分子材料如胶原、明胶、海藻酸钠、壳聚糖等,一般具有无毒、亲水、细胞亲和性及生物相容性好等特点,特别适用于制备人工血管[12-15]。但这些天然高分子材料往往力学性能欠佳,需进行一定处理后方可满足人工血管。 He等[16]将纤维蛋白原蛋白利用静电纺丝技术与聚(L-乳酸)-co-聚(ε-己内酯)共纺组成复合纤维支架。研究结果表明,通过调控二者比例,复合纤维支架具有可调控的降解速率,其抗拉强度和断裂应变也随之变化。同时,这种复合纤维支架还可为细胞附着、扩散和增殖提供良好的微环境。 壳聚糖与丝素蛋白材料作为天然可降解高分子材料,因其良好的生物相容性[17-18],目前在血管组织工程研究中被应用广泛。刘涛[19]制备了新型可降解的壳聚糖-硫酸化丝素蛋白小口径人工血管,评估了该小口径人工血管旁路移植后效果。研究结果表明,该新型可降解的小口径人工血管具有良好的血液相容性,且各项力学性能稳定,但血管吻合处易产生组织增生及纤维化,使得血管在移植早期易产生狭窄或者堵塞现象,尚需对其进一步改进。 2.2.3 合成高分子材料 同天然高分子材料相比,利用合成高分子材料研发人工血管的历史更长。有许多性能优异的材料,如:涤纶、聚四氟乙烯、聚氨酯、聚己内酯等先后被应用于人工血管的研发,且大多都已实现了商业化[20-23]。合成高分子材料具有来源可控、质量稳定性高、加工简单及机械性能好等优点,目前对这些传统高分子材料的研究与改良也是目前的热点方向之一。 Bastijanic等[24]用膨体聚四氟乙烯制作出一种人工血管,并在其上进行表面改性以提高血管通畅率。研究结果表明,在膨体聚四氟乙烯人工血管内壁涂覆一层细胞黏附的含氟表面活性剂,可明显提高膨体聚四氟乙烯人工血管的通畅率,并能够有效减少内皮增生及血栓形成。Hoshi等[25]研究了肝素改性膨体聚四氟乙烯人工血管的血液相容性和细胞相容性,结果表明,生物活性肝素固定化后的膨体聚四氟乙烯人工血管内壁血小板黏附减少,并能有效抑制血液凝固形成血栓,保证了血管的通畅率。 Khorasani等[26]采用相转变技术制备出内径为 4 mm、壁厚为0.3-0.4 mm的微孔聚氨酯人共血管,细胞黏附和增长实验表明,这种微孔人工血管孔隙率优良,有利于细胞的向内生长,具有良好的应用效果与前景。Miyamoto等[27]将聚氨酯制备成一种微孔结构人工血管,比较了这种人工血管与自体静脉移植对机体的影响。研究表明,与自体静脉血管移植相比,将这种微孔结构聚氨酯人工血管植入体内后8周以内,微孔结构聚氨酯人工血管通畅率更高,内膜增生现象更少。 Wang等[28]研究了电纺聚己内酯血管对巨噬细胞极化和动脉再生的影响。结果表明,大孔隙聚己内酯电纺人工血管有利于细胞浸润和细胞外基质分泌,血管可保持较长时间的通畅性,并且电纺丝聚己内酯血管可促进血管再生及巨噬细胞在重塑过程转化为M2表型。 2.3 人工血管新技术 虽然传统的人工血管产品已在市场上应用多年,但血栓率高,组织相容性不佳等问题依然存在,特别是小口径人工血管(内径≤4 mm)尚未有令人满足的产品推出。所以对于如何解决人工血管,特别是小口径人工血管(内径≤4 mm)的抗凝血、抗组织增生、炎性反应等方面工作一直是研究热点。目前很多新的方向已在人工血管领域开始应用,例如生物涂层技术、静电纺丝技术、组织工程等方向是目前研究较多的领域。 2.3.1 生物涂层技术 理想的人工血管材料应该具有抗血栓、抗血小板聚集、组织相容性好、无炎性反应等特点。目前Gore公司的Proapaten和Acuseal人工血管在膨体聚四氟乙烯表面固定肝素涂层,虽然肝素涂层在抗凝血和血栓方面取得了明显效果,但远期来看其对于人工血管与自体血管组织的长期接触与融合帮助不大。目前,研究者们将研究目光投向了与生物体组成更为相似的多肽类物质[29-32],期望可形成与自体更为相似的表面,改善长期留存的问题。 Tang等[33]设计了一种适用于膨体聚四氟乙烯人工血管的表面改性剂,主要由含氟表面活性剂聚合物组成,包含黏合肽和多糖。该表面改性剂主要通过促进快速表明内皮化来改善移植物血液相容性。研究结果表明,与精氨酸-甘氨酸-天冬氨酸和经氟表面活性剂改性的环状精氨酸-甘氨酸-天冬氨酸相比,寡聚糖(M-7)和环状半胱氨酸-精氨酸-精氨酸-谷氨酸-苏氨酸-丙氨酸-色氨酸-丙氨酸-半胱氨酸能有效减少血小板黏附,这些结果说明该表面改性可促进表面内皮化,同时减少血小板黏附,最终明显改善移植物的血液相容性。Walluscheck等[34]研究了一种在膨体聚四氟乙烯人工血管表面耦合可促进细胞黏合的精氨酸-甘氨酸-天冬氨酸合成多肽方法,结果表明可通过具有促进黏附作用的精氨酸-甘氨酸-天冬氨酸肽和人造材料之间的特异性结合来改善膨体聚四氟乙烯上的内皮细胞附着。 Liu等[35]为了解决材料与血液接触时的血栓和凝血等问题,将赖氨酸与肝素制成混合微球固定在有多巴胺沉积的316L不锈钢表面。检测表明,材料的抗凝血酶Ⅲ大幅度增加,活化部凝血活酶时间和凝血酶时间延长,血管细胞也可在材料表面大量增殖与分化,表明这种涂层技术能有效提高人工血管抗凝血性能。 2.3.2 静电纺丝技术 静电纺丝技术是利用高压静电场作用,使材料溶液形成带电的喷射流,并在电场中被拉伸,最后接收形成无纺状态的纳米纤维层。这种纤维层具有与人体组织细胞外基质膜类似的结构,且具有高孔隙率等特点,有利于自体细胞的黏附、增殖,提高人工血管的生物相容性。 Catto等[36]用静高压电纺丝的方法将丝素蛋白制备成1.5 mm和4.5 mm口径人工血管,并且对比了大鼠主动脉及市售Gore-tex同类型产品。结果表明,静电纺丝素蛋白血管具有更高的爆破强度和顺应性,血管表面呈纳米级孔洞分布,平滑肌细胞可在其上黏附及增殖,将其植入大鼠皮下15 d后能很好地与大鼠组织细胞融合。 Yin等[37]用同轴静电纺的方式制备了一种具有肝素缓释功能的人工血管。同轴静电纺制备的人工血管具有壳-芯结构,内核为肝素,外层为胶原蛋白/壳聚糖/聚己内酯。研究表明,该人工血管的肝素封装率高达75%,肝素可持续释放达45 d,3周后依然具有较好的抗血小板黏附性能,同时其力学性能也优于人体血管。 Zhang等[38]以聚己内酯为内核、胶原蛋白为外层,采用同轴静电纺工艺将胶原蛋白/聚己内酯制作成纳米纤维支架(图1),并将这种纤维支架与胶原涂层聚己内酯纤维基做对比。 Tan等[39]用静电纺丝技术制备了聚己内酯/明胶/聚乙烯醇多孔人工血管,并进行了肝素接枝改性。这种人工血管在植入小鼠体内8周后仍然具有良好生物相容性,无明显炎症反应、溃烂及肿胀发生,并且可见毛细血管黏附在血管表面,说明了这种多孔结构血管可促进内皮细胞化。 Xiang等[40-41]将聚己内酯/蛛丝蛋白/明胶混合液制备成静电纺管状支架,并检测了这种血管的机械性能及生物相容性。实验结果表明,这种复合管状材料孔隙率达到了(86.2±2.9)%,平均纤维直径(166±85) nm,亲水性能良好。与非静电纺聚己内酯管及聚己内酯/蛛丝蛋白管相比较,这种复合管状支架更有利于内皮细胞的黏附及增殖。 Fukunishi等[42]用聚己内酯和壳聚糖共混溶液通过静电纺丝制备组织工程血管,并评估了用这种快速降解材料制造小口径动脉组织工程血管的可行性。将1.0 mm 和5.0 mm的组织工程血管分别植入小鼠和绵羊体内6个月。结果表明,所有1.0 mm和5.0 mm组织工程血管均无血栓或动脉瘤形成,并且细胞外的沉积基质成分有弹性蛋白和胶原蛋白生成。 2.3.3 组织工程 组织工程作为一门组织和器官重建的新兴交叉学科,从再生角度为血管移植提供了新的途径。其方法是将血管种子细胞接种于天然或合成材料支架上,进而构建从形态到功能均与活体血管接近的组织工程化血管[43-47]。 Badhe等[48]将壳聚糖-明胶混合材料采用溶液浇铸法制备出一种可模拟人体血管结构的双层组织工程支架,其具有多孔的内层,孔径为100-230 μm,孔隙率约82%,细胞实验证明细胞可以在支架内生长与爬行,体外实验结果显示了该支架适合作为人工血管使用。 Aper等[49]利用高度压缩纤维蛋白基质制备了组织工程化血管,将该血管植入绵羊体内6个月取材检测,结果表明该组织工程血管与天然动脉血管结构高度相似。该技术可能成为构建最优人工血管移植物的有力手段。 目前学者们将静电纺丝技术、组织工程等多种手段相结合,希望可取得更大的进展。Augustine等[50]利用静电纺丝制备了具有增强细胞黏附性的聚偏氟乙烯-三氟乙烯/氧化锌纳米复合材料人工血管组织工程支架,并对其进行了血液相容性和细胞毒性实验,结果均显示其具有优异的生物相容性,细胞活力良好。将这种组织工程人工血管植入大鼠体内21 d后,切片显示材料无炎性和排异反应。Ahn等[51]用静电纺丝技术与组织工程技术制备小口径血管,通过适当的培养,将自体细胞与天然/合成的支架结合起来制备功能性血管并植入体内。结果表明,与传统的细胞接种方法相比,平滑肌细胞薄片能与静电纺丝血管支架结合产生更成熟的平滑肌层,有利于血管支架与血管细胞相结合。 Yazdanpanah等[52]利用静电纺丝技术制备了聚L-丙交酯/凝胶化管状支架,研究了4种纤维支架(梯度聚L-丙交酯/明胶,层状聚L-丙交酯/明胶,聚L-丙交酯和明胶支架)的可降解性、孔隙率、微孔尺寸和机械性能,结果表明,梯度聚L-丙交酯/明胶的机械强度和爆破压力显著增加。 "
| [1] 王维慈,欧阳晨曦,周飞,等.高分子材料小口径人工血管的相关研究[J].中国组织工程研究与临床康复, 2008,12(1):125-128.[2] 张家庆,王武军,闫玉生.小口径人工血管材料应用进展[J].实用医学杂志,2014,130(21):3520-3521.[3] Begovac PC,Thomson RC,Fisher JL,et al.Improvements in GORE-TEX1 vascular graft performance by Carmeda1 bioactive surface heparin immobilization.Eur J Vasc Endovasc Surg. 2003; 25:432-437.[4] McClurken ME,McHaney JM,Colone W.Physical Properties and Test Methods for Expanded Polytetra fluoroethylene (PTFE) Grafts.Vascular Graft Update: Safety and Performance.ASTM STP 898,1986.[5] Twine CP,McLain AD.Graft type for femoro-popliteal bypass surgery (review). Cochrane Database Syst Rev. 2010;5: CD001487.[6] Lösel-Sadée H,Alefelder C.Heparin-bonded expanded polytetrafluoroethylene graft for infragenicular bypass: five-year results.J Cardiovasc Surg.2009;50(3):339-343.[7] Kirkwood ML,Wang GJ,Jackson BM,et al.Lower limb revascularization for PAD using a heparin-coated PTFE conduit.Vasc Endovasc Surg.2011;45(4):329-334.[8] Pulli R,Dorigo W,Castelli P,et al.Propaten Italian Registry Group. Midterm results from a multicenter registry on the treatment of infrainguinal critical limb ischemia using a heparin- bonded ePTFE graft.J Vasc Surg. 2010;51(5):1167-1177.[9] 涂秋芬,张怡,陈槐卿,等.以脱细胞犬动脉为基质的血管支架体外再细胞化[J].航天医学与医学工程,2007,20(5):358-363.[10] 冉峰,刘长建,周敏,等.脱细胞支架复合兔骨髓间充质干细胞构建组织工程血管[J].中国组织工程研究与临床康复, 2009,13(47): 9226-9230.[11] 武欣,谷涌泉,段红永,等.利用脱细胞血管基质体外构建小口径组织工程血管[J].中国实验动物学报,2010,18(5):377-382.[12] Nagai N,Nakayama Y,Zhou YM,et al.Development of salmon collagen vascular graft: Mechanical and biological properties and preliminary implantation study.J Biomed Mater Res B Appl Biomater. 2008;87(2):432-439.[13] 虞希高.明胶基电纺小直径人造血管的制备及性能研究[D]. 杭州: 浙江大学, 2011.[14] 王叶香,闫星儒,王璐,等.人工血管用海藻酸钠-聚丙烯酰胺水凝胶的制备及性能[J].东华大学学报(自然科学版),2016,42(5):647-653.[15] 孔晓颖,韩宝芹,王海霞,等.可降解性壳聚糖基小口径人工血管的生物安全性[J].青岛大学医学院学报, 2012,48(4):334-336.[16] He C,Xu X,Zhang F,et al.Fabrication of fibrinogen/P (LLA‐CL) hybrid nanofibrous scaffold for potential soft tissue engineering applications.J Biomed Mater Res A. 2011,97(3):339-347.[17] 唐景梁,沈雳,吴轶喆,等.壳聚糖/肝素层层自组装涂层与CD133+内皮祖细胞生物相容性的实验研究[J].中国分子心脏病学杂志, 2009, 9(6):342-347.[18] Thein-Han WW,Misra RDK.Biomimetic chitosan– nanohydroxyapatite composite scaffolds for bone tissue engineering.Acta Biomaterialia.2009;5(4):1182-1197.[19] 刘涛.壳聚糖—硫酸化丝素蛋白小口径人工血管动物实验研究[D]. 北京: 首都医科大学,2016.[20] 湛权.涤纶人造血管材料表面改性及其性能研究[D].上海:东华大学, 2012.[21] 张明,刘长建,刘晨,等.膨体聚四氟乙烯人工血管表面肝素固化替代犬下腔静脉的表面抗凝血性能[J].中国组织工程研究与临床康复, 2011,15(47):8833-8836.[22] 周飞,徐卫林,欧阳晨曦,等.小口径微孔聚氨酯人造血管生物力学性能研究[J].医用生物力学,2008, 23(4):270-274.[23] Zheng W,Wang Z,Song L,et al.Endothelialization and patency of RGD-functionalized vascular grafts in a rabbit carotid artery model.Biomaterials.2012;33(10):2880.[24] Bastijanic JM,Kligman FL,Marchant RE,et al.Dual biofunctional polymer modifications to address endothelialization and smooth muscle cell integration of ePTFE vascular grafts.J Biomed Mater Res A. 2016;104(1):71-81.[25] Hoshi RA,Van Lith R,Jen MC,et al.The blood and vascular cell compatibility of heparin-modified ePTFE vascular grafts. Biomaterials.2013;34(1):30-41.[26] Khorasani MT,Shorgashti S.Fabrication of microporous thermoplastic polyurethane for use as small‐diameter vascular graft material. I. Phase-inversion method.J Biomed Mater Res B Appl Biomater. 2006;76(1):41-48.[27] Miyamoto K,Sugimoto T,Okada M,et al.Usefulness of polyurethane for small-caliber vascular prostheses in comparison with autologous vein graft.J Artif Organs. 2002;5(2):113-116.[28] Wang Z,Cui Y,Wang J,et al.The effect of thick fibers and large pores of electrospun poly (ε-caprolactone) vascular grafts on macrophage polarization and arterial regeneration.Biomaterials. 2014;35(22):5700-5710.[29] Aldenhoff YB,van Der Veen FH,ter Woorst J,et al.Performance of a polyurethane vascular prosthesis carrying a dipyridamole (Persantin®) coating on its lumenal surface.J Biomed Mater Res. 2001;54(2):224-233.[30] Zhang K,Liu T,Li JA,et al.Surface modification of implanted cardiovascular metal stents: from antithrombosis and antirestenosis to endothelialization.J Biomed Mater Res A. 2014;102(2):588-609. [31] Natterodt JC,Petri-Fink A,Weder C,et al.Cellulose Nanocrystals: Surface Modification, Applications and Opportunities at Interfaces.Chimia(Aarau). 2017;71(6):376-383. [32] Liu T,Hu Y,Tan J,et al.Surface biomimetic modification with laminin-loaded heparin/poly-l-lysine nanoparticles for improving the biocompatibility.Mater Sci Eng C. 2017;71:929-936.[33] Tang C,Kligman F,Larsen CC,et al.Platelet and endothelial adhesion on fluorosurfactant polymers designed for vascular graft modification.J Biomed Mater Res A.2009;88(2):348-358.[34] Walluscheck KP,Steinhoff G,Kelm S,et al.Improved endothelial cell attachment on ePTFE vascular grafts pretreated with synthetic RGD-containing peptides.Eur J Vasc Endovasc Surg. 1996;12(3): 321-330.[35] Liu T,Liu Y,Chen Y,et al,Immobilization of heparin/ poly-L-lysine nanoparticles on dopamine-coated surface to create a heparin density gradient for selective direction of platelet and vascular cells behavior.Acta Biomaterialia.2014;10:1940-1954.[36] Catto V,Fare S,Cattaneo I,et al.Small diameter electrospun silk fibroin vascular grafts: Mechanical properties, in vitro biodegradability, and in vivo biocompatibility.Mater Sci Eng C Mater Biol Appl.2015; 54:101-111. [37] Yin A,Luo R,Li J,et al.Coaxial electrospinning multicomponent functional controlled-release vascular graft: Optimization of graft properties.Colloids Surf B Biointerfaces.2017;152:432-439. [38] Zhang YZ,Venugopal J,Huang ZM,et al.Characterization of the surface biocompatibility of the electrospun PCL-collagen nanofibers using fibroblasts.Biomacromolecules. 2005;6(5):2583.[39] Tan Z,Wang H,Gao X,et al.Composite vascular grafts with high cell infiltration by co-electrospinning.Mater Sci Eng C Mater Biol Appl.2016;67:369-377. [40] Ping X,Min L,Chaoying Z,et al.Cytocompatibility of electrospun nanofiber tubular scaffolds for small diameter.Int J Biol Macromol. 2011;49:281-288.[41] Xiang P,Wang SS,He M,et al.The in vitro and in vivo biocompatibility evaluation of electrospun recombinant spider silk protein/PCL/gelatin for small caliber vascular tissue engineering scaffolds.Colloids Surf B Biointerfaces. 2018;163:19-28.[42] Fukunishi T,Best CA,Sugiura T,et al.Tissue-engineered small diameter arterial vascular grafts from cell-free nanofiber PCL/chitosan scaffolds in a sheep model.PloS One. 2016;11(7): e0158555.[43] Sankaran KK,Subramanian A,Krishnan UM,et al. Nanoarchitecture of scaffolds and endothelial cells in engineering small diameter vascular grafts.Biotechnol J. 2015;10(1):96-108.[44] Wilhelmi M,Jockenhoevel S,Mela P.Bioartificial fabrication of regenerating blood vessel substitutes: Requirements and current strategies.Biomed Tech (Berl).2014;59(3):185-195. [45] Benrashid E,McCoy CC,Youngwirth LM,et al.Tissue engineered vascular grafts: Origins, development, and current strategies for clinical application.Methods.2016;99:13-19.[46] Drews JD,Miyachi H,Shinoka T.Tissue-engineered vascular grafts for congenital cardiac disease: Clinical experience and current status.Trends Cardiovasc Med.2017;27(8):521-531.[47] Nieponice A,Soletti L,Guan J,et al.Development of a tissue-engineered vascular graft combining a biodegradable scaffold, muscle-derived stem cells and a rotational vacuum seeding technique. Biomaterials.2008;29(7):825-833.[48] Badhe RV,Bijukumar D,Chejara DR,et al.A composite chitosan- gelatin bio-layered, biomimetic macroporous scaffold for blood vessel tissue engineering.Carbohydr Polym. 2017;157:1215-1225. [49] Aper T,Wilhelmi M,Gebhardt C,et al.Novel method for the generation of tissue-engineered vascular grafts based on a highly compacted fibrin matrix.Acta Biomaterialia. 2016;29:21-32. [50] Augustine R,Dan P,Sosnik A,et al.Electrospun poly (vinylidene fluoride -trifluoroethylene)/zinc oxide nanocomposite tissue engineering scaffolds with enhanced cell adhesion and blood vessel formation. Nano Res. 2017;10(10):3358-3376. [51] Ahn H,Ju YM,Takahashi H,et al.Engineered small diameter vascular grafts by combining cell sheet engineering and electrospinning technology.Acta Biomaterialia.2015;16:14-22.[52] Yazdanpanah A,Tahmasbi M,Amoabediny G,et al.Fabrication and characterization of electrospun poly-L-lactide/gelatin graded tubular scaffolds: Toward a new design for performance enhancement in vascular tissue engineering. Prog Nat Sci Mater Int.2015;25(5):405-413. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||