Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (11): 1768-1773.doi: 10.3969/j.issn.2095-4344.0177
Previous Articles Next Articles
Application prospect and value of finite element modeling in lumbar spondylolysis
Xu Ze-chuan, Wei Bing, Yang Hong-sheng, Cao Zong-rui, Yan Xiao-hu, Li Yu-gang, Chang Shan
- Department of Spine Surgery, First Affiliated Hospital, Chengdu Medical College, Chengdu 610500, Sichuan Province, China
-
Online:2018-04-18Published:2018-04-18 -
Contact:Chang Shan, Master, Chief physician, Professor, Department of Spine Surgery, First Affiliated Hospital, Chengdu Medical College, Chengdu 610500, Sichuan Province, China -
About author:Xu Ze-chuan, Master candidate, Department of Spine Surgery, First Affiliated Hospital, Chengdu Medical College, Chengdu 610500, Sichuan Province, China
CLC Number:
Cite this article
Xu Ze-chuan, Wei Bing, Yang Hong-sheng, Cao Zong-rui, Yan Xiao-hu, Li Yu-gang, Chang Shan. Application prospect and value of finite element modeling in lumbar spondylolysis[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(11): 1768-1773.
share this article

2.1 有限元模型在研究脊柱疾病的发展过程 20世纪50年代,有限元方法首先用于分析飞机力学问题[1],随着医学领域对有限元方法认识,有限元模型的建立经历了两个重要的阶段:早期有限元模型基本完全按照理工科方法重建,建模方法采用图形绘制结合骨科理论参数的方法建立有限元模型;随着计算机仿真技术的发展,建模技术手段日益丰富,有限元模型由早期的图形描绘发展到目前根据CT原始数据直接重建阶段,使有限元模型数据来源更加真实,突出医学研究的个体差异性,使有限元分析结果更加准确。有限元在医学领域研究开始于20世纪60年代,该方法首先用于解决血管流体力学问题。1974年Belytschko等[2]首先在脊柱研究领域内提出有限元方法,并迅速在骨科领域得到发展,1975年Liu等[3]建立了脊柱有限元模型,但未对髓核纤维环等结构单独构建,影响了实验结果的准确性。当研究学者认识到椎间盘纤维环、髓核等组织结构在脊柱生物力学中的作用,开始对椎间缓冲结构进行更加完善的研究,Lin等[4]在20世纪70年代完善了髓核及纤维环的构建、赋值,但缺少对脊柱附件的力学分析。结合Holdsworth于1963年提出后方韧带复合体概念,Hakim等[5]开始认识分析脊柱后方韧带的生物力学效应,在Lin的基础上完善了棘间韧带、棘上韧带等脊柱附件结构的重建,提高模型仿真度,1983年Dennis年提出脊柱三柱原理,对脊柱的力学进行了划分,通过有限元脊柱模型客观反映出脊柱力学分布,使脊柱力学研究更加准确。1988年Goel等[6]首次根据CT原始数据,完成了对脊柱传统模型构建的突破,由原来工科物理参数建模转变为医学原始CT数据建模,让有限元发展真正进入到医疗仿真模拟时代,使医学生物力学分析可行性、真实性由量变到质变质的飞跃,让有限元分析的准确性达到更高的水平。同时Goel根据不同的解剖结构赋予相应的材料属性,让模型力学分析结果更为准确。2006年Rohlmann等[7]结合脊柱解剖层次结构,为提高模型仿真度,在骨性模型上增加了肌肉模型,进一步完成了对脊柱附属结构的完善。随着脊柱有限元分析的完善,有限元开始对脊柱相关疾病进行分析。20世纪90年代,国内戴力扬[8]建立了腰椎活动节段、椎弓根峡部裂模型。2010年顾晓民[9]建立了腰椎峡部裂有限元模型,并对有限元模型进行体外实验进行验证,证明了模型的有效性。 2.2 腰椎峡部裂有限元模型的建立及其验证 2.2.1 腰椎峡部裂有限元模型的建立 从19世纪50年代,医学上开始对腰椎峡部裂进行分析[10],随着医学进展,学者们认识到腰椎峡部裂(lumbar spondylolysis)的解剖学基础是腰椎峡部骨质缺损不连续,且大多发生于儿童及青少年时期,一般无症状,但部分患者也可有剧烈下腰痛,是引起儿童及青少年腰痛症状的常见原因,青少年发病率为 3%-7%[11],体育运动员高发,峡部裂有20%-30%出现椎体滑脱[12],成为峡部裂滑脱症。 目前主要有两种腰椎峡部裂有限元建模方法被研究者所认可。第一种由Rnau等[13]首先建立,其方法是建立完整的脊柱有限元模型,并在其基础上建立病理模型,材料属性参考以往经典数据,最后得到椎体峡部裂模型,分析实验结果,大量后续研究证实该方法可行性较好。第二种是直接采用腰椎峡部裂患者原始数据[8,14],将薄层CT扫描所得全部DICOM图像导入建模软件中,利用腰椎水平位、冠状位、矢状位的横断图像,对模型进行重建,其模型的材料赋值与几何形态更接近真实病理类型。后者避免了Rnau等[13]的建模方法无法真实反映峡部裂椎体退变(如骨质疏松、退变增生)的弊端。作者认为,第一种建模方法能够在正常模型的基础上建立研究者需要的病例模型,使模型具有可靠性与实用性,更适用于临床少见多节段的峡部裂病例类型的研究。而第二种方案更接近于实际情况,对CT值赋值方法具有优势,对粗糙的模型(如增生的骨赘)进行光顺,使模型更加规整。但以上建模方法均需与后期体外实验进行准确对比分析。 2.2.2 模型有效性验证 人们认识到有限元法是一种力学分析的近似求解方法,因此,实验模型的验证是有限元可行性分析的重要环节。对于有限元模型的验证,目前大多数学者采用两种方法(体外实验、经典文献验证):目前骨科常用的体外力学测量方法有光弹法、电测法(应变片法)、全息光弹法等[15-17],杨振武等[17]利用光弹法通过分析骨表面光学条纹图像,对腰椎峡部进行应力分析,得出光弹法能直观的反映应力分布,但受模型自身结构参数及分析误差的影响,实验结果的准确性仍有待提高。此外,田勇等[18]利用电测法对猪的峡部进行应变量分析,得到脊柱不同活动(前屈、后伸、侧弯等)状态应变量数据,并得出后仰合并侧弯与侧弯这两种情况应变量变化明显,认为以上两种运动情况是脊柱峡部裂和滑脱研究的重要运动状态。顾晓民等[8、14]采用电测法对尸体腰椎峡部裂进行大量的研究,通过贴附于脊柱的应变片(具有电阻转换性),让电量变化来反映应力变化的情况,通过体外实验与有限元模型对比分析并且证实,有限元方法读取结果为节点应力值,体外生物力学测量结果为应变值,两者测量结果无法直接比较。因此,目前大多学者认为,通过应变(位移)或应力的趋势进行有效性验证,能提高建模的可行性和有效性[19-20]。电测法在动物实验与实体实验的应变量趋势结果与脊柱峡部裂在不同运动状态下经典理论结果相符,证实电测法对于脊柱峡部裂有限元模型的力学验证具有可行性。全息光弹技术在体外应力分析研究具有实验数据准确,分析结果可靠等特点,目前在理工科方面应力分析方面的应用较多,随着生物力学的研究发展,全息光弹法对微应变以及脊柱ROM值(脊柱活动度)能进行较好分析[15];另一种方法则是通过经典文献数据重复结果,朱立新[21]采用了以往文献中相同约束条件和力学加载,最终模型实验结果与文献中的经典数据结果进行对比,得到相似结果,同样验证了有限元模型的有效性。但是,鉴于体外实验的仪器及实体模型来源相对困难,目前多数学者主要根据与以往经典文献数据结果对比的方法来验证有限元模型,见表1。"

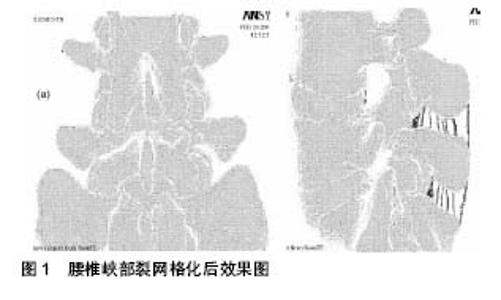
2.3 腰椎峡部裂有限元模型的研究热点 2.3.1 腰椎峡部裂病理模型的研究 脊柱承载了人体质量的2/3,而腰椎是脊柱的主要力学承载结构,因腰椎峡部裂患者低龄化的发病特点,会使腰椎过早的出现力学不平衡,从而腰椎滑脱、椎间盘退变、椎管狭窄症等的发生率明显增加,尤其是对椎间盘、终板、小关节突的应力有明显影响。朱高明等[22]采用动物实验对猪的L4单、双侧峡部裂模型进行分析研究,得出L4单侧峡部裂比双侧峡部裂对下位椎间盘、关节突的应力影响小,通过动物实验反映了脊柱峡部裂对椎间盘、关节突影响。人体实验对峡部裂椎间盘退变的研究,绝大多数都根据研究对象MRI检查,通过对T2像椎间盘信号强度来反映椎间盘退变情况。1987年Schneiderman根据椎间盘信号强度将退变椎间分为3级。2001年Pfirrmann在Schneiderman等的研究基础上将椎间盘分为5级,虽然Pfirrmann提出的分级相对于Schneiderman更加细化,但是其本质都是根据T2像上椎间盘信号强度定性的对退变椎间盘进行分析。而有限元方法通过对峡部裂椎间盘的网格化,定量的对椎间盘进行力学分析,使得峡部裂椎间盘退变的研究结果更加准确(图1)。顾晓明等[14、19-20]建立的腰椎峡部裂模型得出在前屈、后伸、旋转等状态下脊柱的稳定性比正常状态明显下降,刘瀚忠[23]建立的L5椎体双侧峡部裂模型,得出病椎临近椎间盘的纤维环、髓核压力增大,以下位椎间盘增大更为明显。这样分析结果对脊柱外科医生在手术方式的选择及手术中处理带来较大帮助。这样就能研究者对峡部裂病理状态下腰椎关节突及椎间缓冲结构(椎间盘、终板等)认识更加深入。此外,有关正常腰椎模型的峡部的应力分析研究也更加清晰,苏再发[24]通过建立腰椎三维有限元模型,得出峡部应力逐节段增加,L5应力集中明显,椎弓峡部在前屈、后伸位均出现明显的应力集中,其中后伸位时应力值最大,认为后伸与椎弓峡部裂的发生关系最为密切,分析结果使得腰椎峡部的受力机制、好发部位同流行病学一致,让腰椎峡部裂研究分析更加严谨与完整,同时,对峡部裂患者功能锻炼也提出了科学的指导方案。若未来能更加准确的模拟椎间盘组织,通过应力分析得出一个促使髓核细胞退变的应力值,就能使椎间盘退变的力学机制发展到更高的水平。 2.3.2 腰椎峡部裂手术以及内固定器械力学分析 由于峡部发病流行病学特点,好发人群主要为青少年,因此,峡部裂治疗方案的选择存在争议,有学者认为通过保守治疗,能较好的保留脊柱活动度,对临近节段的影响较小,同时通过外支具的保护及药物的治疗,能明显缓解症状[25]。Kurd等[26]得出,低龄的峡部裂患者通过外支具保护及3个月物理治疗,症状(疼痛)缓解有效率能够达到95%。但Lundin等[27]认为保守治疗症状缓解情况虽然良好,但骨性融合率低。研究发现腰椎峡部在腰椎活动中具有抗剪切力作用,当出现腰椎峡部裂后,腰椎整体受力出现失稳,由于峡部裂存在解剖学上缺损,使得整个椎体峡部后方的骨性结构(下关节突、棘突、椎板)与前方椎体分离,并在肌肉软组织的牵拉下处于异常活动状态,特别是腰椎在后伸时,椎体向前剪切力加大,增加椎体前滑的趋势,如果无良好的稳定内固定,椎体将出现滑脱症状,最终将表现出椎管狭窄等症状。因此,手术治疗峡部裂是目前大多数学者推崇的治疗方案,对于峡部裂的治疗目前临床大多采用内固定加峡部植骨融合手术方式,但随着大量术后随访,临床医生发现在内固定周围出现了应力遮挡等情况,使的内固定周围出现骨质疏松、吸收、溶解等改变,这使得内固定失败率的风险明显增加,同时由于应力遮挡,使得临近椎体活动度加大,加速了临近节段椎间盘的退变,使得邻椎病的发生率增加,让内固定手术的治疗效果受到一定影响,如何选择一种合适的内固定及手术方式,是目前临床医生急需解决的一个难题。 目前,鉴于内固定器械的更新及手术方式进展,内固定器械因其不同弹性模量及力学稳定效果对腰椎自身力学结构都会产生影响。这使得临床医生对腰椎峡部裂内固定器械及手术方式选择需要更充分的力学分析及验证,选择更加符合腰椎正常力学稳定性的方案,减少因腰椎力学改变而带来的并发症。而有限元方法能很好的模拟不同手术方式及内固定装置,并对其进行应力分析,得出一个相对更加合理的治疗方案。目前,峡部裂手术主要分为3类:病椎单纯植骨融合术、单病椎内固定手术、单节段内固定手术。但由于病椎单纯植骨融合术利用有限元分析,在仿真模拟条件下,误差相对较大,目前研究较少,对于该方法的研究大多通过患者后期症状随访及影像学表现来评估其效果,而针对单病椎、单节段内固定的仿真研究,模拟条件影响较小,具有很好研究价值。顾晓明[28]分别对L4双侧峡部裂单椎节、单节段2种手术方式建模,得出单椎节峡部裂固定系统不仅能提供有效固定,且对临近节段椎间盘、终板影响较小,对减缓椎间盘退变、减少终板炎的发生提供了理论依据。同时,由于峡部裂患者大多数合并腰椎滑脱,手术方式有多种选择。车纯庆[29]针对L5峡部裂性滑脱分别采用后外侧融合及经后路椎间融合手术,发现螺钉尾部都出现应力集中,具有较大断钉风险。因此对于峡部裂滑脱的患者,病椎融合率需要提出了更高的要求,同时,对于后期患者随访中,医生评估内固定失败的风险有了更明确的关注点。峡部裂内固定选择的多样性,促使了更多的研究者对于新型内固定的研发,于博[30]在建立的峡部裂模型基础上,对比分析了U型内固定与常规内固定,得出U型内固定应力分布均匀,断钉风险降低;朱立新[21]研究峡部裂机翼型固定模型,发现侧翼、底座的连接处在后伸和旋转时应力集中明显,容易发生内固定断裂。周初松[31]运用翼状记忆合金固定峡部裂,得出翼状内固定能较好地恢复脊柱稳定性,且未出现明显集中。目前针对腰椎峡部裂新型内固定的研发是较为新兴的热点,结合患者低龄发病等特点,研发更加接近正常生物力学的内固定,尽力避免内固定装置以及腰椎正常结构的应力集中,降低内固定的失败率,延缓邻椎病以及椎间盘加速退变等并发症的发生,是未来需要努力的方向。 "
| [1] Baruch M,Bar Itzhack IY. Optimal weighted orthog-onalization of measured modes. AIAA J. 1979;17(8): 927-928.[2] Belytschko T, Kulak RF,Schultz AB, et al. Finite element stress analysis of an intervertebral disc. J Biomech.1974;7(3): 277-285.[3] Liu YK, Ray G, Hirsch C. The resistance of the lumbar spine to direct shear. Orthop Clin North Am.1975;6(1): 33-49.[4] Lin HS, Liu YK, Adams KH. Mechanical response of the lumbar intervertebral joint under physiological (complex) loading. J Bone Joint Surg Am.1978;60(1):41-55.[5] Hakim NS, King AI. A three dimensional finite element dynamic response analysis of a vertebra with experimental verification. J Biomech. 1979;12(4):277-292.[6] Goel VK, Kim YE, Lim TH, et al.An analytical investigation of the mechanics of spinal instrumentation. Spine. 1988;13(9): 1003-1011.[7] Rohlmann A, Bauer L, Zander T, et al. Determination of trunk muscle forces for flexion and extension by using a validated finite element model of the lumbar spine and measured in vivo data. J Biomech. 2006;39(6): 981-989.[8] 戴力扬.腰椎椎弓峡部裂的生物力学研究[J].中国运动医学杂志, 1990,11(2):67-68.[9] 顾晓民.腰椎椎弓峡部裂三维有限元模型的建立与验证[J].医用生物力学,2010,10(1):45-50.[10] Lamble DZ.Thesen uber Spondylolisthesis. Zbl gynak Urol. 1855;9:250.[11] Lundin DA,Wiseman D,Ellenbogen RG,et al. Direct repair of the pars interarticularis for spondylolysis and spondylolisthesis. Pediatr Neurosurg. 2003;39 (4):195-200. [12] 孙广林,孙义清,吴玉琳,等.后天性腰椎峡部不连发生机制的解剖学分析[J].中国临床解剖学杂志,1994,12(1):21-23.[13] Ranu HS.Three dimensional surgical simulations of the spine. J Biomech Eng.1982;4(4):285-288.[14] 顾晓民,贾连顺,陈雄生,等.腰椎椎弓峡部裂单椎节经椎弓根钉棒固定体外生物力学研究[J].中华实验外科杂志,2009,26(6): 718-720. [15] Vishteh AG,Crawford NR,Chamberlain RH,et al. Biomechanical comparison of anterior versus posterior lunmbar threaded interbody fusion cages.Spine. 2005;30(3): 302-310.[16] Cripton PA,Jain JM,Wittenberg RH,et al.Load-sharing characteristics of stabilized lumbar spine segments.Spine. 2000;25(2):170-179.[17] 杨振武,高瑞亭.运动员腰椎峡部骨折的生物力学研究[J].中国运动医学杂志,1997,6(16):299-302.[18] 田勇,刘成.弯曲力矩对脊柱峡部裂的影响的生物力学分析[J]. 生物骨科材料与临床研究,2015,7(6):15-19.[19] Wong C,Gehrchen PM,Darvann T,et al. Nonlinearfinite-element analysis and biomechanical evaluation of the lumbar spine. IEEE Trans Med Imaging. 2003;22(6):742-746. [20] 唐小君,刘耀升,陈其昕,等.基于CAD技术的个体化退变腰椎有限元模型库的建立[J].国际生物医学工程杂志,2007,30(2):65-69.[21] 朱立新.腰椎峡部裂机翼型记忆合金固定装置的有限元分析[J].中国临床解剖学杂志,2012,30(3):333-336.[22] 朱高明.腰椎峡部裂后相应关节突关节生物力学变化研究[J].海南医学,2010,21(16):42-44. [23] 刘瀚忠.L5峡部裂对脊柱生物力学的有限元分析[D].汕头大学, 2011.[24] 苏再发.腰椎椎弓根峡部裂的应力分析[J].中国矫形外科杂志, 2006,14(15):1169-1171.[25] Lim MR. Symptomatic spondylolysis:diagnosis and treatment. Curr Opin Pediatr. 2004;16(1):37- 46.[26] Kurd MF, Patel D, Norton R, et al. Nonoperative treatment of symptomatic spondylolysis.J Spinal Disord Tech. 2007;20: 560- 564.[27] Lundin DA,Wiseman D,Ellenbogen RG,et al. Direct repair of the pars interarticularisfor spondylolysis and spondylolisthesis. Pediatr Neurosurg. 2003;39 (4):195-200. [28] 顾晓明.单椎节与单节段内固定治疗腰椎椎弓峡部裂的有限元分析[J].医用生物力学, 2011,12(1):65-68.[29] 车纯庆.骶骨倾斜角对 L5峡部裂性滑脱不同手术方式后螺钉应力影响的有限元分析[D].苏州大学,2015.[30] 于博.腰椎弹性内固定系统的设计与力学研究[D].南方医科大学,2009.[31] 周初松.腰椎峡部裂翼状记忆合金节段内固定器的研制[J].中国脊柱外科杂志,2006,9(1):33-37.[32] 关海山,杨惠林,冯皓宇.有限元分析肌肉力对胸腰椎运动节段椎间盘压力的影响[J].苏州大学学报(医学版),2007,27(2):209-213, 221.[33] 刘雷,沈根标.胸腰椎脊柱损伤的生物力学及有限元分析[J].实用骨科杂志,2001,7(5):354-357.[34] Rohlmann A, Bauer L, Zander T, et al. Determination of trunk muscle forces for flexion and extensionby using a validated finite element model of the lumbar spine and measured in vivo data. J Biomech. 2006;39(6):981-989.[35] Wagnac E, Arnoux PJ, Garo A, et al. Finite element analysis of the influence of loading rate on a model of the full lumbar spine under dynamic loading conditions. Med Biol Eng Comput. 2012;50(9):903-915. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Chen Xinmin, Li Wenbiao, Xiong Kaikai, Xiong Xiaoyan, Zheng Liqin, Li Musheng, Zheng Yongze, Lin Ziling. Type A3.3 femoral intertrochanteric fracture with augmented proximal femoral nail anti-rotation in the elderly: finite element analysis of the optimal amount of bone cement [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1404-1409. |
| [3] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [4] | Cai Qunbin, Zou Xia, Hu Jiantao, Chen Xinmin, Zheng Liqin, Huang Peizhen, Lin Ziling, Jiang Ziwei. Relationship between tip-apex distance and stability of intertrochanteric femoral fractures with proximal femoral anti-rotation nail: a finite element analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 831-836. |
| [5] | Song Chengjie, Chang Hengrui, Shi Mingxin, Meng Xianzhong. Research progress in biomechanical stability of lateral lumbar interbody fusion [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 923-928. |
| [6] | Liu Zhao, Xu Xilin, Shen Yiwei, Zhang Xiaofeng, Lü Hang, Zhao Jun, Wang Zhengchun, Liu Xuzhuo, Wang Haitao. Guiding role and prospect of staging and classification combined collapse prediction method for osteonecrosis of femoral head [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 929-934. |
| [7] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [8] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [9] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [10] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [11] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [12] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [13] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [14] | Chen Lu, Zhang Jianguang, Deng Changgong, Yan Caiping, Zhang Wei, Zhang Yuan. Finite element analysis of locking screw assisted acetabular cup fixation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 356-361. |
| [15] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||