Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (36): 6533-6540.doi: 10.3969/j.issn.2095-4344.2013.36.024
Insight into induced pluripotent stem cells in retinal diseases
Deng Jun, Chen Xiao, Yan Ying, Zhou He-zheng
- Wuhan General Hospital of Guangzhou Military Region, Wuhan 430070, Hubei Province, China
-
Received:2013-01-18Revised:2013-03-29Online:2013-09-03Published:2013-09-03 -
Contact:Chen Xiao, M.D., Associate chief physician, Wuhan General Hospital of Guangzhou Military Region, Wuhan 430070, Hubei Province, China chenxiao1972@sohu.com -
About author:Deng Jun★, Studying for master’s degree, Wuhan General Hospital of Guangzhou Military Region, Wuhan 430070, Hubei Province, China 407365113@qq.com
CLC Number:
Cite this article
Deng Jun, Chen Xiao, Yan Ying, Zhou He-zheng. Insight into induced pluripotent stem cells in retinal diseases[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(36): 6533-6540.
share this article
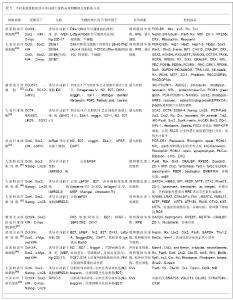
2.1 诱导多功能干细胞的起源和研究进展 2006年,最初由Takahashi和Yamanaka等[1]利用反转录病毒载体导入4种基因Oct4、Sox2、C-Mye和Klf4,将小鼠成纤维细胞重编程为一种类似胚胎干细胞具有多潜能分化能力的干细胞,即诱导多功能干细胞。2007年,他们又成功地将人皮肤成纤维细胞重编程,诱导出人源性诱导多功能干细胞[2]。与此同时,Liang等[4]利用慢病毒作为载体导入Oct4、Sox2、Nanog和Lin28也成功地将人的体细胞诱导成为诱导多功能干细胞。从此拉开了诱导多功能干细胞研究的序幕。 2.1.1 诱导多功能干细胞来源的多样化 Park等[5-6]可以将胚胎、新生儿和成人的体细胞诱导为诱导多功能干细胞,并还从遗传病患者的成纤维细胞中诱导得到了疾病特异性诱导多功能干细胞。此外,诱导多功能干细胞还可以从各个胚层来源的成熟体细胞中所诱导得到,如肝细胞、成熟的B淋巴细胞、神经干细胞和血细胞等[7-10]。因此,诱导多功能干细胞的细胞来源十分广泛。 2.1.2 载体及导入技术的多样化 通常诱导多功能干细胞是经过病毒载体转入重排因子生成的,由于病毒是随机、永久地整合到基因中,可能引起插入位点的突变。因此,很多学者研究尝试用其他相对安全的载体来代替病毒载体,如质粒、piggyBac转座子、重组蛋白[11-12]。一般是向体细胞中导入4个重排因子- Oct4、Sox2、c-Myc和Klf4诱导体细胞为诱导多功能干细胞,Myc主要是参与调节细胞增殖、代谢、生物合成途径,它的转录可以提高重排的效率,但不是必需的,而且MYC和肿瘤的形成存在密切关系。因此,有研究用通过Nanog代替Mye也能重编程体细胞,更有甚者,用Oct4、Klf4或只是Oct4联合小分子也能成功获得诱导多功能干细胞[13]。通过改进载体的导入技术也可以降低突变风险,如切除cre-重组酶系统将基因转入成体细胞至转化为诱导多功能干细胞后,再运用ere-酶将病毒载体切除[14]。此外还可用病毒表达一个包含4个多潜能基因的干细胞盒,再结合基因标靶技术,使基因插入已定义的位置,避免其随机插入宿主DNA带来的潜在致癌性[15]。但是这些方式不足之处在于转化率很低,在保证安全的前提下,如何提高效率有待进一步探索。 2.1.3 提高重编程的效率 细胞凋亡、衰老、细胞周期阻滞阻碍重排,沉默主要调节这些反应的基因如p53、p21,或者促进细胞周期循环可以提高诱导多功能干细胞生成的效率及动力[16-17]。研究表明在重排过程中间质细胞如成纤维细胞需要经历一个间质细胞上皮转化态(MET)的过程[18],通过增强促进间质细胞上皮转化态的信号通路如骨形态发生蛋白,或者抑制阻碍间质细胞上皮转化态的信号通路转化生长因子β可以提高重排的效率[19]。染色体的状态也和重排密切相关。体细胞和pre-诱导多功能干细胞中多潜能性相关基因的调节区域,存在高度的甲基化,没有组蛋白标志(H3K4me3)。染色体的这种抑制状态阻碍重排因子的绑定及转录,是诱导重排的主要障碍。在重排的早期,这些区域需要去甲基化并且获得组蛋白标志,这种组蛋白修饰决定了重排因子转录的激活[20]。通过调节BNF复合物组件的高表达,增强其对染色体修饰作用,促进Oct4绑定,可以很大程度地提高重排效率[21]。此外由于Nanog具有协同基因去甲基化作用,通过增强它的表达也可以提高重排的效率[22]。 2.2 诱导多功能干细胞在视网膜疾病中的应用 2.2.1 诱导多功能干细胞诱导分化为感光细胞 在诱导多功能干细胞诞生以前,已有学者将胚胎干细胞在体外成功诱导分化为感光细胞。2009年Hirami等[23]将同样方法首次运用于鼠和人成纤维细胞来源的诱导多功能干细胞,成功诱导出感光细胞。先在SFEB培养模式下联合胚胎干细胞定向分化培养基(含有KSR、巯基乙醇)诱导诱导多功能干细胞向神经样细胞分化,再加入Wnt信号通路抑制剂DKK-1和Nodal通路抑制剂Lefty-A,诱导分化为视网膜前体细胞,再将视网膜前体细胞在的RA/T培养基(含有视黄酸和牛磺酸中)中诱导细胞分化为感光细胞,鼠诱导多功能干细胞在在分化9 d,表达神经细胞标志物nestin、βIII-tubulin,45 d时可检测到表达感光细胞前体标志物-Crx,以及成熟感光细胞标志物-恢复蛋白和视紫红质。DKK1和Lefty A等重组蛋白来自于动物细胞或大肠杆菌,为了避免其在细胞移植时带来物种间污染的问题,Osakada等[24]用小分子化学化合物CKI-7和SB-431542代替DKK1和Lefty A在Wnt和Nodal信号通路抑制作用,同样可以将诱导多功能干细胞诱导分化感光细胞。这样无血清、无异种蛋白的培养条件,不仅能减少将来细胞移植带来的生物污染问题,而且更利于用诱导多功能干细胞运用于疾病的模型或药物筛选等研究。接着,有学者对诱导多功能干细胞源性感光细胞的功能及体内移植做了进一步的研究。Tucker等[25]将小鼠表皮成纤维细胞诱导成诱导多功能干细胞,分化为光感受器前体细胞。并在分化的 21 d,他用免疫磁珠技术去除了表达SSEA的细胞,这些细胞未完全分化,具有多潜能性存在致瘤风险。诱导多功能干细胞分化33 d后,产生了视网膜前体细胞、光感受器前体细胞、成熟的光感受器细胞等细胞,这些细胞对谷氨酸刺激有反应,具有正常视网膜细胞的生理学特点。将这些细胞群移植到视网膜变性小鼠的视网膜下28 d后,即在外核层分化为成熟的视锥、视杆细胞,并且与宿主细胞形成新的突触联系整合到视网膜中。通过ERG及功能性解剖分析证实接受移植小鼠的视功能得到了部分恢复。Lamba等[26]将将人的成纤维细胞诱导多功能干细胞体外培养向光感受器细胞分化,用维生素A类结合蛋白为启动子表达绿色荧光蛋白的慢病毒转染细胞,采用流式细胞仪分选后,100%的表达绿色荧光蛋白的细胞同时表达CRX,大部分细胞同时表达NRL,AIPL1,rhodopsin。这提示们可以用维生素A结合蛋白作为标志物,用流式细胞筛选可以获得纯化的光感受器细胞。并将细胞移植到正常小鼠视网膜中,移植的光感受器细胞可以整合到视网膜中的外核层,表达光感受器标志物Otx2,recoverin及rhodopsin。这些研究均说明,诱导多功能干细胞可以为光感受器细胞的移植提供可用资源,使视网膜功能得到部分的恢复。Zhou等[27]诱导猪的诱导多功能干细胞分化为视杆细胞,移植到视杆细胞缺失的猪视网膜下,3个星期后,外核层出现诱导多功能干细胞来源的视杆细胞。这些研究均说明,诱导多功能干细胞可以为光感受器细胞的移植提供可用资源,使视网膜功能得到部分的恢复。 此外,还能利用患者体细胞来源的诱导多功能干细胞分化为光感受器细胞阐明疾病的发病机制和筛选特异性的药物。Tucker等[28]先通过外显子测序筛选出因纯合子Alu在男性生殖细胞相关激酶(male germ cellassociated Kinase,MAK)的外显子9插入而致病的视网膜色素变性患者。然后将这类MAK-视网膜色素变性患者、与男性生殖细胞相关激酶不相关的视网膜色素变性患者和正常人的皮肤成纤维细胞来源的诱导多功能干细胞诱导分化为感光细胞。通过对各组感光细胞研究结果表明,男性生殖细胞相关激酶-视网膜色素变性组不表达外显子9,各组表达的男性生殖细胞相关激酶大小不一样。正常视网膜细胞表达只有一种98 ku男性生殖细胞相关激酶,男性生殖细胞相关激酶-视网膜色素变性组为58 ku,视网膜色素变性对照组为两种都有。这提示Alu插入影响正确外显子9的正确拼接从而导致不能产生正常MAK可能这类患者致病原因。Jin等[29]分别取5名因不同基因突变而致病的视网膜色素变性患者皮肤成纤维细胞诱导为诱导多功能干细胞,即K11(视网膜色素变性9)-、K10(视网膜色素变性9)-、K21(视网膜色素变性1) -、P101(P视网膜色素变性H2)-、P59(RHO)- 诱导多功能干细胞,再分化得到的感光细胞。研究发现视网膜色素变性9-诱导多功能干细胞(K10和K11)分化为视杆细胞过程中表达氧化应激标志物。而在RHO-诱导多功能干细胞源性的视杆细胞中,视紫红质蛋白表达在细胞质中,不在正常的位置细胞膜上,并且该细胞表达内质网应激标志物。上述表现在正常人或其他类型的基因突变患者来源的诱导多功能干细胞不存在。用维生素E、维生素C和胡萝卜素这3种抗氧化药物作用不同类型的诱导多功能干细胞源性感光细胞,结果提示只有维生素E有显著的保护效果,并只限于视网膜色素变性9-诱导多功能干细胞来源的感光细胞。上述研究均表明,视网膜变性疾病和基因突变紧密相关,不同类型的基因突变的致病机制不同,对药物的反应也不同。基因诊断对患者将来个体化治疗是非常必要的。视网膜是难以获得的组织,以往大多是用动物模型来获取相应的视网膜细胞,耗费时间长,和人还是有差距,阻碍了视网膜疾病机制的研究进展。现在可以通过患者体细胞来源的诱导多功能干细胞,进行基因测序、RT-PCR、蛋白印迹等方法研究其致病机制,为以后个体化诊断和治疗防奠定了基础。 2.2.2 诱导多功能干细胞诱导分化为视网膜色素上皮细胞 视网膜色素上皮细胞是存在于感光细胞、脉络膜毛细血管层之间由一单层的立方形、色素细胞构成,它对于维持感光细胞生长及功能具有重要的作用。视网膜色素上皮细胞的缺失或者功能不全,是许多视网膜疾病如老年性视网膜黄斑变性的根本原因。事实上,目前已经有视网膜色素上皮细胞移植成功治疗与视网膜色素上皮细胞损害相关疾病的经验,例如,将年龄相关性黄斑变性患者自体视网膜周边的视网膜色素上皮细胞移植到黄斑部可以提高患者的视力,但是这种手术操作极其复杂,具有很高风险,未能得到广泛应用[29]。胚胎干细胞可以分化为视网膜色素上皮细胞已经得到证实和应用,同样地诱导多功能干细胞也可被诱导分化为视网膜色素上皮细胞细胞。2009年Hirami Y用同样方式首次将Oct4、Sox2、C-Myc和Klf4重编排的鼠胚胎成纤维细胞的诱导多功能干细胞为视网膜色素上皮细胞。先在SFEB培养模式下联合胚胎干细胞定向分化培养基(含有KSR、巯基乙醇)的诱导诱导多功能干细胞向神经样细胞分化,再加入Wnt信号通路抑制剂DKK-1和Nodal通路抑制剂Lefty-A,可使细胞分化为视网膜前体细胞,继而部分细胞分化为视网膜色素上皮细胞,在15 d时约22.3%细胞表达RX,36.5%表达视网膜色素上皮细胞前体细胞标志物Mitf,30 d可见细胞表现多角形的细胞形态,免疫组化结果显示细胞外侧缘表达紧密连接的标志物-紧密连接蛋白1,45 d时部分细胞表达成熟视网膜色素上皮细胞标志物。用类似的方法,研究者同时将人表皮成纤维细胞来源的诱导多功能干细胞进行诱导分化,35 d时细胞表达神经细胞标志物,约29.8%可表达MITF/PAX6,40 d时可见有色素的细胞生成,60 d时,细胞具有立方形、多角样形态。实验证明,诱导多功能干细胞按照胚胎干细胞诱导分化条件下,也能视网膜前体细胞分化,继而分化为视网膜色素上皮细胞,其时间和效率上和胚胎干细胞没有区别。Ma等[30]学者对诱导多功能干细胞来源的视网膜色素上皮细胞进行了详细的分析,研究中选用来源于胎肺成纤维细胞诱导多功能干细胞系-诱导多功能干细胞(IMR90)以及婴儿包皮成纤维细胞来源诱导多功能干细胞系诱导多功能干细胞(foreskin),在培养基中去除碱性成纤维细胞生长因子,使其自发的分化为RFE样细胞。与Hirami Y不同的是,这些诱导多功能干细胞系是利用Oct4,Sox2,Nanog,Lin28这四种因子重编排而来的。研究发现IMR90比foreskin在时间上早1-3周更自发分化为含色素细胞。这提示不同来源的诱导多功能干细胞向某种细胞分化能力不一样。并在细胞形态、基因表达、蛋白质表达、吞噬视杆细胞外节(ROS)上将IMR90-视网膜色素上皮细胞与胎儿色素上皮细胞、胚胎干细胞-视网膜色素上皮细胞进行了详细的比较。在形态上,这种诱导多功能干细胞-视网膜色素上皮细胞同样具有含黑色素,立方形、多角形态,在基因上,定量PCR显示表达眼部早期发育的基因-Pax6、Rax、Six,定向分化为视网膜色素上皮细胞基因-Mitf、Otx2,有关合成黑色素的基因-Tyrosinase、Tyrp1、Tyrp2、SILVER,有关细胞紧密连接的基因-claudin3、紧密连接蛋白1,编码视网膜色素上皮细胞向视网膜神经细胞层分泌蛋白的基因-transthyretin、PEDF,编码视网膜色素上皮细胞膜蛋白基因-bestrophin 和EMMPRIN。免疫印迹及免疫组化也同样表明诱导多功能干细胞-视网膜色素上皮表达紧密连接蛋白1、EMMPRIN、Otx2、Mitf、PEDF。并且诱导多功能干细胞-视网膜色素上皮具有ROS功能,和其他视网膜色素上皮一样基于利用整合蛋白αvβ5实现的,结果表明3种视网膜色素上皮在基因表达、蛋白表达及吞噬功能是非常的相似。但是Pax6在诱导多功能干细胞-视网膜色素上皮和胚胎干细胞-视网膜色素上皮有表达,而在视网膜色素上皮细胞前体细胞没有。Pax是在视网膜色素上皮细胞发育过程中表达,而会在视网膜色素上皮细胞成熟后消失。CRALBP、RPE65 在诱导多功能干细胞-视网膜色素上皮细胞和胚胎干细胞-视网膜色素上皮细胞表达比在视网膜色素上皮前体细胞要低很多,CRALBP、视网膜色素上皮65为视循环的基因,并在成熟的视网膜色素上皮表达,这些都提示诱导多功能干细胞-视网膜色素上皮可能仍不成熟。Carr等[32]对其进行了电镜下观察,和正常视网膜色素上皮一样具有极性的形态,表现为基地部的核,顶部的微绒毛结构、紧密连接及凹点,并分泌细胞外基质。还做了进一步的体内实验,证明诱导多功能干细胞-视网膜色素上皮在体内也具有吞噬功能,他们将诱导多功能干细胞视网膜色素上皮视网膜下腔注射移植到视网膜营养不良的大鼠模型中,虽然没有形成单层结构,而是细胞圆团,可是在3周内,这些细胞能通过吞噬感光细胞外节,起到保护感光细胞的作用,外核层的数量明显多于对照组,并且视动测试提示移植后的大鼠视功能得到显著提高;13周后,尽管移植的细胞完全消失了,但是实验组大鼠外核层还能得到保留,视功能优于对照组,这可能与移植细胞能分泌神经营养因子或者激活宿主炎症或免疫反应有关。Ukrohne等[33]用一种重排因子-Oct4联合小分子化合物诱导重排的诱导多功能干细胞诱导分化为视网膜色素上皮,值得一提的是,单因子重排的诱导多功能干细胞来源的视网膜色素上皮相对于两因子重排的以及传统上四因子重排的诱导多功能干细胞在基因表达、蛋白表达及代谢特征上更接近视网膜色素上皮细胞前体细胞。并且对它进行了为期更长的移植后体内观察,视网膜下移植到RCS鼠后,4-18周观察中,移植的细胞与正常的视网膜色素上皮一样,电镜证实,可以形成成单层的、极化的结构,具有吞噬视杆细胞外节及维持视循环功能,防止外核层变薄。6个月时,虽然移植组和对照组的视网膜厚度无明显差异,但是通过局部视网膜电图分析,移植部位的具有相对高的电反应。7个月后,视网膜下仍有存活的移植细胞。 将诱导多功能干细胞-视网膜色素上皮细胞运用于临床上,需要良好规范的培养方案以及制定评价分化为视网膜色素上皮细胞的标准Rowland等[34]在去除碱性成纤维细胞生长因子条件下诱导诱导多功能干细胞分化为视网膜色素上皮细胞,并比较各种细胞外基质对诱导多功能干细胞-视网膜色素上皮细胞色素形成,增殖,诱导效率,成熟的影响,从而探索出更优化培养方案。Liao等[35]对人诱导多功能干细胞-视网膜色素上皮细胞、人类胚胎干细胞-视网膜色素上皮细胞、正常的视网膜色素上皮细胞以及培养的胚胎视网膜色素上皮进行了全基因表达谱的比较。结果显示,人类胚胎干细胞-视网膜色素上皮细胞和胚胎视网膜色素上皮非常接近,诱导多功能干细胞-视网膜色素上皮细胞的分化水平相对于人类胚胎干细胞-视网膜色素上皮细胞不成熟;此外还鉴定了针对胚胎视网膜色素上皮的一组87个标志基因,大部分在人类胚胎干细胞-视网膜色素上皮细胞、人类胚胎干细胞-视网膜色素上皮细胞也有表达。这些结果建立了一组基因标志用于评估干细胞转化为视网膜色素上皮细胞的准确度。 诱导多功能干细胞-视网膜色素上皮细胞移植将来有望成为治疗视网膜疾病的手段,但是仍然面临着许多困难。第一,诱导多功能干细胞需要诱导为成熟的视网膜色素上皮细胞才能发挥功能,诱导成为符合标准的视网膜色素上皮细胞效率有待提高。第二, 如何在宿主组织内为视网膜色素上皮细胞移植提供一个生长平台,将其准确的定位于病变组织,并使胚胎视网膜色素上皮在病变的微环境中发挥作用还有很多工作要做。第三,老年性黄斑变性患者年龄偏大,这些来源的细胞更老,更难以被诱导为诱导多功能干细胞,以及患者来源的诱导多功能干细胞-视网膜色素上皮细胞本身具有的缺陷,如Kobbinaki等[36]研究发现人诱导多功能干细胞-视网膜色素上皮细胞的端粒急剧变短,染色体DNA损伤,p21表达增加;患者体细胞来源的诱导多功能干细胞的可能携带着与疾病有关的基因。如何避免或减少这些缺陷有待进一步研究。因此,还需要进一步的基础以及动物体内移植研究,获得安全、可信赖的诱导多功能干细胞-视网膜色素上皮细胞应用于临床。 2.2.3 诱导多功能干细胞分化为视网膜神经节细胞 Parameswaran等[37]将小鼠的成纤维细胞诱导的多功能干细胞先向神经前体细胞诱导,使其表达神经细胞标志物-Mash1, Otx2,and Nestin,b-tubulin,neurofilament,培养基中添加FGF2和Noggin诱导为视网膜前体细胞,再用来自E14大鼠视网膜细胞培养液得到视网膜神经节细胞。Mengfei等[38]指出Sox-2在眼的发育中起关键的作用,sox2与Pax6相关和Otx2共同协调眼的发育。Sox2做为一个的重排因子,使诱导多功能干细胞具有分化为视网膜神经细胞的潜能。其研究表明诱导多功能干细胞本身就表达视网膜祖细胞相关基因如Pax6、Rx、Otx2、Lhx2、Nestin。在培养基中添加DKK1、Noggin、DPAT等,并且用质粒转染诱导多功能干细胞使Matb5过度表达,可以将诱导多功能干细胞直接培养成视网膜神经节细胞。表达相应的标志物-Thy1.2,Brn3b,Islet-1。然后将诱导多功能干细胞来源的视网膜神经节细胞通过玻璃体腔注射移植到到正常的小鼠眼内。注射2周后发现,大部分细胞集中在注射的区域,几乎没有细胞整合到宿主的视网膜内。导致这个结果可能的原因是正常视网膜具有完整的屏障,阻碍了移植细胞整合进入。因此需要改变注射部位或使用靶向蛋白结合使其向视网膜迁移才有可能克服这个问题。 诱导多功能干细胞真正运用临床修复视神经重建视功能还有很长的路要走。视网膜神经节细胞有很多类型,不同类型的都非常重要,因为每一类视网膜神经节细胞代表着一个独立的视觉通道。不仅要获得各类型的视网膜神经节细胞,而且关键是移植的视网膜神经节细胞轴突伸向正确的位置,并和其他细胞形成有有效的突触联系,构成复杂的网络,成功接收到输入信号,并传递给更高级的视觉中心形成视觉。所以通过诱导多功能干细胞移植重建视功能的挑战是巨大的。相关细胞诱导多能干细胞分化见表1。"
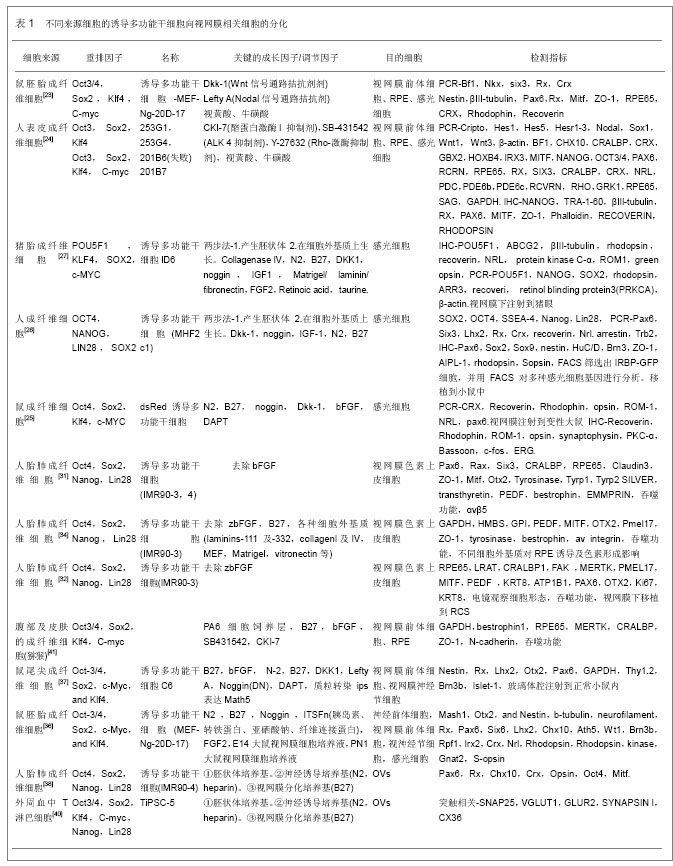

2.2.4 诱导多功能干细胞分化产生视泡样(Optic Vesicle-like,OV)结构 Meyer等[39]可以将胚胎干细胞及诱导多功能干细胞逐步在胚状体培养基、神经诱导培养基、视网膜分化培养基中诱导培养出视泡样结构的视网膜细胞团,相应的表达感光细胞,RPE标志物。接着他们又将更多种诱导多功能干细胞诱导产生视泡样结构,其中有由于编码鸟氨酸-转氨酶(OAT)基因突变而致视网膜回旋性萎缩病人来源的诱导多功能干细胞。这类患者来源的诱导多功能干细胞-视网膜色素上皮细胞的OAT活性低,提高维生素B6水平能提高诱导多功能干细胞-视网膜色素上皮细胞的OAT活性,他们还通过同源重组染色体对这类诱导多功能干细胞进行基因矫正,结果证明,经过基因矫正的诱导多功能干细胞-视网膜色素上皮细胞具有正常的OAT活 性[40]。最近Phillips等[41]将T淋巴细胞来源的诱导多功能干细胞诱导产生视泡样结构,最里层的细胞大部分表达视神经节细胞标志物-BRN3、TUJ1,CALRETIN+/BRN-无长突样细胞在中间层,RECOVERIN+ 感光样细胞位于最外层,实验还表明,细胞与细胞具有突触链接,表达视网膜细胞突触标志物。上述研究提示,诱导多功能干细胞产生的视泡样结构细胞群,不仅可以作为视网膜细胞的来源,也是一个非常良好的研究视网膜发育的模型,同时患者体细胞来源的诱导多功能干细胞产生视泡结构可以为体外研究筛选特异性药物试验,基因修饰以及疾病机制研究提供一个良好的平台。"

| [1] Takahashi K, Yamanaka S. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell. 2006;126(4):663-676.
[2] Takahashi K, Tanabe K, Ohnuki M, et al. Induction of pluripotent stem cells from adult human fibroblasts by defined factors. Cell. 2007;131(5):861-872.
[3] Zwi-Dantsis L, Gepstein L. Induced pluripotent stem cells for cardiac repair. Cell Mol Life Sci. 2012;69(19):3285-3299.
[4] Liang P, Lan F, Lee AS, et al. Drug Screening Using a Library of Human Induced Pluripotent Stem Cell-Derived Cardiomyocytes Reveals Disease Specific Patterns of Cardiotoxicity. Circulation. 2013 Mar 21.
[5] Park IH, Zhao R, West JA, et al. Reprogramming of human somatic cells to pluripotency with defined factors. Nature. 2008;451(7175):141-146.
[6] Aoi T, Yae K, Nakagawa M, et al. Generation of pluripotent stem cells from adult mouse liver and stomach cells. Science. 2008;321(5889):699-702.
[7] Hanna J, Markoulaki S, Schorderet P, et al. Direct reprogramming of terminally differentiated mature B lymphocytes to pluripotency. Cell. 2008;133(2):250-264.
[8] Eminli S, Utikal J, Arnold K, et al. Reprogramming of neural progenitor cells into induced pluripotent stem cells in the absence of exogenous Sox2 expression. Stem Cells. 2008; 26(10):2467-2474.
[9] Ebihara Y, Ma F, Tsuji K. Generation of red blood cells from human embryonic/induced pluripotent stem cells for blood transfusion. Int J Hematol. 2012;95(6):610-616.
[10] Yu J, Hu K, Smuga-Otto K, Tian S, et al. Human induced pluripotent stem cells free of vector and transgene sequences. Science. 2009;324(5928):797-801.
[11] Woltjen K, Michael IP, Mohseni P, et al. piggyBac transposition reprograms fibroblasts to induced pluripotent stem cells. Nature. 2009;458(7239):766-770.
[12] Zhou H, Wu S, Joo JY, et al. Generation of induced pluripotent stem cells using recombinant proteins. Cell Stem Cell. 2009;4(5):381-384.
[13] Zhu S, Li W, Zhou H, et al. Reprogramming of human primary somatic cells by OCT4 and chemical compounds. Cell Stem Cell. 2010;7(6):651-655.
[14] Soldner F, Hockemeyer D, Beard C, et al. Parkinson's disease patient-derived induced pluripotent stem cells free of viral reprogramming factors. Cell. 2009;136(5):964-977.
[15] Sommer CA, Stadtfeld M, Murphy GJ, et al. Induced pluripotent stem cell generation using a single lentiviral stem cell cassette. Stem Cells. 2009;27(3):543-549.
[16] Ruiz S, Panopoulos AD, Herrerías A, et al. A high proliferation rate is required for cell reprogramming and maintenance of human embryonic stem cell identity. Curr Biol. 2011;21(1): 45-52.
[17] Hong H, Takahashi K, Ichisaka T, et al. Suppression of induced pluripotent stem cell generation by the p53-p21 pathway. Nature. 2009;460(7259):1132-1135.
[18] Li R, Liang J, Ni S, et al. A mesenchymal-to-epithelial transition initiates and is required for the nuclear reprogramming of mouse fibroblasts. Cell Stem Cell. 2010; 7(1):51-63.
[19] Samavarchi-Tehrani P, Golipour A, David L, et al. Functional genomics reveals a BMP-driven mesenchymal-to-epithelial transition in the initiation of somatic cell reprogramming. Cell Stem Cell. 2010;7(1):64-77.
[20] Koche RP, Smith ZD, Adli M,et al. ogramming factor expression initiates widespread targeted chromatin remodeling. Cell Stem Cell. 2011;8(1):96-105.
[21] Singhal N, Graumann J, Wu G, et al. omatin-Remodeling Components of the BAF Complex Facilitate Reprogramming. Cell. 2010;141(6):943-955.
[22] Theunissen TW, van Oosten AL, Castelo-Branco G, et al. nog overcomes reprogramming barriers and induces pluripotency in minimal conditions. Curr Biol. 2011;21(1):65-71.
[23] Hirami Y, Osakada F, Takahashi K, et al. Generation of retinal cells from mouse and human induced pluripotent stem cells. Neurosci Lett. 2009;458(3):126-131.
[24] Osakada F, Jin ZB, Hirami Y, et al. In vitro differentiation of retinal cells from human pluripotent stem cells by small-molecule induction. J Cell Sci. 2009;122(Pt 17): 3169-3179.
[25] Tucker BA, Park IH, Qi SD, et al. Transplantation of adult mouse iPS cell-derived photoreceptor precursors restores retinal structure and function in degenerative mice. PLoS One. 2011;6(4):e18992.
[26] Lamba DA, McUsic A, Hirata RK, et al. Generation, purification and transplantation of photoreceptors derived from human induced pluripotent stem cells. PLoS One. 2010;5(1):e8763.
[27] Zhou L, Wang W, Liu Y, et al. Differentiation of induced pluripotent stem cells of swine into rod photoreceptors and their integration into the retina. Stem Cells. 2011;29(6): 972-980.
[28] Tucker BA, Scheetz TE, Mullins RF, et al. Exome sequencing and analysis of induced pluripotent stem cells identify the cilia-related gene male germ cell-associated kinase (MAK) as a cause of retinitis pigmentosa. Proc Natl Acad Sci U S A. 2011;108(34):E569-576.
[29] Jin ZB, Okamoto S, Osakada F, et al. Modeling retinal degeneration using patient-specific induced pluripotent stem cells. PLoS One. 2011;6(2):e17084.
[30] Ma Z, Han L, Wang C, et al. Autologous transplantation of retinal pigment epithelium-Bruch's membrane complex for hemorrhagic age-related macular degeneration. est Ophthalmol Vis Sci. Invest Ophthalmol Vis Sci. 2009;50(6): 2975-2981.
[31] Buchholz DE, Hikita ST, Rowland TJ, et al. Derivation of functional retinal pigmented epithelium from induced pluripotent stem cells. Stem Cells. 2009;27(10):2427-2434.
[32] Carr AJ, Vugler AA, Hikita ST, et al. Protective effects of human iPS-derived retinal pigment epithelium cell transplantation in the retinal dystrophic rat. PLoS One. 2009;4(12):e8152.
[33] Ukrohne TU, Westenskow PD, Kurihara T, et al. Generation of retinal pigment epithelial cells from small molecules and OCT4 reprogrammed human induced pluripotent stem cells. Stem Cells Transl Med. 2012;1(2):96-109.
[34] Rowland TJ, Blaschke AJ, Buchholz DE, et al. Differentiation of human pluripotent stem cells to retinal pigmented epithelium in defined conditions using purified extracellular matrix proteins. J Tissue Eng Regen Med. 2012 Apr 18.
[35] Liao JL, Yu J, Huang K, et al. Molecular signature of primary retinal pigment epithelium and stem-cell-derived RPE cells. Hum Mol Genet. 2010;19(21):4229-4238.
[36] Kokkinaki M, Sahibzada N, Golestaneh N. Human induced pluripotent stem-derived retinal pigment epithelium (RPE) cells exhibit ion transport, membrane potential, polarized vascular endothelial growth factor secretion, and gene expression pattern similar to native RPE. Stem Cells. 2011; 29(5):825-835.
[37] Parameswaran S, Balasubramanian S, Babai N, et al. Induced pluripotent stem cells generate both retinal ganglion cells and photoreceptors: therapeutic implications in degenerative changes in glaucoma and age-related macular degeneration. tem Cells. 2010;28(4):695-703.
[38] Chen M, Chen Q, Sun X, et al. Generation of retinal ganglion-like cells from reprogrammed mouse fibroblasts. Invest Ophthalmol Vis Sci. 2010;51(11):5970-5978.
[39] Meyer JS, Shearer RL, Capowski EE, et al. Modeling early retinal development with human embryonic and induced pluripotent stem cells. Proc Natl Acad Sci U S A. 2009;106 (39):16698-16703.
[40] Meyer JS, Howden SE, Wallace KA, et al. Optic vesicle-like structures derived from human pluripotent stem cells facilitate a customized approach to retinal disease treatment. Stem Cells. 2011;29(8):1206-1218.
[41] Phillips MJ, Wallace KA, Dickerson SJ,et al. Blood-derived human iPS cells generate optic vesicle-like structures with the capacity to form retinal laminae and develop synapses. Invest Ophthalmol Vis Sci. 2012;53(4):2007-2019.
[42] Okamoto S, Takahashi M. Induction of retinal pigment epithelial cells from monkey iPS cells. Invest Ophthalmol Vis Sci. 2011;52(12):8785-8790. |
| [1] | Wang Jian-ji, Yang Long, Li Jing, Sun Qi, Zuo Wei-min, Ren Qi-feng, Sun Yu, Wu Zhan-yu, Zou Qiang, Ma Min-xian, Ye Chuan. Development and application of special-purpose grafter by femoral head decompression combined with bone marrow mesenchymal stem cells transplantation based on three-dimensional printing technology [J]. Chinese Journal of Tissue Engineering Research, 2016, 20(44): 6636-6642. |
| [2] | Zhou Chang-yan, Zhou Qing-huan, Bian Jing, Chen Ke, Chen Wen. Bone marrow mesenchymal stem cells combined with calcium phosphate cement to repair articular cartilage defects in rabbits [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(8): 1195-1199. |
| [3] | Xu Xiang, Yin He-ping. Platelet-rich plasma accelerates the proliferation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2144-2148. |
| [4] | Ma Fa-ku, Wang Huan, Liu Bin, Yang Yan-li, Su Qin-jun, Qian Zhen, Dong Liang. Expression of CD44+/C-myc+ cancer stem cells and its relationship with the prognosis of patients in colorectal tumors [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2161-2166. |
| [5] |
Chen Ping, Wang Jian.
Enrichment of lung cancer stem cells and expression of related markers
[J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2167-2171.
|
| [6] | Fan Zhi-gang, Fan Hong-liang. Oxidative stress response in diabetic nephropathy rats following injection of embryonic stem cells via the tail vein [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2199-2204. |
| [7] | Wang Yong, Zhao Wei, Feng Jian-zhou, Chen Xiao-chun. Nerve growth factor-modified adipose derived stem cells for repair of spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2224-2229. |
| [8] | Sha Wen-qiong, She Rui-lian, Wang Zi-neng, Ke Ru. Ultrastructure and phagocytotic function of human placental mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2230-2235. |
| [9] | Du Qing-hua, Cao Jun-kai, Dong Xi-xi, E Ling-ling, Wei Li-jun. Osteogenic differentiation of pluripotent stem cells induced by akermanite extracts [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2236-2242. |
| [10] | Wu Yan, Huang Lan . Bone morphogenetic protein 9-induced osteogenic differentiation of dental follicle cells in vitro [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2255-2260. |
| [11] | Rao Li-jia, Li Qi-meng, Li Jin-ling, Xu Qiong. Expression pattern of ten-eleven translocation family during differentiation of human dental pulp cells [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2261-2266. |
| [12] | Gao Zhuo-yue, Liu Yong-qi, He Jian-xin, Wu Zhi-wei, Luo Ya-li, Su Yun, Zhang Li-ying, Zhang Qi, Wu You-ming, Zhou Ni-na. Regulatory effects of warming yang and invigorating qi treatment on the inflammatory balance and genetic stability of bone marrow mesenchymal stem cells under tumor microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2267-2272. |
| [13] | Wang Fang, Chen Shao-wei. In vitro culture of embryos and establishment of embryonic stem cell lines [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2273-2277. |
| [14] |
Du Wei-bin, Quan Ren-fu, Zheng Xuan, Wang Tuo.
Hair follicle stem cells promote the healing of skin wound
|
| [15] | Du Hua, Shi Ying-xu . Bone marrow microenvironment controls the “fate” of hematopoietic stem cells [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2283-2290. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||