Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (10): 1611-1617.doi: 10.3969/j.issn.2095-4344.0724
Previous Articles Next Articles
Three-dimensional bioprinting of tissue/organ analogues: a review on techniques, materials and processes
- 1Department of Plastic and Burn Surgery, the Clinical School of Tianjin Medical University, Tianjin 300070, China; 2Department of Plastic and Burn Surgery, Tianjin First Central Hospital, Tianjin 300192, China; 3Department of Plastic and Burn Surgery, Tianjin Third Central Hospital, Tianjin 300170, China
-
Received:2017-11-26Online:2018-04-08Published:2018-04-08 -
Contact:Zhang Ming-jian, Professor, Chief physician, Master’s supervisor, Department of Plastic and Burn Surgery, Tianjin First Central Hospital, Tianjin 300192, China -
About author:Wang Xue-xin, Master candidate, Department of Plastic and Burn Surgery, the Clinical School of Tianjin Medical University, Tianjin 300070, China
CLC Number:
Cite this article
Wang Xue-xin, Zhang Ming-jian, Li Xiao-bing, Han Wei-xin, Li Jin-qiao. Three-dimensional bioprinting of tissue/organ analogues: a review on techniques, materials and processes[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(10): 1611-1617.
share this article
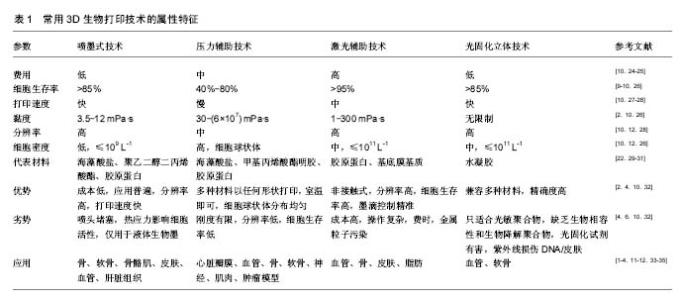
2.1 3D生物打印的概念 利用医学图像数据[如核磁共振成像(MRI)和电子计算机X射线断层扫描技术(CT)]创建患者缺失部分或损害部分植入物的几何形状和大小,是3D打印技术在医学领域的应用基础[2];而通过打印不同组织/器官的活细胞并添加各种生物活性材料的“生物墨”,能够彻底改变3D结构的生物、化学和机械性能,以适应不同组织/器官的印刷要求,达到增强组织/器官最优功能化的技术,称为3D生物打印技 术[1]。因此,3D生物打印中的打印技术、细胞类型、生物材料、细胞基质及生化支持因素等均直接关系到3D打印组织/器官类似物活细胞的生存力和最终特定功能。 2.2 3D生物打印技术及其特点 目前可用的3D生物打印技术主要有以下几种类型:喷墨式生物打印技术、压力辅助生物打印技术、激光辅助生物打印技术、光固化立体印刷技术。每种方法都有较广泛的研究,均存在各自的优势和局限性(表1)。"
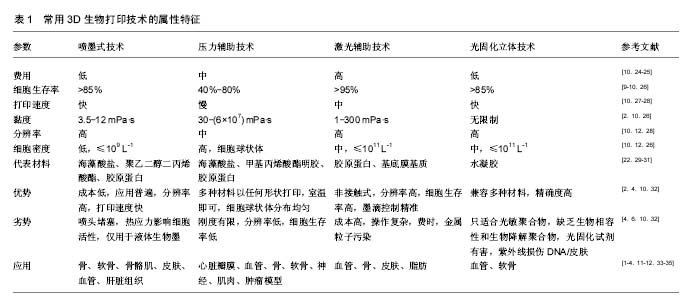
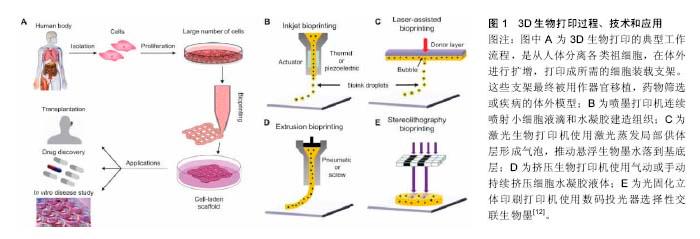
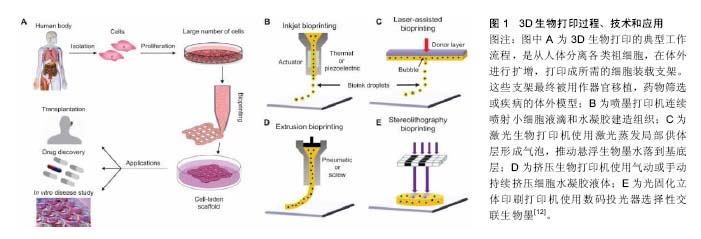
2.2.1 喷墨式技术 喷墨技术是常用的3D组织/器官打印技术,在计算机的控制下,通过热或电形成生物墨滴,从喷墨头的喷嘴以微升为单位非接触式逐出,并精确印刷到水凝胶基质或培养皿的特定位置[5]。其中,热喷墨技术通过将打印头内部局部加热至200-300 ℃范围,利用泡沫膨胀的力量将墨水从狭窄的喷嘴逐出,这种技术因成本低而被广泛使用,然而,使用热技术混合的生物墨往往出现与热能相关的一些问题:导致墨滴大小不均、种类无序;墨滴频繁的堵塞喷嘴,很难满足打印组织的光滑度;剪切和热应力也会影响其细胞和蛋白质活性[6]。压电喷墨技术使用压电晶体脉冲执行器产生的脉冲定期喷出小水滴,因其过程不使用热能,不会引起喷孔堵塞且保证了液滴均一大小和定向喷射;但是,过于频繁的使用压电喷墨技术会破坏细胞膜、产生细胞溶解作用[7]。 2.2.2 压力辅助技术 压力辅助技术是一种基于物理挤压生物墨滴定向沉积的原理来创建所需的3D结构的方法,用于打印的生物材料通常是液体或分散体,通过以气动压力或柱塞/螺杆压力的形式协调挤压运动在微尺度喷嘴孔或固定在底物上的微针孔形成连续长丝[4]。其中气压辅助技术使用了一组机电微阀门,通过在恒定气压下打开微阀门可产生液滴,这项技术的优势是可使用各种类型的液体生物材料,直接将细胞均匀分布,黏度可高达200 Pa•s,且在室温下即可操作处理[1]。 2.2.3 激光辅助技术 激光辅助技术通常由3部分组成:脉冲激光源、沉积在金属薄膜上涂有液体生物材料的丝带和接收基质层[8]。实验室主要使用纳秒激光与紫外线或近紫外线波长作为能源,打印水凝胶、细胞、蛋白质等生物材料。激光照射丝带导致液体生物材料蒸发,以液滴形式到达接收层,接收层包含一个生物聚合物或细胞培养基来支持细胞黏附和后续增长。生物材料的厚度、流变特性、激光脉冲的能量、基板润湿性、印刷速度和组织结构类型均会影响激光打印组织的分辨率[9]。另外,因这种技术只能使用低黏度或液体生物材料制造组织/器官类似物,所以往往没有足够的机械强度维持其形状,且使用激光源的费用较高,激光脉冲的控制方面也极具复杂性。 2.2.4 光固化立体印刷技术 光固化立体印刷技术是最古老的3D打印技术,其原理是控制照射的光,如紫外、红外或可见光作用于液态感光性树脂上,产生光聚合或光交联反应后固化一个2D模式层;然后,在每层固化完成后通过移动z轴覆盖一层新的液态树脂,再次固化一个2D模式层,完成层层堆积后,最终构建完整的3D结构[10]。 目前,光固化具有单光子和双光子2种类型。利用单光子固化的方式又分为2种:波束扫描和图像投影。波束扫描法采用选择性聚焦激光束的扫描,在激光束的扫描路径上形成一个固化的2D模式层;图像投影方法则是利用数字微镜装置将生成的2D模式图像投射到液态光敏聚合物上,然后通过一个单一投影图像的模式完成完整的2D层固化,这个印刷过程可明显减少打印时间。双光子固化立体印刷技术是在液态光敏聚合物上同时同点吸收2个光子,当作拥有双波长的一个光子,移动焦点后使三维结构凝固,而无需使用液态光敏聚合物内部构建平台,这种技术可直接实现空间凝固,分辨率高达100 nm,在所有3D打印技术中分辨率最高[11]。 随着可溶于水的光敏聚合物的发展,应用光固化立体印刷技术创建3D组织/器官类似物已成为可能,并且以可见光作为光固化立体印刷技术的能源不会损害细胞DNA,目前利用该技术已经打印出了血管和软 骨[12](图1)。但是,它仍然具有自身的局限性,例如该技术只能使用光敏感性强且具有良好生物相容性的生物材料。 2.3 组成“生物墨”的生物材料 相比使用金属、塑料和聚合物作为传统3D打印的材料,3D生物打印必须兼容活细胞并模仿原生组织的细胞基质体系结构和机械性能,保证细胞及基质的生物学功能[3]。目前还没有专门用于细胞打印的理想的“生物墨”,已知各种水凝胶材料可用来构造3D组织结构,但必须考虑相关材料的诸多因素,比如印刷适应性与交叉连接能力、流变特性与机械性能、生物相容性与聚合机制、细胞毒性与降解可控性等[12]。 2.3.1 原生活细胞 细胞是构成“生物墨”的基础成分,打印不同组织/器官类似物需要培养相应的原生活细胞。例如,成骨祖细胞、软骨细胞、纤维细胞、角质细胞、肝细胞、血管内皮细胞、心脏瓣膜间质细胞及平滑肌细胞、心肌祖细胞等自身已分化细胞和组织干细胞等均在组织工程领域被广泛应用和尝试。 2.3.2 天然聚合物 天然聚合物即提炼水凝胶,具有与机体组织微环境相似的天然生物活性,支持细胞/组织集成和生物相容性,通常被广泛应用在各种类型的生物打印。它还可提供特定组织生化和生理刺激引导细胞迁移、增殖、分化和成熟等行为。 胶原蛋白是细胞外基质的一种结构蛋白质,主要存在于动物结缔组织中,对机体和脏器起着支持、保护、结合及形成界隔等作用,胶原蛋白含有大量甘氨酸、脯氨酸和羟脯氨酸残基,并参与细胞-细胞、细胞-基质间信号转导、生长因子和细胞因子运输等功能,并且,胶原蛋白在生理条件下可通过热凝胶作用促进交联[13]。因此,3D生物打印中大多数基质由这种材料构成。 明胶来源于变性的胶原蛋白,是一种热可逆性的混合物,其富含的蛋白质包括纤连蛋白、波形蛋白、玻连蛋白、RGD肽等均通过整合素受体促进细胞黏附[14]。明胶作为一种天然的水溶性高分子材料,降解后的产物易被吸收而不产生炎症反应,且与生物体结构相似,具有良好的生物相容性,因此这种材料在食品、医药、化妆品领域被广泛应用。此外,明胶溶液可形成具有一定硬度、不能流动的水凝胶,其中水为致孔剂,冷冻干燥后形成多孔支架,可根据不同组织的修复要求设计理想的组织工程材料。 纤维蛋白是一种高度不溶的蛋白质多聚体。在人体内,纤维蛋白原和凝血酶之间相互作用形成纤维蛋白,主要在凝血机制中发挥重要作用[15]。同时,纤维蛋白参与机体伤口的愈合过程,也由于其快速凝胶化的性质被广泛用作外科胶,具有高度的细胞黏附性。值得注意的是,应用喷墨式生物打印技术制造的纤维蛋白结构柔软且脆弱、机械稳定性欠佳,很难保持理想的形状。 透明质酸是由D-葡萄糖醛酸及N-乙酰葡糖胺组成的双糖单位,属酸性黏多糖,带负电荷,是一种在生物医学领域被广泛使用的材料[16]。这种材料具有良好的生物相容性、黏弹性、亲水性和生物降解性,透明质酸接合丙烯酸甲酯团体在紫外线照射下通过自由基聚合反应形成凝胶。 藻朊酸盐是一种由来源于褐藻类的天然阴离子多聚糖海藻酸与多价阳离子包括Ca2+、Ba2+和Fe3+络合而成的水凝胶[17]。海藻酸可很容易地被修饰,为各种组织工程的应用提供生物活性分子;交联海藻酸也有与人体细胞基质类似的结构,具有良好的生物相容性,并且凝胶化时间较短,在组织工程领域比海藻酸更受欢迎。 琼脂糖是由半乳糖及其衍生物构成的中性物质,不带电荷,是理想的惰性载体,通常在水中加热到90 ℃以上溶解,温度下降到40 ℃左右形成良好的半固体状凝胶,被广泛应用于生物化学实验室,作为电泳、层析等技术的支持物[18]。近年来,因其特殊的凝胶性质,具有显著的稳固性、滞后性,并且吸水能力强,可产生特殊的稳定效应,在组织工程领域倍受关注。 壳聚糖是甲壳质经脱乙酰反应后的产品,不溶于水,溶于酸,能被人体吸收;无毒无害,具有优良的生物相容性;可生物降解,降解产物无毒,能被生物体完全吸收[19]。目前,壳聚糖的主要应用包括与磷酸钙结合作为骨修补和牙的填料,与聚酯结合制造人造血管;与甲壳素混合后制作可吸收手术缝线等方面。关于壳聚糖凝胶的研究尚需进一步开展。 2.3.3 合成聚合物 近年来,在生物医学领域使用合成聚合物的比例明显增加,除了其具有“量体裁衣”与生物可降解属性。相比天然聚合物,合成聚合物可改变其物理、化学与力学性能,以适应不同组织/器官类似物的制造。同时,这些材料可以低成本生产且不存在病原体寄宿的风险。有时为了改善细胞反应的影响,可选择使用合成和天然聚合物的混合物。 聚己内酯是一种无毒害、具有良好的生物相容性与降解可控性的合成聚合物,可用来代替细胞外基质构造组织工程支架,满足装载细胞形成精确形状的需求[20]。同时,因其有一个低熔点温度(59-64 ℃)且具有极大伸展性而被广泛应用于微挤压技术成型。此外,聚己内酯热稳定性与适当的流变特性对3D打印结构的分辨率十分有益。 聚乳酸-羟基乙酸共聚物是由乳酸和羟基乙酸随机聚合而成的一种功能高分子有机化合物,在美国已被正式作为药用辅料收录进美国药典[21]。乳酸和羟基乙酸两者的比例决定了聚乳酸-羟基乙酸共聚物的生物相容性和可控降解性(两者比例为50∶50,降解速度更快),其降解产物亦无毒副作用,目前已被用来制作为人工导管、药物缓释载体、组织工程支架材料。聚乳酸-羟基乙酸共聚物属热塑性材料,因此在3D生物激光打印技术中备受欢迎。 聚乙烯乙二醇是经食品和药物管理局(FDA)批准的在生物医学领域允许集中使用的合成聚合物[22]。可通过微调分子量、分子分布、交联密度改变凝胶性质,由于其缺乏天然生物活性肽的序列或构象,聚乙烯乙二醇往往需要额外进行化学修饰建立细胞交流支持生物相容性和集成。又因其具有水溶性属性,聚乙烯乙二醇可作为临时支撑材料代表用于制作复杂的3D组织工程结构。 普朗尼克F127是一种热可逆凝胶,克服了普朗克尼本身只具有良好的印刷适应性但不适宜长期培养细胞的难题,该特点对3D组织/器官打印十分有利[23]。其热可逆的性质表现为在4.0-5.0 ℃以下呈液态,超过16 ℃时可转变成凝胶,且形成的凝胶是永久可逆的。 2.4 3D生物打印的应用 3D生物打印含有活细胞的组织/器官类似物,在组织工程领域显示出巨大的潜力。尽管已有较广泛的研究,但目前的印刷技术只能完成相对简单的组织结构和生物功能,含有活细胞的3D组织/器官生物打印仍然是在非常早期的探索阶段。 2.4.1 骨 在人体组织中,骨组织要求具有最强的机械性能,所有用于骨组织工程的生物支架要求必须是高浓度和高黏度的材料,如聚己酸内酯、聚乳酸和聚乙醇酸、双相磷酸钙、磷酸三钙或这些水凝胶相互组合。出于同样的原因,压力辅助打印技术常被选为其制造方法。此外,为了促进骨形成,可在印刷过程中将骨母细胞和间充质干细胞嵌入到支架里或播种在支架表面,生长因子如骨形成蛋白和血管内皮生长因子也常与支架材料混合印刷,以增强骨形成和血管生成[3]。Sawkins等[36]的体外实验证明了利用活细胞和活性蛋白加强骨组织修复的可行性:在温和条件下,活细胞和活性蛋白可耐受混合和挤压过程,同时维护生存能力,完成植入到缺陷骨的打印过程。 2.4.2 软骨 软骨是无神经、无血管的带状组织结构。3D生物打印技术可通过控制每个印刷层不同生物材料属性和细胞类型,生成精确的空间格局并创建不同梯度的软骨组织。例如,关节软骨组织成分在不同的区域存在不同的细胞密度、形态、黏多糖成分和机械性能:将软骨细胞和聚乙二醇二丙烯酸酯精确沉积在3D打印设定的位置,模仿不同的解剖区域制造软骨结构,通过改变纤维间距或纤维沉积,可使支架产生不同孔隙度和弹性模量,也可将人类软骨细胞和成骨细胞添加在不同的解剖区域模拟骨软骨组织结构。除了物理区分不同的区域,也可通过合并印刷封装人类间充质干细胞、骨形成蛋白2、转化生长因子β1的材料,实现生物化学梯度的要求[37]。Kundu等[20]利用聚己内酯、鼻中隔软骨细胞和转化生长因子β1通过3D打印技术完成了软骨形态制造。 2.4.3 心脏瓣膜 各种病理条件均可导致心脏瓣膜的频繁损坏,迫切需要科学家们利用3D生物打印技术开发组织工程心脏瓣膜。虽然其几何形状相对特殊,3D生物打印技术可进行个体化设计制造某个心脏瓣膜,并充分考虑其显微结构的复杂性,使得达到内在生物力学和血流动力学功能。因此,组织工程心脏瓣膜的制造需要具有强大的机械性能,只有足够强度生物材料可以使用:Duan等[30]将透明质酸凝胶和人类主动脉瓣膜间质细胞混合,应用微挤压生物打印技术完成三瓣心脏瓣膜制造,在7 d内具有较高存活力且显示出了巨大的重构潜力;Hockaday等[38]应用海藻酸和聚乙二醇二丙烯酸酯打印了一个具有复杂的解剖结构和异质性的工程主动脉瓣,结果显示瓣膜形状保真,但细胞黏附力较差。这些研究证明3D生物打印技术创建多细胞组织阀门有实现临床使用的可能性。 2.4.4 皮肤 在皮肤组织工程中,3D生物打印过程必须考虑细胞基质精确的细胞层定位和细胞-细胞、细胞-基质间生物信号的交流。胶原蛋白Ⅰ、纤维蛋白和人工脱细胞异体真皮是一些流行的皮肤组织工程支架材料,角质细胞、成纤维细胞或皮肤细胞的干细胞是皮肤印刷的主要细胞[39]。Lee等[40]使用3D喷墨打印技术创建了一个皮肤组织结构:胶原蛋白、角化细胞、成纤维细胞分别印刷在不同的结构层,模拟皮肤组织真皮和表皮的多层结构,然后将打印的皮肤放置在气液界面培养2周,发现角化细胞正常分化形成多层表皮角质层。Koch等[41]同样用胶原蛋白、成纤维细胞、角质细胞通过激光辅助细胞印刷技术制造皮肤类似物,体外培养后观察到基底膜和细胞间连接的形成;随后进行的体内组织工程皮肤测试,采用裸小鼠背侧皮肤移植方法,移植皮肤下发现一些血管从伤口边缘向打印细胞方向增长,提示打印的皮肤与宿主组织的整合。 2.4.5 肝脏 肝脏是人体最大的实质性器官,它的体系结构复杂,有广泛的生物功能和独特的再生能力。然而,随着肝脏疾病的发病率增长,全球需要进行肝脏移植手术的病患数量增加,导致了持续的供肝短缺问题。 肝细胞移植、生物打印人工器官成为了目前解决这个问题的核心方案。Lee等[35]专门针对组织工程肝细胞来源进行了分类和总结:人类原始肝细胞主要用于肝细胞移植,生物相容性好,但多存在来源局限、分离困难、体外复制能力差和功能迅速衰退等问题;猪肝细胞用于生物型人工肝的制造,容易获取,但生物相容性差、有免疫原性且在体外功能衰退明显;人类干细胞的分化肝细胞已成为目前肝细胞移植的研究热点,但其获取标准仍有争议。Alkhouri等[42]正在探索使用3D生物打印技术制造微型肝脏,在实验室培育出来替代终末期肝衰竭病患的肝脏。此外,高频率的药物使用容易引起肝损伤,这是药物开发和临床试验阶段最应担忧的问题,因此,肝组织模型的创建,有利于肝毒性测试,是药物筛选工程的一个重大进步。 2.4.6 血管 组织结构血管化对人类活组织/器官的生存至关重要。然而,血管的创建在组织工程领域仍然是一个巨大的挑战。为了解决这个问题,可利用临时支撑材料或构建独立的管状结构去创建空心通道。Wu等[43]使用普朗尼克F127作为临时支撑材料打印3D仿生全方位微血管网络,随后播种内皮细胞使通道内皮化;Miller等[44]应用水溶性生物玻璃印刷脉管系统,将玻璃纤维作为临时支撑材料溶解在缓冲溶液或培养基后,形成互相连接的网络通道。Lee等[45]提出了一个打印血管的方法学,首先创建更大的血管通道(0.5-1.0 mm),然后通过自然成熟过程创建相邻毛细管网,在模型中,微血管床被建立在2个大流体血管之间,并通过发芽方式生成小血管连接到来自大通道边缘的血管分支。 2.4.7 肿瘤模型与药物开发 长久以来,肿瘤研究主要依赖于动物模型,但在人类和动物之间关于肿瘤的生物学和免疫学研究存在不可避免的显著性差异。若成功创建3D生物打印体外组织/器官模型并用于测试各种各样的药物,将推动肿瘤研究领域的快速发展并缩短抗肿瘤药物的研发时间。 Zhao等[46]使用纤维蛋白原、明胶和海藻酸的混合水凝胶与海拉细胞(实验用增殖表皮癌细胞)成功打印出体外子宫颈肿瘤的3D模型,并发现与2D肿瘤模型相比,有超过90%的细胞成活,并且3D肿瘤模型显示出不同的细胞活动,如增殖、基质金属蛋白酶蛋白表达、细胞的药物抗性等,这些差异可归因于3D模型的培养条件促进了细胞-细胞和细胞-基质之间信息交互作用。同时,King等[47]研究了3D打印乳腺癌组织用于测试新的抗癌治疗方法,成功地在没有聚合物支架的情况下用乳房肿瘤间质、乳腺癌细胞、内皮细胞和成纤维细胞重建乳腺癌组织模型。此外,3D生物打印可研究肿瘤的发展过程,包括肿瘤的异质性、转移途径、特殊患者的抗肿瘤药物测试等方面。这些结果均表明3D生物打印在创建肿瘤模型和药物开发中具有巨大的价值。 "
| [1]Park JH,Jang J,Lee JS,et al.Three-Dimensional Printing of Tissue/Organ Analogues Containing Living Cells.Ann Biomed Eng.2017;45(1):180-194. [2]Zhang X,Zhang Y.Tissue Engineering Applications of Three-Dimensional Bioprinting.Cell Biochem Biophys. 2015; 72(3):777-782. [3]Lee VK,Dai G.Printing of Three-Dimensional Tissue Analogs for Regenerative Medicine.Ann Biomed Eng. 2017;45(1):115-131. [4]Li J,Chen M,Fan X,et al.Recent advances in bioprinting techniques: approaches, applications and future prospects.J Transl Med.2016;14:271. [5]Boland T,Xu T,Damon B,et al.Application of inkjet printing to tissue engineering.Biotechnol J.2006; 1(9):910-917. [6]Cui X,Dean D,Ruggeri ZM,et al.Cell damage evaluation of thermal inkjet printed Chinese hamster ovary cells.Biotechnol Bioeng.2010;106(6):963-969. [7]Saunders RE,Gough JE,Derby B.Delivery of human fibroblast cells by piezoelectric drop-on-demand inkjet printing. Biomaterials. 2008;29(2):193-203. [8]Catros S,Fricain JC,Guillotin B,et al.Laser-assisted bioprinting for creating on-demand patterns of human osteoprogenitor cells and nano-hydroxyapatite. Biofabrication. 2011;3(2):025001. [9]Guillemot F,Souquet A,Catros S,et al.Laser-assisted cell printing: principle, physical parameters versus cell fate and perspectives in tissue engineering.Nanomedicine. 2010;5(3): 507-515.[10]Melchels FP,Feijen J,Grijpma DW.A review on stereolithography and its applications in biomedical engineering. Biomaterials.2010;31(24):6121-6130. [11]Lee JW.3D Nanoprinting Technologies for Tissue Engineering Applications.J Nanomater.2015; (11):1-14. [12]Mandrycky C,Wang Z,Kim K,et al.3D bioprinting for engineering complex tissues.Biotechnol Adv. 2016;34(4): 422-434. [13]Kim S,Kim BS.Control of Adult Stem Cell Behavior with Biomaterials.Tissue Eng Regen Med.2014;11(6):423-430. [14]Tabata Y,Ikada Y.Protein release from gelatin matrices.Adv Drug Deliver Rev.1998;31(3):287-301. [15]Hakam MS,Imani R,Abolfathi N,et al.Evaluation of fibrin-gelatin hydrogel as biopaper for application in skin bioprinting: An in-vitro study.Biomed Mater Eng.2016;27(6): 669-682. [16]Kim DH,Martin JT,Elliott DM,et al.Phenotypic stability, matrix elaboration and functional maturation of nucleus pulposus cells encapsulated in photocrosslinkable hyaluronic acid hydrogels. Acta Biomaterialia.2015;12:21-29. [17]Lee SH,Jo AR,Choi GP,et al.Fabrication of 3D Alginate Scaffold with Interconnected Pores using Wire-Network Molding Technique.Tissue Eng Regen Med. 2013;10(2): 53-59.[18]Kopf M,Campos DF,Blaeser A,et al.A tailored three-dimensionally printable agarose-collagen blend allows encapsulation, spreading, and attachment of human umbilical artery smooth muscle cells. Biofabrication.2016;8(2):025011. [19]Singarapu K,Sundararajan MV.Evaluation of Chitosan-Gelatin Thermo-Sensitive Hydrogels for Bioprinting. Tissue Eng Pt A.2014;20:S94-S95. [20]Kundu J,Shim JH,Jang J,et al.An additive manufacturing- based PCL-alginate-chondrocyte bioprinted scaffold for cartilage tissue engineering.J Tissue Eng Regen Med.2015; 9(11):1286-1297. [21]Mironov AV,Grigoryev AM,Krotova LI,et al.3D printing of PLGA scaffolds for tissue engineering. J Biomed Mater Res A.2017;105(1):104-109. [22]Akimoto AM,Hasuike E,Tada H,et al.Design of Tetra-arm PEG-crosslinked Thermoresponsive Hydrogel for 3D Cell Culture.Ana Sci.2016;32(11):1203-1205.[23]Muller M,Becher J,Schnabelrauch M,et al.Nanostructured Pluronic hydrogels as bioinks for 3D bioprinting. Biofabrication.2015;7(3):035006. [24]Ozbolat IT,Yu Y.Bioprinting toward organ fabrication: challenges and future trends.IEEE Trans Biomed Eng.2013; 60(3):691-699. [25]Orloff ND,Truong C,Cira N,et al.Integrated bioprinting and imaging for scalable, networkable desktop experimentation. Rsc Adv.2014;4(65):34721-34728. [26]Murphy SV,Atala A.3D bioprinting of tissues and organs.Nat Biotechnol.2014;32(8):773-785.[27]Michael S,Sorg H,Peck CT,et al.Tissue engineered skin substitutes created by laser-assisted bioprinting form skin-like structures in the dorsal skin fold chamber in mice.PloS One. 2013;8(3): e57741. [28]Tack P,Victor J,Gemmel P,et al.3D-printing techniques in a medical setting: a systematic literature review.Biomed Eng Online.2016;15(1):115. [29]Chia HN,Wu BM. Recent advances in 3D printing of biomaterials. J Biol Eng.2015;9:4. [30]Duan B,Hockaday LA,Kang KH,et al.3D bioprinting of heterogeneous aortic valve conduits with alginate/gelatin hydrogels.J Biomed Mater res A.2013;101(5):1255-1264. [31]Zadpoor AA,Malda J.Additive Manufacturing of Biomaterials, Tissues, and Organs.Ann Biomed Eng.2017;45(1):1-11.[32]Patra S,Young V.A Review of 3D Printing Techniques and the Future in Biofabrication of Bioprinted Tissue.Cell Biochem Biophys. 2016;74(2): 93-98. [33]Kim JJ,Hou L,Huang NF.Vascularization of three-dimensional engineered tissues for regenerative medicine applications. Acta Biomaterialia.2016;41:17-26.[34]Shi D,Liu K,Zhang X,et al.Applications of three-dimensional printing technology in the cardiovascular field.Intern Emerg Med.2015;10(7):769-780. [35]Lee SY,Kim HJ,Choi D.Cell sources, liver support systems and liver tissue engineering: alternatives to liver transplantation. Int J Stem Cells.2015;8(1):36-47. [36]Sawkins MJ,Mistry P,Brown BN,et al.Cell and protein compatible 3D bioprinting of mechanically strong constructs for bone repair.Biofabricatio.2015;7(3):035004.[37]Fedorovich NE,Schuurman W,Wijnberg HM,et al. Biofabrication of Osteochondral Tissue Equivalents by Printing Topologically Defined, Cell-Laden Hydrogel Scaffolds.Tissue Eng Part C Methods.2012;18(1): 33-44. [38]Hockaday LA,Kang KH,Colangelo NW,et al.Rapid 3D printing of anatomically accurate and mechanically heterogeneous aortic valve hydrogel scaffolds. Biofabrication. 2012;4(3): 035005.[39]Lee W,Debasitis JC,Lee VK,et al.Multi-layered culture of human skin fibroblasts and keratinocytes through three-dimensional freeform fabrication.Biomaterials. 2009; 30(8):1587-1595.[40]Lee V,Singh G,Trasatti JP,et al.Design and fabrication of human skin by three-dimensional bioprinting.Tissue Eng Part C Methods.2014;20(6):473-484. [41]Koch L,Deiwick A,Schlie S,et al.Skin tissue generation by laser cell printing.Biotechnol Bioeng.2012;109(7):1855-1863.[42]Alkhouri N,Zein NN.Three-dimensional printing and pediatric liver disease.Curr Opin Pediatr. 2016;28(5):626-630. [43]Wu W,Deconinck A,Lewis JA.Omnidirectional printing of 3D microvascular networks.Adv Mater.2011;23(24): H178-183. [44]Miller JS,Stevens KR,Yang MT,et al.Rapid casting of patterned vascular networks for perfusable engineered three-dimensional tissues.Nat Mater.2012;11(9):768-774. [45]Lee VK,Kim DY,Ngo H,et al.Creating perfused functional vascular channels using 3D bio-printing technology. Biomaterials. 2014;35(28):8092-8102. [46]Zhao Y,Yao R,Ouyang L,et al.Three-dimensional printing of Hela cells for cervical tumor model in vitro.Biofabrication. 2014;6(3):035001. [47]King SM,Presnell SC,Nguyen DG.Development of 3D bioprinted human breast cancer for in vitro drug screening. Cancer Res.2014;74(19):2034. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [3] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [4] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [5] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [6] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [7] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||